Ситуационные задачи по биохимии. Сборник ситуационных задач по биохимии по специальности 060301-. Сборник ситуационных задач с эталонами ответов для студентов, обучающихся по специальности
 Скачать 0.53 Mb. Скачать 0.53 Mb.
|
ОТВЕТЫХИМИЯ АМИНОКИСЛОТ И БЕЛКОВ  Глицин и аланин останутся на старте; глутамат будет двигаться к положительно заряженному аноду (+), аргинин, лизин, гистидин будут двигаться к отрицательно заряженному катоду (-). Метионин-триптофан-треонин. Молекулярная масса альбумина около 35000. Хранить в холодильнике при температуре не выше 10ОС, растворять сухие препараты охлажденной до комнатной температуры кипяченой водой (чтобы избежать денатурации). Возможно, отщепились аминокислоты с гидрофильными радикалами, поэтому растворимость белка снизилась. Известно, что устойчивость белков в изоэлектрической точке (ИЭТ) к действию неблагоприятных факторов снижается. Изоэлектрическая точка казеина лежит в кислой среде, поэтому устойчивость белка к нагреванию снизилась, он денатурировал. Они обладают высокой гидрофильностью, так как имеют ОН-группы, благодаря которым образуют водородные связи и изменяют конформацию белков вплоть до денатурации. Можно предположить, что их длительный и более сильный эффект связан с тем, что модифицированные лиганды медленнее разрушаются в организме, а значит действуют на белки больший период времени. ФЕРМЕНТЫ  Специфичность пептидаз свертывающей системы крови выше, чем специфичность пептидаз пищеварительного тракта. Это объясняется количеством и разнообразием субстратов. Пептидазы каскада свертывания крови входят в состав 3-х ферментативных комплексов и количество субстратов для них ограничено. Пептидазы пищеварительного тракта действуют на определенные связи в любых пищевых белках и таких белков множество. д. Для сохранения сладкого вкуса початков кукурузы требуется прекратить превращение глюкозы в крахмал. Для этого необходимо денатурировать, и таким образом, инактивировать ферменты, катализирующие этот процесс. Это достигается путем кипячения початков сразу после сбора. Протеинкиназа переносит фосфат с АТФ на белки, фосфорилируя их. цАМФ является аллостерическим активатором этого фермента. АТФ и цАМФ содержат в своем составе аденин и рибозу, но отличаются по количеству остатков фосфорной кислоты. В АТФ содержится 3 остатка фосфорной кислоты, в цАМФ – только один остаток. Кроме того, в цАМФ фосфорная кислота связана с 3 и 5 атомами углерода рибозы, образуя цикл. Таким образом, АТФ и цАМФ отличаются по своему составу и строению, поэтому будут связываться с разными центрами протеинкиназы: АТФ присоединяется к активному центру, цАМФ – к аллостерическому. Активность кислой фосфатазы равна разности общей активности (без добавления тартрат-ионов) и активности после добавления этих ионов. 5 х 1014 минут а) класс оксидоредуктаз; б) класс лиаз; в) класс гидролаз; г) класс трансфераз. Типы регуляции: аллостерический, химическая модификация, взаимодействие белок-белок, конкурентное ингибирование. 1 –аллостерическая регуляция; 2 – химическая модификация (фосфорилирование-дефосфорилирование); 3 – ограниченный протеолиз; 4 – взаимодействие белок-белок. Ингибиторы пептидаз свертывающей системы приводят к снижению свертываемости. Так как свертываемость уже снижена, применять ингибиторы нельзя, так как их применение еще больше снизит свертываемость. Метанол под действием алкогольдегидрогеназы превращается в ядовитый формальдегид, накопление которого приводит к гибели организма. Этанол конкурирует с метанолом за активный центр данного фермента. Поэтому при отравлении метанолом введение этанола в больших дозах может спасти человека, так как вероятность связывания этанола с алкогольдегидрогеназой будет выше, и ядовитый формальдегид не будет образовываться. Субстраты ферментов в активном центре связываются с определёнными функциональными группами, и эти связи стабилизируют структуру молекулы фермента, делая её более устойчивой к нагреванию. По сравнению со свободным ферментом, нужна дополнительная энергия для их разрыва, прежде чем начнётся тепловая инактивация молекулы белка. Аммиак проявляет основные свойства. Его накопление в больших количествах сдвигает рН в щелочную сторону, что приводит к снижению активности ферментов из-за изменения их конформации. Фосфорная кислота присоединяется фосфоэфирными связями к гидроксильным группам серина, тирозина или треонина. Это приведет к изменению конформации фермента и, вследствие этого, изменит его активность. Аланин имеет гидрофобный радикал, который участвует в образовании гидрофобных связей. Глутамат содержит отрицательно заряженный радикал, который участвует в образовании ионных связей. Поэтому замена аланина на глутамат вызовет изменение конформации фермента и, следовательно, к потере его активности.   1) СО2 + Н2О Н2СО3 Н+ + НСО3- 1) СО2 + Н2О Н2СО3 Н+ + НСО3-2) график зависимости активности фермента от рН смотрите в учебнике и лекции. 3) накопление углекислого газа в организме приводит к метаболическому ацидозу, что изменяет конформацию ферментов в результате разрыва водородных или ионных связей. Присоединение к ферменту метильных групп приводит к изменению конформации фермента, вследствие образования дополнительных гидрофобных связей, а, следовательно, к изменению его активности. Химическая модификация является одним из механизмов регуляции активности ферментов, при которой регулятор ковалентно присоединяется к их белковым молекулам. Присоединение к белкам глюкозы ковалентной связью также приводит к изменению конформации этих белков, а, следовательно, к изменению их свойств. Гликозилирование белков является разновидностью химической модификации. Однако в организме гликозилирование белков не является способом регуляции ферментов, так как глюкоза присоединяется к белкам необратимо. Соли тяжелых металлов даже в низких концентрациях могут связывать функциональные группы радикалов аминокислот активного центра, изменять конформацию или денатурировать ферменты, что приводит к их инактивации. При 38оС происходит синтез интерферона. Повышение температуры выше 38оС приводит денатурации ферментов и их инактивации. Повышение температуры до 70оС приводит тепловой денатурации белков и гибели клеток. Локальное нагревание опухоли приводит к разрушению раковых клеток. Сходство: в обоих случаях изменяется конформация ферментов. Различия: при химической модификации регулятор ковалентно присоединяется к ферменту, а при аллостерической регуляции регулятор присоединяется нековалентно к особому (аллостерическому) центру. При воспалении повышается проницаемость клеточных мембран и в сыворотку крови могут выйти цитоплазматические ферменты. При некрозе ткани разрушаются все клеточные структуры. В сыворотке крови в этом случае могут быть обнаружены ферменты митохондрий, ядер и других клеточных структур. е      г б ж д а г б ж д аБольшинство лекарств действуют как конкурентные ингибиторы ферментов. Эффективность ингибирования зависит от концентрации ингибитора. Поэтому лекарство (ингибитор) необходимо принимать через определенные промежутки времени в определенной концентрации для того, чтобы эффективность ингибирования не снижалось. В незаживающих ранах накапливаются вещества из разрушенных клеток и лейкоциты, поэтому раны долго не заживают. Для их удаления используют трипсин и гиалуронидазу, которые расщепляют белки и гиалуроновую кислоту соответственно, что приводит к очищению раны. БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕ  Скорость цикла Кребса снизится, так как эти витамины входят в состав кофакторов дегидрогеназ: В1, В2, РР входят в состав 2-оксоглутаратдегидрогеназы, РР – в состав изоцитратдегидрогеназы и малатдегидрогеназы, В2 – в состав сукцинатдегидрогеназы. Изоцитратдегидрогеназа, 2-оксоглутаратдегидрогеназа и малатдегидро-геназа (смотрите учебник или лекцию). Напишите в формулах реакции цикла Кребса, укажите положение метки. Продукты: сукцинат; 2 молекулы СО2; 2 молекулы НАДН; 1 молекула АТФ (субстратное фосфорилирование). Если дегидрогеназные реакции этого этапа будут сопряжены с дыхательной цепью, то образуются ещё 6 АТФ (окислительное фосфорилирование). Таким образом, превращение цитрата в сукцинат приведет к синтезу 7 молекул АТФ. НАДН образуется путем восстановления НАД+ в пиридинзависимых реакциях цикла Кребса (ИЦДГ, 2-оксоглутаратДГ, малатДГ). Образованный НАДН поступает в дыхательную цепь и НАДН-дегидрогеназой окисляется до НАД+, который далее используется выше указанными дегидрогеназами. Таким образом, если НАДН не окисляется в дыхательной цепи, цикл Кребса остановится из-за отсутствия НАД+. Для ответа на вопрос напишите в формулах цикл Кребса, укажите положение метки в каждом метаболите. Для ответа на вопрос подсчитайте количество НАДН и ФАДН2, образованных на указанных участках. Окисление НАДН в дыхательной цепи сопровождается образованием 3 АТФ, а ФАДН2 – 3 АТФ. На участке между пируватом и 2-оксоглутаратом образуется 2 НАДН. Это приводит к образованию 6 АТФ. На участке между изоцитратом и сукцинатом образуется 2 НАДН и 1 АТФ (субстратное фосфорилирование). Это приводит к образованию 7 АТФ. На участке между сукцинатом и оксалоацетатом образуется 1 НАДН и 1 ФАДН2. Это приводит к образованию 5 АТФ. Более мощным ядом будет антимицин, так как он блокирует поступление водорода на участке убихинола, а значит, водород не поступает не только от ФАД-зависимых дегидрогеназ, но и от НАДН-дегидрогеназы. Кокарбоксилаза входит в состав пируватдегидрогеназы и 2-оксоглутаратдегидрогеназы. Продукты пируватдегидрогеназы: ацетил-КоА, СО2, НАДН. Продукты 2-оксоглутаратдегидрогеназы: сукцинил-КоА, СО2, НАДН. СО2 выделяется с выдыхаемым воздухом или используется в реакции карбоксилирования. НАДН окисляется в дыхательной цепи с образованием 3 АТФ. Ацетил-КоА и сукцинил-КоА окисляются в цикле Кребса. 1 – В; 2 – Б; 3 – Г; 4 – Д; 5 – А. а) 3; б) 0; в) 2; г) 1. Разобщители повышают потребление кислорода и скорость переноса электронов по дыхательной цепи, но разобщают окисление и фосфорилирование. В результате образование АТФ резко снижается, что может вызвать гибель организма. а) правильное утверждение; б) правильное утверждение; в) неправильное утверждение, зависит; г) неправильное утверждение, влияют. Гипоэнергетическое состояние – это разнообразные состояния, при которых снижается синтез АТФ. а) гипоэнергетическое из-за недостаточности кислорода; б) гипоэнергетическое из-за недостаточности витаминов, которые необходимы для образования кофакторов ферментов, участвующих в реакциях энергетического обмена; в) гипоэнергетическое, так как не образуется электрохимический потенциал; г) гиперэнергетическое. 1 – А; 2 – А; 3 – А; 4 – А; 5 – А; 6 – В. При нормоксии окисление ацетил-КоА приводит к образованию 12 АТФ; при гипоксии образуется 1 АТФ в результате субстратного фосфорилирования в цикле Кребса. Скорость окисления пирувата и глюкозы снизится из-за ингибирующего влияния НАДН и ацетил-КоА на соответствующие процессы. Биологическое значение этого явления заключается в сохранении концентрации глюкозы в крови на нормальном уровне. Источниками тепловой энергии являются: 1) реакции расщепления сложных веществ (углеводов, жиров и белков) до СО2 и Н2О; б) работа дыхательной цепи в разобщенном режиме; в) любые окислительно-восстановительные реакции; г) расщепление АТФ. Мороз-Синий нос не смог заморозить мужика, так как он занимался физическим трудом, при котором используется АТФ на сокращение мышц. Расщепление АТФ сопровождается образованием тепла и человеку становится жарко. Кроме того, при охлаждении из окончаний симпатических нервов выделяется норадреналин, который активирует липазу в жировой ткани. В результате усиливается расщепление жира, повышается концентрация свободных жирных кислот, которые разобщают окисление и фосфорилирование в дыхательной цепи. Это тоже усиливает выделение тепла. Мороз-Багровый нос, одетый в теплую одежду, быстро замерз, так как выделение тепла у него было невысоким. Вместо того, чтобы двигаться и таким образом согреваться, он продолжал кутаться в свою одежду. Пируваткарбоксилаза превращает пируват в оксалоацетат, который используется в цикле Кребса, в глюконеогенезе, в реакции переамирования аминокислот. Дефект этого фермента приведет к недостатку оксалоацетата и, следовательно, к торможению цикла Кребса, а также торможению использования пирувата, полученного из аминокислот, в ГНГ. Нет, потому что два атома углерода теряются в цикле Кребса на двух стадиях декарбоксилирования (изоцитратдегидрогеназа и 2-оксоглутаратдегидрогеназа). Следовательно, накопления оксалоацетата происходить не будет. УГЛЕВОДНЫЙ ОБМЕН  ПЕРЕВАРИВАНИЕ УГЛЕВОДОВ. ОБМЕН ГЛИКОГЕНА Активность ферментов определяется по скорости убывания субстрата или по скорости образования продукта. При острых панкреатитах и при обострении хронического воспаления поджелудочной железы повышается проницаемость клеточных мембран и происходит разрушение клеток. Внутриклеточные ферменты поджелудочной железы освобождаются в кровь, в том числе и амилаза. Её активность в сыворотке повышается. Амилаза расщепляет α-1,4-гликозидные связи. Активность данного фермента определяется по скорости убывания крахмала. Сахароза, введенная животному внутривенно, появится в моче, так как она не будет использоваться клетками организма из-за отсутствия в них фермента, её метаболизирующего. Попав в ЖКТ, сахароза будет расщепляться под действием сахаразы кишечника до глюкозы и фруктозы, которые всасываются в кровь и далее потребляются клетками. Можно предположить дисахаридоз, вызванный отсутствием сахаразы. При отсутствии данного фермента сахароза не расщепляется в кишечнике до моносахаридов, а подвергается сбраживанию ферментами микроорганизмов с образованием кислот и газов. У больного можно предположить гликогеноз, при котором нарушен распад гликогена, но не изменен синтез. Так как мышцы не могут использовать собственный гликоген в качестве источника энергии, необходимо изменить образ жизни. Больному рекомендуется избегать напряженной кратковременной физической работы, которая совершается за счет энергии углеводов; прием пищи должен быть частым, небольшими порциями, чтобы мышца могла окислять поступившие в неё питательные вещества полностью, а не накапливать излишки в виде гликогена. При недостаточности галактокиназы накапливается галактоза. При недостаточности галактозо-1-фосфат-уридилтрансферазы накаплива-ется галактозо-1-фосфат. Он является более токсичным. Очевидно, нарушено всасывание продуктов переваривания углеводов, которые подвергаются брожению под действием кишечной микрофлоры с образованием газов и кислот. 1 – А; 2 – Б; 3 – Б; 4 – С. ГЛИКОЛИЗ. ГЛЮКОНЕОГЕНЕЗ ЛДГ    а) пируват лактат а) пируват лактатНАДН НАД+ б) гликолитическая оксидоредукция – это две сопряженных дегидрогеназных реакций: ЛДГ и глицеральдегиддегидрогеназа (ГАДГ) ЛДГ   пируват лактат пируват лактат  НАДН НАД+ НАДН НАД+ ГАДГ 3-фосфоглицериновый 1,3-дифосфоглицериновая альдегид кислота ЛДГ переводит НАДН в НАД+ и делает гликолиз не зависимым от дыхательной цепи и кислорода. Таким образом, благодаря ЛДГ клетка может получать энергию в анаэробных условиях. В присутствии ингибитора ЛДГ гликолиз будет заторможен или выключен полностью, АТФ образовываться не будет, эритроцит погибнет. Гликоген в работающей мышце расщепляется с образованием лактата и энергии. Лактат поступает в кровь и переносится в печень, где превращается в глюкозу, которая затем поступает в мышцу. Таким образом, опосредующим органом является печень. Стимулирует распад гликогена адреналин. Поскольку он действует на все мышцы, то и в неработающей мышце тоже будет расщепляться гликоген. При дефекте фосфорилазы мышц будет наблюдаться мышечная слабость, глюкоза в крови в норме, глюкагон вызывает гипергликемию, при физической нагрузке уровень лактата не меняется. При дефекте фосфорилазы печени будут увеличены размеры этого органа, наблюдается гипогликемия, введение глюкагона не вызывает повышения глюкозы крови, уровень лактата в крови при нагрузке повышается за счет стимуляции глюконеогенеза. Содержание лактата в крови у спортсмена, пробежавшего 100 м, будет выше, чем у спортсмена, пробежавшего 5000 м. Это объясняется тем, что сердечнососудистая система не успевает доставлять клеткам достаточное количество кислорода, поэтому они вынуждены получать энергию анаэробно за счет гликолиза, конечным продуктом которого является лактат. При беге на длинную дистанцию система кровообращения успевает подстроиться и обеспечить нормальное поступление кислорода в мышцы, в результате глюкоза окисляется до СО2 и Н2О. Схема: ц     итрат реакции цикла Кребса оксалоацетат реакции глюконеогенеза глюкоза итрат реакции цикла Кребса оксалоацетат реакции глюконеогенеза глюкоза Для синтеза одной молекулы глюкозы в этом случае потребуется 2 молекулы цитрата и 4 макроэрга (2 ГТФ и 2 АТФ). Фосфофруктокиназа 1 – В; 2 – Д; 3 – Д; 4 - С а, б, г, д Схема:    фруктоза реакции унификации ДОАФ+ 3-фосфоглицериновый фруктоза реакции унификации ДОАФ+ 3-фосфоглицериновый   альдегид альдегид С     АХАРОЗА глюкоза реакции гликолиза пируват АХАРОЗА глюкоза реакции гликолиза пируват 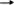 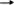 ацетил-КоА реакции цикла Кребса и дыхательной цепи ацетил-КоА реакции цикла Кребса и дыхательной цепиСО2, Н2О и 76 АТФ Схему процесса смотрите в учебнике или лекции. На синтез 10 молекул глюкозы из пирувата потребуется 60 макроэргов (40 АТФ и 20 ГТФ). Схему глюконеогенеза смотрите в учебнике или лекции. В условиях полного выключения цикла Кребса и дыхательной цепи глюконеогенез не будет протекать, так как будут ингибированы ферменты пируваткарбоксилаза и фосфоенолпируваткарбоксикиназа. При длительном голодании глюконеогенез является единственным процессом, позволяющим поддерживать гомеостаз глюкозы в крови, которая в этом случае используется только эритроцитами и головным мозгом. При окислении глюкозы в гликолизе образуется 2 АТФ, в гликогенолизе – 3 АТФ. Поэтому депонировать глюкозу в виде гликогена энергетически выгодно. Кроме этого, депонирование углеводов в форме глюкозы вызывает повышение осмотического давления в клетках, накопление глюкозы в виде гликогена осмотическое давление не изменяет. Физиологическое значение депонирования углеводов в мышцах заключается в том, что они являются легко усвояемым источником энергии. На синтез 1 молекулы глюкозы используется 2 молекулы лактата и 6 молекул АТФ. Для синтеза 30 молекул глюкозы потребуется 60 молекул лактата и 180 молекул АТФ. Чтобы получить это количество АТФ, необходимо окислить до воды и углекислого газа 10 молекул лактата, так как при окислении 1 молекулы лактата образуется 18 АТФ. Таким образом, для синтеза 30 молекул глюкозы требуется 70 молекул лактата. АЭРОБНОЕ ОКИСЛЕНИЕ УГЛЕВОДОВ. ГЛЮКОЗА КРОВИ Регенерация НАД+ (т.е. перевод НАДН в НАД+), необходимого для окисления новых молекул глицеральдегидфосфата, происходит: - При аэробном гликолизе с помощью цепи переноса электронов (дыхательной цепи). Для этого водород транспортируется из цитозоля в митохондрии с помощью специальных челночных механизмов. Синтез АТФ осуществляется путем окислительного фосфорилирования за счет энергии переноса электронов по дыхательной цепи. - При анаэробном гликолизе НАДН переводится в НАД+ с помощью лактатдегидрогеназы, которая осуществляет восстановление пирувата в лактат за счет водорода НАДН в цитозоле. Синтез АТФ в этом случае происходит в результате субстратного фосфорилирования, то есть с использованием энергии макроэргической связи субстрата. Метка будет находиться в 5-ом атоме углерода рибозо-5-фосфата. Нет, не будет, так как меченый атом углерода был удален в виде СО2 в результате декарбоксилирования 6-фосфоглюконовой кислоты. 1 – В, С; 2 – А; 3 – Д; 4 – Д. 1 – А; 2 – Е; 3 – Д; 4 – В; 5 – Е; 6 – Д Активируется пентозофосфатный путь. Целесообразно исследовать активность ключевых ферментов обоих процессов, например, фосфофруктокиназы (гликолиз) и глюкозо-6-фосфатдегидрогеназы (ПФП). Отклонений от нормы нет. Студент находился в состоянии стресса, выделился адреналин, который вызвал гипергликемию. Гипергликемическими гормонами являются глюкагон, норадреналин, адреналин, глюкокортикостероиды, соматотропин. Глюкагон и норадреналин усиливают расщепление гликогена в печени и глюконеогенез. Адреналин кроме этого усиливают гликолиз в мышцах, что приводит к гиперлактатемии. Соматотропин стимулирует освобождение глюкагона. Глюкокортикостероиды усиливают глюконеогенез и снижают использование глюкозы периферическими тканями. Гипогликемическим действием обладает инсулин, который усиливает проницаемость клеточных мембран для глюкозы, тормозит процессы – источники глюкозы и усиливает процессы – потребители глюкозы. Глюкоза постоянно извлекается из кровяного русла клетками и это приводит к гипогликемии. Состояние гипергликемии возникает только после приема пищи и стресса. Поэтому гипогликемия возникает чаще, чем гипергликемия. Таким образом, гипергликемических гормонов требуется больше, чем гипогликемических. Для нормализации состояния необходимо ввести инсулин. Введение глюкозы одновременно с инсулином не окажет отрицательного воздействия. Адреналин вызывает гипергликемию в результате усиления ГНГ и распада гликогена. Оба процесса локализованы в печени, поэтому у животных с удаленной печенью введение адреналина глюкозу в крови не повышает. ЛИПИДНЫЙ ОБМЕН  ПЕРЕВАРИВАНИЕ ЖИРА. ЛИПОЛИЗ И ЛИПОГЕНЕЗ Да влияет, так как не будут в полной мере проявляться функции желчных кислот. Это состояние называется гиперлипидемия. Да может, если кровь взяли у пациента после еды. В этом случае кровь богата хиломикронами. Через 5 часов после еды в крови можно обнаружить липоротеины, в основном ЛПНП (60%), ЛПОНП (15%). ЛПВП (25%). Нужны для всасывания жирорастворимых витаминов. 0,96 г. Гиповитаминозы А, Д, Е, К. Q В полости тонкой кишки пищевые жиры под действием панкреатической липазы расщепляются с образованием жирных кислот и моноглицеринов. В слизистой тонкой кишки из них происходит ресинтез жира, который включается в состав незрелого хиломикрона. Незрелый хиломикрон превращается в зрелый путем включения в его состав апопротеинов Е и С-II. Донором этих апопротеинов являются ЛПВП. Хиломикроны являются транспортной формой ресинтезированных к стенке кишечника липидов, в основном жиров. ТГ под действием панкреатической липазы расщепляются с образованием жирных кислот и моноглицеринов. Желчных кислоты эмульгируют пищевые жиры, активируют панкреатическую липазу, необходимы для всасывания нерастворимых продуктов переваривания жиров. Снижение секреции или активности панкреатической липазы, что наблюдается при панкреатите, или нарушение эмульгирования жиров вследствие недостаточного поступления желчи в просвет кишечника (например, при желчнокаменной болезни) приводит к стеаторее. Больному необходимо использовать фармакопрепараты, содержащие липазу и желчные кислоты, диету с небольшим содержанием жиров. Потребуется 4 АТФ, из них 3 АТФ будут использованы на активацию 3 молекул пальмитиновой кислоты и 1 АТФ – на активацию глицерина. Жиры являются гидрофобными молекулами, их взаимодействие друг с другом позволяет создать самую компактную форму хранения энергии, так как молекулы жира «прилипают» друг к другу и между ними нет воды. Жиры хранятся в адипоцитах жировой ткани. Гликоген представляет собой разветвленный полисахарид, мономером которого является глюкоза. Он является полярной, но плохо растворимой в воде молекулой, хранится в цитозоле клеток в форме гранул. Если бы энергия, содержащаяся в липидах, запасалась в виде гликогена, то масса тела была бы значительно большей. ОБМЕН ЖИРНЫХ КИСЛОТ, ГЛИЦЕРИНА И КЕТОНОВЫХ ТЕЛ Глицерин вначале активируется путем фосфорилирования под действием глицеролкиназы с образованием глицерофосфата, который в печени используется в синтезе жиров, глицерофосфолипидов. Кроме того, глицерофосфат под действием глицерофосфатдегидрогеназы превращается в диоксиацетонфосфат, который может использоваться в гликолизе или глюконеогенезе. Путь использования глицерина в печени зависит от энергообеспеченности клетки. В жировой ткани активность глицеролкиназы низкая, поэтому глицерин практически не используется. Окисление 1 молекулы глюкозы приводит к образованию 38 АТФ, а окисление пальмитиновой кислоты – 130 АТФ. Для синтеза бутановой кислоты потребуется 1 АТФ, 2 ацетил-КоА, 2 НАДФН. На синтез 3 молекул стеариновой кислоты требуется 24 АТФ. При окислении 1 молекулы ацетил-КоА образуется 12 АТФ. Таким образом, чтобы покрыть эти энергетические затраты, нужно окислить 2 молекулы ацетил-КоА до СО2 и Н2О. Окисление НАДН и ФАДН2, образованных в β-окислении, происходит в дыхательной цепи, которая работает только в аэробных условиях. Ацетил-КоА образуется в ходе β-окисления жирных кислот и в результате пируватдегидрогеназной реакции из пирувата. Если метка обнаружена в ацетил-КоА, но не обнаружена в пирувате, значит она находилась в жирных кислотах жиров, поступивших с пищей. Окисление 1 молекулы глюкозы образуется 38 АТФ. Трипальмитин состоит из 3 молекул пальмитиновой кислоты и глицерина. Окисление пальмитиновой кислоты приводит к образованию 130 АТФ, окисление глицерина дает 21АТФ. Таким образом, окисление трипальмитина приводит к образованию 130х3+21=411 АТФ. Это в 10,8 раза больше, чем при окислении глюкозы. У пациента А, получавшего гипергликемическую диету, соотношение инсулин/глюкагон будет выше, так как избыток калорий будет использован на синтез жиров. У этого же пациента количество ацетил-КоА–карбоксилазы будет высоким, так как она является ключевым ферментом синтеза жирных кислот, которые будут образовываться из ацетил-КоА, полученного из углеводов. Тристеарин состоит из 3 молекул стеариновой кислоты и глицерина. Окисление стеариновой кислоты (С18) приводит к образованию 147 АТФ, окисление глицерина дает 21АТФ. Таким образом, окисление трипальмитина приводит к образованию 147х3+21=462 АТФ. Содержание кетоновых тел может быть повышено при сахарном диабете (патологический кетоз), голодании, тяжелой мышечной работе, беременности (физиологический кетоз). Необходимо определить глюкозу в сыворотке крови. Окисление 1 моля β-гидроксибутирата до СО2 и Н2О приводит к образованию 27 АТФ. С 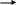 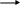 хема процесса: β-гидроксибутират Ацетоацетат + НАДН хема процесса: β-гидроксибутират Ацетоацетат + НАДН 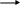 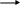 2 Ацетил-КоА 2х12АТФ + 3АТФ = 27 АТФ 2 Ацетил-КоА 2х12АТФ + 3АТФ = 27 АТФКетоновыми телами являются два вещества: ацетоацетат и β-гидроксибутират. Оба вещества содержат 4 атома углерода. Синтез кетоновых тел происходит в митохондриях гепатоцитов печени и для их синтеза требуется 3 молекулы ацетил-КоА. При этом 1 молекула ацетил-КоА служит затравкой. Таким образом, для синтеза 100 молекул β-кетобутирата потребуется 200 + 1 молекула ацетил-КоА. Для полного расщепления молекулы стеариновой кислоты до СО2 и Н2О, если она уже находится в митохондриях, потребуется 2 молекулы НS-КоА (1 молекула для образования ацил-КоА, 1 молекула для тиолазной реакции). ОБМЕН ХОЛЕСТЕРИНА. ЛИПИДЫ КРОВИ. ПАТОЛОГИИ ЛИПИДНОГО ОБМЕНА Эфиры холестерина, фосфолипиды и жиры пищи расщепляются под действием эстераз пищеварительных соков. Для всасывания продуктов переваривания требуются желчные кислоты. Всосавшиеся продукты используются в ресинтезе липидов, в том числе и триацилглицеринов. Поэтому меченая олеиновая кислота попадет не только в эфиры холестерина, но и во фракцию триацилглицеринов. Ресинтезированные липиды включаются в состав хиломикронов, а вместе с ними и метка. Г 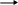 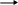 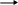 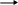 люкоза Пируват Ацетил-КоА ГМГКоА Холестерин люкоза Пируват Ацетил-КоА ГМГКоА Холестерин Это делают для того, чтобы увеличить выведение желчных кислот с фекалиями. Так как для синтеза желчных кислот используется холестерин, чем больше желчных кислот будет выведено из организма, тем больше холестерина потребуется для синтеза новых молекул этих кислот. При облучении разрушаются клетки. Холестерин необходим для построения клеточных мембран новых клеток, поэтому синтез холестерина будет увеличен. В печень из кишечника поступают аминокислоты, глицерин, моносахариды, которые могут превращаться в жир. 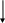 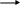    Аминокислоты Глюкоза Пируват Ацетил-КоА Ацил-КоА Аминокислоты Глюкоза Пируват Ацетил-КоА Ацил-КоА  Диоксиацетонфосфат Диоксиацетонфосфат |
