Сборник тестов по общей химии для студентов лечебнопрофилактического, педиатрического, медикопсихологического и медикодиагностического факультетов
 Скачать 201.82 Kb. Скачать 201.82 Kb.
|
|
n – это: величина заряда окисленной или восстановленной формы; разность между величинами заряда окисленной и восстановленной форм; число электронов переходящих от окисленной формы на металлическую пластинку; число электронов, которые принимает одна молекула или ион окисленной формы, превращаясь в восстановленную форму. 63.Величина редокс-потенциала при Т=298К может быть рассчитана по уравнению: E = E0 – 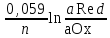 ; ;E = E0 – 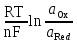 ; ;E = E0 + 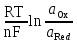 ; ;E = E0 + 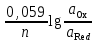 . .64.Имеются пять окислительно-восстановительных систем: 1) Fe3+/ Fe2+; 2) Cu2+/Cu+; 3) Cl2/2Cl- ; 4) BrO-/Br-; 5) Sn4+/Sn2+. Значения их редокс-потенциалов равны, соответственно: 1) 0,771В; 2) 0,16В; 3) 1,36В; 4) 0,76В; 5) 0,153В. В роли окислителя по отношению к системе Fe3+/ Fe2могут выступать: Cu2+/Cu+; Cl2/2Cl- ; BrO-/Br-; Sn4+/Sn2+. 65. Имеется пять окислительно – восстановительных систем: 1) Fe3+/ Fe2 ; 2) Cu2+/Cu+; 3) Cl2/2Cl- ; 4) BrO-/Br-; 5) Sn4+/Sn2+. Значения их редокс- потенциалов равны соответственно: 1)0,771В; 2) 0,16В; 3) 1,36В; 4) 0,76В; 5) 0,153В. В роли восстановителя по отношению к системе BrO– /Br– могут выступать: Cu2+/Cu+; Cl2/2Cl- ; Fe3+/ Fe2 ; Sn4+/Sn2+. 66. Пластина из инертного металла в редокс- электроде: выступает в качестве посредника при обмене электронами между окисленной и восстановленной формами; подвергается окислению за счет химического взаимодействия с компонентами редокс – системы; подвергается восстановлению за счет химического взаимодействия с компонентами редокс – системы; заряжается положительно или отрицательно в зависимости от соотношения между окисленной и восстановленной формами. 67.Величина редокс-потенциала зависит от: природы инертного металла; формы и размеров металлической пластинки; природы частиц, образующих редокс-систему; концентрации компонентов редокс-системы в растворе. 68.Значения Е0 для редокс-электродов: определяют экспериментально относительно стандартного водородного электрода; рассчитывают по уравнению Нернста; определяют экспериментально относительно любого металлического электрода; рассчитывают по уравнению Петерса. 69. При определении значения Е0 для редокс-электрода: концентрации или активности окисленной и восстановленной форм в растворе должны быть одинаковыми; активность других частиц (Н+, ОН- и т.д.), принимающих участие в процессе перехода окисленной формы в восстановленную, должна быть равна активности окисленной или восстановленной форм; активность других частиц (Н+, ОН- и т.д.), принимающих участие в процессе перехода окисленной формы в восстановленную, должна быть равна 1моль/дм3; активность воды в растворе должна быть равна 1моль/дм3. 70.Для окислительно-восстановительной системы MnO4-/Mn2+, в которой осуществляется следующий электродный процесс: Mn+7O4– + 8H+ + 5ē Mn2+ + 4H2O редокс-потенциал рассчитывается по формуле: E = E0 + 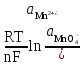 ; ;E = E0 + 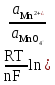 ; ;E = E0 + 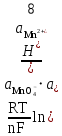 ; ;E = E0 + 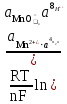 . .71.Диффузионные потенциалы возникают: на границе соприкосновения двух растворов с одинаковой концентрацией одного и того же вещества; на границе соприкосновения двух растворов с разными концентрациями одного и того же вещества; на границе соприкосновения двух растворов разных веществ с одинаковой концентрацией; на границе соприкосновения двух растворов разных веществ с неодинаковой концентрацией. 72.Причина возникновения диффузионного потенциала заключается в: различной природе растворённых веществ; специфических свойствах растворителя; влиянии внешних условий (температуры, давления и т.д.); различной подвижности ионов растворённых веществ. 73.Диффузионный потенциал возникнет при соприкосновении: двух растворов одного и того же неэлектролита с различными концентрациями; двух растворов одного и того же неэлектролита с одинаковыми концентрациями; двух растворов одного и того же электролита с разными концентрациями; двух растворов разных электролитов с одинаковыми концентрациями. 74.При смешивании растворов одного и того же вещества, но с разной концентрацией: более разбавленный раствор приобретает заряд, совпадающий по знаку с зарядом более подвижных ионов; более разбавленный раствор приобретает заряд, совпадающий по знаку с зарядом менее подвижных ионов; более концентрированный раствор приобретает знак заряда, совпадающий по знаку с зарядом менее подвижных ионов; более концентрированный раствор приобретает знак заряда, совпадающий по знаку с зарядом более подвижных ионов. 75.Диффузионный потенциал: существует в системе продолжительное время; возникает в биологических объектах при повреждении оболочек клеток; постепенно с завершением процесса диффузии в течение 1-2 часов уменьшается до нуля; сохраняет неизменным своё значение на протяжении всего периода существования. 76.Мембранный потенциал возникает: при неравномерном распределении ионов одного и того же вида по обе стороны мембраны; в результате обмена ионами между самой мембраной и раствором; в результате обмена электронами между мембраной и ионами в растворе; вследствие перехода электронов через мембрану от одних ионов к другим. 77.Особенностью мембранного потенциала является то, что в соответствующей ему электродной реакции: принимают участие только электроны; не принимают участие электроны; происходит обмен только ионами между мембраной и раствором; происходит обмен, как ионами, так и электронами между мембраной и раствором. 78.В ионо-селективных или мембранных электродах по обе стороны мембраны: в растворе присутствуют одни и те же ионы с одинаковой концентрацией; в растворе присутствуют разные ионы, но с одинаковой концентрацией; в растворе присутствуют одни и те же ионы, но с разной концентрацией; в растворе присутствуют разные ионы с неодинаковой концентрацией. 79.Концентрация определяемых ионов в мембранном электроде должна быть: постоянной с внутренней стороны мембраны; постоянной как с внешней, так и с внутренней стороны мембраны; постоянной с внешней стороны мембраны; одинаковой как с внешней, так и с внутренней стороны мембраны. 80.Разность потенциалов мембранного электрода зависит: только от потенциала, возникающего на внутренней стороне мембраны; только от потенциала, возникающего на внешней стороне мембраны; как от потенциала, возникающего на внутренней стороне мембраны, так и от потенциала, возникающего на внешней стороне мембраны; от концентрации определяемых ионов в растворе с внешней стороны мембраны. 81. Гальванические элементы: являются источниками постоянного тока; являются источниками переменного тока; преобразуют химическую энергию, выделяющуюся при протекании окислительно – восстановительной реакции в электрическую; преобразуют химическую энергию, выделяющуюся при протекании окислительно – восстановительной реакции, в тепловую или механическую. 82. Химическим гальваническим элементом является: элемент, составленный из двух различных металлических электродов с неодинаковыми электродными потенциалами; элемент, составленный из двух одинаковых металлических электродов, погруженных в растворы одной и той же соли, но с различной активностью ионов металла; элемент, составленный из двух одинаковых металлических электродов, погруженных в растворы одной и той же соли и с одинаковой активностью в них ионов металла; элемент, составленный из двух разных редокс – электродов, имеющих неодинаковые значения электродных потенциалов. 83. Концентрационным гальваническим элементом является: элемент, составленный из двух различных металлических электродов, опущенных в растворы соответствующих солей с одинаковой концентрацией ионов металла в них; элемент, составленный из двух одинаковых металлических электродов, погруженных в растворы одной и той же соли, но с разной концентрацией ионов металла. элемент, составленный из двух разных редокс – электродов, имеющих одинаковое значение электродных потенциалов; элемент, составленный из двух различных мембранных электродов. 84. В гальваническом элементе процесс окисления протекает: на электроде, имеющем большее значение электродного потенциала; на катоде; на электроде, имеющем меньшее значение электродного потенциала; на аноде. 85. В гальваническом элементе процесс восстановления протекает: на электроде, имеющем большее значение электродного потенциала; на катоде; на электроде, имеющем меньшее значение электродного потенциала; на аноде. 86. Для гальванического элемента электродвижущая сила определяется по уравнению э.д.с. = Е2 – Е1, где: Е2 – потенциал анода; Е2 – потенциал катода; Е1 – потенциал анода; Е1 – потенциал катода. 87. Для медно – цинкового элемента Якоби – Даниэля электродвижущая сила равна: э.д.с. = ЕZn – ЕCu; э.д.с. = ЕZn +ЕCu; э.д.с. = ЕCu – ЕZn; э.д.с. = ЕZn = ЕCu. 88. Для гальванического элемента Якоби – Даниэля потенциал медного электрода ЕCu = 0,337В, а потенциал цинкового электрода ЕZn = – 0,763В. Величина э.д.с. при этом будет равна: 1,1В; 0,426В; – 0,426В; 0,824В. 89.Схема гальванического элемента, образованного стандартными железным и серебряным электродами может быть представлена следующим образом: Ag AgNO3 Fe(NO3)2 Fe; Fe Fe(NO3)2 AgNO3 Ag ; Ag Fe(NO3)2 AgNO3 Fe ; Fe Fe(NO3)3 AgNO3 Ag . 90.При работе концентрационного химического элемента: происходит протекание химической реакции; выравниваются концентрации (активности) ионов металла около обоих электродов; происходит переход ионов металла против градиента их концентрации; происходит осаждение ионов металла из раствора на обоих электродах. 91.При работе концентрационного химического элемента: в раствор переходят ионы металла с электрода, имеющего меньшее значение электродного потенциала; в раствор переходят ионы металла с электрода, имеющего большее значение электродного потенциала; оседают из раствора ионы металла на электроде, имеющем большее значение электродного потенциала; оседают из раствора ионы металла на электроде, имеющем меньшее значение электродного потенциала. 92.Э.д.с. концентрационного гальванического элемента рассчитывается по формуле (a2>a1): э.д.с. = E1 + E2 +  ; ;э.д.с. = E1 – E2 +  ; ;э.д.с. = E1/ E2 –  ; ;э.д.с. =  . .93.Контрационный гальванический элемент будет работать до тех пор пока: активности ионов металла в обоих растворах не станут меньше 1моль/дм3; активности ионов металла в обоих растворах не станут равны нулю; активности ионов металла в обоих растворах не сравняются между собой; потенциалы обоих его электродов не сравняются между собой. 94. Схема концентрационного гальванического элемента представлена в случае: а) Cu Cu(NO3)2 Cu(NO3)2 Cu; а1<а2 б) Zn Zn(NO3)2 AgNO3 Ag; а1<а2 в) Ag AgNO3 AgNO3 Ag; а1=а2 г) Fe Fe(NO3)2 Cu(NO3)2 Cu. а1=а2 95. Рабочим или индикаторным электродом в потенциометрии является электрод: потенциал которого остается постоянным и не зависит от состояния исследуемого раствора; потенциал которого зависит от концентрации исследуемого вещества; потенциал которого условно принят равным нулю; потенциал которого имеет меньшее значение. 96. Электродом сравнения в потенциометрии является электрод, потенциал которого: сохраняет постоянное значение независимо от состояния исследуемого раствора; условно принят равным нулю; всегда имеет положительное значение; имеет большее значение. 97. В отличие от титриметрических потенциометрические методы анализа: позволяют проводить определения только в прозрачных растворах; позволяют проводить определения в мутных и окрашенных растворах; не требуют присутствия индикатора; могут осуществляться непосредственно в биологических объектах, т.е. «in vivo». 98. Прямая потенциометрия (ионометрия) – это потенциометрический метод, в котором индикаторным электродом является: соответствующий мембранный электрод; металлический электрод; водородный электрод; стеклянный электрод. 99. С помощью потенциометрического титрования можно определить: концентрацию ионов Н+ в растворе; концентрацию ионов ОН– в растворе; концентрацию кислоты в анализируемом растворе; концентрацию основания в анализируемом растворе. 100. При определении кислоты в растворе с помощью метода потенциометрического титрования в качестве индикаторного электрода используют, как правило: водородный электрод; хингидронный электрод; хлорсеребряный электрод; стеклянный электрод. 101. Недостатком стеклянного электрода является то, что он: не может быть использован в широком диапазоне значений рН; чувствителен к различным примесям, содержащимся в растворе и способен «отравляться» ими; не может быть использован, если в исследуемом растворе содержатся сильные окислители или восстановители; обладает большой хрупкостью. 102. Солевой мостик в гальванических элементах используют для: осуществления контакта между электродами; устранения влияния диффузионного потенциала; ускорения процессов диффузии между растворами; предохранения электродов от коррозии. 103. Солевой мостик в гальванических элементах заполняется обычно раствором хлорида калия, так как: этот электролит в растворе не подвергается гидролизу; данная соль не может химически взаимодействовать с материалом любого электрода; ионы К+ и Сl– обладают одинаковой подвижностью в водном растворе; ионы К+ не могут восстанавливаться на катоде, а ионы Сl– окисляться на аноде. 104. Потенциал повреждения, образующийся в биологических системах при разрушении оболочек клеток: по своей природе является диффузионным; обычно достигает величины порядка 30 – 40 мV; может достигать величины нескольких десятков вольт; сохраняет неизменным свое значение на протяжении нескольких суток, а затем практически мгновенно уменьшается до нуля. 105. В уравнении Нернста, используемом для расчета электродного потенциала значение температуры приводится по: шкале Фаренгейта; шкале Цельсия; шкале Кельвина; любой из трех вышеперечисленных шкал. 106. В уравнении Нернста, с помощью которого рассчитывается потенциал металлического электрода, для количественной характеристики ионов металлов используют их: процентную концентрацию; молярную концентрацию; моляльную концентрацию; мольную долю в растворе. |
