Содержание 14. А
 Скачать 3.72 Mb. Скачать 3.72 Mb.
|
|
Митохондриальные заболевания обусловлены генетическими, структурными, биохимическими дефектами митохондрий, приводящими к нарушениям тканевого дыхания. Они передаются только по женской линии к детям обоих полов, так как сперматозоиды передают зиготе половину ядерного генома, а яйцеклетка поставляет и вторую половину генома, и митохондрии. Патологические нарушения клеточного энергетического обмена могут проявляться в виде дефектов различных звеньев в цикле Кребса, в дыхательной цепи, процессах бета-окисления и т. д. Не все ферменты и другие регуляторы, необходимые для эффективного функционирования митохондрий, кодируются митохондриальной ДНК. Большая часть митохондриальных функций контролируется ядерной ДНК[1]. Можно выделить 2 группы митохондриальных заболеваний:
Митохондрии наследуются иначе, чем ядерные гены. Ядерные гены в каждой соматической клетке обычно представлены двумя аллелями (за исключением большинства сцепленных с полом генов у гетерогаметного пола). Один аллель унаследован от отца, другой от матери. Однако митохондрии содержат собственную ДНК, причем в каждой митохондрии человека обычно содержится от 5 до 10 копий кольцевой молекулы ДНК (см. Гетероплазмия), и все они наследуются от матери. . Когда митохондрия делится, копии ДНК слеучайным образом распределяются между ее потомками, а затем происходит удвоение ДНК. Если только одна из исходных молекул ДНК содержит мутацию, в результате случайного распределения такие мутантные молекулы могут накопиться в некоторых митохондриях. Митохондриальная болезнь начинает проявляться в тот момент, когда заметное число митохондрий во многих клетках данной ткани приобретают мутантные копии ДНК (пороговая экспрессия). Мутации в митохондриальной ДНК происходят по разным причинам намного чаще, чем в ядерной. Это означает, что митохондриальные болезни достаточно часто проявляются из-за спонтанных вновь возникающих мутаций. Иногда темп мутирования увеличивается из-за мутаций в ядерных генах. кодирующих ферменты, которые контролируют репликацию ДНК митохондрий. 17.Общие принципы генетического контроля экспрессии генов. Важнейшим фактором регуляции генной активности являются элементы генома, отвечающие за синтез регуляторных белков,— гены-регуляторы. Соединяясь с определенными нуклеотидными последовательностями ДНК, предшествующими структурной части регулируемого гена,—операторами, белки-регуляторы способствуют или препятствуют соединению РНК-полимеразы с промотором. Если белок-регулятор взаимодействует с оператором, занимающим часть промотора или расположенным между ним и структурной частью гена, то это не дает возможности РНК-полимеразе соединиться с промоторной последовательностью и осуществить транскрипцию. Такой белок называют репрессором, и в этом случае осуществляется негативный контроль экспрессии гена со стороны гена-регулятора (рис. 3.85). Если промотор обладает слабой способностью соединяться с РНК-полимеразой, а ему предшествует область, узнаваемая белком-регулятором, присоединение последнего непосредственно перед промотором к молекуле ДНК облегчает связывание РНК-полимеразы с промотором, вслед за чем следует транскрипция. Такие белки называют активаторами (или апоиндукторами), а контроль экспрессии гена со стороны гена-регулятора — позитивным (рис. 3.85). 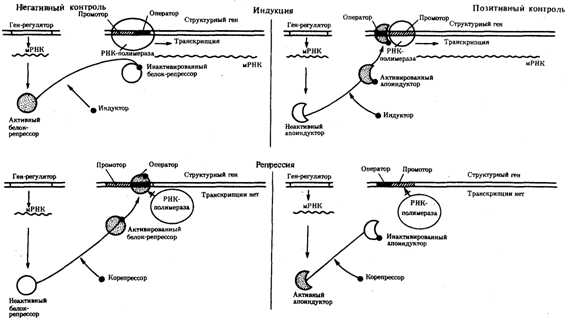 18.Нейтральные мутации. Генетический полиморфизм. Нейтральные. Нейтральные мутации, не дающие организму преимуществ или недостатков, не поддаются действию естественного отбора. С генетической точки зрения, эти мутации изменяют кодон так, что он не меняет кодируемой аминокислоты или меняет ее на другую, вполне приемлемую. Нейтральные мутации имеют тенденцию уходить из популяции посредством генетического дрейфа. Генетический полиморфизм - сосуществование в пределах популяции, двух или нескольких различных наследственных форм, находящихся в динамическом равновесии в течение нескольких и даже многих поколений. Чаще всего Г. п. обусловливается либо варьирующими давлениями и векторами (направленностью) отбора в различных условиях (например, в разные сезоны), либо повышенной относительной жизнеспособностью гетерозигот. Один из видов Г. п. — сбалансированный Г. п. — характеризуется постоянным оптимальным соотношением полиморфных форм, отклонение от которого оказывается неблагоприятным для вида, и автоматически регулируется (устанавливается оптимальное соотношение форм). В состоянии сбалансированного Г. п. у человека и животных находится большинство генов. Различают несколько форм Г. п., анализ которых позволяет определять действие отбора в природных популяциях. 19.Классификация генов человека по структуре и функциям. Ген представляет собой последовательность нуклеотидов ДНК размером от нескольких сотен до миллиона пар нуклеотидов, в которых закодирована генетическая информация о первичной структуре белка (число и последовательность аминокислот). Для регулярного правильного считывания информации в гене должны присутствовать: кодон инициации, множество смысловых кодонов и кодон терминации. Три подряд расположенных нуклеотида представляют собой кодон, который и определяет, какая аминокислота будет располагаться в данной позиции в белке. Например, в молекуле ДНК последовательность оснований ТАС является кодоном для аминокислоты метионина, а последовательность ТТТ кодирует фенилаланин. В молекуле иРНК вместо тимина (Т) присутствует основание урацил (У). Таблица генетического кода во всех руководствах представлена именно символами иРНК. Из 64 возможных кодонов смысловыми являются 61, а три триплета — УАА, УАГ, УГА — не кодируют аминокислоты и поэтому были названы бессмысленными, однако на самом деле они представляют собой знаки терминации трансляции. Для прокариот характерна относительно простая структура генов. Так, структурный ген бактерии, фага или вируса, как правило, контролирует одну ферментативную реакцию. Специфичным для прокариот является оперонная система организации нескольких генов. Гены одного оперона (участка генетического материала, состоящего из 1, 2 и более сцепленных структурных генов, которые кодируют белки (ферменты), осуществляющие последовательные этапы биосинтеза какого-либо метаболита; в оперон эукариот входит, как правило, 1 структурный ген; оперон содержит регуляторные элементы) расположены в кольцевой хромосоме бактерии рядом и контролируют ферменты, осуществляющие последовательные или близкие реакции синтеза (лактозный, гистидиновый и др. опероны). Структура генов у бактеориофагов и вирусов в основном схожа с бактериями, но более усложнена и сопряжена с геномом хозяев. Например, у фагов и вирусов обнаружено перекрывание генов, а полная зависимость вирусов эукариот от метаболизма клетки-хозяина привела к появлению экзон-интронной структуры генов. Эукариотические гены, в отличие от бактериальных, имеют прерывистое мозаичное строение. Кодирующие последовательности (экзоны) перемежаются с некодирующими (интронами). Экзон [от англ. ex(divssi)on — выражение, выразительность] - участок гена, несущий информацию о первичной структуре белка. В гене экзоны разделены некодирующими участками — интронами. Интрон (от лат. inter — между) - участок гена, не несущий информацию о первичной структуре белка и расположенный между кодирующими участками — экзонами. В результате структурные гены эукариот имеют более длинную нуклеотидную последовательность, чем соответствующая зрелая иРНК, последовательность нуклеотидов в которой соответствует экзонам. В процессе транскрипции информация о гене списывается с ДНК на промежуточную иРНК, состоящую из экзонов и интронов. Затем специфические ферменты — рестриктазы — разрезают эту про-иРНК по границам экзон-интрон, после чего экзонные участки ферментативно соединяются вместе, образуя зрелую иРНК (так называемый сплайсинг). Количество интронов может варьировать в разных генах от нуля до многих десятков, а длина — от нескольких пар оснований до нескольких тысяч. Ген может кодировать различные РНК-продукты путем изменения инициирующих и терминирующих кодонов, а также альтернативного сплайсинга. Альтернативная экспрессия гена осуществляется и путем использования различных сочетаний экзонов в зрелой иРНК, причем полипептиды, синтезированные на таких иРНК, будут различаться как по количеству аминокислотных остатков, так и по их составу. Наряду со структурными и регуляторными генами обнаружены участки повторяющихся нуклеотидных последовательностей, функции которых изучены недостаточно, а также мигрирующие элементы (мобильные гены), способные перемещаться по геному. Найдены также так называемые псевдогены у эукариот, которые представляют собой копии известных генов, расположенные в других частях генома и лишенные интронов или инактивированные мутациями. 3. Классификация генов Накопленные знания о структуре, функциях, характере взаимодействия, экспрессии, мутабильности и других свойствах генов породили несколько вариантов классификации генов. По месту локализации генов в структурах клетки различают расположенные в хромосомах ядра ядерные гены и цитоплазматические гены, локализация которых связана с хлоропластами и митохондриями. По функциональному значению различают структурные гены, характеризующиеся уникальными последовательностями нуклеотидов, кодирующих свои белковые продукты, которые можно идентифицировать с помощью мутаций, нарушающих функцию белка, и регуляторные гены — последовательности нуклеотидов, не кодирующие специфические белки, а осуществляющие регуляцию действия гена (ингибирование, повышение активности и др.). По влиянию на физиологические процессы в клетке различают летальные, условно летальные, супервитальные гены, гены-мутаторы, гены-антимутаторы и др. Следует отметить, что любые биохимические и биологические процессы в организме находятся под генным контролем. Так, деление клеток (митоз, мейоз) контролируется несколькими десятками генов; группы генов осуществляют контроль восстановления генетических повреждений ДНК (репарация). Онкогены и гены — супрессоры опухолей участвуют в процессах нормального деления клеток. Индивидуальное развитие организма (онтогенез) контролируется многими сотнями генов. Мутации в генах приводят к измененному синтезу белковых продуктов и нарушению биохимических или физиологических процессов. Гомеозисные мутации у дрозофилы позволили открыть существование генов, нормальной функцией которых является выбор или поддержание определенного пути эмбрионального развития, по которому следуют клетки. Каждый путь развития характеризуется экспрессией определенного набора генов, действие которых приводит к появлению конечного результата: глаза, голова грудь, брюшко, крыло, ноги и т. д. Исследования генов комплекса bithorax дрозофилы американским генетиком Льюисом показали, что это гигантский кластер тесно сцепленных генов, функция которых необходима для нормальной сегментации груди (thorax) и брюшка (abdomen). Подобные гены получили название гомеобоксных. Гомеобоксные гены расположены в ДНК группами и проявляют свое действие строго последовательно. Такие гены обнаружены и у млекопитающих, и они имеют высокую гомологию (сходство). 4. Функции генов В процессе реализации наследственной информации, заключенной в гене, проявляется целый ряд его свойств. Определяя возможность развития отдельного качества, присущего данной клетке или организму, ген характеризуется дискретностью действия (от лат. discretus — разделенный, прерывистый), прерывностью (интроны и экзоны). Дискретность наследственного материала, предположение о которой высказал еще Г. Мендель, подразумевает делимость его на части, являющиеся элементарными единицами, - гены. В настоящее время ген рассматривают как единицу генетической функции. Он представляет собой минимальное количество наследственного материала, которое необходимо для синтеза тРНК, рРНК или полипептида с определенными свойствами. Ген несет ответственность за формирование и передачу по наследству отдельного признака или свойства клеток, организмов данного вида. Кроме того, изменение структуры гена, возникающее в разных его участках, в конечном итоге приводит к изменению соответствующего элементарного признака. Ввиду того что в гене заключается информация об аминокислотной последовательности определенного полипептида, его действие является специфичным. Однако в некоторых случаях одна и та же нуклеотидная последовательность может детерминировать синтез не одного, а нескольких полипептидов. Это наблюдается в случае альтернативного сплайсинга у эукариот и при перекрывании генов у фагов и прокариот. Очевидно, такую способность следует оценить как множественное, или плейотропное, действие гена (хотя традиционно под плейотропным действием гена принято понимать участие его продукта – полипептида – в разных биохимических процессах, имеющих отношение к формированию различных сложных признаков). Например, участие фермента в ускорении определенной реакции (см. рис.), которая является звеном нескольких биохимических процессов, делает зависимыми результаты этих процессов от нормального функционирования гена, кодирующего этот белок. Нарушение реакции A→B, катализируемой белком α, в результате мутации гена ведет к выключению последующих этапов формирования признаков D и E. E Определяя возможность транскрибирования мРНК для синтеза конкретной полипептидной цепи, ген характеризуется дозированностью действия, т.е. количественной зависимостью результата его экспрессии от дозы соответствующего аллеля этого гена. Примером может служить зависимость степени нарушения транспортных свойств гемоглобина у человека при серповидно-клеточной анемии от дозы аллеля НЬS. Наличие в генотипе человека двойной дозы этого аллеля, приводящего к изменению структуры β-глобиновых цепей гемоглобина, сопровождается грубым нарушением формы эритроцитов и развитием клинически выраженной картины анемии вплоть до гибели. У носителей только одного аллеля НЬS при нормальном втором аллеле лишь незначительно изменяется форма эритроцитов и анемия не развивается, а организм характеризуется практически нормальной жизнеспособностью. 20.Генетически модифицированные продукты. Польза или вред? Генетически модифицированные организмы (ГМО, genetically modified organism, GMO) создаются методами генной инженерии (genetic engineering) - науки, которая позволяет вводить в геном растения, животного или микроорганизма фрагмент ДНК из любого другого организма с целью придания ему определенных свойств. Например, томаты получили ген морозоустойчивости от арктической камбалы, картофель получил ген бактерии, чей яд смертелен для колорадского жука, рис получил ген человека, отвечающий за состав женского молока, который делает злак более питательным. кспериментальное создание генетически модифицированных организмов началось еще в 70-е годы XX века. В 1992 г. в Китае стали выращивать табак, устойчивый к пестицидам. В 1994 г. в США появились генетически модифицированные (ГМ, genetically modified, GM) помидоры, устойчивые к транспортировке. С этого времени производство ГМП набирало обороты и сейчас мы можем встретить ГМ сою, кукурузу, рис, картофель, помидоры, рапс, сахарную свеклу, пшеницу, горох, подсолнечник, папайю, хлопок, табак, коров с повышенной жирностью молока, лосося, который может жить как в соленой, так и в пресной воде и многих других организмов. Сторонники ГМП утверждают, что генная инженерия спасет растущее население земли от голода, ведь генетически модифицированные растения могут существовать на менее плодородных почвах и давать богатый урожай, а затем долго храниться. Для многих вопрос о генной инженерии носит нравственный характер. Научный интерес толкает генетиков на создание таких мутантов, как, например, светящийся в темноте кролик, получивший от медузы ген, отвечающий за флуоресценцию. Многие люди считают подобные эксперименты насилием над природой. 21.Организация геномов РНК- и ДНК- содержащих вирусы. ДНК-содержащие вирусы К ДНК-содержащим вирусам относятся многие вирусы бактерий – бактериофаги (или просто фаги). Некоторые мелкие фаги (например, фаг М13) при репродукции не разрушают клетку. Репродукция крупных фагов (например, фага Т–4) приводит к гибели клетки. Фаг Т–4 – это один из наиболее сложно организованных вирусов. Белковый капсид включает не менее 130 белков, образующих головку, воротничок, сократимый хвост, базальную пластинку и хвостовые нити. Такое строение капсида позволяет впрыскивать ДНК в бактериальную клетку через толстую оболочку, поэтому подобные вирусы образно называют «живыми шприцами». Т–фаги могут существовать в виде профага длительное время. К ДНК-содержащим вирусам относятся возбудители многих заболеваний человека и животных: вирусы оспы, герпеса, гепатита В, аденовирусы млекопитающих и человека (вызывают желудочно-кишечные заболевания, ОРВИ, конъюнктивиты), вирусы бородавок человека. К ДНК-содержащим вирусам относятся и некоторые вирусы растений (вирус золотистой мозаики фасоли, вирус мозаики цветной капусты). Некоторые вирусы используются в генной инженерии для переноса генов от одних организмов к другим. Вирионы ДНК-содержащих вирусов содержат ДНК. Объемом ДНК определяется количество белков в вирионе: один полипептид кодируется отрезком ДНК длиной примерно 1 тысяча нуклеотидов (нуклеотидных пар). После проникновения в клетку вирусная ДНК становится матрицей для синтеза ДНК и РНК. 1. Кольцевая двухцепочечная ДНК длиной около 5 тпн. 2. Кольцевая одноцепочечная ДНК длиной около 5 тн; может быть как кодирующей, так и антикодирующей. 3. Линейная двухцепочечная ДНК длиной 30-150 тпн. 4. Линейная одноцепочечная ДНК длиной около 5 тн; ДНК может быть как кодирующей, так и антикодирующей. У человека известны как спутники аденовирусов. 5. Двухцепочечная ДНК, замкнутая в кольцо из перекрывающихся сегментов. Длина ДНК – 3-8 тн. РНК-содержащие вирусы К РНК-содержащим вирусам относятся многие вирусы растений, возбудители заболеваний человека и животных: вирус полиомиелита, вирусы гриппа А, В и С, вирусы паротита (свинки), кори, чумы плотоядных животных (чумки), бешенства, вирус иммунодефицита человека (ВИЧ). В отдельную группу выделяются арбовирусы, которые переносятся членистоногими (клещами, москитами), например, вирусы клещевого энцефалита, желтой лихорадки. Многие РНК-содержащие вирусы вызывают ОРВИ (например, коронавирусы), желудочно-кишечные заболевания (реовирусы птиц, млекопитающих и человека). Некоторые РНК-содержащие вирусы используются в биотехнологии, например, вирусы полиэдроза насекомых. Вирионы РНК-содержащих вирусов содержат РНК. После проникновения в клетку вирусная РНК становится матрицей для синтеза ДНК и РНК. Примеры организации генома РНК-содержащих вирусов 1. Линейная одноцепочечная мРНК (плюс–цепь) длиной около 4 тн; в виде единой молекулы или в виде нескольких разных молекул. Плюс-цепь сразу же может использоваться для трансляции. Вегетативно-репродуктивная фаза этих вирусов протекает в цитоплазме. В плюс-цепи закодирована РНК-репликаза (РНК-зависимая РНК-полимераза). Представители: 2. Линейная одноцепочечная кРНК (минус–цепь, порядок нуклеотидов комплементарен по отношению к мРНК). Минус–цепь не может служить для трансляции и используется как матрица для синтеза плюс–цепи. Плюс-цепь служит для трансляции вирусных белков и используется как матрица для синтеза вирусной кРНК. Вегетативно-репродуктивная фаза этих вирусов также протекает в цитоплазме. 3. Линейная двухцепочечная РНК 4. Две линейные одноцепочечные одинаковые молекулы мРНК длиной около 10 тн. Ретровирусы. Способны интегрироваться в ДНК. В состав вирионов входит фермент обратная транскриптаза (ревертаза). Имеется дополнительная липопротеиновая оболочка. Многие ретровирусы вызывают онкологические заболевания: лейкозы, саркомы, опухоли молочных желез. К ретровирусам относится и вирус иммунодефицита человека, вызывающий СПИД. 22.Признаки клеток, трансформированных опухолеродными вирусами. пухолеродные вирусы, опухолевые, онкогенные вирусы, возбудители некоторых доброкачественных и злокачественных опухолей животных и, по-видимому, человека. Успешные эксперименты по воспроизведению у животных опухолей с помощью фильтрующихся агентов (вирусов) были осуществлены ещё в начале 20 в., однако в самостоятельное научное направление онковирусология (учение об Опухолеродные вирусы) оформилась в 50-60-х гг. Прогресс в изучении природы Опухолеродные вирусы и механизма их опухолеобразующего действия тесно связан с возникновением и развитием молекулярной биологии. Опухолеродные вирусы - разнородная группа вирусов,различающихся по ряду существенных признаков: по типу нуклеиновой кислоты(РНК-содержащие Опухолеродные вирусы, или онкорнавирусы, и ДНК-содержащие Опухолеродные вирусы); по морфологии вирионов (их форме, размерам, типу симметрии, наличию или отсутствию внешней оболочки); по месту размножения вируса в клетке хозяина (в цитоплазме или в ядре); по способу передачи вируса (от родителей к детям и от клетки к дочерней клетке - «вертикальная» передача, от особи к соседней особи и от клетки к соседней клетке - «горизонтальная» передача); по опухо-леобразующей активности (слабо- и сильноонкогенные Опухолеродные вирусы). Некоторые ДНК-содержащие вирусы в разных клеточных системах могут вести себя по-разному, инициируя в одних случаях неконтролируемое размножение клеток (опухолевый рост), в других - инфекционный процесс, проявляющийся обычно в разрушении клеток. Правомерно поэтому (применительно к ДНК-содержащим вирусам) «говорить не об опухолевых и инфекционных вирусах, а о неопластическом и инфекционном действии вирусов» (Л. А. Зильбер). Деление РНК-содержащих вирусов на опухолеродные и инфекционные более оправдано: РНК-вирусы обладают, как правило, либо опухолеобразующим, либо инфекционным действием. Кроме того, онкорнавирусы отличаются от большинства инфекционных РНК-содержащих вирусов по способу воспроизведения нуклеиновой кислоты: у первых она воспроизводится по схеме РНК ® ДНК ® РНК, у вторых - по схеме РНК (+) ® -РНК (–) ® РНК (+). Способность онкорнавирусов синтезировать на своей РНК-матрице вирусспецифический ДНК (т. н. обратная транскрипция) и существовать таким образом в 2 формах - в форме полного вируса (РНК + белок) и в форме ДНК-«провируса» - доказана в 1970 американскими исследователями Х. Темином, С. Мицутани и независимо от них Д. Балтимором. Открытие у РНК-содержащих Опухолеродные вирусы ДНК-формы существенно укрепило вирусогенетическую теорию Зильбера, согласно которой в основе опухолевого превращения клетки лежит объединение её генома с геномом Опухолеродные вирусы Во 2-й половине 60-х гг. экспериментально установлено наличие в хромосомах «безвирусных» (не продуцирующих вирус) опухолевых клеток, трансформированных ДНК-содержащими Опухолеродные вирусы, геномов этих Опухолеродные вирусы, а также функционирование этих геномов (проявляющееся в синтезе вирусспецифических информационных РНК). К концу 60-х гг. выяснилось, что генетическая информация онкорнавирусов (по-видимому, в ДНК-форме) имеется не только в опухолевых, но и во всех изученных в этом отношении нормальных клетках позвоночных. Основываясь на этих данных, Р. Хюбнер и Дж. Тодаро (США) выдвинули гипотезу, согласно которой различные способствующие возникновению опухоли агенты (химические канцерогенные вещества, радиация, нормальный процесс старения, экзогенные вирусы) действуют по единому механизму, - активируя эндогенную онкогенную информацию, которая в подавленном («зарепрессированном») состоянии имеется в любой клетке. Действительно, под влиянием указанных агентов, а иногда и самопроизвольно (при длительном культивировании) многие клетки начинают выделять частицы, которые по морфологическим, физико-химическим и др. признакам сходны с онкорнавирусами. Однако эти частицы, в отличие от онкорнавирусов, выделенных из опухолевых клеток, почти или полностью не онкогенны. По мнению Темина, нормальные клетки не содержат онкогенной информации: онкогенные свойства приобретают на случайной основе «ошибочные» молекулы РНК или ДНК, транскрибируемые с первоначально неонкогенных ДНК-оригиналов («протовирусов»); при включении таких «ошибочных» ДНК-копий в геном исходной или соседней клетки и происходит, по мысли Темина, опухолевая трансформация. В 60-70-х гг. вирусные частицы, сходные с возбудителями опухолей и лейкозов у птиц и мышей, удалось обнаружить и в новообразованиях человека, а также в перевиваемых культурах человеческих тканей (опухолевых и нормальных). Исследуется возможное значение этих вирусов как специфических возбудителей опухолей и лейкозов у человека. 23.Механизмы онкогенеза.Наше тело состоит из бесчисленного числа различных клеток. Клетки очень различаются по строению и функции: клетки кожи, нервов, сердца, легких, крови, иммунной системы совершенно различны. Однако, вне зависимости от «профессии», все клетки умеют делится и созревать из своих более ранних предшественников (иначе как они могли возникнуть?). Кроме того, все клетки умеют погибать вовремя. Их гибель не случайна и тщательно контролируется: организм точно регулирует численность клеток в тканях. Запрограммированная гибель клеток называется апоптоз. Эти три свойства - деление, созревание и апоптоз совершенно необходимы для жизни клеток в большом многоклеточном организме. Вместе с тем, нарушения этих трех основ жизнедеятельности клетки приводят к развитию опухолей. Накопление опухолевых клеток происходит из за того, что они бесконтрольно делятся, либо из за того, что они не могут созреть и превратиться в своих высоко-профессиональных потомков («заморожены» на стадии развития), либо из за того, что они не могут умереть вовремя. Кроме того, опухоль всегда клональна. Это означает, что все клетки опухоли произошли из одной и представляют собой точные копии (клоны) исходной клетки. Строго говоря, все клетки организма клональны - ведь они возникли из зиготы, образовавшейся после слияния сперматозоида и яйцеклетки. Но во время роста и созревания организма клетки сильно специализируются и становятся совсем не похожи одна на другую. Так, «профессия» лимфоцитов - защищать нас от инфекций. Лимфоциты отличаются друг от друга тем, что отвечают на разных возбудителей, а также своей ролью в иммунной системе. Поскольку деление, созревание и запрограммированная смерть свойственны всем клеткам, опухоль может развиться практически из любого типа клеток, в том числе из лимфоцитов. Нарушения деления, созревания и запрограммированной гибели возникают из-за повреждений генов. Клетки имеют множество встроенных систем защиты против этих внутренних генетических ошибок, но эти защитные системы могут ошибаться, поврежденная клетка выживает и образует множество себе подобных (клонов). Повреждения некоторых генов могут наследоваться, предрасполагая к опухоли. 24.Онкогенные вирусы. Жизненный цикл ретровирусов. Особый интерес среди вирусных болезней вызывает СПИД (синдром приобретенного иммунодефицита человека), поскольку это относительно новая болезнь. Впервые сообщение о ней появилось в США в 1981 г. СПИД вызывается вирусом иммунодефицита человека, или сокращенно ВИЧ. Интерес к этому вирусу объясняется еще и тем обстоятельством, что ВИЧ относится к группе вирусов, получивших название ретровирусов — название, отражающее следующую особенность этого вируса. Обычно перенос генетической информации идет в направлении ДНК—> РНК, т. е. информация, закодированная в определенном отрезке ДНК (гене) транскрибируется, т. е. считывается, с образованием соответствующей РНК. У ретровирусов же, у которых наследуемым генетическим материалом служит РНК, происходит обратная транскрипция, т. е. генетическая информация считывается в обратном направлении: от РНК к ДНК. Фермент, участвующий в обратной транскрипции, называется обратной транскриптазой. Он широко используется в генетической инженерии. ВИЧ инфицирует и разрушает лейкоциты определенной группы, называемые Т-хелперными лимфоцитами, подавляя в результате активность иммунной системы.  25.Роль вирусов в неопластической трансформации клеток. Знаю 26.Морфофизиологические особенности опухолевых клеток. Внешний вид опухоли разнообразен. Она может иметь форму узла, шляпки гриба или напоминать цветную капусту. Поверхность ее бывает гладкой, бугристой или сосочковой. Опухоль может быть расположена в толще органа или на его поверхности. В одних случаях она диффузно пронизывает орган и тогда границы ее не определяются, в других - расположена на поверхности органа (слизистой оболочки) в виде полипа. В компактных органах опухоль может выступать над поверхностью, прорастать и разрушать капсулу, аррозировать (разъедать) сосуды, вследствие чего возникает внутренее кровотечение. Она часто подвергается некрозу и изъязвляется (раковая язва). На разрезе опухоль имеет вид однородной, обычно бело-серой или серо-розовой ткани, напоминая иногда рыбье мясо. Иногда ткань опухоли пестрая в связи с наличием в ней кровоизлияний, очагов некроза; опухоль может быть и волокнистого строения. В некоторых органах (например, в яичниках) опухоль имеет кистозное строение. Размеры опухоли различные, что зависит от скорости и продолжительности ее роста, происхождения и расположения; консистенция зависит от преобладания в опухоли паренхимы или стромы: в первом случае она мягкая, во втором - плотная. Вторичные изменения в опухолях представлены очагами некроза и кровоизлияний, воспалением, ослизнением и отложением извести (петрификация) . Иногда эти изменения происходят в связи с применением лучевой терапии и химиотерапии. Микроскопическое строение опухоли отличается большим разнообразием. Однако все опухоли имеют некоторые общие черты строения: опухоль состоит из паренхимы и стромы, соотношения которых могут сильно варьировать. Паренхиму опухоли образуют клетки, которые характеризуют данный вид опухоли, ими определяется морфологическая ее специфика. Строма опухоли образована как соединительной тканью органа, в котором она развилась, так и клетками самой опухоли. Между паренхимой и стромой опухоли существуют сложные связи, причем особенности паренхимы опухоли во многом определяют характер ее стромы. Опухолевые клетки по мере роста индуцируют пролиферацию фибробластов, синтез ими компонентов стромы. Эта способность опухолевых клеток в значительной мере определяется их генетическими свойствами, она неодинаково выражена в опухолях разного гистологического строения, что объясняет различное количество волокнистых структур в строме разных опухолей. Клетки паренхимы опухоли не только индуцируют активность фибробластов, но и сами могут вырабатывать межклеточное вещество стромы, или экстрацеллюлярный матрикс (например, коллаген IV типа базальных мембран). Опухолевые клетки, кроме того, продуцируют специфическое вещество белковой природы - ангиогенин, под воздействием которого происходит формирование капилляров в строме опухоли. Большинство опухолей по строению напоминают орган, т. е. имеют паренхиму и выраженную в той или иной степени строму. Такие опухоли называют органоидными. В некоторых, особенно недифференцированных, опухолях преобладает паренхима, строма развита слабо и состоит лишь из тонкостенных сосудов и капилляров. Такие опухоли называют гистиоидными. Они обычно быстро растут и рано подвергаются некрозу. В ряде случаев в опухоли преобладает строма, клеток паренхимы крайне мало. Примером может служить фиброзный рак, или скирр. Опухоли, строение которых соответствует строению органа (ткани), в котором они развиваются, называют гомологичными. Когда клеточное строение опухолей отличается от строения органа (ткани), в котором они возникают, говорят о гетерологичных опухолях. Гомологичные опухоли - зрелые, дифференцированные, гетерологичные - незрелые, мало- или недифференцированные. Опухоли, возникающие в результате гетеротопий, т. е, эмбриональных смещений, называют гетеротопическими (например, опухоль из костной ткани в стенке матки или легком). Морфологический атипизм опухоли может быть тканевым и клеточным. Тканевый атипизм характеризуется нарушением тканевых взаимоотношений, свойственных данному органу. Речь идет о нарушении формы и величины эпителиальных структур, соотношений паренхимы и стромы в эпителиальных (особенно железистых) опухолях; о различной толщине волокнистых (соединительнотканных, гладкомышечных и др.) структур, о хаотичном их расположении в опухолях мезенхимального происхождения. Тканевый атипизм наиболее характерен для зрелых, доброкачественных опухолей. Клеточный атипизм на светооптическом уровне выражается в полиморфизме или, напротив, мономорфизме клеток, ядер и ядрышек, гиперхромии ядер, полиплоидии, изменениях ядерно-цитоплазматического индекса в пользу ядер в связи с их укрупнением, появлении множества митозов. Клеточный атипизм может быть выражен в разной степени. Иногда он так значителен, что опухолевые клетки по внешнему виду становятся непохожими на клетки исходной ткани или органа. Когда морфологическая ка- таплазия достигает крайней степени, строение опухоли упрощается и она становится мономорфной. В связи с этим анапластические опухоли различных органов очень похожи друг на друга. Важным проявлением морфологического атипизма опухолевой клетки является патология митоза. Установлено, что в клетках опухоли нарушена продукция кейлонов, которые в нормальных условиях регулируют митотическую активность клеток и действуют как ингибиторы клеточного деления. Патология митоза в опухолевых клетках подтверждает воздействие онкогенных факторов на генетический аппарат клетки, что и определяет нерегулируемый рост опухоли. Клеточный атипизм характерен для незрелых, злокачественных опухолей. Биохимический атипизм опухолевой ткани выражается рядом особенностей обмена, отличающих их от нормальных. Выяснено, что спектр биохимических характеристик каждой из опухолей неповторим и включает разные комбинации отклонений от нормы. Такая вариабельность злокачественной опухоли является закономерной. Ткань опухоли богата холестерином, гликогеном и нуклеиновыми кислотами. В опухолевой ткани гликолитические процессы преобладают над окислительными, содержится мало аэробных ферментных систем, т. е. цитохромоксиды, каталазы. Выраженный гликолиз сопровождается накоплением в тканях молочной кислоты. Это своеобразие обмена опухоли усиливает ее сходство с эмбриональной тканью, в которой также преобладают явления анаэробного гликолиза.Вопросы биохимической анаплазии опухоли более подробно освещаются в курсе патологической физиологии. Гистохимический атипизм отражает в известной мере биохимические особенности опухоли. Он характеризуется изменениями обмена в опухолевой клетке белков и, в частности, их функциональных групп (сульфгидрильных и дисульфидных), накоплением нуклеопротеидов, гликогена, липидов, гликозаминогликанов и изменениями окислительно-восстановительных процессов. В клетках разных опухолей определяется неоднородная картина гистохимических изменений, и каждая опухоль в гистохимическом отношении, так же как и в биохимическом, неповторима. Для ряда опухолей выявлены специфические ферменты (ферменты-маркеры), определен «ферментный профиль», характерный для данного вида опухоли. Так, в клетках рака предстательной железы обнаружена высокая активность кислой фосфатазы, эстеразы и неспецифической А,-экзонуклеазы - ферментов, свойственных эпителию этого органа в норме. В гепатоцеллюлярном раке в отличие от холангиоцеллюлярного выявляется аминопептидаза; в опухолях из экзокринной части поджелудочной железы в отличие от опухолей из ее островков сохраняется высокая активность эстеразы. Количественное гистохимическое исследование показало, что однозначные в гистологическом отношении и по степени дифференцировки формы рака легкого, желудка и молочной железы отличаются друг от друга активностью ряда ферментов (оксидоредуктаз). 27.Использование новых технологий в создании генетической рекомбинации организмов (генотерапия, клеточная терапия). рекомбинантная структура (англ. Recombinant structure) — гибридная (англ. recombination — рекомбинация) нуклеиновая кислота (ДНК или РНК) или белок, полученные в результате объединения in vitro чужеродных фрагментов и содержащие новые сочетания последовательностей нуклеотидов или аминокислот соответственно. |
