Краткий справочник гальванотехника - 1993 - Ильин. Справочник гальванотехника санктПетербург " политехника"
 Скачать 3.02 Mb. Скачать 3.02 Mb.
|
Глава 14БЕСТОКОВЫЕ (ХИМИЧЕСКИЕ) МЕТАЛЛИЧЕСКИЕ ПОКРЫТИЯ39. Химическое никелированиеХимическое (бестоковое) никелирование широко распространено во всех отраслях промышленности благодаря высокой равномерности покрытия, его большой твердости и износоустойчивости. Покрытия характеризуются также значительной коррозионной стойкостью в различных средах, что обусловливается их меньшей пористостью по сравнению с покрытиями из электролитического никеля. Наличие в составе покрытия от 3 до 10% фосфора придает ему повышенную устойчивость в атмосфере перегретого пара, горячих щелочных растворов. Химическое никелирование нашло большое применение для металлизации диэлектриков — пластмасс, керамики, ферритов и других материалов. В табл. 170 представлены данные о толщине слоя покрытия в зависимости от условий эксплуатации. Одной из важнейших характеристик никель-фосфорного покрытия является его высокая твердость, которая в 1,5—2 раза Таблица 170. Толщина слоя химического никеля в зависимости от условий эксплуатации
превосходит твердость электролитического никеля. Свежеосажденное покрытие имеет твердость 4500—5000 МПа. Нагрев покрытия приводит к повышению твердости, что связано со структурными изменениями в осадках. Максимальная твердость никель-фосфорного покрытия достигается при нагреве до температуры 400 °С и составляет более 10000 МПа. На рис. 17 представлена зависимость твердости покрытия от условий термообработки. Образование покрытия происходит в результате восстановления никеля из его солей фосфорноватистокислым натрием (гипофосфитом натрия) в кислой или щелочной среде. Процесс химического никелирования протекает очень сложным путем и восстановление никеля описывается следующей суммарной реакцией: NiCl2 + 2NaH2PO2 + 2H2O 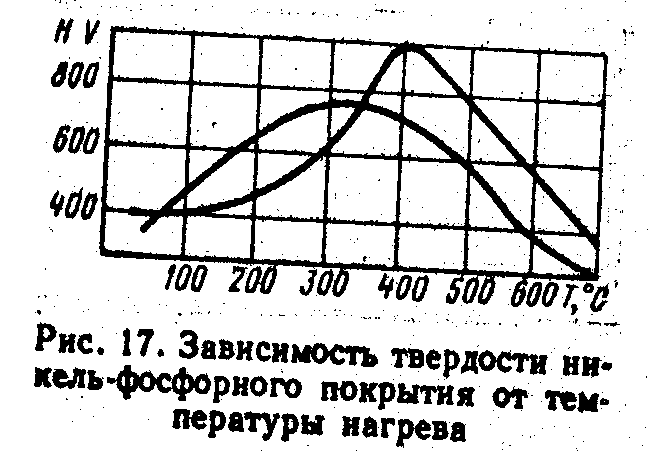 Одновременно с восстановлением никеля протекает реакция восстановления фосфорноватистокислого натрия (гипофосфита натрия) до элементарного фосфора, который включается в состав покрытия: Н2РО2– + e Из этой реакции следует подтверждённое практикой влияние рН раствора на содержание фосфора в покрытии: чем ниже величина рН, тем больше фосфора в покрытии. Эта зависимость для кислых растворов выражаетсяследующим образом: рН … . . . . . . . .. 5,8 5,0 4,5 3,0 Р, массовая доля, % . . . 2,2 3,5 11,4 14,1 В процессе осаждения никеля в растворах накапливаются фосфиты, изменяется кислотность среды и происходят другие изменения, влияющие на скорость осаждения покрытия. Введение в состав растворов комплексообразующих, буферных и стабилизирующих добавок улучшает характеристики кислых растворов. К таким добавкам относятся многие Органические кислоты: лимонная, яблочная, янтарная. Хорошим стабилизатором раствора служат серосодержащие соединения: тиомочевина, сульфид свинца. В табл. 171 и 172 приведены составы наиболее употребительных растворов химического никелирования и режимы процесса, к которым относятся такие параметры, как температура раствора, скорость осаждения покрытия. Скорость осаждения никеля, приведенная в табл. 17!, дана как средняя величина применительно к свежим растворам; она Таблица 171. Состав кислых растворов для химического никелирования и режим осаждения покрытий
Таблица 172. Состав щелочных растворов для химического никелирования и режим осаждения покрытий
зависит от многих факторов и, в первую очередь, от температуры раствора, величины рН, которая в процессе восстановления никеля непрерывно снижается, а также от концентрации соли никеля и накопления продуктов реакции (фосфита никеля). Указанные факторы затрудняют определение продолжительности процесса для достижения заданной толщины никеля, поэтому в производственных условиях рекомендуется использова-ние «свидетелей» в виде металлических полосок, загруженных одновременно с деталями, толщину покрытия на которых определяют весовым способом, принимая плотность никеля 8,2 г/см3. Эта величина является средней: при малом содержании фосфора она равна 8,52 г/см3, а при высоком его содержании — 7,85 г/см3, Корректирование растворов химического никелирования обычно осуществляют добавлением концентрированных растворов солей никеля (130—150 г/л) и гипофосфита натрия (25—50 г/л). Кислотность раствора корректируется добавлением едкого натра до значения рН, рекомендованного составом. При рН < 3 покрытие становится шероховатым и скорость его осаждения резко падает. При рН > 5,5 покрытие становится хрупким и растрескивается. Никелевое покрытие легко осаждается на такие металлы, как железо, кобальт, алюминий,- никель. Для покрытия деталей из медных сплавов необходимо прикоснуться к ним алюминиевой проволокой в момент загрузки деталей в раствор и после начала осаждения никеля контакт прекратить, а на такие металлы, как олово, свинец, кадмий, цинк, висмут, сурьма покрытие не осаждается. В щелочных растворах по сравнению с кислыми скорость осаждения покрытия несколько ниже, а пористость покрытия выше и, соответственно, коррозионная устойчивость покрытий из щелочных растворов ниже. Вместе с тем щелочные растворы характеризуются большей стабильностью, обусловленной присутствием в растворах более сильных лигандов и более высокой растворимостью продукта реакции (фосфита) в щелочной среде. Содержание фосфора в осадках никеля составляет 5—7%. Представленные в табл. 172 варианты растворов равноценны по скорости осаждения никеля, за исключением раствора № 1. Скорость осаждения никеля в щелочных растворах резко падает по мере снижения температуры раствора и величины рН. Так, при снижении температуры раствора от 95 до 90 °С скорость осаждения снижается на 20—25%, а при снижении рН от 8,0 до 5,0 скорость осаждения снижается на 15—20%. Химическое никелирование стальных деталей и деталей из меди и ее сплавов производится в любом из приведенных выше растворов. Дли покрытия сложнопрофилированных алюминиевых деталей, в том числе и деталей, полученных методом литья из литейных сплавов алюминия, хорошие результаты получаются при непосредственном никелировании деталей в растворе состава, г/л: никель сернокислый (кристаллогидрат)—20—25; натрий фосфорноватистокислый — 15—18; натрий уксуснокислый — 10—12; натрий фтористый — 0,8—1,0; тиомочевина — 0,002—0,003. Величина рН 4,1—4,3 устанавливается введением уксусной кислоты (6—6,5 г/л). Температура раствора 85—90 °С. Фторид натрия выполняет функции активатора поверхности, растворяя тонкие оксидные пленки на поверхности алюминия, поэтому такие подготовительные операции, как контактное цинкование или никелирование, не производятся. При всех вариантах химического никелирования следует иметь в виду, что малые плотности загрузки не выгодны из-за увеличения потерь гипофосфита вследствие термического разложения по отношению к количеству осажденного никеля. Удаление недоброкачественных покрытий производят в растворе следующего состава: Кислота серная (плотность 1,84), части по объему. ... 1 азотная (плотность 1,4), части по объему. ... 2 Железо сернокислое (окисное), г/л 5—10 Температура раствора, "С 18—25 Для снятия недоброкачественных покрытий можно применять также раствор, состоящий из 7 частей по объему азотной кислоты плотностью 1,4 и 3 частей по объему уксусной кислоты (98%-ной). Покрытие никель—бор. В последние годы все большее применение получает химическое никелирование в растворах, содержащих в качестве восстановителя соединения бора и главным образом борогидрида натрия NaBH4. Суммарное уравнение реакции восстановления никеля имеет следующий вид: ВН4 + 4Н2О + 2Ni2+ Большим преимуществом борогидрида натрия является его высокая восстановительная емкость, выражающаяся в том, что на 1 г выделяемого никеля требуется 0,3 г борогидрида натрия, тогда как для гипофосфата натрия эта величина в 10 раз больше, т. е. 3 г. Небольшое количество бора в составе покрытия значительно увеличивает его твердость и износоустойчивость, в то же время электрические свойства покрытия по сравнению с покрытием никель—фосфор улучшены. Составы растворов для осаждения покрытия никель—бор представлены в табл. 173. Существенной особенностью растворов является большое содержание щелочи во избежание гидролиза борогидрида. По этой причине осаждение никеля можно вести только на материалы, устойчивые к сильно щелочной среде и высокой температуре. Стабилизаторы значительно повышают стабильность раствора и позволяют увеличить скорость осаждения. Стабилизирующей добавкой в растворе № 1 служит ацетат таллия или смесь меркаптофталиевой кислоты (0,5 г/л) и ацетата свинца (0,04 г/л). Приготовление борогидридных электролитов осуществляется в следующем порядке: сначала в водный раствор Таблица 173. Состав борогидридных растворов химического никелирования и режимы осаждения покрытия
соли никеля добавляют этилендиамин, или триэтилентриамин, или калий — натрий виннокислый и раствор подогревают; затем добавляют борогидрид натрия, предварительно растворенный в небольшом количестве концентрированного раствора щелочи и вводят стабилизатор. Полученный раствор тщательно перемешивают и вводят в рабочую ванну, где подогревают до заданной температуры. Проведение процесса химического никелирования встречает определенные трудности при выборе материала ванны, который должен быть химически стойким к растворам с кислотностью в пределах рН 3—11 и выдерживать температуру до 100 °С. Металлические ванны не могут быть использованы из-за осаждения никеля на стенки. Применение свинца для футеровки недопустимо, так как ионы свинца отрицательно влияют на процесс. Наиболее приемлемыми материалами являются фарфор, эмали, стекло, полиэтилен. При небольшом количестве деталей и их малых размерах используют эмалированные бочки или полиэтиленовые ведра, устанавливаемые в водяные бани для подогрева раствора. Применяют также специализированные установки типа УХН-901 (установка химического никелирования), поставляемые разработчиками подобных установок на договорных началах. При отсутствии подобных установок можно производить химическое никелирование в ваннах, сваренных из листовой коррозионно-стойкой стали Х18Н9Т с анодной защитой корпуса ванны от осаждения на нее никеля. На рис. 18 показана схема анодной защиты корпуса ванны. Корпус ванны подключается к положительному полюсу источника постоянного тока (аккумулятору или выпрямителю), который подбирается в зависимости от размеров ванны, определяющей потребную силу тока. Катодами служат стальные проволочки диаметром 0,5—1,0 мм, помещенные в перфорированные полиэтиленовые трубки, заглушенные в нижней части полиэтиленовыми пробками. Нижняя часть трубки, как показано на рис. 18, перфорации не имеет. Подобное устройство необходимо для того, чтобы осыпающиеся с проволочек крупинки никеля не падали на дно ванны, а задерживались внутри трубки. 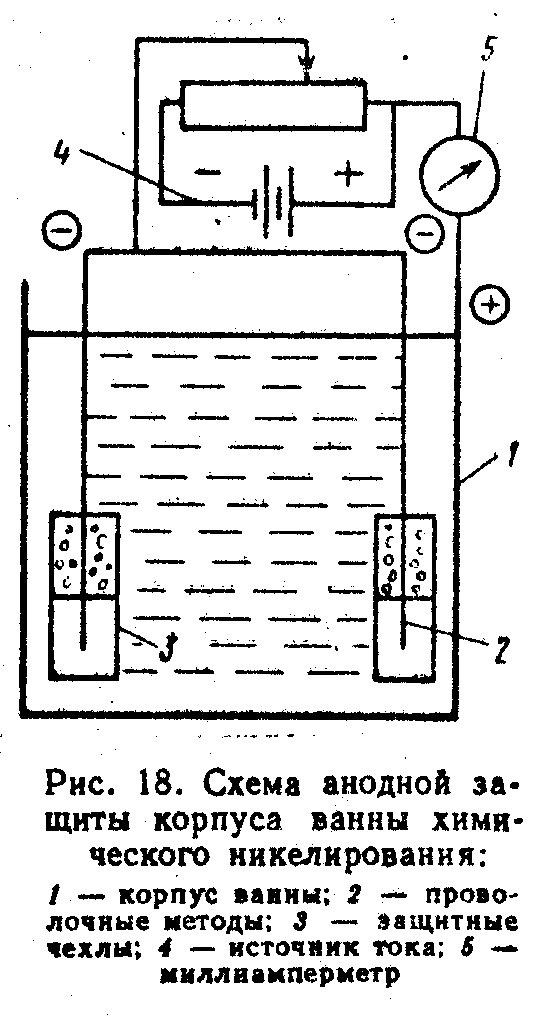 Перед тем, как заливать ванну рабочим раствором, производится пассивирование металла путем заливки ванны раствором азотной кислоты концентрацией 700— 900 г/л. Раствор выдерживается при подогреве до 30—40 °С в течение 3 ч. Затем раствор сливается в запасную емкость (бутыль) для последующего использования. Стенки ванны промываются и ванна заполняется холодным рабочим раствором. По четырем углам ванны закрепляются полиэтиленовые трубки со встав ленными проволочками, которые соединяются между собой, образуя катодную поверхность. Через систему пропускается ток, анодная плотность которого составляет 0,001—0,004 А/дм2 (1—4 мА/дм2). Площадь поверхности катода (проволочная) должна быть меньше анодной в 300— 350 раз. Анодный потенциал корпуса ванны поддерживает пассивное состояние хромо-никелевой стали и никель на стенках ванны не осаждается. При случайном соприкосновении покрываемых деталей со стенками ванны, или попадании частиц никеля на дно ванны может начаться осаждение никеля на корпус ванны. В этом случае раствор сливается, а ванна обрабатывается раствором HNO3 для удаления осевшего металла и для повторной пассивации. 40. Бестоковое (химическое) осаждение олова, серебра, золота, палладияХимическое оловянирование. Химическое или оловянирование без внешнего тока осуществляется за счет ионного обмена, когда потенциал покрываемого металла имеет более отрицательное значение по сравнению с потенциалом олова. При оловяиировании меди и ее сплавов это достигается путем введения в раствор хлористого олова карбамида или цианидов, комплексующих ионы меди. Таблица 174. Состав растворов и режимы химического оловянирования
Возможен и другой механизм осаждения олова, когда покрываемый металл контактируется в растворе с электроотрицательным металлом (цинк), и в результате образовавшейся гальванопары ионы олова из раствора восстанавливаются на катодной поверхности покрываемых деталей. Алюминий и его сплавы, обладающие более отрицательным потенциалом, чем олово, во всех случаях покрываются без дополнительного контакта. Химическое оловянирование деталей применяют для обеспечения пайки или защиты от окисления при межоперационном хранении. В табл. 174 приведены составы растворов и режимы оловянирования деталей. Растворы № 1, 2 и б применяются для оловянирования методом погружения; растворы № 3 и 4 рекомендуются для покрытия оловом стальных деталей и деталей из медных сплавов с применением контакта из цинка. Практически это осуществляется загрузкой деталей в раствор на оцинкованных сетках. Раствор № 5 предназначен для покрытия алюминиевых сплавов. Толщина осаждаемого покрытия в растворах № 1, 2, б до 1 мкм. В растворе № 6 можно создать сплав олова со свинцом типа ПОС-18 (содержание олова от 16 до 25%) в растворе состава, г/л: хлорид олова — 16—20; хлорид свинца — 10—13; тиомочевина — 60; хлористый натрий — 40. Температура раствора 70°, продолжительность 45 мин. В производстве печатных плат в ряде случаев применяют химическое оловянирование медных проводников с целью облегчения пайки радиокомпонентов на плату. Оловянное покрытие толщиной до 3 мкм, легированное кадмием, получают погружением печатных плат на 20—30 мин в раствор следующего состава, г/л: Хлористое олово 8 Хлористый кадмий 6 Тиомочевина 45 Кислота серная 40 Температура раствора 18—25 °С. Растворы химического оловянирования, как правило, не корректируются и после каждой загрузки заменяются на свежие. Химическое серебрение. Химическое восстановление серебра из его аммиачного комплекса Ag(NH3)+ сахаром применяется для металлизации диэлектриков (стекла, полимерных материалов) с целью придания хорошей электропроводности в тонком слое металла. Технология осаждения серебра этим способом описана в гл. 10 справочника. Для серебрения металлических деталей пользуются другим способом: покрываемые детали контактируют с алюминием или магнием вне раствора, а в растворе этот же контакт осуществляют через чехол из капрона. В результате работы короткозамкнутого элемента серебро из раствора восстанавливается на поверхности катода, т. е. на деталях. Этот метод называют методом внутреннего электролиза. Состав растворов представлен в табл. 175. Раствор № 1 применяют для получения очень тонких (менее 0,1 мкм) серебряных покрытий; раствор № 2 — для покрытий толщиной до 15—20 мкм со скоростью осаждения 5 мкм/ч, осуществляя метод внутреннего электролиза. Бестоковое (химическое) золочение. Химическое золочение осуществляется в одном из растворов, представленных в табл. 176. Таблица 175. Состав растворов и режим химического серебрения деталей
Таблица 176. Состав растворов для химического золочения и режимы работы
Раствор № 1 применяют для осаждения покрытий толщиной около 0,1 мкм (время выдержки 3 мин) на детали с никелевым покрытием. Растворы № 2 и 3 предназначены для деталей из меди и медных сплавов. В качестве восстановителей в растворе № 1 принят гипофосфит натрия, а в растворе № 2 — борогидрид натрия. Покрытия золотом получаются плотные и блестящие. Бестоковое палладирование. Бестоковое палладирование можно осуществить в растворе состава: хлорид палладия — 2 г/л; кислота соляная (38%-ная) — 4 мл/л; аммиак (25%-ный) — 160 мл/л; хлорид аммония — 27 г/л; гипофосфит натрия — 10 г/л. Величина рН 9,6—10,0. Температура раствора 30—70 °С. Скорость осаждения палладия при температуре 70 °С составляет 10 мкм/ч, при температуре 30 °С — 3—4 мкм/ч. Глава 15БЕЗОТХОДНАЯ ТЕХНОЛОГИЯВ ГАЛЬВАНИЧЕСКОМ ПРОИЗВОДСТВЕ41. Малоотходная технология. Утилизация отходовНа предприятиях приборостроения и машиностроения наиболее экологически опасными являются гальванохимические производства. В гальванохимических процессах используются многочисленные химические материалы, значительное количество которых переходит в твердые, жидкие и газообразные отходы, часто содер- Таблица 177. Расход металлов на покрытие 1 м2 площади поверхности детали
жащие токсичные вещества и вещества, имеющие большую ценность для народного хозяйства. Наибольшую опасность для окружающей среды представляю сточные воды, с которыми в системы очистных сооружений выносятся соли различных металлов, создающие повышенную концентрацию катионов тяжелых металлов в водоемах, так как системы водоочистки не всегда обеспечивают необходимую степень очистки стоков. Унос металлов в сточные воды иллюстрируется данными представленными в табл. 177 и 178. Таблица 178. Предельно допустимые концентрации (ПДК) вредных веществ в воде, водных объектах хозяйственно-питьевого и культурно-бытового водопользования
Таблица 179. Допустимые концентрации загрязнений (мг/л) в промышленных сточных водах перед сбросом в городскую канализацию по бассейну стока Северных городских очистных сооружений (пусковой комплекс)
С целью охраны окружающей среды количество содержащихся в стоках различных материалов, в том числе катионов тяжелых металлов, нормируется величиной ПДК (предельно-допустимых концентраций) и величиной ПДС (предельно-допустимых сбросов), которые устанавливаются органами санитарного надзора с учетом специфики района, где находится предприятие. Предельно-допустимые сбросы (ПДС) устанавливаются для каждого предприятия органами санитарной инженерии (водокана лом) с учетом местных условий, мощности общегородских очистных сооружений, объемов городских сточньтх вод. Предельно-допусти мые сбросы могут отличаться от ПдК как в сторону ужесточения, так и в сторону увеличения допустимых концентраций. В неко торых городах, например в Петербурге, установлены более уже сточенные ПДС по сравнению с ПДК (табл. 179) Утилизация отходов. Наиболее распространенная система обезвреживания сточных вод гальванических цехов предусматри вает перевод особо токсичных материалов, таких, как цианиды и соединения шестивалентного хрома, в нетоксичные соединения реагентным методом. Затем в отдельных резервуарах соединяются кислотные и щелочные стоки с продуктами обезвреживания, образуя нерастворимые гидроокиси металлов. Гидроокиси метал лов в виде шламов увозятся для захоронения. Чаще всего случай- ные места захоронения служат источником загрязнения почвы, водоемов, болот и других объектов окружающей среды. Более совершенные ионообменный метод и метод электрокоогуляции обеспечивают высокую степень очистки воды, однако и эти методы также влекут за собой значительные потери металлов в виде шламов. С целью охраны природы от катионов тяжелых металлов, содержащихся в шламах, предложены различные способы их утилизации, в том числе: передача шламов предприятиям, выпу скающим керамические изделия (например, предприятия Литвы передают шламы Каунасскому заводу, производящему черепицу для кровли домов; отходы шламов вносятся в глинистую массу); передача шламов, содержащих большое количество гидроокиси железа лакокрасочным заводам в качестве пигмента (такую прак тику приняли предприятия, применяющие электрокоагуляцион ный метод очистки); сдача медьсодержащих отходов от травильных операций в производстве печатных Ь Ь плат после соответствующей обработ ки медеплавильным заводам. Перечисленные выше способы, как и другие, не решают главной задачи по ресурсосбережению возврату в производство используемых в гальва нотехнике материалов или же по ре- кому сокращению их потерь. 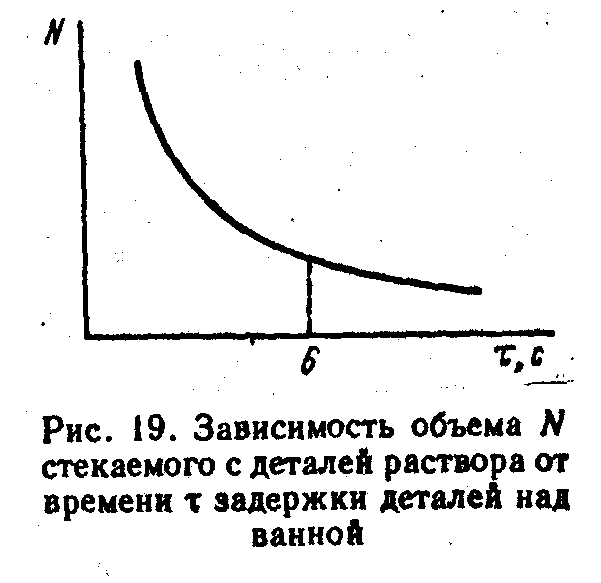 Малоотходная технология. На первом этапе внедрения безотходных технологий, когда предприятие еще не имеет необходимых технических средств, можно простыми способами сократить отходы гальванического цеха (участка). Основным условием создания малоотходного производства является сокращение водопотребления посредством установок промывочных ванн каскадного типа, струйных промывок и других способов. Сокращение объектов стоков позволит производить более качественную их обработку в системах очистных сооружений. Уменьшить сброс растворов, содержащих различные химические материалы, можно нижеперечисленными способами. Задержка выгружаемых из ванн деталей над зеркалом электролита для более полного стекания растворов с деталей в ванну. На рис. 19 представлен график, характеризующий зависимость объема стекаемого раствора от времени выдержки деталей над ванной. При выдержке 5—6 с стекает до 80—85% раствора, увлекаемого деталями. Для реализации этого мероприятия необходимо в автоматических линиях гальванообработки внести в программу движения автооператоров задержку деталей над ванной на 5—б с. На ваннах ручного обслуживания целесообразно установить над ними дополнительную штангу на стойках, на которую завешивать подвески с деталями при их выгрузке из ванны. Промывать детали необходимо, снимая подвески с этой штанги в том же порядке, что и при завешивании их на штангу. Установка около каждой из гальванических ванн ванны-улавливателя (ванны-сборника) с непроточной водой для задержки в ней большей части раствора, выносимого деталями из рабочей ванны. С целью повышения эффективности ванны-сборника необходимо периодически содержимое этой ванны переливать в рабочую ванну, однако если рабочая ванна не подогревается, то уровень раствора в ней остается неизменным и переливку из сборника выполнить невозможно. По этой причине в сборнике растет концентрация солей и он перестает выполнять свои функции улавливателя. В этом случае рекомендуется несколько изменить обычный маршрут перемещения деталей в соответствии со схемой, представленной на рис. 20. Окуная подготовленные к покрытию детали вначале в ванну-сборник, затем в гальваническую ванну, и по окончании гальванического процесса снова в сборник и далее в промывку, достигается возможность частичного возврата растворенных веществ из ванны-сборника в рабочую ванну. Легко подсчитать, что даже при очень длительном употреблении ванны-сборника в ней накапливаются растворенные вещества не более 50% от их концентрации в рабочей ванне, тогда как при обычной последовательности операций эта величина доходит до 96%. Пересмотр состава электролитов и растворов с целью снижения в них концентраций катионов тяжелых металлов без ущерба для качества покрытий. Например, в ваннах кислого меднения вместо 200 г/л сульфата меди можно принять 80—100 г/л, увеличив содержание серной кислоты до 100 г/л. Применение цинкатных электролитов цинкования, где концентрация цинка составляет до 10 г/л. В составы электролитов хромирования обязательно вводить добавки «Хромина», или «Хромоксана», снижающих вынос электролита деталями. Замена растворов травления медных сплавов с повышенной концентрацией HNO3 на раствор, приведенный в п. 11 настоящего справочника. Внедрение способов регенерации растворов бестокового осаждения меди и никеля, исключающих залповый сброс отработанных растворов с содержащимися в них солями меди или никеля. Исключение из практики слива «отработанных» электролитов в виде залпового сброса. Для этого следует проанализировать причины, вызывающие необходимость смены электролитов, устранить эти причины, учитывая, что при внимательном и бережном отношении к электролитам, своевременной корректировке составов, исключении путей внесения вредных примесей электролиты должны эксплуатироваться многие годы без замены. Если появилась необходимость замены, то перед сливом электролита необходимо методом электролиза осадить практически весь металл на пластинчатых катодах, не допуская его попадания в очистные сооружения. 5. Соблюдение основных правил работы на ваннах: а) для обеспечения постоянства состава электролита поддерживать отношение площади растворимых анодов к площади катодов, равное 2:1; желательно в качестве анодов применять титановые перфорированные кассеты, в которые металл анода засыпается в виде мелких кусочков; в этом случае всегда сохраняется стабильная анодная поверхность; б) использовать для приготовления электролитов дистиллированную или обессоленную воду, имеющую жесткость не более 5 мг∙экв/л; при многоступенчатой каскадной промывке достигается возможность использования обессоленной воды и для промывок, так как потребность в воде значительно сокращается; в) не допускать падения деталей с подвесочных приспособлений на дно ванны, так как упавшие детали, растворяясь, загрязняют электролит солями меди, железа, цинка, свинца, олова; г) следить за тем, чтобы крючки, к которым крепятся аноды, не омывались электролитом при повышении уровня электролита в ванне, так как в этом случае происходит их анодное растворение и попадание в электролит меди и цинка; д) тщательно обезжиривать и промывать детали во избежание заноса с деталями органических примесей и травильных растворов; е) не допускать попадания смазочных масел в электролит с монорельсов тельферных устройств и других узлов механизированных и автоматических линий, расположенных над ваннами; ж) установить строгий порядок обслуживания ванн, исключающий возможность ошибок при подборе анодов, подвесок, материалов. 42. Безотходная технологияПод безотходной технологией имеют в виду такую организацию технологического процесса, при которой исключается или сводится к минимуму сброс катионов тяжелых металлов в очистные сооружения и, соответственно, образования гидроокисных шламов не происходит, или они получаются в таком количестве, которое не вызывает трудности в их утилизации. Ниже приведены различные методы осуществления безотходной технологии, получившие развитие в отечественной и мировой практике с указанием области применения. Дистилляция. Дистилляция, или метод упаривания, осуществляется в двух вариантах: первый — упаривание промывных вод с целью получения дистиллята в качестве оборотной воды и концентрированного раствора электролита, который возвращается в рабочую ванну (упаривание происходит в специальных установ- ках под вакуумом для снижения точки кипения воды до 70—75 °С); второй — атмосферное испарение части электролита рабочей ванны в небольшой по объему испарительной ванне, помещаемой над рабочей ванной. Интенсивность испарения обеспечивается вентилятором, который подает горячий воздух на поверхность электролита в испарительной ванне. Одна из установок такого типа, весьма распространенная в США, представлена на рис. 21. Электролит ванны непрерывно концентрируется, а компенсация испарившейся воды осуществляется подачей свежей воды через многоступенчатую (3—4 ступеней) каскадную промывку. Этот способ представляет собой классический пример безотходной и даже бессточной технологии, как это видно из схемы на рис. 22. Имеются отечественные аналоги подобных технических средств. Методы упаривания дают большой эффект применительно к таким процессам, как покрытия драгоценными металлами, никелирование, хромирование и др., в которых используются электролиты с подогревом и электролиты, содержащие дорогостоящие компоненты (соли цветных металлов, блескообразователи). Обратный осмос. Метод заключается в «продавливании» разбавленных растворов через мембраны, имеющие микропоры диаметром в 10–9 нм, т. е. размер, соизмеримый с размерами молекул воды. В результате, этого действия происходит отделение растворенных в воде солей от воды. Соли и другие компоненты электролитов возвращаются в электролитическую ванну, а вода поступает в промывочные ванны. Обратному осмосу подвергают разбавленные растворы электролитов, находящихся в ваннах-сборниках. Способ обратного осмоса более энергоемок по сравнению с методом упаривания, но он удобен применительно к холодным растворам и полностью исключает нежелательные процессы, сопутствующие упариванию, например гидролиз растворенных солей, окисление отдельных компонентов. Для внедрения метода обратного осмоса используется установка УРЖ-1200, разработанная Горьковским технологическим институтом. Мембраны для установки поставляет Владимирский институт синтетических смол. Установка помещается непосредственно в гальваническом цехе рядом с ванной-сборником и служит хорошим средством осуществления безотходной технологии. Электролиз. Одним из эффективных способов извлечения катионов тяжелых металлов из растворов является катодное осаждение, режимы которого определяются составом растворов. Применение электролиза для извлечения металлов из сточных вод основано на том, что наибольшую ценность и экологическую опасность представляют катионы, а к анионам требования ПДК менее жестки и в общем потоке кислотно-щелочных стоков от гальванического цеха такие анионы, как SO42–, Cl–, ОН–, СО32– проблем не создают. Электролитическое извлечение металлов из концентрированных растворов, например из электролитов гальванических ванн, трудностей не представляет. Более сложная задача извлекать металл из сильно разбавленных растворов, какими является содержимое ванн-сборников или промывная вода. В этом случае диффузионные ограничения тормозят электроосаждение металла и в прикатодном слое концентрация ионов металла становится равной нулю и практически вместо металла выделяется водород. Для преодоления диффузионных ограничений необходимо вести электролиз при очень интенсивном перемешивании и при малой плотности тока, а для обеспечения достаточной скорости извлечения металла катод должен иметь максимально большую поверхность. Реализация данного способа может быть осуществлена в следующих двух вариантах: 1. Установка вблизи ванны-улавливателя (ванны-сборника) промышленно изготавливаемого электролизера со скоростью осаждения металлов от 20 до 100 г в час. Из ряда конструкций электролизеров наиболее эффективной является установка, в которой принят метод электролиза в псевдоожиженном слое. На рис. 23 представлено устройство такого электролизера. Рабочее пространство электролизера ограничено перфорированными перегородками; через нижнюю перегородку под напором поступает раствор из ванны-сборника, а через верхнюю перегородку раствор возвращается в ванну-сборник. Все пространство между перегородками заполнено мелкими стеклянными шариками, которые под напором жидкости сталкиваются между собой, и электро- дами, производя эффект интенсивного перемешивания, в результате чего преодолеваются диффузионные ограничения при электроосаждении и, кроме того, ударяясь о поверхность катодов, шарики уплотняют образующееся покрытие. Катоды периодически извлекаются из установки и завешиваются в качестве анодов в соответствующей гальванической ванне для растворения металла и возврата таким образом в производство ценных материалов. Электролизер данного типа целесообразно устанавливать около гальванических линий с высокой производительностью, в которых одна ванна-сборник обслуживает 4—5 однотипных гальванических ванн. Конструкция подобной установки разработана институтом общей и неорганической химии в г. Киеве. 2. Использование в составе гальванических линий ванны-электролизера. В качестве катода рекомендуется применять углеткань (углеволокно) марки УУТ, которая обеспечивает возможность значительного увеличения катодной поверхности при ее небольших геометрических размерах. На катодной поверхности осажденный металл удаляется путем его анодного растворения, для чего катод завешивают на анодную штангу рабочей ванны, и после растворения металла катод снова используют в электролизере. На поверхности нерастворимых анодов протекают различные процессы. Так, при использовании кислых сульфатных растворов на свинцовых анодах выделяется кислород, а в растворе накапливается серная кислота в количестве, эквивалентном количеству осажденного металла. В связи с этим ванну можно даже использовать в качестве ванны активации (декапирования). В цианистых электролитах на анодной поверхности из стали или никеля происходит частичное окисление цианида в цианат и далее до азота и углекислого газа по схеме 2CN– + 8OH– Таким образом, применение электролизера облегчает проведение процесса обезвреживания, цианидов в системе очистных сооружений. Следует иметь в виду, что приведенные реакции окисления более активно протекают при анодной плотности тока 3—4 А/дм2, поэтому анодная поверхность должна во много раз быть менее катодной. Для хлоридных электролитов электролиз в ваннах более сложен. В качестве анодов следует применять платинированный титан или графит и на их поверхности возможно образование газообразного хлора, если в растворе не содержатся легко окисляемые компоненты (например, NH4+). В связи с наличием газовыделений на электродах во всех случаях электролиза ванна должна оборудоваться бортовым вентиляционным отсосом. Рабочие чертежи на конструкцию ванны высылаются по запросам предприятий. Имеющийся опыт применения электролиза в ваннах свидетельствует о возможности практически исключить сброс катионов тяжелых металлов в стоки предприятия, так как концентрация катионов в отдельных случаях снижается до 0,5 мг/л, и в стоках предприятий вследствие многократного разбавления катионы не обнаруживаются. Электродиализ. Разделение ионов в электрическом поле может также использоваться для очистки промывочной воды от растворенных в ней минеральных веществ. Электродиализ в сочетании с окислительно-восстановительными процессами на электродах, например, использован в установке для электрохимической регенерации меди из кислого травильного раствора. Электродиализ дает весьма существенный эффект для отделения катионов и анионов из промывных вод с целью получения деминерализованной воды, используемой как оборотной воды для многих гальванических процессов. Электродиализ легко используется в потоке жидкостей, что значительно повышает производительность данного метода. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
