пособие. ТТД ч1 учебное пособие. Техническая термодинамика
 Скачать 4.15 Mb. Скачать 4.15 Mb.
|
|
В случае если процесс сушки осуществляется воздухом, имеющим 100 % - ную относительную влажность, его влагосодержание может увеличиваться только за счет механического уноса потоком воздуха капелек воды. Этот процесс в H,d- диаграмме будет идти в области тумана по изотерме (рис.7.12, процесс 12), поскольку при отсутствии испарения воды температура воздуха изменяться не будет. Энтальпия воздуха в конце такого процесса будет больше, чем энтальпия воздуха в начале процесса (H2>H1). Такое возрастание энтальпии обусловлено появлением слагаемого 4,187tdж/1000 в расчетном выражении энтальпии влажного воздуха в области тумана. Поскольку унос капель воды в нашем процессе приводит к увеличению dж от нуля до dж2, то, несмотря на постоянство температуры воздуха в процессе 12, его энтальпия будет возрастать. Только в случае наличия потерь теплоты во внешнюю среду данный процесс может идти со снижением температуры и энтальпии. Для определения по H,d- диаграмме конечного состояния воздуха в этом случае необходимо определить опытным путем его температуру и количество унесенной влаги в пересчете на 1 кг сухого воздуха (dж2=d2-d1). Процесс поглощения влаги из воздуха объектом, имеющим одинаковую с ним температуру, при отсутствии теплообмена с окружающей средой будет идти при постоянной температуре в сторону уменьшения влагосодержания воздуха (процесс АВ, рис.7.12). Относительная влажность, энтальпия и парциальное давление водяного пара будут уменьшаться, если весь процесс идет в области ненасыщенного влажного воздуха. В том случае, если такой процесс идет в области тумана (процесс 21, рис.7.12), уменьшение влагосодержания воздуха будет происходить только за счет поглощения из воздуха капелек воды. Этот процесс обратный процессу сушки 12 за счет уноса капелек влаги. В процессе 21 температура и парциальное давление водяного пара остаются неизменными, а влагосодержание и энтальпия воздуха уменьшаются. Е 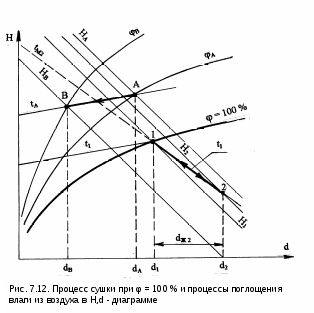 сли процесс поглощения влаги из воздуха идет с потерями теплоты в окружающую среду, температура воздуха будет уменьшаться. В технологических установках температуры воздуха и объекта, с которым контактирует воздух, могут быть различными. Поэтому конечная температура, энтальпия, влагосодержание и другие параметры воздуха в конце таких процессов определяются с учетом этих факторов. Однако данный вопрос выходит за пределы курса технической термодинамики и требует дополнительных знаний из области тепломассообмена. Подробное рассмотрение данных процессов осуществляется в специальных курсах и литературе по сушильным аппаратам и кондиционированию после изучения курсов технической термодинамики и тепломассообмена. 8. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ Второй закон термодинамики так же, как и первый, не имеет никаких доказательств, кроме человеческого опыта в земных условиях. Если первый закон термодинамики количественно характеризует термодинамические процессы, то второй закон термодинамики дает качественную их оценку. Он отвечает на вопросы, в каком направлении и до какого предела идет тот или иной процесс, при каких условиях возможно преобразование теплоты в работу, что необходимо для передачи теплоты от холодного тела к горячему, что характеризует реальные процессы и т.п. [1, 7]. Поскольку в природе происходит множество термодинамических процессов, то единой формулировки второго закона термодинамики быть не может. Однако к каждому классу этих процессов можно дать свою трактовку второго закона термодинамики. Вот некоторые из формулировок [1] второго закона термодинамики, данные разными авторами. Теплота не может самопроизвольно переходить от более холодного тела к более нагретому телу (Р.Клаузиус). В круговом процессе теплота горячего источника не может быть полностью превращена в работу (В.Томсон – Кельвин). Наиболее холодное тело системы не может служить источником работы (В.Томсон – Кельвин). Все естественные процессы являются переходом системы от менее вероятных состояний к более вероятным состояниям (Л.Больцман). Любой реальный процесс является необратимым (Л.Больцман). Изучение второго закона термодинамики возможно только на конкретных процессах. Применительно к этим процессам и даются формулировки второго закона термодинамики. Поэтому изложение материала этой главы идет параллельно со знакомством с новыми термодинамическими процессами и изучением второго закона термодинамики, объясняющего возможность и особенности прохождения этих процессов. 8.1. Замкнутые процессы (циклы) Процессы, в которых термодинамические состояния рабочего тела в начале и в конце совпадают, называются замкнутыми процессами или циклами. В  термодинамических диаграммах циклы представляют собой замкнутые линии. При этом, если цикл идет по часовой стрелке, его называют прямым. В результате этого цикла получается положительная работа. Такие циклы осуществляются в теплоэнергетических установках (рис. 8.1) для получения работы за счет использования термической неравновесности термодинамической системы. Циклы, идущие против часовой стрелки, называются обратными. На осуществление таких циклов затрачивается работа. Эти циклы (рис. 8.2) предназначены для передачи теплоты от тел с низкой температурой телам с более высокой температурой. Такие циклы используются в холодильных машинах и тепловых насосах. Циклы могут состоять из различных процессов. Внутренне равновесные циклы могут изображаться во всех термодинамических диаграммах. 8.1.1. Коэффициенты, характеризующие тепловую экономичность обратимых циклов Изобразим прямой обратимый цикл в T,s- координатах (рис.8.3). Необходимо отметить, что для обратимых циклов в диаграммах, как правило, изображаются только процессы для рабочего тела. Процесс 1а2 характеризуется подводом теплоты к рабочему телу, т.к. здесь увеличивается энтропия. Эту теплоту обозначают как q1 и называют теплотой, подведенной в цикл. Эта теплота берется от горячего источника теплоты. Поскольку процесс передачи теплоты обратимый, то для горячего источника процесс соответствует кривой 2а1. Он совпадает с обратимым процессом получения теплоты рабочим телом, изображать его не принято, но забывать о его наличии не следует. П 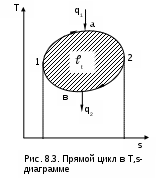 роцесс 2в1 характеризуется отводом теплоты от рабочего тела к холодному источнику теплоты. Поскольку это тоже обратимые процессы, то для холодного источника процесс соответствует кривой 1в2. Величину отведенной теплоты из цикла принято обозначать как q2 и брать по модулю, а соответствующий ей отрицательный знак присваивать в расчетах. роцесс 2в1 характеризуется отводом теплоты от рабочего тела к холодному источнику теплоты. Поскольку это тоже обратимые процессы, то для холодного источника процесс соответствует кривой 1в2. Величину отведенной теплоты из цикла принято обозначать как q2 и брать по модулю, а соответствующий ей отрицательный знак присваивать в расчетах.Таким образом, для реализации цикла необходимо три тела: горячий источник теплоты, рабочее тело (оно совершает замкнутый процесс) и холодный источник теплоты. Суммарная теплота прямого цикла 1а2в1 в соответствии с первым законом термодинамики будет определяться выражением q1 - q2 = (u2 - u1 + 1a2) + (u1 - u2 + 2в1) = = 1a2 + 2в1 = t. (8.1) Следовательно, работа цикла t представляет разность подведенной и отведенной теплоты цикла. В Р,v- и в T,s- координатах она представляет площадь внутри цикла. Индекс t обозначает, что это работа обратимого цикла. Термодинамическая, или тепловая, эффективность прямого обратимого цикла оценивается термическим коэффициентом полезного действия (КПД) ηt. Он представляет отношение полученной работы t (полезный продукт) к подведенной теплоте в цикл q1 (затраты на получение полезного продукта). Термический КПД цикла всегда меньше единицы, поскольку отвод теплоты из цикла происходит при положительной абсолютной температуре (см. разд. 8.1.6), и q2 не может быть равна нулю. Основываясь на этом факте, получили еще одну формулировку второго закона термодинамики: невозможно создать тепловую машину, в которой вся теплота горячего источника преобразуется в работу. В соответствии с первым законом термодинамики такой вывод сделать нельзя, поскольку по первому закону термодинамики возможно всю теплоту, подведенную к телу, преобразовать в механическую работу (например, в изотермическом процессе идеального газа q=). Однако о том, что для получения этой теплоты требуется второе тело с большей температурой, первый закон термодинамики ничего не сообщает. При равенстве подведенной и отведенной теплоты (q1=q2) работа цикла и его термический КПД равны нулю. В соответствии с этим утверждением, можно дать следующие формулировки второго закона термодинамики: невозможно получить работу в тепловой машине при наличии только одного источника теплоты; д 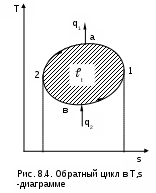 ля работы тепловой машины необходимо наличие горячего и холодного источников теплоты. ля работы тепловой машины необходимо наличие горячего и холодного источников теплоты.Рассмотрим в диаграмме Т,s обратный обратимый цикл (рис.8.4). Обозначим теплоту, отведенную от рабочего тела, q1 (процесс 1а2), а подведенную к рабочему телу от холодного источника – q2 (процесс 2в1). Величину q1 примем с обратным знаком, т.е. положительную. Для совершения этого цикла требуется затратить работу t = q1-q2. Эта работа отрицательная, хотя в расчетах, как и q1, она будет приниматься по модулю. Эффективность обратных обратимых циклов, в зависимости от их предназначения, характеризуют определенные коэффициенты. Холодильный цикл, где нижний уровень температур обычно находится ниже температуры окружающей среды, характеризуется холодильным коэффициентом: где q2 – отведенная от холодного тела теплота (полезный продукт – холод); t – работа, затраченная на осуществление цикла (затраты на получение полезного продукта – холода). Холодильный коэффициент может быть как меньше, так и больше единицы. Отопительный цикл, где нижний уровень температур обычно соответствует температуре окружающей среды, а верхний – температуре потребителя теплоты, характеризуется отопительным коэффициентом: где q1 – теплота, подведенная к потребителю (полезный продукт); t – работа, затраченная на осуществление цикла (затраты на получение полезного продукта). Отопительный коэффициент всегда больше единицы. Необходимо отметить, что, имея отопительный и холодильный коэффициенты больше единицы, нет противоречий ни с первым, ни со вторым законами термодинамики. Эти коэффициенты нельзя называть КПД, поскольку полезного действия в виде работы в обратных циклах нет. В этом случае мы получаем теплоту более высокого температурного потенциала за счет преобразования работы в теплоту. КПД не можем иметь величину даже равную единице, т.е. целиком преобразовать q1 в работу нельзя, обязательно должны быть потери теплоты q2. На основании рассмотренных ранее положений для обратных циклов можно сформулировать следующую трактовку второго закона термодинамики: для передачи теплоты от холодного тела к горячему необходим дополнительный компенсационный процесс (например, совершение работы). 8.1.2. Цикл Карно Французский инженер Сади Карно в 1824 году впервые дал теоретическое объяснение работы тепловых машин. В то время еще использовалась теория теплорода и не была установлена единая природа теплоты и работы как меры энергетического взаимодействия. Однако С. Карно в своей теории тепловой машины были высказаны основные положения второго закона термодинамики [1, 7]. Основное положение теории С. Карно, впоследствии получившее название принципа Карно, состоит в том, что для получения работы в тепловой машине необходимы по крайней мере два источника теплоты с разными температурами. Карно предложил идеальный цикл тепловой машины, в котором используются два источника теплоты с постоянными температурами: источник с высокой температурой – горячий источник и источник с низкой температурой – холодный источник. Поскольку цикл идеальный, то он состоит из обратимых процессов теплообмена между рабочим телом и источниками теплоты, соответствующих двум изотермам, и двум идеальным адиабатам перехода рабочего тела с одной изотермы на другую. Графическое изображение цикла Карно в P,v- и T,s- диаграммах, использующего в качестве рабочего тела идеальный газ, представлено на рис.8.5. В цикле Карно горячий источник теплоты с Т1=const передает теплоту (процесс 14) рабочему телу, это обратимый процесс, поэтому рабочее тело получает теплоту q1 по изотерме Т1 (процесс 41). На процессе 12 рабочее тело расширяется по обратимой адиабате от Т1 до Т2. В обратимом процессе 23 рабочее тело передает теплоту q2 холодному источнику по изотерме Т2=const (для горячего источника это процесс 23). На процессе 34 рабочее тело сжимается по обратимой адиабате от Т2 до Т1. Д 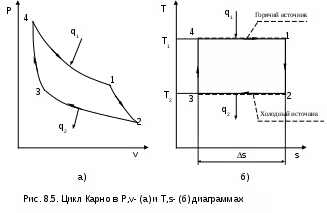 ля цикла Карно в T,s- диаграмме подведенная теплота к рабочему телу q1 и отведенная от него q2 представляют площади под изотермическими процессами 41 и 23, которые соответствуют прямоугольникам с определенными сторонами: для q1 – с Т1 и Δs, для q2 – с T2 и Δs. Величины q1 и q2 определяются по формулам изотермического процесса: q1 = T1Δs; (8.5) q2 = T2Δs. (8.6) Работа цикла Карно равна разности подведенной и отведенной теплоты: tк = q1 - q2 = (T1-T2) Δs. (8.7) В соответствии с выражением (8.7) получить работу возможно только при наличии разности температур у горячего и холодного источников теплоты. Максимальная работа цикла Карно теоретически была бы при Т2=0, но в качестве холодного источника в тепловых машинах, как правило, используется окружающая среда (вода, воздух) с температурой около 300 К. Кроме этого, достижение абсолютного нуля в природе невозможно (этот факт относится к третьему закону термодинамики). Таким образом, в цикле Карно не вся теплота q1 превращается в работу, а только ее часть. Оставшаяся после получения работы теплота q2 отдается холодному источнику, и при заданных Т1 и Т2 она не может быть использована для получения работы, величина q2 является тепловыми потерями (тепловым отбросом) цикла. Термический КПД цикла Карно может быть записан в виде Таким образом, КПД цикла Карно будет тем больше, чем больше Т1 и меньше Т2. При Т1=Т2 КПД равен нулю, т.е. при наличии одного источника теплоты получение работы невозможно. Невозможность существования Т2=0 К указывает на то, что КПД цикла Карно не может быть равен единице, и на то, что он всегда меньше единицы. Анализ выражений (8.7) и (8.8) включает в себя выводы, которые относятся к формулировкам второго закона термодинамики: получение работы в тепловой машине возможно только при наличии двух источников теплоты, имеющих разную температуру; в тепловой машине невозможно преобразовать всю теплоту горячего источника в работу; невозможно создание вечного двигателя второго рода, в котором в качестве источника теплоты используется окружающая среда. Необходимо отметить, что любой цикл имеет термический КПД ниже КПД цикла Карно, проходящего в интервалах максимальной и минимальной температур данного цикла. Это утверждение легко доказать, представив сравниваемые циклы в T,s- диаграмме (рис.8.6). Сравним термический КПД произвольного цикла abcd (ηt) с КПД цикла Карно 1234 (ηtк), проходящего в интервалах максимальной – T1max и минимальной – T2min температур данного цикла – abcd. Из рис.8.6 видно, что q1к > q1 на величину площади 1ad и 4dc, а q2 > q2к на величину площади а2b и 3cb. В результате имеем q2/q1 > q2к/q1к, следовательно, получаем соотношение η 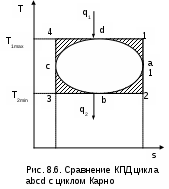 tк = 1 - tк = 1 - Термический КПД цикла Карно зависит только от температур горячего и холодного источников теплоты (Т1 и Т2). Зная температуры цикла Карно, легко определить его КПД и сопоставить его с КПД другого цикла Карно. Любой обратимый цикл можно представить в виде эквивалентного цикла Карно, т.е. цикла с такими же q1 и q2, а соответственно и с такой же работой и термическим КПД, как у исходного цикла. Понятие эквивалентного цикла Карно позволяет сопоставить между собой термические КПД различных по конфигурации обратимых циклов, используя только Т1 и Т2. Для преобразования произвольного обратимого цикла в эквивалентный цикл Карно вводится понятие среднетермодинамической температуры. |
