Гистология реферат. Тема 1 клетка Вопрос Химический состав, организация плазмолеммы. Функции плазмолеммы
 Скачать 3.29 Mb. Скачать 3.29 Mb.
|
|
Часть кровяных пластинок используется эндотелиальными клетками сосудов в качестве источника питания. Вопрос 16. Кроветворение у эмбриона и плода. Основные стадии, их характеристика. Развитие крови как ткани (гистогенез). Первичная (мезобластическая) стадия. В течение 3 недели развития во внезародышевой мезодерме желточного мешка формируются скопления мезенхимных клеток – кровяные островки. Клетки по периферии каждого островка формируют эндотелий первичных кровеносных сосудов. В ходе мегалобластического эритропоэза клетки центральной части островка образуют первые клетки крови – первичные эритробласты – крупные клетки, содержащие ядро и эмбриональные гемоглобины. Лейкоцитов и тромбоцитов на этой стадии нет. На 12 неделе кроветворение в желточном мешке заканчивается. Гепатоспленотимическая стадия. В течение второго месяца развития стволовые клетки крови заселяют печень, селезёнку и тимус, и в этих органах образуют разные типы клеток крови. В печени кроветворение начинается на 5-6 неделе развития. Здесь образуются гранулоциты, тромбоциты и как дефинитивные эритробласты (ядросодержащие), так и эритроциты (безъядерные). К концу 5 месяца интенсивность гемопоэза в печени уменьшается, но в небольшой степени продолжается ещё несколько недель после рождения. В селезёнке гемопоэз наиболее выражен с 4 по 8 месяц внутриутробного развития. Здесь образуются эритроциты и небольшое количество гранулоцитов и тромбоцитов. Непосредственно перед рождением важнейшей функцией селезёнки становится образование лимфоцитов. В тимусе образуются лимфоциты (различные типы Т-клеток). Костномозговое кроветворение. В течение 5 месяца развития гемопоэз начинается в костном мозге, где образуются все типы клеток крови. Дополнительное количество лимфоцитов формируется в лимфоидных органах. К моменту рождения, после рождения и у взрослого кроветворение ограничивается костным мозгом и лимфоидной тканью. Вопрос 17. Строение костного мозга, его функции. Главная функция красного костного мозга – кроветворение. Кроме того, в костном мозге, как в селезёнке и печени, происходит удаление из кровотока старых и дефектных клеток крови. Он играет центральную роль в иммунной системе, т.к. в нём образуются В-лимфоциты, а также присутствует большое количество плазматических клеток, синтезирующих антитела. В красном костном мозге преобладают созревающие эритроциты, что придаёт костномозговым очагам гемопоэза красный цвет. Строма костного мозга состоит из ретикулярных клеток с длинными отростками, ретикулиновых волокон, синусоидных капилляров; здесь же расположены макрофаги и жировые клетки. С элементами стромы гемопоэтические клетки связаны с помощью ламинина и фибронектина. Ретикулиновые волокна вместе с отростками ретикулярных клеток формируют трёхмерную сеть и образуют полости, заполненные островками гемопоэтических клеток. Зрелые клетки крови попадают в кровоток через щели, расположенные между эндотелиальными клетками и в базальной мембране (синусоидные капилляры). Макрофаги расположены в непосредственной близости от синусоидов и образуют длинные отростки, проникающие между клетками эндотелия в просвет сосудов. Жировые клетки составляют почти половину объёма костного мозга. Жёлтый костный мозг. У взрослых большая часть костного мозга становится неактивной; в связи с преобладанием в нем жировых клеток его назвали жёлтым. Жёлтый костный мозг может восстановить свою активность, если необходимо усилить гемопоэз. Вопрос 18. Понятие о стволовых клетках крови и колониеобразующих единицах. Свойства стволовой кроветворной клетки. Унипотентные коммитированные клетки, клетки-предшественницы. Последовательность образования клеток крови из стволовой кроветворной клетки (схема гемопоэза). Стволовая кроветворная клетка (СКК) – родоначальница всех форменных элементов крови, медленно размнжающаяся и дифференцирующаяся в несколько различных типов коммитированных клеток, которые дифференцируются в отдельные линии - эритроциты, гранулоциты, моноциты и тромбоциты. Коммитированные клетки интенсивно делятся, в результате чего образуются предшественники зрелых клеточных типов. Пролиферативную активность СКК модулируют колониестимулирующие факторы и интерлейкины (ИЛ). СКК – клетка мезенхимного происхождения, способная к повторным делениям и дифференцировке в различные зрелые клетки крови (CFU-blast). Часть таких клеток циркулирует в крови и имеет сходство с малыми лимфоцитами. СКК делится редко. Потомки СКК – полипотентные клетки-предшественницы лимфоцитопоэза (CFU-Ly) и миелопоэза (CFU-GEMM), в результате их деления их потомки остаются полипотентными или дифференцируются в один из нескольких типов коммитированных унипотентных стволовых клеток, также способных делиться, но дифференцирующихся только в одном направлении. СКК дифференцируется в различные типы клеток. Она выходит в кровоток и циркулирует в крови. Для стволовых клеток характерна способность к самообновлению. Унипотентные коммитированные клетки имеют ограниченные потенции, коммитированы к дифференцировке в один клеточный тип, пролиферируют и в присутствии факторов роста дифференцируются в клетки-предшественницы. Унипотентные клетки морфологически НЕ ОТЛИЧАЮТСЯ от СКК. Коммитирование (программирование клетки на определённый путь дифференцировки) происходит, скорее всего, случайным образом. Клетки-предшественницы – клетки одной линии дифференцировки, отличающиеся морфологически и образующиеся последовательно в каждой линии, начинающейся с коммитированной унипотентной клетки и завершающейся формированием зрелой клетки крови. Схема гемопоэза
Вопрос 19. Эритропоэз. Дифферон эритроцитов и характеристика клеток разных стадий по мере созревания эритроцита. Начало эритроидного ряда – взрывообразующая единица эритропоэза (BFU-E), происходящая из CFU-бласт’а. Из BFU-E формируется унипотентный предшественник эритроцитов (CFU-E). На дальнейших стадиях эритропоэза дифференцируются проэритробласты, эритробласты, ретикулоциты и эритроциты. Длительность эритропоэза – 2 недели. Интенсивность эритропоэза контролирует эритропоэтин, основным стимулом для быработки эритропоэтина является гипоксия. BFU-E реагируют на ИЛ-3, но нечувствительны к эритропоэтину. Пролиферация и дифференцировка CFU-E зависят от эритропоэтина. От BFU-E до CFU-E 12 делений, а от CFU-E до зрелой клетки – 6 делений. Проэритробласты – первые морфологически опознаваемые предшественники эритроцитов – крупные клетки с многочисленными органеллами, но без гемоглобина. Центрально в клетке расположено ядро. Они подвергаются многократным митозам. На дальнейших стадиях развития происходят уменьшение размера клетки, конденсация хроматина и уменьшение диаметра ядра, прогрессирующая потеря органелл и РНК, постепенное увеличение содержания гемоглобина, элиминация ядра. Последовательно различают ЭРИТРОБЛАСТЫ: базофильный эритробласт содержит ядро с более плотным, чем у проэритробласта, хроматином, имеет меньший диамнтр, клетка сохраняет способность к митозу и активно синтезирует гемоглобин. полихроматофильный эритробласт содержит много гемоглабина, цитоплазму серого цвета, что обусловлено базофильным окрашиванием рибосом и оксифильным окрашиванием гемоглобина. Размеры ядра уменьшаются, клетки могут делиться. оксифильный эритробласт (нормобласт) имеет меньшие размеры и ацитофильную цитоплазму, ядро небольшое, ещё сохраняют способность к делению, постепенно утрачивая её и выталкивая дегенерирующее ядро. В костном мозге имеются островки эритробластов, состоящие из макрофага, окружённого предшественниками эритроцитов. Макрофаг образует длинные отростки, по поверхности которых по направлению к концу отростка макрофага перемещаются дифференцирующиеся эритроидные клетки. Далее эритробласт вступает в контакт с эндотелинм ближайшего синуса, проходит через его стенку и попадает в общий кровоток. Как раз во время этих событий выталкивается ядро эритробластов, которое факоцитируется макрофагами. Ретикулоциты содержат остатки рибосом и РНК, они выходят в кровоток и составляют до 1% общего числа циркулирующих эритроцитов. После выхода в кровоток в течение 24-48 часов они завершают созревание и становятся эритроцитами. При этом клетка приобретает форму двояковогнутого диска, а последние органеллы разрушаются ферментами. Вопрос 20. Гранулоцитопоэз. Характеристика клеток разных стадий по мере созревания нейтрофилов, эозинофилов, базофилов. Гранулоциты образуются в костном мозге. Нейтрофилы и базофилы происходят из полипотентной клетки-предшественницы нейтрофилов и базофилов (CFU-G), а эозинофилы – из унипотентного предшественника эозинофилов (CFU-E0). При этом CFU-G и CFU-E0 – потомки полипотентной клетки-предшественницы гранулоцитов и моноцитов (CFU-GM). По мере дифференцировки размеры клеток уменьшаются, хроматин конденсируется, изменяется форма ядра, в цитоплазме накапливаются гранулы. В развитии гранулоцита выделяют 6 стадий: Миелобласт – малодифференцированная клетка, содержащая крупное округлое ядро и 1-3 ядрышка. Их цитоплазма лишена гранул и более базофильна в сравнении с их предшественниками. Промиелоцит – крупные клетки, содержащие более конденсированный хроматин, эксцентрично расположенное ядро, базофильную цитоплазму, содержащую азурофильные гранулы. По мере деления и созревания количество азурофильных гранул уменьшается. Миелоцит – клетка меньших размеров, содержащая специфические гранулы, что позволяет различать нейтрофильные, эозинофильные и базофильные миелоциты. Образование и накопление этих гранул продолжаются в течение трёх последующих клеточных делений. Ядро приобретает бобовидную форму. Метамиелоцит – клетка ещё меньших размеров, содержащая ещё больше специфических гранул, в ядре появляются глубокие вырезки, хроматин продолжает конденсироваться. NB! Способность к митозу на этой стадии утрачивается! Палочкоядерный гранулоцит – клетки, предшествующие зрелым формам гранулоцитов, имеющее подковообразной формы ядро. Они могут выходить в кровоток и составлять 3-5% от общего количества циркулирующих лейкоцитов. Сегментарный гранулоцит – зрелая форма гранулоцита. Вопрос 21. Тромбоцитопоэз. Характеристика клеток разных стадий. Образование тромбоцитов. Тромбоцитам дают начало мегакариоциты – самые крупные клетки костного мозга. Предшественником мегакариоцита является мегакариобласт – потомок унипотентной клетки-предшественницы мегакариоцитов (CFU-Meg). Мегакариоцит – крупная клетка с полиплоидным и дольчатым ядром, имеющая базофильные гранулы. В нём формируются везикулы и демаркационные мембраны; количество свободных рибосом и выраженность гранулярной ЭПС уменьшаются. В цитоплазме зрелого мегакариоцита различают 3 зоны: Перинуклеарная зона содержит комплекс Гольджи, гладкую и гранулярную ЭПС, гранулы, центриоли и трубочки. Эта зона остаётся связанной с ядром после отделения тромбоцитов. Промежуточная зона содержит демаркационную мембранную систему - развитую систему взаимосвязанных пузырьков и трубочек, переходящую в клеточную мембрану и выполняющую разграничительную функцию при формировании тромбоцитарных полей. Наружная зона содержит элементы цитоскелета и пересекается мембранами, связанными с системой демаркационных мембран. NB! Тромбоциты формируются путём фрагментации цитоплазмы мегакариоцита: мегакариоцит в костном мозге образует протромбоцитарную псевдоподию, которая проникает сквозь стенку синуса в просвет синуса, после чего от псевдоподии отделяются тромбоциты и поступают в кровоток. Вопрос 22. Лимфоцитопоэз. Стадии развития B- и T-лимфоцитов. Из стволовой кроветворной клетки (CFU-blast) происходит полипотентная клетка-предшественница лимфоцитопоэза (CFU-Ly). В-лимфоциты образуются в костном мозге, созревание Т-лимфоцитов происходит в тимусе (см. тема: «Иммунная система»). При образовании лимфоцитов выделяют 2 стадии – лимфобласт (более крупный) и пролимфоцит. Главная особенность лимфоцитопоэза – постепенное и значительное уменьшение клеточного объёма. Однако, многие циркулирующие лимфоциты реагируют на антигенную стимуляцию увеличением объёма клетки, приобретая морфологию лимфобласта. В отличие от других клеток крови, лимфоциты могут пролиферировать и вне костного мозга – в тканях иммунной системы в ответ на стимуляцию. (см. тема: «Иммунная система»: Вопросы 5, 6). Вопрос 23. Гормональная регуляция гемопоэза, роль микроокружения. Гемопоэтические факторы роста: Фактор стволовых клеток в ходе эмбрионального гемопоэза способствует выживанию, пролиферации и миграции ранних потомков СКК; Колониестимулирующий фактор гранулоцитов и макрофагов способствует образованию моноцитов и гранулоцитов, влияет на ранние стадии гемопоэза, стимулируя пролиферацию практически всех классов ранних клеток-предшественников гранулоцитов и макрофагов. Его продуцируют моноциты, Т-лимфоциты, фибробласты, клетки эндотелия; Колониестимулирующий фактор гранулоцитов влияет на полипотентную клетку-предшественницу нейтрофилов и базофиов, стимулируя её дифференцировку в унипотентные клетки-предшественницы нейтрофилов и базофилов. Его синтезируют макрофаги и фибробласты; Колониестимулирующий фактор макрофагов стимулирует полипотентную клетку-предшественницу гранулоцитов и моноцитов и унипотентный предшественник моноцитов к дифференцировке в моноциты и далее в макрофаги. Оказывает противоопухолевое действие. Синтезируется макрофагами и фибробластами. Интерлейкин-3 (ИЛ-3) действует на СКК и полипотентную клетку-предшественницу миелопоэза, на большинство клеток-предшественниц миелоидного ряда, стимулируя формирование эритроцитов, гранулоцитов, моноцитов и тромбоцитов. Вырабатывается Т-лимфоцитами и клетками костного мозга; ИЛ-5 стимулирует образование эозинофилов; ИЛ-7 способствует образованию Т- и В-лимфоцитов, воздействуя на их клетки-предшественницы. Продуцируется клетками стромы костного мозга; Эритропоэтин регулирует эритропоэз, стимулируя пролиферацию и дифференцировку унипотентных клеток-предшественниц эритроцитов. Синтезируется в почке и печени. Интенсивность синтеза зависит от рО2 в этих органах; Тромбопоэтин – фактор пролиферации предшественников мегакариоцитов, их созревания и увеличения количества тромбоцитов. Синтезируется в печени. Факторы транскрипции – связывающиеся с ДНК белки различных семейств, функционирующие с ранних стадий развития и регулирующие экспрессию генов кроветворных клеток. Фолиевая кислота и витамин D необходимы активного синтеза ДНК при массовом образовании новых клеток крови. Вопрос 24. Кровь новорожденного. Возрастные изменения крови. Изменения соотношения лейкоцитов (физиологические перекресты). Эритроциты. При рождении и в первые часы жизни количество эритроцитов в крови повышено и составляет 6,0-7,0x1012/литр. У новорождённых наблюдается анизоцитоз с преобладанием макроцитов, а также повышенное содержание ретикулоцитов. В течение первых суток постнатального периода количество эритроцитов снижается, к 10-14 суткам достигает уровня взрослого и продолжает снижаться. Минимальный показатель количества эритроцитов наблюдается на 3-6 месяце – физиологическая анемия, - что связано с переносом синтеза эритропоэтина из печени в почку (во время переключения образуется пониженное количество эритропоэтина). Содержание эритроцитов достигает нормы взрослого в период полового созревания. Лейкоциты. Количество лейкоцитов у новорождённых повышено и составляет 10-30х109/л. В течение первых двух недель их количество снижается до 9-15х109/л, а к 14 годам достигает уровня, характерного для взрослого. Физиологические перекрёсты обусловлены изменениями содержания нейтрофилов и лимфоцитов. Первый перекрёст. У новорождённого соотношение содержания этих клеток такое же, как у взрослого. В последующем содержание нейтрофилов падает, а лимфоцитов возрастает, так что на 3-4 сутки их количество уравнивается. В дальнейшем количество нейтрофилов продолжает снижаться и к 1-2 годам достигает 25%. В этом же возрасте количество лимфоцитов составляет 65%. Второй перекрёст. В течение следующих лет число нейтрофилов постепенно повышается, а лимфоцитов – понижается, так что у 4-летних детей эти показатели снова уравниваются. Количество нейтрофилов продолжает повышаться, а лимфоцитов - снижаться, и к 14 годам эти показатели соответствуют таковым у взрослого. 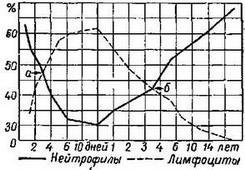 | ||||||||||||||||||||||
