|
|
Биология_лекции. Тема Сущность и субстрат жизни. Свойства живого. Уровни организации живой материи. Типы клеточной организации
Тема 2. Молекулярный и клеточный уровень
организации жизни.
План
Строение и свойства биологических макромолекул - белков, жиров, углеводов, нуклеиновых кислот.
Строение клетки. Органоиды клетки.
Растительные и животные клетки.
Обмен веществ и поток энергии в клетке (анаболизм, катаболизм)
Размножение клеток (митоз, амитоз, мейоз).
Химические вещества клетки
В состав клетки входит около 70 химических элементов
I группа - макроэлементы (около 98 % массы клетки) образуют четыре элемента: водород, кислород, углерод и азот. Это главные компоненты всех органических соединений.
II группа - сера и фосфор, калий, натрий, кальций, магний, железо, хлор
Вместе элементами I группы сера и фосфор являются биоэлемен�тами (необходимые компоненты молекул биологических полимеров)
Роль химических элементов в клетке
Элементы
|
Роль в клетке
|
Na, К, CI
|
проницаемость клеточных мембран для различных веществ и проведение импульса по нервному волокну
|
Са и Р
|
участвуют в формировании костной ткани, определяя
прочность кости.
|
Са
|
один из факторов свертываемости крови.
|
Fe
|
входит в состав гемоглобина
|
Mg
|
включен в хлорофилл (растения)
входит в состав ряда ферментов (животные)
|
III группа – микроэлементы (0,02 % массы клетки): цинк, медь, иод, фтор, кобальт, марганец, молибден, бор и др.) Микроэлементы входят в состав ферментов, витаминов и гормонов — веществ, обладающих боль�шой биологической активностью.
Роль микроэлементов в клетке
Элементы
|
Роль в клетке
|
йод
|
входит в состав гормона щитовидной железы тироксина
Недостаток – у взрослых развивается зоб (увеличение щитовидной железы). У детей недостаток йода сопровождается резкими изменениями всей структуры тела. Ребенок перестает расти, умственное развитие задерживается (кретинизм).
Избыток - может наблюдаться при гипертиреозе, может развиться и базедова болезнь с зобом, тахикардией. Кроме этого наблюдается раздражительность, мышечная слабость, потливость, исхудание, склонность к диарее. Основной обмен повышается, наблюдается гипертермия, дистрофические изменения кожи и ее придатков, раннее поседение, депигментация кожи на ограниченных участках (витилиго), атрофия мышц.
|
Кобальт
|
необходимый компонент витамина В12 (участвует в процессах синтеза нуклеиновых кислот, белковом обмене, кроветворении).
|
Молибден
|
входит в состав ферментов, влияя на рост, принимает участие в обмене азота, оказывает влияние на обмен меди, способствует метаболизму углеводов и жиров, является важной частью фермента, отвечающего за утилизацию железа, в результате чего помогает предупредить анемию.
|
Цинк
|
входит в состав ряда ферментов, гормона инсулина;
оказывает влияние на активность половых и гонадотропных
гормонов гипофиза. Увеличивает активность ферментов: фосфатаз кишечной и костной, катализирующих гидролиз. Участвует также в жировом, белковом и витаминном обмене, в процессах кроветворения.
Недостаток - задержка роста, перевозбуждение нервной
системы и быстрое утомление, бесплодие. Поражение кожи происходит с утолщением эпидермиса, отеком кожи, слизистых оболочек рта и пищевода, ослаблением и выпадением волос. Дефицит цинка может приводить к усиленному накоплению железа, меди, кадмия, свинца. . При недостатке цинка дети отстают в развитии, страдают гнойничковыми заболеваниями кожи и слизистых оболочек.
Избыток - задерживает рост и нарушает минерализацию костей, отмечается дефицит железа, меди, кадмия.
|
Селен
|
оказывает антиоксидантное действие, замедляя старение, способствует предупреждению роста аномальных клеток, укрепляет иммунную систему. В сочетании с витаминами А, С и Е предохраняет от возникновения онкологических заболеваний, помогает при артрите, разрушает вредные для организма вещества (защищает организм от тяжёлых металлов). Увеличивает выносливость организма благодаря увеличению поступления кислорода к сердечной мышце. Необходим для образования белков; поддерживает нормальную работу печени, щитовидной железы, поджелудочной железы, важен для поддержания репродуктивной функции.
Недостаток –организме усиленно накапливаются мышьяк и кадмий, которые, в свою очередь, усугубляют дефицит селена.
Избыток - может вызывать увеличение печени до 3-х см и боли в правом подреберье, боли в конечностях, судороги, чувство онемения; может привести к дефициту кальция.
|
Марганец
|
важен для репродуктивных функций и нормальной работы центральной нервной системы. Помогает устранить половое бессилие, улучшить мышечные рефлексы, предотвратить остеопороз, улучшить память и уменьшить нервную раздражительность.
Недостаток – нарушаются процессы окостенения во всем скелете, трубчатые кости утолщаются и укорачиваются, суставы деформируются. Нарушается репродуктивная функция.
Избыток - сильная утомляемость, слабость, сонливость, тупые головные боли в лобно-височных областях; тянущие боли в пояснице, конечностях, боли в правом подреберье, в подложечной области, понижение аппетита; медлительность движений, расстройство походки, парестезии, сильная скованность движений; расстройство мочеиспускания, половая слабость; бессонница, подавленное настроение, слезливость. Избыток марганца усиливает дефицит магния и меди.
|
Фтор
|
участвует в костеобразовании и процессах формирования дентина и зубной эмали; стимулирует кроветворную систему и иммунитет, участвует в развитии скелета, стимулирует репаративные процессы при переломах костей. Предупреждает развитие сенильного остеопороза.
Недостаток –резке учащение заболевания зубным кариесом.
Избыток - развивается тяжелое хроническое отравление, называемое флюорозом. При этом поражаются кости и зубы. Внешне флюороз проявляется в виде белых и желтоватых пятнышек на зубах с последующим их разрушением.
Основной источник промышленного загрязнения атмосферы фтористыми соединениями — предприятия по производству алюминия, цемента, химических удобрений.
|
Неорганические вещества, входящие в состав клетки
Вода. Содержание колеблется в широких пределах: в клетках эмали зубов вода составляет по массе около 10%, а в клетках развивающегося зародыша — более 90 %. В среднем в многоклеточном организме вода составляет около 80 % массы тела.
Свойства связаны главным образом с малыми размерами молекул воды, с их полярностью и способностью соединяться друг с другом водородными связями.
Вода — превосходный растворитель для полярных веществ.
Под действием некоторых ферментов вступает в реакции гидролиза, т.е. реакции, при которых к свободным валентностям различных молекул присоединяются группы ОН или Н воды. В результате образуются новые вещества с новыми свойствами.
Вода обладает хорошей теплопроводностью и большой тепло�емкостью, поэтому температура внутри клетки остается неизмен�ной или ее колебания оказываются значительно меньшими, чем в окружающей клетку среде.
-
Вода
свойства
|
растворитель для полярных веществ
реакции гидролиза
хорошая теплопроводность
большая тепло�емкость
|
Минеральные соли.
Большая часть неорганических веществ клетки находится в виде солей — либо в ионном состоянии, либо в виде твердой нерастворимой соли. Среди первых большое значение имеют катионы К+ Na+, Са2+
От концентрации солей зависят буферные свойства клетки.
Буферностью называют способность клетки поддерживать слабощелочную реакцию своего содержимого на постоянном уровне. Внутри клетки буферность обеспечивается главным образом анионами Н2РО4- и HPO42-. (дигидрофосфат-ионы Н2РО4 и гидрофосфат HPO42-
Во внеклеточной жидкости и в крови роль буфера играют Н2СО3 (угольная кислота) и НСО3- (гидрокаобонаты). Анионы слабых кислот и слабые щелочи связывают ионы водорода и гидроксил - ионы (ОН-), благодаря чему реакция внутри клетки практически не меняется.
Органические вещества
Органические соединения составляют в среднем 20—30 % массы клетки живого организма.
К ним относятся биологические полимеры:
- белки
- нуклеиновые кислоты
- углеводы
- жиры
- ряд небольших молекул — гормоны, пигменты, аминокислоты, простые сахара, нуклеотиды и т.д.
Различные типы клеток отличаются количественным содержанием органических соединений. Так, в растительных клетках преобладают углеводы. Наоборот, белки в большем количестве содержатся в животной клетке, чем в растительной (40—50 % против 20—35 %). Тем не менее каждая из групп органических веществ в клетке любого типа выполняет сходные функции.
Белки занимают первое место среди органических веществ клетки как по количеству, так и по значению.
Белки — это высокомолекулярные полимерные соединения, мономером которых служат аминокислоты.
Молекула каждой аминокислоты содержит специфическую часть (боковую группу - R) - аминокислотный остаток и неспецифическую часть.
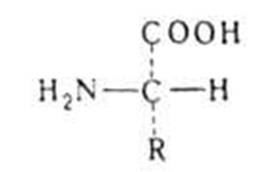
Цепи аминокислот называются пептидами.
Белки - это пептиды, но большей длины (полипептиды). Граница между истинными белками и пептидами условна: белками считают пептиды, цепь которых включает более 50 аминокислотных остатков (молекулярная масса белков от 5 тысяч дальтон и выше).
Аминокислоты соединяются между собой пептидной связью.
Пептидная связь возникает при образовании белков и пептидов в результате взаимодействия аминогруппы (– NH2) одной аминокислоты с карбоксильной группой (–СООН) другой аминокислоты.
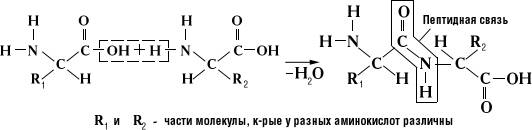
Схема пептидной связи
Всего биохимикам известно около 200 различных природных аминокислот.20 аминокислот, обнаруживаемые в белках - это протеиногенные аминокислоты – то есть аминокислоты, из которых строятся белковые молекулы. В организме человека встречается 5 млн. типов белковых молекул, отличающихся не только друг от друга, но и от белков других организмов.
Четыре уровня структурной организации:
Первичная структура
|
последовательность
аминокислот в полипептидной цепи
(ковалентная структура).
|
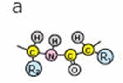
|
Вторичная струк�тура
|
Характеризует различные типы регулярных
структур, встречающихся во многих
белках:
(α-спирали), образованные
единичной полипептидной цепью
(β-структуры), образованные двумя
или не�сколькими участками цепи
Эти структуры стабилизированы
водородными связями, образованными
между — СО- и —NH- группами
пептидных связей в спирали.
|
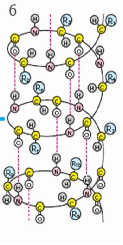
|
третичная структура
|
характеризует пространственную
укладку молекул белка, если она
образована одной полипептидной цепью.
Определена нековалентными
взаимодействиями между спиральными и /3-структурными участками полипептидной
цепи в совокупности с взаимодействиями
R-групп и функциональных групп
остова молекулы.
Третичная структура имеет прямое отношение к форме молекул белка, которая может быть шарообразной (глобулярной) или нитевидной (фибриллярной). Дисульфидные (S—S) связи не определяют характер свертывания полипептидной цепи, но стабилизируют третичную структуру после завершения процесса свертывания. Такие связи образуются самопроизвольно, когда соответствующие—SH-группы оказываются рядом.
|
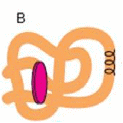
сворачивание спирали в
более тесное образование
за счет дополнительного
«сшивания» слабыми связями
|
Четвертичная структура
|
характеризует пространственное
взаиморасположение субъединиц белка в том случае, если он состоит более чем из одной полипептидной цепи.
|

|
Денатурация белка - нарушение структурной организации белков (утрата структуры, присущей данной белковой молекуле) в результате изменения физических условий, в том числе изменение рН, температуры или обработка водными растворами некоторых неорганических веществ.
При денатурации молекула развертывается и теряет способность выполнять свою обычную биологическую функцию. Это изменение может носить временный или постоянный характер, но аминокислотная последовательность в молекуле белка остается неизменной.
Денатурированный белок существенным образом отличается по своей пространственной организации от белка в естественном (нативном) состоянии и лишен биологической активности. Дена�турирующие воздействия в той или иной степени разрушают нековалентную структуру нативного белка (вторичную, третичную и четвертичную). Некоторые белки при незначительных изме�нениях структуры не теряют биологической активности, другие даже при незначительных перестройках, которые не фиксируются обычными методами, полностью инактивируются.
Ренатурация белка - воссоздание струк�туры белка и его функциональной активности при восстанов�лении нормальных условий среды полностью.
Это свойство белков полностью восстанавливать утраченную структуру широко используется в медицинской и пищевой промышленности для приготовления некоторых медицинских препаратов, например антибиотиков, для получения пищевых концентратов, сохраняющих длительное время в высушенном виде свои питательные свойства, вакцин, сывороток, ферментов.
Функции белков
строительная (структур�ная)
|
белки участвуют в образовании всех клеточных мембран и органоидов клетки, а также внеклеточных структур.
|
каталитическая
|
ферменты — вещества белковой природы, они уско�ряют химические реакции, протекающие в клетке, в десятки и сотни тысяч раз.
|
Двигательная
|
обеспечивается специальными сократительными белками. Эти белки участвуют во всех видах движения, к которым способны клетки и организмы: образование псевдоподий, мерцание ресничек и биение жгутиков у простейших, сокращение мышц у многоклеточных животных, движение листьев у растений и др.
|
Транспортная
|
заключается в присоединении химических элементов (например, кислорода) или биологически активных веществ (гормонов) и переносе их к различным тканям и органам тела.
|
защитная
|
При поступлении в организм чужеродных белков или микро�организмов в белых кровяных тельцах — лейкоцитах — образуют�ся особые белки — антитела. Они связывают и обезвреживают несвойственные организму вещества (антигены)
|
энергетическая
|
При полном расщеплении 1 г белка выделяется 17,6 кДж энергии
|
Углеводы (сахариды)
Органические вещества с общей формулой Сn(Н2О)m
В животной клетке содержание углеводов составляет 1—2 % (5 %).
В растительной клетке достигает 90 % сухой массы (клубни картофеля, семена и т.д.).
Классы углеводов
моноса�хариды
|
простые сахара
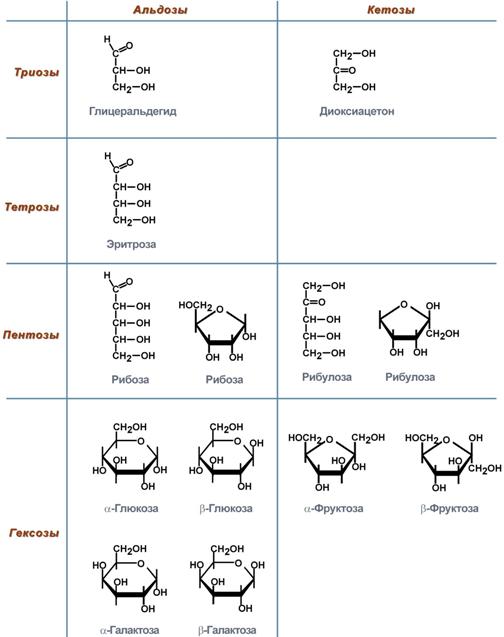
В зависимости от числа атомов углерода в молекуле среди моносахаридов различают
триозы — 3 атома,
тетрозы — 4,
пентозы — 5,
гексозы — 6,
гептозы—7 атомов углерода.
Из шестиуглеродных моносахаридов наиболее важны глюкоза, фруктоза и галактоза. Глюкоза содержится в крови (0,1—0,12%). Пентозы — рибоза и дезоксирибоза — входят в состав нуклеиновых кислот.
| |
|
|
 Скачать 5.67 Mb.
Скачать 5.67 Mb.






