Типовые патологические процессы
 Скачать 7.53 Mb. Скачать 7.53 Mb.
|
19.8.4. Классификация нарушений кислотно-основного состоянияРасстройства КОС проявляются в виде ацидоза и алкалоза. Ацидоз характеризуется появлением в биосреде относительного или абсолютного избытка кислот или недостатком оснований. Алкалоз характеризуется появлением в биосреде избытка оснований или недостатка кислот. Различают следующие основные виды ацидоза и алкалоза:
По степени компенсации ацидозы и алкалозы бывают компенсированными и декомпенсированными. При компенсированных их видах рН существенно не изменяется, т.е. не отклоняется за пределы нормы (7,357,45). На фоне значительных изменений абсолютных количеств угольной кислоты и натрия гидрокарбоната их соотношение остается равным 1:20. Для компенсированного ацидоза рН отклоняется в пределах 7,387,35. Для компенсированного алкалоза — в пределах 7,407,45. При декомпенсированных видах рН существенно отклоняется от нормальной величины, т.е. выходит за пределы нормы. Наряду с изменением абсолютных количеств угольной кислоты и натрия гидрокарбоната изменяется также их соотношение. Для некомпенсированного ацидоза характерны величины рН, равные 7,34 и ниже, для некомпенсированного алкалоза рН составляет 7,46 и выше. 19.8.5. Характеристика основных видов нарушений кислотно-основного состояния Основные клинические симптомы и лабораторные показатели при ведущих, наиболее часто встречающихся, расстройствах кислотно-основного состояния представлены в таблице 19-3. 19.8.5.1. Негазовый ацидозМетаболический (обменный или негазовый) ацидоз возникает в результате интенсивного образования и накопления недоокисленных промежуточных продуктов обмена, особенно при переходе тканей на анаэробный гликолиз. Это обычно встречается при развитии различных видов гипоксии, тяжелых формах нарушения кровообращения (массивная кровопотеря, прогрессирующая сердечно-сосудистая недостаточность, умирание организма и др.), сахарного диабета, распространенных гнойных заболеваниях (перитонит, флегмона, фурункулез, множественные абсцессы и др.). Метаболический ацидоз наиболее часто возникает при относительном избытке нелетучих кислот (соляной, серной, - оксимасляной, ацето-уксусной и др.), обусловленного как накоплением кислых метаболитов, так и потерей оснований с желчью, поджелудочным и кишечным соком в результате: - интенсивной диареи либо формирования желчных, поджелудочных или кишечных свищей; - голодания (полном, неполном и даже частичном); - активизации катаболических процессов в организме; -гормонального дисбаланса (сахарный диабет, гипертиреоз, гиперкортицизм и др.); - недостаточности печени и других как врожденных, так и приобретенных нарушениях обмена веществ; - интенсивных и длительных физических нагрузок. Метаболический ацидоз может развиться также и в результате других патогенетических факторов: - повышенного экзогенного поступления в организм различных кислых соединений (уксусной и др. кислот, отравлении салицилатами и т.д.), - сниженного выведения нелетучих кислот с мочой (в связи с нарушением выделительной функции почек), - избыточных потерь буферных анионов, прежде всего гидрокарбонатов с мочой (в связи с нарушением их реабсорбции в канальцах почек) и т.д. На начальных этапах развития метаболического ацидоза избыток образующихся протонов обычно нейтрализуется имеющимися в организме буферными анионами (гидрокарбонатами, белками), в связи с чем их количество в крови уменьшается. Степень отклонений величины рН в кислую сторону зависит от площади и объема повреждения клеточно-тканевых структур. Таблица 19-3 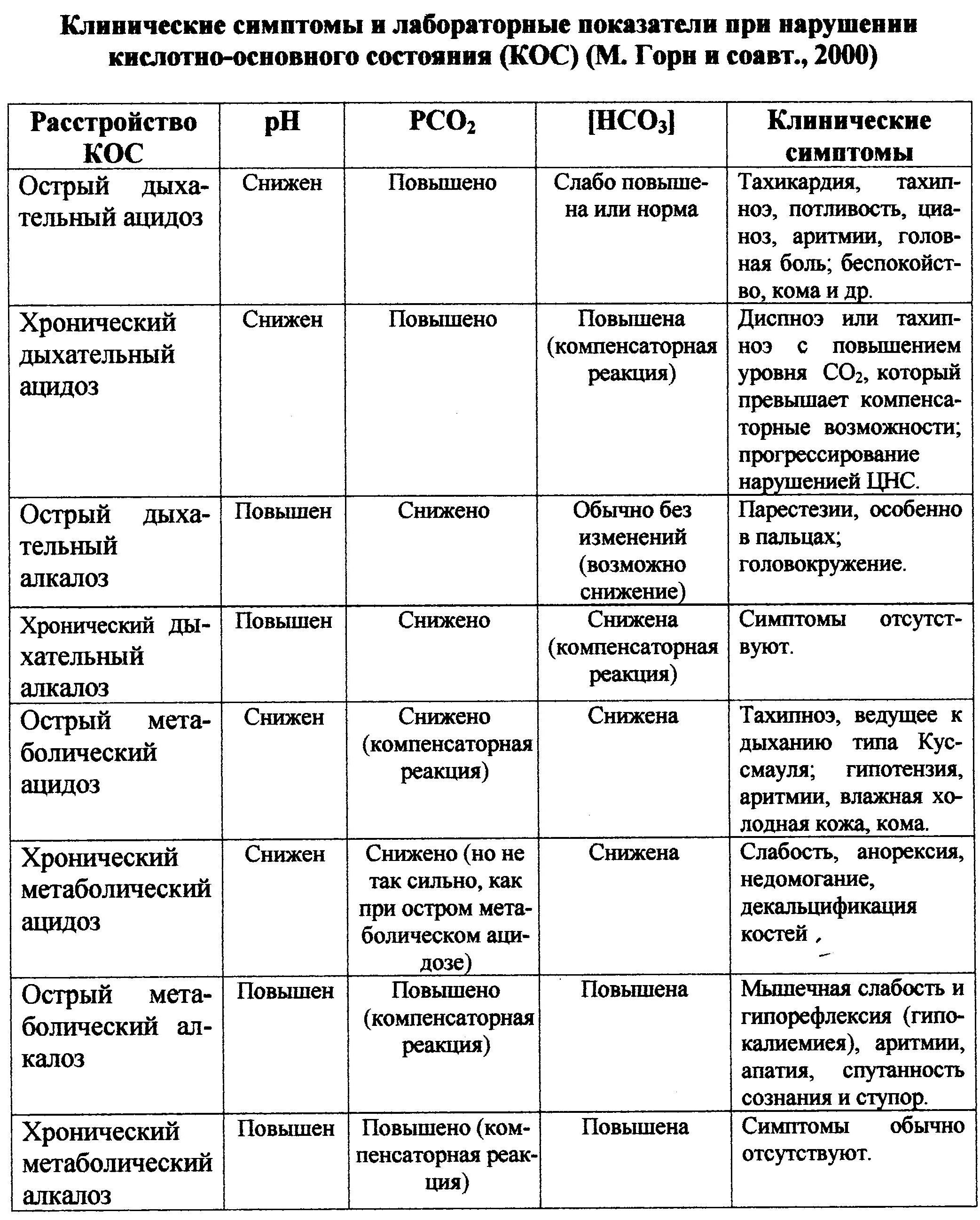 Поддержание кислотно-основного гомеостаза, помимо буферных систем, обеспечивается мобилизацией и других механизмов компенсации, среди которых важное значение имеют следующие. Довольно быстро, на фоне снижения емкости буферных систем, развивается гипервентиляция легких, сопровождающаяся удалением из организма углекислого газа. Это способствует восстановлению равновесия между кислотами и основаниями, а значит нормализации рН среды. Несколько позднее активизируются почечные компенсаторные механизмы. Последние обеспечивают либо увеличение выведения из организма с мочой нелетучих кислот (что приводит к восстанавлению рН крови и одновременно снижению рН мочи), либо сбережение в крови, а значит в организме, гидрокарбонатов (путем усиления их реабсорбции канальцами почек). Следует отметить, что срабатывание этих механизмов компенсации возможно только при сохраненной функции почек. Основными симптомами метаболического ацидоза являются, с одной стороны, снижение величин стандартного SB и буферных оснований ВВ, с другой, — увеличение отрицательной величины сдвига буферных оснований ВЕ. При компенсированном метаболическом ацидозе развивается снижение содержания углекислого газа и углекислоты в крови, в итоге чего величина рН остается нормальной. При декомпенсированном метаболическом ацидозе отмечается существенное снижение величины рН. Лечение негазового ацидоза Оно должно быть своевременным, комплексным и включать: - устранение влияния этиологического фактора; - эффективное лечение основного заболевания; - нормализацию гемодинамики (сердечно-сосудистой системы); - восстановление функций выделительной системы; - улучшение функций легких, особенно, легочной вентиляции; - активизацию полноценных окислительных процессов (тканевого дыхания, окислительного фосфорилирования) в организме; - осуществление мероприятий по нейтрализации кислот в биосредах организма путем как связывания протонов, так и восстановления емкости буферных систем. Это, в частности, достигается введением 1 М раствора натрия гидрокарбоната или 0,3 М раствора тригидрооксиметиламинометана (ТРИС). Следует, однако, помнить, что введение данного раствора противопоказано при почечной недостаточности. 19.8.5.2. Газовый ацидоз Дыхательный (газовый или респираторный) ацидоз развивается при увеличении содержания углекислого газа в организме (pCO2 выше 4,5 мм рт. ст.). Это происходит в результате, главным образом, из-за снижения вентиляции альвеол, а также других нарушений внешнего дыхания либо вследствие увеличения концентрации СО2 во вдыхаемом воздухе. Газовый ацидоз возникает при различных видах патологии (обширная пневмония, непроходимость дыхательных путей, бронхиальная астма, обструктивная форма эмфиземы легких, постоперационное состояние у ослабленных больных и т.д.). Задержка СО2 в организме обычно приводит к увеличению содержания углекислоты, которая при диссоциации высвобождает протон, а значит сопровождается повышением кислотности биосреды. Ведущим органом, компенсирующим газовый ацидоз, являются почки, обладающие способностью усиливать, с одной стороны, канальцевую реабсорбцию гидрокарбоната и, с другой стороны, выводить с мочой Н+. Это характеризуется увеличением значений ВВ (буферных оснований), SB и появлением избытка оснований (ВЕ со знаком плюс). Однако данная компенсаторная реакция, направленная на ослабление дыхательного ацидоза, является биологически целесообразной лишь до определенного момента. В связи с присоединением метаболического алкалоза респираторный ацидоз нарастает и часто становится декомпенсированным. Лечение дыхательного ацидоза направлено, главным образом, на восстановление нарушенной легочной вентиляции, на проведение оксигенотерапии, на использование натрия гидрокарбоната и, особенно ТРИС-раствора. 19.8.5.3. Негазовый алкалоз Метаболический (обменный или негазовый) алкалоз развивается при потерях нелетучих кислот и ионов К+. Это приводит к избыточному выведению ионов Н+ почками и перемещению данного иона в клеточный сектор. Характеризуется избытком (накоплением) в организме оснований по отношению к нелетучим кислотам. Возникает в результате: - избыточного поступления в организм оснований, чаще всего в виде натрия гидрокарбоната (в результате бесконтрольного приема питьевой соды при ожогах, либо избыточного его введения путем инфузий, особенно, после массивной кровопотери, сопровождающейся гиповолемией; - потери соляной кислоты с желудочным содержимым в результате длительной и часто повторяющейся рвоте, а также при токсикозах беременных и декомпенсированных стенозах привратника и т.д.; - дефицита калия в организме, возникающего из-за систематического приема как диуретиков, так и альдостерона. При этом убыль калия во внеклеточном секторе возмещается поступлением его из внутриклеточного сектора, куда в целях сохранения ионного равновесия поступают протоны. В итоге формируется комбинированное расстройство КОС, для которого характерно сочетание внутриклеточного гипокалиемического ацидоза с внеклеточным (внутрисосудистым, плазменным) алкалозом. Следует подчеркнуть, что компенсаторные возможности организма при алкалозах ниже, чем при ацидозах. При развитии метаболического алкалоза, характеризующегося повышением содержания в крови гидрокарбонатов, компенсация обеспечивается за счет: - снижения легочной вентиляции. Однако возможности данного механизма ограничены, так как он приводит к развитию респираторной гипоксии; -повышения экскреции почками гидрокарбонатов, что, с одной стороны, защелачивает мочу, а с другой, задерживает кислые вещества (соединения) в организме; - развития дыхательного ацидоза. Но такая компенсация приводит к раздражению дыхательного центра и возникновению гипервентиляции. Профилактика метаболического алкалоза возможна, но весьма затруднительна и недостаточно эффективна. Лечение метаболического алкалоза сводится, с одной стороны, к устранению причины, основного и ведущих звеньев патогенеза развития метаболического алкалоза, с другой, к активизации механизмов компенсации. В частности, рекомендуется восполнение в крови утраченного калия путем парентерального введения препаратов калия, либо назначением продуктов, богатых ионами калия (сухофрукты: изюм, инжир, финики, чернослив; печеный картофель и др.). Следует прекратить использование диуретиков и альдостерона. Необходимо устранить токсикоз, рвоту, непроходимость привратника и других отделов пищеварительного тракта. В тяжелых случаях показаны инфузии подкисленными растворами глюкозы. 19.8.5.4. Газовый алкалоз Дыхательный (газовый или респираторный) алкалоз возникает при форсированном выведении углекислого газа из легких, из крови, в целом из организма, главным образом, из-за развития гипервентиляции. Это нередко отмечается при проведении длительных операций, во время реанимации умирающих больных, при длительном подъеме в горы и пребывании в условиях высокогорья, при поражении центральной нервной системы (вследствие развития энцефалитов, опухолей, токсикозов, травм). Первичный механизм нарушений при дыхательном алкалозе заключается в снижении напряжения углекислого газа в крови. Механизмы компенсации метаболического алкалоза сводятся к: - повышенному выведению гидрокарбонатов из организма; - выделению НСО3 почками (вследствие чего моча ощелачивается); - задержке протонов почками; - уменьшению возбудимости дыхательного центра, что способствует развитию более редкого дыхания, - задержке ионов Н+, увеличению количества органических кислот, особенно, молочной, Следует отметить, что все компенсаторные реакции при дыхательном алкалозе являются целесообразными лишь относительно, так как они сопровождаются возникновением метаболического ацидоза, в итоге формируется смешанная форма расстройства КОС. Изменение величины такого важного гомеостатического показателя содержания СО2 в крови в ту или иную сторону свидетельствуют о возникновении дыхательного ацидоза или алкалоза. Так, при повышении СО2 в крови развивается дыхательный ацидоз, при снижении его величины дыхательный алкалоз. Изменение величин показателей SB и ВЕ наиболее типично для метаболических расстройств, а изменение величины показателя ВВ характеризует как метаболические, так и дыхательные нарушения, т.е. является суммарным и определяющим показателем КОС. По изменению величин отдельно взятых (перечисленных выше) показателей КОС крайне трудно судить о характере метаболических и дыхательных расстройств. Для правильной оценки того или иного вида ацидоза или алкалоза необходимо проводить комплексную системную оценку возникающих нарушений КОС. Лечение метаболического алкалоза сводится к использованию мероприятий и средств, способных восстановить функциональное состояние системы внешнего дыхания. Рекомендуется назначение дыхательных смесей кислорода и углекислого газа (карбогена). ГЛАВА 20. ПАТОЛОГИЯ ТКАНЕВОГО РОСТА В отличие от нормального роста тканей, в условиях различной патологии как наследственного, так и приобретенного происхождения, может наблюдаться патологический рост тканей на разных этапах развития организма. При патологии, особенно в условиях повреждения клеточно-тканевых структур, как правило, снижается их функциональная полноценность и реактивность, нередко уменьшается жизнеспособность и продолжительность жизни клеток, что имеет важное патогенетическое значение не только на местном, но и на системном уровне. Патологический рост проявляется в виде избытка, недостатка и извращения (качественного нарушения) размножения, дифференцировки, роста и созревания субклеточных, клеточных и межклеточных структур. Патологический рост тканей и органов сопровождается многообразными не только местными, но и общими изменениями. Он обычно возникает в части ткани или органа, но может захватывать всю ткань или весь орган или несколько тканей или органов. 20.1. Нарушение тканевого роста в процессе онтогенеза Те или иные нарушения тканевого роста могут развиваться в различные периоды онтогенеза. В частности, - либо в пренатальном или внутриутробном (у эмбриона – в эмбриональном, у плода – в фетальном периоде), либо в постнатальном (после рождения: у новорожденных, в препубертатном, в пубертатном и в постпубертатном: молодом, зрелом, пожилом, старческом) периодах жизни. Следует отметить, что для каждого из перечисленных периодов онтогенеза имеются свои особенности и даже характерные варианты. Нарушение тканевого роста в эмбриональный период Нарушение эмбрионального развития с формированием пороков развития носит название тератогенез. Тератогенез (от греч. teras, teratos — чудовище, урод иgenesis –происхождение развития) - возникновение порока развития ткани, органа или системы в результате как ненаследственных изменений (различных нарушений зародышевого развития), так и наследственных изменений. Примерами генетически обусловленных нарушений эмбрионального развития могут быть расщепление верхней губы и нёба, короткопалость (брахидактилия) шестипалость (синдактилия), некоторые пороки сердца, нарушения развития половой системы и др. Примерами нарушений эмбрионального развития, связанных с ненаследственными факторами, могут служить отсутствие, недоразвитие или неправильное развитие отдельных органов и др. Факторы, вызывающие тератогенез, называются тератогенными. Тератогенными могут быть химические (в том числе лекарственные), физические или биологические факторы, вызывающие пороки развития, различных структур организма. К основным группам тератогенных факторов относятся: - Ионизирующее излучение. - Инфекции (преимущественно вирусные). - Метаболические нарушения и вредные привычки у беременной. - Лекарственные средства и химические вещества. В зависимости от степени тератогенного действия выделяют следующие категории лекарственных средств. Безвредные вещества, не вызывающие тератогенного действия нив первом триместре, ни в поздние сроки беременности. К ним относятся превалирующее число лекарственных средств. Вещества с маловероятным (но возможнным) тератогенным действием. Эта группа веществ может назначаться во время беременности почти без риска вредного воздействия на плод. Примером лекарственного средства, относящегося к этой категории является инсулин.. Вещества с тератогенным действием. Эту группу лекарственных веществ нельзя принимать во время беременности, особенно на ранних ее сроках. Данную группу препаратов можно разделить на две подгруппы: 1) вещества, применение которых при беременности возможно по жизненным показаниям, когда ожидаемый положительный эффект превышает риск тератогенного воздействия (например, антидепрессанты, противосудорожные, анальгетики, антикоагулянты и др.); 2) вещества, абсолютно противопоказанные при беременности. Примерами лекарственных средств, относящихся к этой категории могут служить талидомид, эстрогены, хинин и некоторые другие препараты. Нарушение тканевого роста в препубертатный и пубертатный периоды Специфические нарушения тканевого роста в этих периодах связаны прежде всего с нарушением формирования скелета, отклонениями от нормального роста, правильных пропорциий тела. Эти нарушения могут быть связаны с генетическими расстройствами (например, различные варианты хондродистрофии, синдром Шерешевского-Тернера и др.), но могут быть не связанными с наследственностью и вызываться другими причинами, например, связанными с нарушением образования и действия гормона роста, гормонов щитовидной железы. Нарушение тканевого роста в постпубертатном (взрослом) периоде Принципиально можно выделить два основных вида нарушений роста тканей: 1) гипербиотический или избыточный рост тканей (гипертрофия, гиперплазия, гиперрегенерация, опухолевый рост); 2) гипобиотический или гипопластический или недостаточный рост тканей (атрофия, гипотрофия, гипоплазия, дистрофия и дегенерация). Данные виды нарушений тканевого роста встречаются также и в другие периоды жизни, например, в пубертатном, препубертатном, , а в отдельных случаях в фетальном и в эмбриональном периодах развития организма. 20.2. Гипобиотические процессы Атрофия и гипотрофия (греч. а - отсутствие, отрицание, hypo - недостаточно и trophe -питание) - прижизненное уменьшение объема клеток, а также межклеточных структур тканей и органов, возникающее за счет либо гипотрофии, либо гипоплазии, либо их сочетания, и сопровождающееся снижением их функции. Различают физиологическую атрофию (например, старческая атрофия хрящей межпозвоночных дисков, костей, половых желез) и патологическую атрофию. Патологическая атрофия как результат развития заболеваний или патологических процессов может быть общей (истощение) и местной. Общая атрофия возникает при:
Местная атрофия возникает при:
Дистрофия (dys - нарушение, расстройство, trophe - питаю) - расстройство состава клеточно-тканевых структур, обусловленное нарушением в них процессов метаболизма (характера и интенсивности обмена веществ) и сопровождающееся либо накоплением, либо уменьшением тех или иных веществ (соединений), либо появлением веществ, которые в норме не встречаются. Виды (паренхиматозные, мезенхимальные и смешанные), их характеристики и исходы (обратимые и необратимые) рассмотрены ранее, в разделе “Патология клетки”. Исходы: обратимые (паранекроз) и необратимые (некробиоз, некроз). Дисплазия - нарушение процесса развития клеток, проявляющееся изменением их структуры (числа, формы, размеров клеток, их органелл, мембран) функции, жизнедеятельности и продолжительности жизни. В патогенезе дисплазий важное значение имеют расстройства процесса дифференцировки клеток. 20.3. Гипербиотические процессы 20.3.1. ГИПЕРТРОФИЯ И ГИПЕРПЛАЗИЯ Гипертрофия – это увеличение объема ткани или органа за счет увеличения объёма их клеток и межклеточных структур. Гипертрофия клеток может быть за счет увеличения объема и числа их субклеточных структур, т.е. гипертрофия клетки обычно сочетается с гипертрофией и гиперплазией ее внутриклеточных ультраструктур. Гиперплазия – это увеличение объёма ткани или органа за счет повышения числа клеток и межклеточных структур. Термин гипертрофия происходит от греч. hyper – чрезмерно и trophe – питание; гиперплазия – от греч. hyper – чрезмерно и plaseo – образую. Гипертрофия и гиперплазия возникают при значительном увеличении нагрузки на орган или ткань или при воздействии стимулирующих рост клеток факторов. Если рассматривать гипертрофию и гиперплазию на тканевом уровне, то они возникают преимущественно в разных тканях. Гипертрофии подвергаются клетки тканей и органов, в которых резко снижен пролиферативный потенциал (например, миоциты); гиперплазии – клетки, сохранившие пролиферативную способность (клеточные элементы соединительной ткани, эпителий слизистых оболочек и различных органов). Однако, разница между гипертрофией и гиперплазией не всегда хорошо просматривается. Нередко в органе протекают параллельно оба процесса: например одновременная гипертрофия мышечных клеток и гиперплазия соединительнотканных структур). Кроме того, поскольку гипертрофия происходит за счет увеличения количества внутриклеточных структур, то такой процесс можно считать внутриклеточной гиперплазией. Виды гипертрофии и гиперплазии |
