Глава 4. ТИТАН И ЦИРКОНИЙ. Титан и цирконий общие сведения
 Скачать 2.64 Mb. Скачать 2.64 Mb.
|
Глава 4. ТИТАН И ЦИРКОНИЙ ОБЩИЕ СВЕДЕНИЯ Элемент титан открыт в 1791 г. английским любителем-минералогом Грегором. в титанистом железняке - менакените и был им назван менакеном. В 1795 г немецкий химик Клапрот открыл в минерале рутиле новый элемент, названный титаном. Несколько лет спустя была доказана идентичность менакена и титана. До 1849 г. за металлический титан принимали металлоподобный карбонитрид титана, найденный в шлаках доменных печей. Металлический титан был получей лишь спустя 120 лет после открытия, в 1910 г., американским химиком Хантером восстановлением тетрахлорида титана натрием. Элемент цирконий открыт почти одновременно с титаном - в 1789 г. Клапротом, который получил диоксид циркония из минерала циркона. Чистый ковкий цирконий был получен лишь в 1925 г. (спустя 136 лет после открытия элемента) термической диссоциацией иодида циркония по методу Ван-Аркеля и де Бура. Химический аналог циркония - гафний, всегда содержащийся в его минералах, был открыт в 1923 г. венгром Хевеши и голландцем Костером на основании теоретических предсказаний Бора. Применение титана и циркония в виде их химических соединений и присадок в сплавах началось в первые десятилетия XX в. Промышленное производство ковких титана и циркония возникло в начале 50-х годов в связи с потребностями в новых конструкционных материалах для реактивной авиации, ракетной техники и атомной энергетики. Свойства титана и циркония Титан и цирконий - элементы IV побочной группы периодической системы. По внешнему виду они напоминают сталь. Чистые металлы ковки и хорошо поддаются механической обработке давлением. Некоторые физико-механические свойства титана, циркония (а также аналога циркония - гафния) приведены ниже:
Физические и особенно механические свойства титана и циркония сильно зависят от чистоты металлов. Характерное свойство металлов - способность растворять кислород, водород, азот и углерод. Примеси этих элементов делают титан и цирконий хрупкими. На воздухе металлы устойчивы. При нагревании до 400—600 °С они покрываются оксидной пленкой, затрудняющей дальнейшее окисление. При более высокой температуре одновременно с увеличением скорости окисления наблюдается растворение кислорода, что сильно понижает пластичность металлов. Активное поглощение водорода титаном и цирконием наблюдается при 300- 400 °С с образованием твердых растворов и гидридов (TiH1.63-2, ZrH1.54-1.63). В отличие от кислорода и азота водород можно удалить из титана и циркония нагреванием в вакууме при 800-1000 °С. Вышч. 800-900 °С металлы быстро поглощают азот и активно взаимодействуют с углеродсодержащими газами (СО, СН4). С азотом и углеродом они образуют твердые и тугоплавкие соединения - нитриды и карбиды. Ниже приведены температура плавления tПЛ и микротвердость H0 ряда нитридов и карбидов:
 * Нитриды имеют широкую область гомогенности TiN0,6-1,0; ZrN0,67-1,0. Титан и цирконий при повышенных температурах реагируют с серой и сероводородом с образованием дисульфидов. С галогенами металлы взаимодействуют при 100-200 °С с образованием низкокипящих или легковозгоняющихся хлоридов, фторидов и иодидов.  * Вследствие близости свойств все, что ниже изложено о химических свойствах циркония, относится и к гафнию. По коррозионной стойкости титан близок к хромоникелевой быстрорежущей стали. Металл не корродирует в холодной и кипящей воде, практически стоек в азотной кислоте любой концентрации на холоду и при нагревании, в разбавленной (до 10%) серной кислоте на холоду; достаточно стоек в разбавленной соляной кислоте (5-10 %-ной) на холоду, растворяется в плавиковой кислоте. Коррозию в НСl можно сильно снизить добавлением окислителей (HN03, KMnO4, солей меди). В растворах щелочей (до концентрации 20 %) на холоду и при нагревании титан стоек. Важное значение имеет коррозионная стойкость титана в морской воде. По антикоррозионной стойкости цирконий и гафний превосходят титан и приближаются к танталу и ниобию. При температурах до 100°С они не корродируют в соляной и азотной кислотах любой концентрации и серной кислоте концентрации до 50 %. Металлы устойчивы на холоду в царской водке, растворяются при нагревании в плавиковой и концентрированно серной кислотах. Оба металла не корродируют в растворах щелочей при температуре кипения. Свойства химических соединений В важнейших и наиболее устойчивых соединениях титан и цирконий находятся в высшей степени окисления 4. Известны соединения, соответствующие степеням окисления 2 и 3. До низших степеней окисления сравнительно легко восстанавливается титан, труднее - цирконий. Так, в отличие от титана, в водных растворах соединения циркония со степенью окисления меньше четырех неизвестны. Ионы Ti4+ и Zr4+ в водных растворах неустойчивы. В результате взаимодействия с водой они образуют гидроксо-ионы Ti(OH) 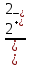 и Zr(OH) и Zr(OH)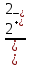 , которым упрощенно приписывают состав TiO2+ (ион титанила), ZrO2+ (ион циркоиила). Соответственно зтому в растворах присутствуют основные соли, например, Ti(OH)2SO4, Zr(OH)2Cl2 или в "титанильной" и "цирконильной" форме TiOSO4 и ZrOCl2. , которым упрощенно приписывают состав TiO2+ (ион титанила), ZrO2+ (ион циркоиила). Соответственно зтому в растворах присутствуют основные соли, например, Ti(OH)2SO4, Zr(OH)2Cl2 или в "титанильной" и "цирконильной" форме TiOSO4 и ZrOCl2.Высшие оксиды титана и циркония TiO2 и ZrO2 имеют амфотерный характер. При их сплавлении с щелочами или нагревании в смеси с оксидами других металлов (CaO, MgO) образуются титанаты и цирконаты. Наиболее характерны мета - и ортосоли типа 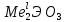 и и 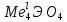 . Кроме того, путем сплавления с щелочами получены более сложные полититанаты и полицирконаты, например Na2Ti2O5, Na2Tl3O7, и др. Титанаты и цирконаты малорасторимы в воде, но растворяются в минеральных кислотах. . Кроме того, путем сплавления с щелочами получены более сложные полититанаты и полицирконаты, например Na2Ti2O5, Na2Tl3O7, и др. Титанаты и цирконаты малорасторимы в воде, но растворяются в минеральных кислотах.Титан образует ряд оксидов: TiO2 (белый, плавится при 1850 °С), Ті2O3 (фиолетовый, плавится при 2130 °С,) ТіО (золотисто-желтый, плавится при 1750 °С) и промежуточный оксид Ti3O5. Известны три аллотропические модификации диоксида тнтаиа, встречающиеся в виде минералов рутила, анатаза и брукита. Теплота образования TiO2 940 кДж/моль. Диоксид циркония ZrO2 - прочный и тугоплавкий оксид. Температура плавления 2900°С, теплота образования 1082 кДж/моль. Чистый диоксид - белого цвета, имеет три кристаллические модификации: до 1000-1100 устойчива моноклинная форма, в интервале 1100-1900 °С - тетрагональная форма, выше 1900 °С - кубическая форма. Существование низших оксидов циркония достоверно не установлено. Имеются указания об образовании монооксида ZrO при восстановлении ZrO2. Со всеми галогенами титан и цирконий образуют галогениды, являющиеся производными четырех-, трех - и двухвалентных элементов. Все высшие галогениды - легколетучие соединения. Среди них важнейшие: ТіС14 - бесцветная жидкость, кипящая при 136 °С; ZrCl4 - твердое бесцветное вещество с температурой возгонки 330 °С. Теплоты образования высших хлоридов равны 796 кДж/моль и 985 кДж/моль соответственно. Фториды титана и циркония образуют с фторидами щелочных металлов комплексные соединения - Me2TiF6 и Ме2ZrF6. Фтороцирконат калия K2ZrF6 легко кристаллизуется из растворов и устойчив на воздухе. Соль используют как исходное соединение для получения циркония. Области применения титана, циркония и гафния Области применения титана Титан и сплавы на его основе. Производство титана и сплавов на его основе возникло в начале 50-х годов в связи с потребностью в новых конструкционных материалах для реактивной авиации и ракетной техники. Сплавы на основе титана обладают высокой удельной прочностью (отношение прочности к плотности). Лучшие современные сплавы на основе титана (легированные добавками А1, Сг, V, Мо, Мn) имеют временное сопротивление (δв = = 1200-1500 МПа, что отвечает удельной прочности 270-330. Легированные стали с тем же δв имеют удельную прочность 155-190. Из сплавов на основе титана изготовляют части фюзеляжа самолетов и детали реактивных двигателей. В ракетостроении из легированного титана изготовляют корпусы двигателей, емкости для жидкого водорода и другие детали. Сплавы на основе титана используют в морском судостроении, перспективно их применение в автомобильном и железнодорожном транспорте. Широко используют титан и сплавы на его основе, как коррозионностойкие, в химическом машиностроении, конденсационных системах ТЭЦ, производстве медицинского инструмента и других областях. Ведущими странами в области производства титана являются СНГ, США и Япония. Промышленный выпуск титана осуществляется также в Англии, Франции. Масштабы прозводства первичного титана в капиталистических странах сильно зависят от конъюктуры рынка. В 1985 г. оно находилось на уровне 60 тыс. т., в том числе в США 30-34, Японии 24-25, Великобритании 5,0. Примерно 75-80 % титана используется в авиации, судостроении и космической технике, остальное в химическом машиностроении и других областях. Титан в сталях. В связи с высоким сродством к кислороду и азоту титан используют как эффективный раскислитель и деазотизатор стали. Кроме того, титан связывает серу, образуя прочный сульфид и устраняя этим образование прослоек легкоплавкой эвтектики Fе-FеS, вызывающих красноломкость стали. Для раскисления и деазотизации в сталь вводят от 0,03 до 0,2 % титана в виде ферротитана (18-25 % Тi). В качестве легирующей присадки титан вводят в марганцовистые, хромистые, хромомолибденовые и хромоникелевые коррозионностойкие стали. В последних титан устраняет межкристаллитную коррозию. Сплавы с цветными металлами. Добавки титана к меди, медным и алюминиевым сплавам улучшают их прочностные свойства и сопротивление коррозии. Для раскисления меди применяют купротитан (сплав меди с 6-12 % титана). В алюминиевые бронзы вводят 0,5-1,55 % титана в виде сплава алютита (40 % А1, 22-50 % Тi, 40 % Сu). Твердые и жаростойкие сплавы. Карбид титана входит в состав инструментальных твердых сплавов (10-40 % ТiС, 85-50 % WС, остальное - кобальт) -наиболее эффективных для обработки сталей и имеющих большое народнохозяйственное значение. В последние годы разработаны и выпускаются безвольфрамовые твердые сплавы на основе карбида и нитрида титана с никельмолибденовой цементирующей связкой. Карбид титана входит также в состав жаростойких и жаропрочных сплавов, применяемых для изготовления деталей газовых турбин в реактивных двигателях. Диоксид титана. Наиболее важно применение диоксида титана для изготовления белого пигмента - титановых белил, обладающих высокой кроющей способностью и неядовитых. Их используют для окраски судов, машин, вводят в состав эмалей, резины, бумажной массы. Природный диоксид титана (рутил) или технический диоксид вводят в состав обмазки электродов для электросварки. Высокая диэлектрическая постоянная рутильной формы ТiO2 (173-180) обусловила ее применение (а также титаната бария) для изготовления твердых диэлектриков в производстве конденсаторов, радиоаппаратуры, высокочастотных печей. Мощность заводов по производству диоксида титана в капиталистических странах составила в 1985 г. 2770 тыс.т. Области применения циркония Цирконий, его сплавы и соединения используют в различных областях техники: атомной энергетике, электронике, пиротехнике, машиностроении, производстве сталей и сплавов с цветными металлами, огнеупоров, керамики и эмалей, в литейном производстве. Атомная энергетика. Цирконий, очищенный от примеси гафния, обладает низким сечением захвата тепловых нейтронов, тугоплавкостью, антикоррозионной стойкостью и хорошими механическими свойствами. Это привлекло к нему внимание в начале 50-х годов как к ценному конструкционному материалу для изготовления защитных оболочек урановых тепловыделяющих элементов, труб, в которых циркулирует теплопередающая жидкость, и других конструктивных элементов ядерных реакторов. Для улучшения свойств циркония его легируют добавками олова (1,4-1,6%); железа (0,1-0,15%), хрома (0,08 -0,12%), никеля (0,04-0,06%). Электроника. В этой области используют способность циркония поглощать газы (служить геттером) для поддержания высокого вакуума в электронном приборе. С этой целью порошок циркония наносят на поверхность анодов, сеток и других деталей. Циркониевую фольгу применяют в качестве фильтра в рентгеновских трубках с молибденовыми антикатодами. Пиротехника и производствобоеприпасов. Порошки циркония, имеющие низкую температуру воспламенения и высокую скорость сгорания, применяют в качестве воспламенителя в смесях капсулей-детонаторов, а также в смесях для фотовспышки. В смеси с окислителями [В(NO)3)2, КClO3] порошки циркония образуют бездымный порох. Машиностроение. В связи с расширением производства ковкого циркония и сплавов на его основе привлечено внимание к его использованию в химическом машиностроении как кислотостойкого материала (детали центрифуг, насосы, конденсаторы, испарители и др.), в общем машиностроении (поршни, шатуны, тяги и др.) И турбостроении (лопасти турбин и другие детали). Стали и сплавы с цветными металлами. Цирконий - эффективный раскислитель и деазотизатор сталей. Кроме того, он ценный легирующий элемент вводимый в некоторые сорта броневых и орудийных сталей, коррозионностойких и жаропрочных сталей. Для введения в стали используют ферросиликоцирконий (40-45 % Zг, 20-24 % Si, остальное железо). Цирконий входит в состав ряда сплавов на основе цветных металлов. Цирконием легируют медь (0,1-5 % Zr) для улучшения прочностных характеристик. Получили распространение сплавы магния, легированные цирконием для придания им мелкозернистой структуры. Цирконий добавляют в свинцовистые бронзы, что предотвращает сегрегацию свинца в сплаве. Высокой прочностью и электропроводностью обладают меднокадмиевые сплавы, содержащие 0,35 % Zr. В последние годы разработаны сверхпроводящие сплавы, содержащие цирконий. В частности, сплав 75 % Nb- 25 % Zr используют для изготовления электромагнитов с высоким напряжением магнитного поля. Производство огнеупоров, фарфора, эмалей и стекла. В этих областях используют более половины общего потребления циркония. В качестве огнеупора применяют минерал циркон ZrSiО4и диоксид циркония. Последний обычно стабилизируют добавками оксидов кальция, магния или иттрия, исключающих растрескивание изделий при нагревании вследствие стабилизации высокотемпературной кубической модификации. Из диоксида циркония и циркона изготовляют кирпич для металлургических печей, тигли и другие изделия. Диоксид циркония и его минералы вводят в состав электротехнического фарфора для линий электропередач, высокочастотных установок и запальных свечей двигателей внутреннего сгорания. Их вводят также в состав эмалей (для придания им белого цвета и кислотостойкости) и в состав некоторых сортов стекла (повышается устойчивость стекла против действия растворов щелочей). Литейное производство. В этой области используют значительную долю цирконовых концентратов для присыпки литейных форм с целью получения хорошей поверхности отливок. Прочие области применения. Среди других областей следует упомянуть применение ZrО2 в синтезе пьезокерамических материалов (цирконотитанаты свинца и др.) и I для полировки оптического стекла; применение ZrО2 или смеси ZrО2-V2О3 в качестве твердого электролита в высокотемпературных топливных элементах (1000 °С и выше); использование двойных сульфатов циркония в качестве дубителя в сожевенной промышленности; тетрахлорида и оксихлорида циркония для приготовления катализаторов, используемых в синтезе органических соединений. Примерное распределение циркония по областям потребления следующее, %: литейное производство 42, огнеупоры 30, керамика 12, абразивы 4, металл, сплавы и другое применение 12. Области применения гафния Промышленное производство гафния возникло в 1950-1951 гг. Вследствие высокого сечения захвата тепловых нейтронов (115 • 10-24 см2) металл и его соединения (HfО2, НfB2) используют в регулирующих и защитных устройствах ядерных реакторов. Вторая перспективная область -производство тугоплавких и жаропрочных материалов. Так, перспективно использование карбида гафния (температура плавления 3890 °С), а также твердого раствора 25 % НfС + 75 % ТаС (tпл = 4200 °С). Высокой жаропрочностью отличаются сплавы гафния с другими тугоплавкими металлами (танталом, ниобием, вольфрамом). Намечается использование гафния в электровакуумной технике (катоды накаливания радиоламп и газоразрядных трубок) и для изготовления нитей накаливания электроламп. Примерные масштабы мирового производства гафния в 1985 г. 100 т. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
