Целая. Учебник для студентов высших учебных заведений, обучающихся по специальностям Летательные аппараты
 Скачать 32.33 Mb. Скачать 32.33 Mb.
|
|
| Тип частицы | Способ получения |
| Сферические Округлые неправильной формы: каплевидные, вытянутые и рваные. Гранные формы: простые пластинчатые многогранники, дендритные, игольчатые, нитевидные. Осколочные. Чешуйчатые. Иррегулярной формы. | Распыление расплавов, преимущественно газом или ультразвуком; конденсация паров; химический способ. Распыление расплавов, преимущественно водой или воздушное центробежное распыление; конденсация паров. Газовое осаждение; электролитическое осаждение; химический способ. Механическое диспергирование - дробление; размол; точение. Механическое диспергирование; распыление расплавов с расплющиванием капель о твердые поверхности. Механическое диспергирование |
7.1.1.4. МИКРОТВЕРДОСТЬ
Твердость - это свойство поверхностного слоя материала, состоящее в его способности сопротивляться упругой и пластической деформации или разрушению при местных контактных воздействиях со стороны более твердого тела (индентора) определенной формы и размера.
Микротвердость - это твердость малых (микроскопических) объемов материала. Ее определяют измерением диагонали отпечатка на приборе микротвердости ПМТ-3. Для этого порошок смешивают с бакелитовым лаком или оргцементом, затем прессуют в небольшие брикеты, которые полимеризуют при температуре 140 °С. Готовят шлиф и при нагрузке 20...30 г определяют микротвердость, которая является характеристикой пластичности порошков. Например, для армко железа микротвердость составляет 1300... 1400 МПа.
где Р - нагрузка; d - диаметр частицы; S - площадь отпечатка.
Здесь учтен пространственный угол в вершине пирамиды индентора (α = 136°).
7.1.1.5. УДЕЛЬНАЯ ПОВЕРХНОСТЬ
Удельной называется поверхность единицы массы или объема порошка. Ее величина для большинства металлических порошков колеблется от 0,01 до нескольких десятых квадратного метра на 1 грамм. Она зависит не только от размера частиц, но и от степени развитости поверхности, которая определяется условиями получения порошков.
От величины удельной поверхности зависит содержание адсорбированных газов, коррозионная стойкость, спекаемость порошков и ряд других характеристик. С уменьшением размера частиц их удельная поверхность увеличивается. Эта зависимость имет следующий вид:
где a и b - константы; d - диаметр частицы.
Пунктирной линией изображен график зависимости для сферических частиц.
К
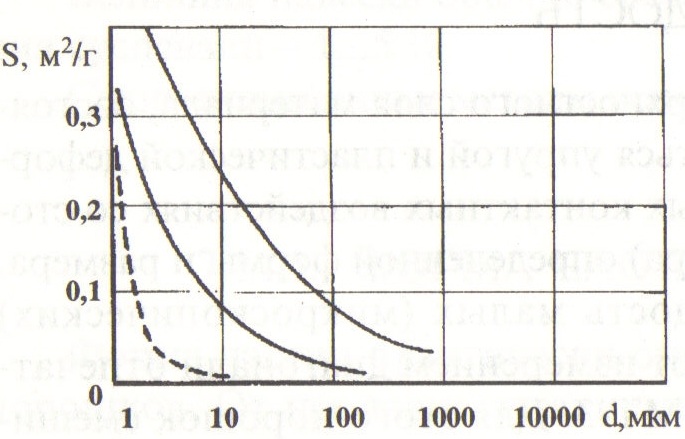 оэффициент шероховатости - это отношение удельной поверхности реальных частиц к удельной поверхности сферических частиц того же размера. Он колеблется в пределах 10...14 для вихревых порошков (рис.64). Величина удельной поверхности значительно снижается при отжиге, так как частица, как и всякая система, стремится к минимуму поверхностной энергии:
оэффициент шероховатости - это отношение удельной поверхности реальных частиц к удельной поверхности сферических частиц того же размера. Он колеблется в пределах 10...14 для вихревых порошков (рис.64). Величина удельной поверхности значительно снижается при отжиге, так как частица, как и всякая система, стремится к минимуму поверхностной энергии:Рис.64. Зависимость удельной
поверхности от размера частицы. Е= σ · S,
Где σ – поверхностное натяжение или поверхностная энергия. Минимум энергии не соответствует сферической частице, так как существует анизотропия поверхностного натяжения у кристаллических тел.
Удельная поверхность косвенно определяется измерением газопроницаемости или величины адсорбции. Газопроницаемость определяется в режиме молекулярного (Кнудсевого) течения газа.
Адсорбционные методы основаны на величине сорбции азота или другого газа навеской порошка ( 30 г), обезгаженного при температуре 200...300 °С и остаточном давлении в вакуумной камере 10-4...10-5 мм. рт. ст. (тор).
В качестве характеристики, определяющей внутреннюю пористость частиц, применяется пикнометрическая плотность, которая измеряется на специальных приборах - пикнометрах.
7.1.1.6. СОСТОЯНИЕ КРИСТАЛЛИЧЕСКОЙ СТРУКТУРЫ МЕТАЛЛИЧЕСКИХ ПОРОШКОВ
Металлические и другие порошки, как правило, получают в неравновесных условиях. Это относится ко всем видам порошков, полученных различными методами. Искажения полностью не устраняются и при отжигах, вплоть до температуры плавления. Искажениями являются вакансии, атомы в междоузлиях решетки, дислокации, примеси, оксиды.
Для исследования несовершенства кристаллического строения применяются методы калориметрии и рентгенографии.
Металлические порошки с искажениями кристаллической решетки хорошо спекаются , но плохо прессуются и могут активно поглощать газы и окисляться.
7.2. ТЕХНОЛОГИЧЕСКИЕ СВОЙСТВА ПОРОШКОВ
7.2.1. НАСЫПНОЙ ВЕС
Насыпной вес - это вес единицы объема свободно насыпанного порошка. Он зависит от плотности укладки частиц и определяется их размером, распределением по фракциям и формам. Значение величины насыпного веса очень существенно при конструировании прессформ, а также при прессовании и дозировке порций порошка. От этого зависит постоянство размеров и плотность спрессованных брикетов. Величина насыпного веса оговаривается в ТУ или ГОСТах.
Н
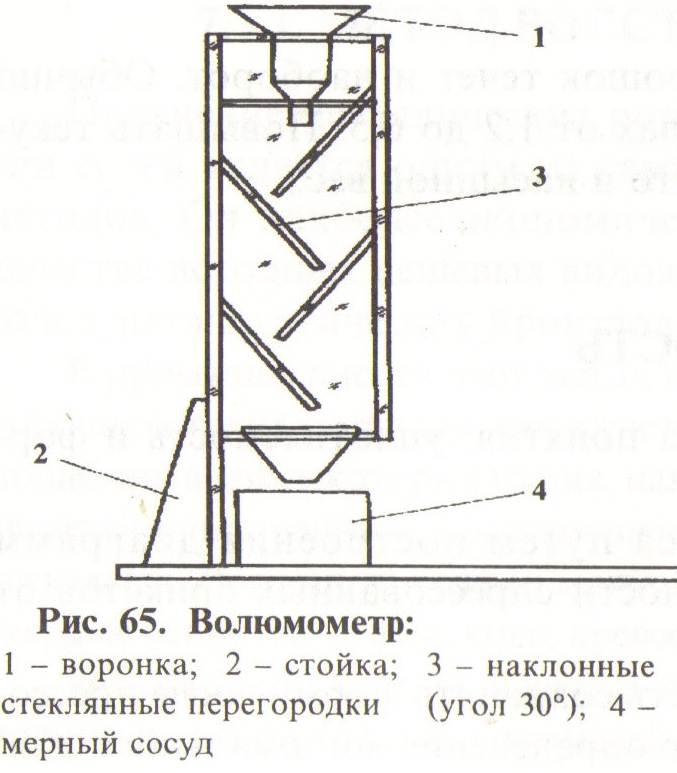 асыпной вес определяется с помощью простого прибора - волюмометра, который представлен на рис. 65.
асыпной вес определяется с помощью простого прибора - волюмометра, который представлен на рис. 65.Через воронку 1 порошок засыпается и попадает в мерный сосуд, объемом примерно 25 см3. Избыток порошка в мерке срезается стеклянной пластинкой и проба взвешивается. Операция повторяется несколько раз и рассчитывается среднее значение.
Наличие неровностей на поверхности частиц затрудняет их перемещение относительно друг друга, поэтому для увеличения насыпного веса производят обкатку в шаровых мельницах или отжиг порошков. Лучше, конечно, регулировать его при изготовлении порошка. Наиболее низким насыпным весом обладают порошки, полученные газовым восстановлением, что связано с развитой формой частиц, наличием внутренних пор в них и большим количеством мелких фракций. В зависимости от того, для каких изделий используются порошки, выбирают нужный насыпной вес. Например, при изготовлении конструкционных силовых деталей, выбирают порошки с высоким насыпным весом, для пористых - с низким.
Кроме обычного насыпного веса применяется и такая характеристика, как насыпной вес утряски, который на 20...50 % выше вследствие лучшей укладки частиц при встряхивании.
7.2.2. ТЕКУЧЕСТЬ ПОРОШКОВ
Текучесть порошка - это его способность быстрее или медленнее вытекать из отверстий под действием силы тяжести. Определяется она как и вязкость жидкости, но выражается отношением навески в граммах ко времени вытекания в секундах. Кроме того, применяют коэффициент текучести
K=trn/F
Где t - время вытекания порошка, с; r - радиус отверстия, мм; F - навеска порошка, r.; n = 2,58.
Чем больше К, тем хуже порошок течет и наоборот. Обычно значения его колеблются в пределах от 1,2 до 6,5. Повышать текучесть можно теми же методами, что и насыпной вес.
7.2.3. ПРЕССУЕМОСТЬ
Прессуемость объединяет два понятия: уплотняемость и формуемость порошка.
Уплотняемость определяется путем построения диаграмм прессования - зависимости плотности спрессованных брикетов от давления прессования.
Формуемость - это способность сохранять форму после прессования. Для ее оценки используют определение минимального давления прессования, при котором спрессованный образец не рассыпается и кромки его устойчивы.
Хуже уплотняются порошки наклепанные и неотожженные, окисленные и газонасыщенные, а также тонкие. Однако и такие порошки, и с развитой формой частиц характеризуются хорошей формуемостью. Но порошки с хорошей формуемостью обладают невысокой уплотня- емостью и наоборот. Чем выше насыпной вес порошка, тем ниже его формуемость.
Так, для получения устойчивых форм из восстановленных порошков требуется давление 2...5 т/см2, соответственно. Перед запуском в производство порошки проверяются по этим показателям.
7.3. ПРОИЗВОДСТВО ПОРОШКОВ
Существуют следующие основные способы получения металлических порошков:
- восстановление оксидов металлов или их солей;
- электролитическое осаждение;
- механическое дробление;
- распыление струи расплавленного металла;
- термическая диссоциация;
- специальные методы.
7.3.1. МЕТОД ВОССТАНОВЛЕНИЯ
Получение металлических порошков восстановлением оксидов или солей является одним из самых древних и распространенных методов. Он наиболее экономичен при условии использования в качестве исходных дешевых видов сырья: непосредственно руд, отходов металлургических производств и др.
В промышленности этот метод широко применяется для получения порошков таких металлов, как железо, медь, никель, кобальт, вольфрам, молибден, а для некоторых из них, например для вольфрама и молибдена, является единственным. Восстановленные порошки хорошо прессуются и спекаются. Восстановителями могут быть водород, СО, природный газ; твердые вещества - сажа, кокс, древесный уголь, щелочные металлы.
Недостатком метода является то, что полученные с его помощью порошки содержат много примесей, в том числе оксиды, карбиды.
7.3.1.1. ФИЗИКО–ХИМИЧЕСКИЕ
ОСНОВЫ ВОССТАНОВЛЕНИЯ
Под восстановлением понимают превращение оксида или соли в элемент или низший оксид (низшую соль). Согласно адсорбцион- но-автокаталитической теории, процесс восстановления складывается из следующих этапов:
- адсорбция газа-восстановителя на поверхности оксидной пленки;
- разрушение кристаллической решетки оксида;
- образование новых оксидных фаз;
- десорбция газообразных продуктов с поверхности частиц.
В общем виде реакцию восстановления можно записать как:
MeOn + mX ↔ Me + XmOn,
где МеО - оксид металла; X - восстановитель; mиn- стехиометрические коэффициенты.
Для смещения процесса вправо, т. е. для восстановления, необходимо, чтобы химическое сродство элемента X к кислороду было больше, чем у металла М. За меру химического сродства к кислороду обычно принимают изменение изобарного термодинамического потенциала ʌG(энергия Гиббса):
ʌG= -A =R T ln Kρ,
где ʌG- максимальная работа реакции при постоянном давлении; R - универсальная газовая постоянная; Т - абсолютная температура; Кρ - константа равновесия.
Чтобы оценить направление реакции, необходимо определить величины ʌG для МеО и ХО. В соответствии с выражением для ʌG запишем:
2Ме + О2 → 2МеО ʌG1= 4,575 lg (Ро2) МеО
2Х + О2 → 2X0 ʌG1= 4,575 lg (Ро2) ХО,
Где (Ро2) Ме0 и (Ро2) хо - упругости диссоциации оксидов МеО и ХО.
Чем выше сродство к кислороду, тем больше понижение термодинамического потенциала, т. е. условием реакции восстановления металла будет ʌG2<ʌG1 или по абсолютной величине |ʌG2| >|ʌG1|.
Металл, у которого сродство с кислородом больше, может восстанавливать металлы с меньшим сродством. Различают восстановление газами, углеродом и металлами.
7.3.1.2. ВОССТАНОВЛЕНИЕ ГАЗАМИ И УГЛЕРОДОМ
Активными газами-восстановителями являются СО и Н2 и различные газы их содержащие.
Восстановление происходит по следующим реакциям:
МеО + Н2 →Ме + Н2О,
МеО + СО →Me + СО2.
По термодинамическим соображениям СО более активен до 800 °С, а Н2 - при более высокой температуре.
Водород используется для восстановления оксидов таких металлов, как Fe, Ni, Сu, Со, W, Мо; окись углерода - для Fe, Сu, Ni.
При восстановлении оксидов в качестве восстановителя часто используется углерод. В противоположность металлам для углерода aGуменьшается с ростом температуры. При высоких температурах углерод применяется для восстановления Fe, Mo, Cr, Nb и др. В реакциях углерода с оксидами почти всегда присутствует и СО, участвующий в восстановлении.
Недостатком восстановления углеродом является возможность науглероживания конечного продукта.
Восстановление оксидов твердым углеродом происходит при температурах выше 900... 1000 °С, так как образования СO2 в этом случае не происходит, т. е. реакция 2СО СO2 + С смещена влево.
Для получения тонких порошков следует применять тонкодисперсные оксиды и низкие температуры восстановления. Использование высоких температур нежелательно еще и тем, что в приповерхностном слое восстанавливаемого порошка образуется плотная корка, затрудняющая диффузию газов. Конечно, понятие низкой температуры здесь относительно, т. е. она должна быть такой, чтобы шла реакция восстановления.
Восстановление обычно проводится в проходных муфельных печах с внешним обогревом муфеля и циркуляцией восстановительной атмосферы в муфелях, в которых помещена шихта.
В последнее время для восстановления вместо водорода применяют конвертированный природный газ, который получается по реакции
СН4 + H2O(пары) → СО + 3Н2.
Конверсия осуществляется при температуре 1 100 °С, а в присутствии специальных катализаторов- при более низкой.
7.3.2. ПОЛУЧЕНИЕ ПОРОШКОВ ЭЛЕКТРОЛИЗОМ
Получение порошков электролизом среди физико-химических методов является одним из наиболее распространенных. Электролитическим осаждением можно получать порошки всех металлов. Важным преимуществом этого метода является высокая чистота продукта за счет очистки от примесей во время электролиза, хотя и следует отметить высокую стоимость порошков из-за низкой производительности и большого расхода электроэнергии. В основе метода лежит разложение водных растворов металлических соединений и расплавленных солей при протекании постоянного тока. Сущность осаждения металлов состоит в разряде металлических ионов на катоде (Mene+ пе). Схематически процесс показан на рис. 66.
И
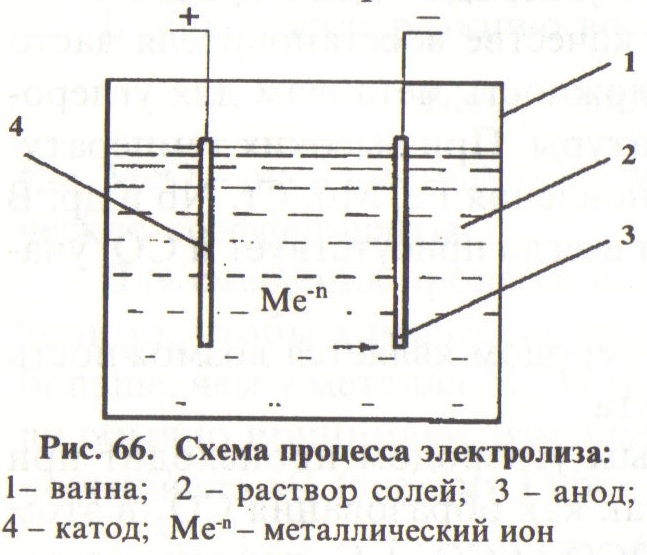 сточником металлических ионов в общем случае является анод, состоящий из металла, подверженного электролизу, и электролит, содержащий соль этого металла. В некоторых случаях анод может быть нерастворимым.
сточником металлических ионов в общем случае является анод, состоящий из металла, подверженного электролизу, и электролит, содержащий соль этого металла. В некоторых случаях анод может быть нерастворимым.Протекание процесса зависит от подвижности ионов, которая обусловлена температурой электролита, вязкостью раствора, размером ионов, скоростью перемешивания. А в общем все характеризуется скоростью диффузии.
В зависимости от условий протекания процесса получают порошки трех видов:
- твердые хрупкие осадки в виде плотных слоев, чешуек или кристаллов;
- губчатые мягкие осадки - мелкие кристаллы, легко поддающиеся растиранию;
- рыхлые (черные) осадки, представляющие собой мелкодисперсные порошки.
Первые два из этих осадков дополнительно подвергаются механическому размолу, рыхлые же в измельчении не нуждаются. Вид осадка в основном зависит от плотности тока:
і = 0,2 К С,
где і - плотность тока, А/см2; С - концентрация электролита, моль/л; К - константа, зависящая от вида солей и находящаяся в пределах 0,5...0,9.
Метод электролиза широко используется для получения легированных порошков путем совместного осаждения компонентов сплава из растворов солей. Этим методом можно получать субмикроскопические порошки с размером зерна 0,01...0,1 мкм, которые применяются для изготовления магнитных и других материалов.
