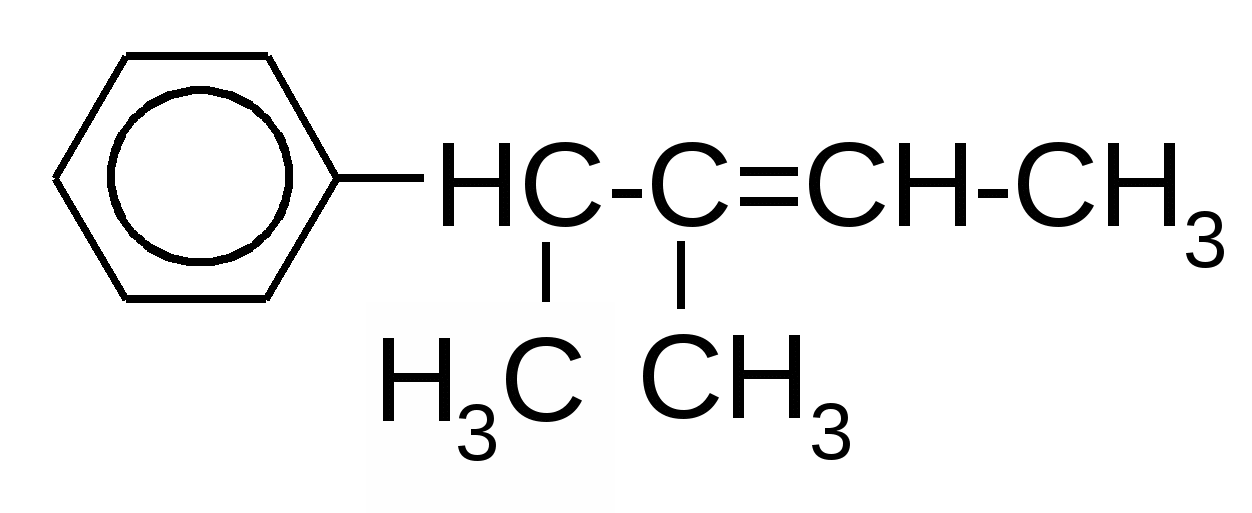Методичка+д\з по химии. Учебнометодическое пособие для практических занятий и самостоятельной работы студентов инженернотехнических направлений подготовки бакалавров всех форм обучения
 Скачать 3.51 Mb. Скачать 3.51 Mb.
|
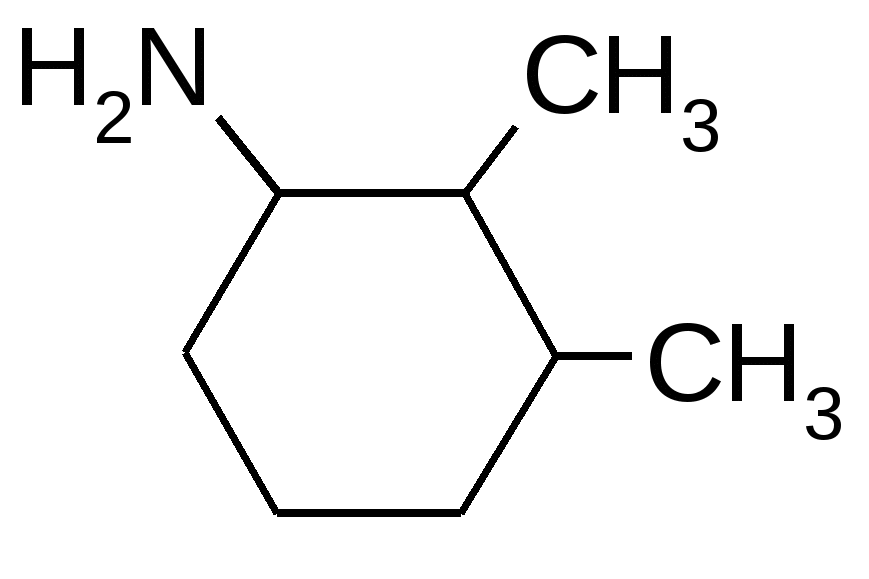
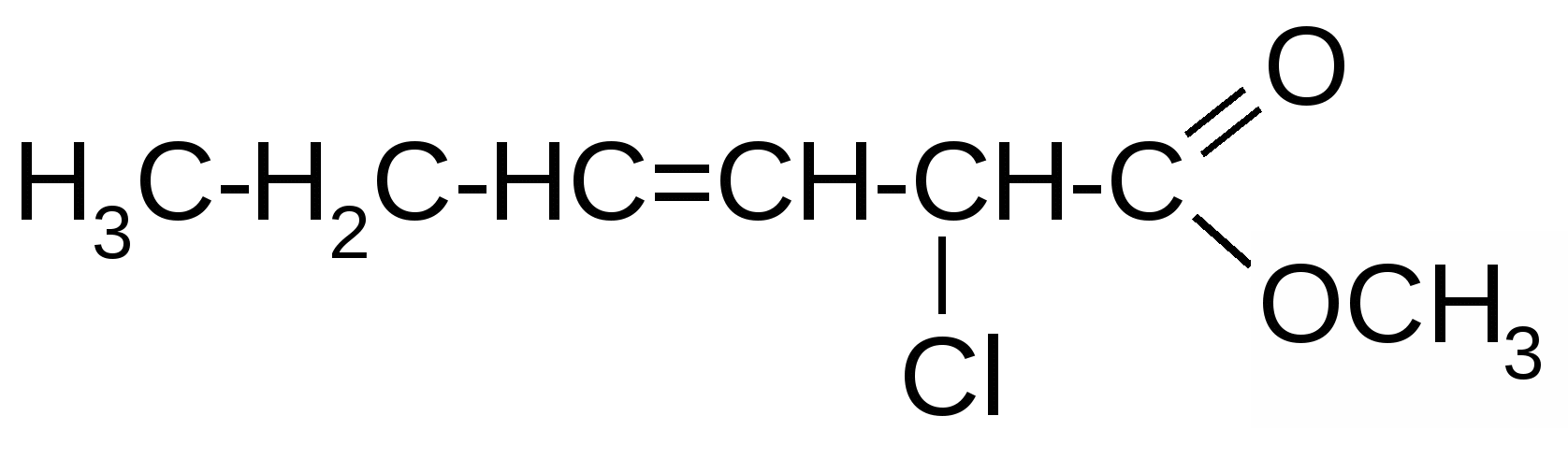
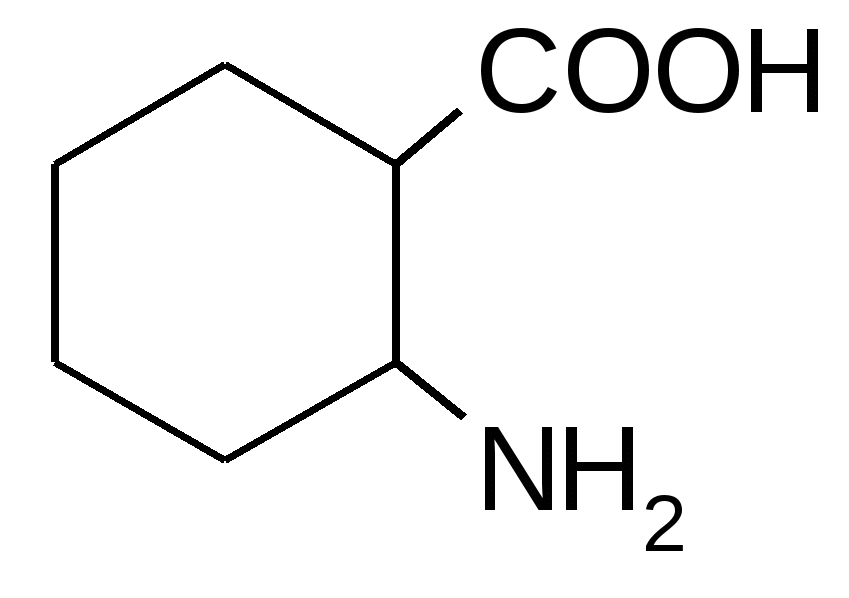
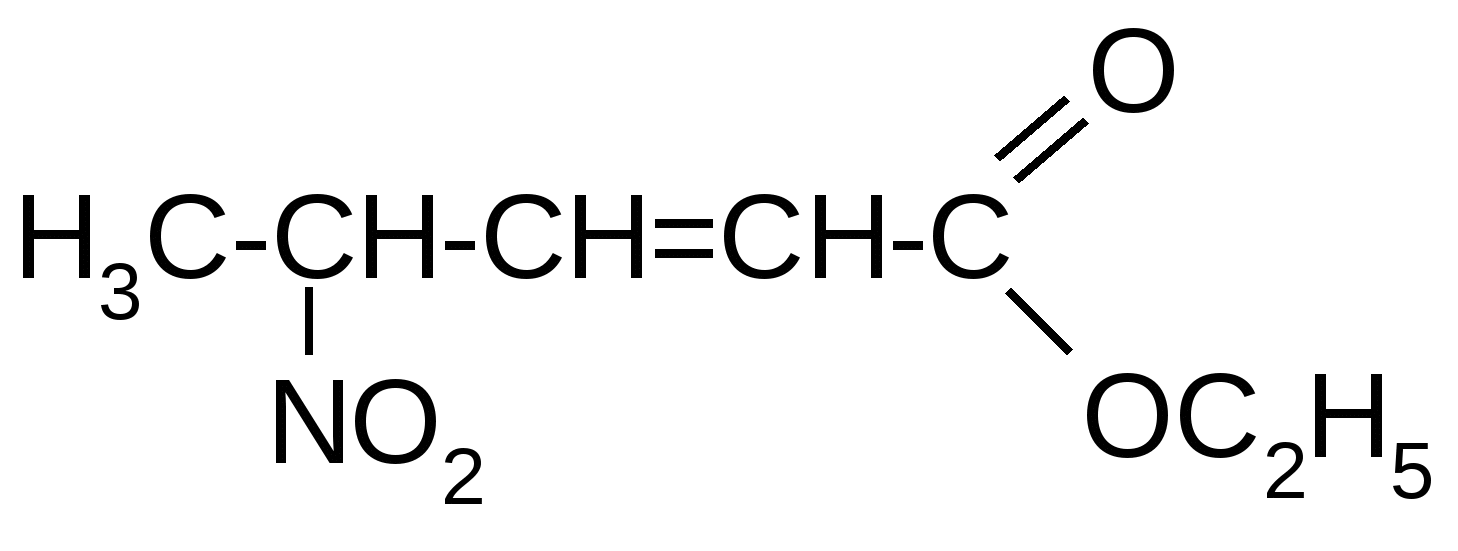
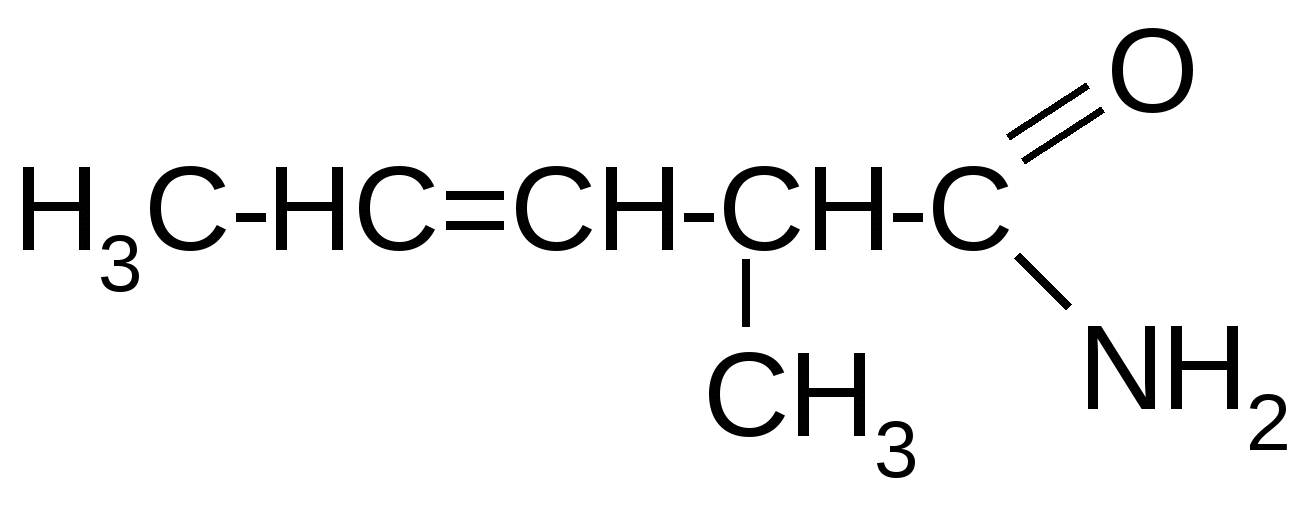
1. Вопросы, которые необходимо изучить и уметь дать на них ответ:1.1. Что представляет собой явление гибридизации атомных орбиталей и почему оно происходит. 1.2. Какова электронно-графическая формула атома углерода в основном и возбужденном состояниях; как обозначаются и простанственно изображаются разные виды гибридизации его атомных орбиталей. 1.3. Какова пространственная направленность гибридизованных орбиталей sp, sp2 и sp3 и какие значения имеют валентные углы между ними. 1.4. Как образуются -связи в молекулах органических соединений, какие орбитали и каким образом перекрываются при их образовании. 1.5. Как образуются -связи, какие орбитали и каким образом перекрываются при их образовании . 1.6. Какие существуют разновидности кратных связей (в зависимости от вида гибридизации орбиталей атомов углерода, их образующих), каковы различия между их прочностью и поляризуемостью. 1.7. Какова сущность явления сопряжения в органических молекулах, в чем заключается различие между - и p,-сопряжением. Уметь изобразить в виде схем различные виды сопряжения, возникающие в молекулах органических соединений. 1.8. Как различаются по степени прочности -, - и сопряженные связи, и с чем это связано. 1.9. Что представляют собой пространственные изомеры, какие существуют разновидности (типы) пространственных изомеров. 1.10. Каковы признаки строения молекулы органического соединения, указывающие на наличие у него геометрических (цис-, транс-) изомеров; чем геометрические изомеры отличаются друг от друга. Уметь привести примеры таких изомеров. 1.11. Каковы признаки строения молекулы органического соединения, указывающие на наличие у него оптических (зеркальных) изомеров; чем оптические изомеры отличаются друг от друга. Уметь привести примеры таких изомеров. 2. Письменное задание для контроля усвоения темы:В таблице 3.52 даны структурные формулы органических соединений. Для данного в Вашем варианте соединения: 2.1. Изобразите в структурном виде его функциональные группы. 2.2. Определите его класс и дайте название по систематической номенклатуре. 2.3. Укажите символами (sp, sp2, sp3) вид гибридизации атомных орбиталей каждого атома углерода, в том числе и в составе углеродсодержащих функциональных групп. 2.4. Для данной молекулы постройте схемы перекрывания атомных орбиталей (с полным изображением всех орбиталей каждого атома): – при образовании одной углерод-углеродной одинарной -связи (по выбору с указанием номеров углеродных атомов); – кратной связи (- и -связей в ней); – связи углерод – гетероатом (С-Х). 2.5. Укажите пространственную направленность гибридизованных орбиталей при образовании -связей в схемах, построенных по п. 2.3 (линейная, тригональная, тетраэдрическая), и значения соответствующих валентных углов. 2.6. Для данного вещества изобразите два геометрических и два оптических изомера; объясните, почему эти виды изомерии в данном случае возможны. Укажите, в чем заключается различие между изображенными Вами каждыми двумя изомерами. Таблица 3.52
Продолжение таблицы 3.52
Комплексное тестовое задание 13 по теме "Химическая связь, строение молекул и пространственная изомерия органических соединений" Правильные ответы по п. А приведены в конце пособия в таблице 4.2. В таблице 3.53 даны органические соединения различных классов. А. Из набора ответов выберите вещество, которое является структурным изомером исходного соединения. Б. Определите, к каким классам органических соединений принадлежат исходное вещество и его изомер, изобразите их структурные формулы. Укажите разновидность данной структурной изомерии и признак, по которому Вы это определили. Определите, какие разновидности пространственной изомерии характерны для исходного соединения. Таблица 3.53 – Тестовое задание 26 (Т-26)
Продолжение таблицы 3.53 – Тестовое задание 26 (Т-26)
Задание 19. Химические свойства и химическая идентификация углеводородов (по разделам стандартов: реакционная способность и химическая идентификация веществ (органических); связь химических свойств со структурой молекул; мономеры) Рекомендуемая литература: [1], гл. 29, § 29.5-29.8; [2], гл. 13, § 13.2; лекции. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||