Коллоквиум по липидам. коллок по липидам (1). Важнейшие липиды тканей человека. Классификация липидов. Характеристика отдельных групп
 Скачать 1.28 Mb. Скачать 1.28 Mb.
|
|
ЛПВП отдают апоЕ- и апоСII-белки на первичные формы ЛПОНП и ХМ, и потом забирают обратно апоСII-белки от остаточных форм. Таким образом, при метаболизме ЛПВП в нем происходит накопление свободного ХС, МАГ, ДАГ, ТАГ, лизоФХ и утрата фосфолипидной оболочки. Функциональные способности ЛПВП снижаются. 6. Далее ЛПВП2 захватывается гепатоцитами при помощи апоА-1-рецептора, происходит эндоцитоз и частица разрушается. 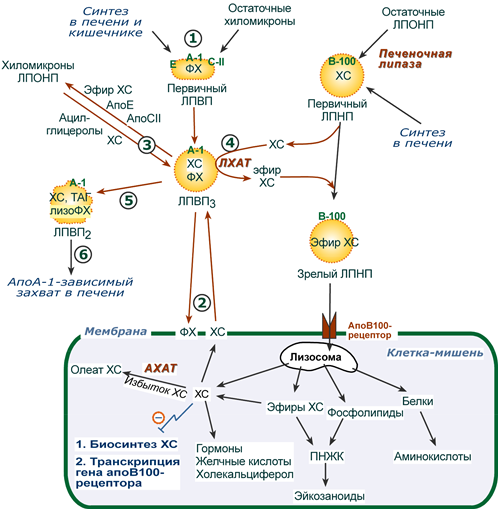 Транспорт холестерола и его эфиров в организме (цифры соответствуют пунктам метаболизма ЛПВП по тексту) Липопротеины низкой плотности Общая характеристика образуются в гепатоцитах de novo и в сосудистой системе печени под воздействием печеночной ТАГ-липазы из ЛПОНП, в составе преобладают холестерол и его эфиры, другую половину массы делят белки и фосфолипиды (38% эфиров ХС, 8% свободного ХС, 25% белки, 22% фосфолипидов, 7% триацилглицеролов), основным апобелком является апоВ-100, нормальное содержание в крови 3,2-4,5 г/л, самые атерогенные. Функция 1. Транспорт холестерола в клетки, использующих его для реакций синтеза половых гормонов (половые железы), глюкокортикоидов и минералокортикоидов (кора надпочечников), для превращения в холекальциферол (кожа), для образования желчных кислот (печень), для выведения в составе желчи (печень). 2. Транспорт полиеновых жирных кислот в виде эфиров ХС в некоторые клетки рыхлой соединительной ткани (фибробласты, тромбоциты, эндотелий, гладкомышечные клетки), в эпителий гломерулярной мембраны почек, в клетки костного мозга, в клетки роговицы глаз, в нейроциты, в базофилы аденогипофиза. Клетки рыхлой соединительной ткани активно синтезируют эйкозаноиды. Поэтому им необходим постоянный приток полиненасыщенных жирных кислот (ПНЖК), что осуществляется через апо-В-100-рецептор, т.е. регулируемым поглощением ЛПНП, которые несут ПНЖК в составе эфиров холестерола. Особенностью клеток, поглощающих ЛПНП, является наличие лизосомальных кислых гидролаз, расщепляющих эфиры ХС. У других клеток таких ферментов нет. Иллюстрацией значимости транспорта ПНЖК в указанные клетки служит ингибирование салицилатами фермента циклооксигеназы, образующей эйкозаноиды из ПНЖК. Салицилаты успешно применяются в кардиологии для подавления синтеза тромбоксанов и снижения тромбообразования, при лихорадке, как жаропонижающее средство за счет расслабления гладких мышц сосудов кожи и повышения теплоотдачи. Однако одним из побочных эффектов тех же салицилатов является подавление синтеза простагландинов в почках и снижение почечного кровобращения. Также в мембраны всех клеток, как сказано выше (см "Метаболизм ЛПВП"), ПНЖК могут переходить в составе фосфолипидов от оболочки ЛПВП. Метаболизм 1. В крови первичные ЛПНП взаимодействуют с ЛПВП, отдавая свободный ХС и получая этерифицированный. В результате в них происходит накопление эфиров ХС, увеличение гидрофобного ядра и "выталкивание" белка апоВ-100 на поверхность частицы. Таким образом, первичный ЛПНП переходит в зрелый. 2. На всех клетках, использующих ЛПНП, имеется высокоафинный рецептор, специфичный к ЛПНП – апоВ-100-рецептор. Около 50% ЛПНП взаимодействует с апоВ-100-рецепторами разных тканей и примерно столько же поглощается гепатоцитами. 3. При взаимодействии ЛПНП с рецептором происходит эндоцитоз липопротеина и его лизосомальный распад на составные части – фосфолипиды, белки (и далее до аминокислот), глицерол, жирные кислоты, холестерол и его эфиры. ХС превращается в гормоны или включается в состав мембран, излишки мембранного ХС удаляются с помощью ЛПВП, принесенные с эфирами ХС ПНЖК используются для синтеза эйкозаноидов или фосфолипидов. при невозможности удалить ХС часть его этерифицируется с олеиновой или линолевой кислотами ферментом ацил-SКоА:холестерол-ацилтрансферазой (АХАТ-реакция), 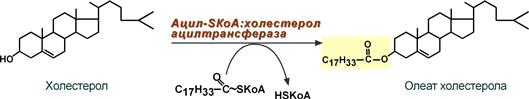 Синтез олеата холестерола при участии ацил-SKoA-холестерол-ацилтрансферазы На количество апоВ-100-рецепторов влияют гормоны: инсулин, тиреоидные и половые гормоны стимулируют синтез этих рецепторов, глюкокортикоиды уменьшают их количество. 15. Ресинтез жиров в кишечнике. Образование и метаболизм хиломикронов. Роль липопротеинлипазы в метаболизме хиломикронов. Регуляция активности этого фермента. В стенке кишечника происходит ресинтез жира Всасывание липидов После расщепления полимерных липидных молекул полученные мономеры всасываются в верхнем отделе тонкого кишечника в начальные 100 см. В норме всасывается 98% пищевых липидов. 1. Короткие жирные кислоты (не более 10 атомов углерода) всасываются и переходят в кровь без каких-либо особенных механизмов. Этот процесс важен для грудных детей, т.к. молоко содержит в основном коротко- и среднецепочечные жирные кислоты. Глицерол тоже всасывается напрямую. 2. Другие продукты переваривания (длинноцепочечные жирные кислоты, холестерол, моноацилглицеролы) образуют с желчными кислотами мицеллы с гидрофильной поверхностью и гидрофобным ядром. Их размеры в 100 раз меньше самых мелких эмульгированных жировых капелек. Через водную фазу мицеллы мигрируют к щеточной каемке слизистой оболочки. Здесь мицеллы распадаются и липидные компоненты диффундируют внутрь клетки, после чего транспортируются в эндоплазматический ретикулум. Желчные кислоты также здесь могут попадать в энтероциты и далее уходить в кровь воротной вены, однако бóльшая их часть остается в химусе и достигает подвздошной кишки, где всасывается при помощи активного транспорта. Ресинтез липидов в энтероцитах Ресинтез липидов – это синтез липидов в стенке кишечника из поступающих сюда экзогенных жиров, иногда могут использоваться и эндогенные жирные кислоты. Основная задача этого процесса – связать поступившие с пищей средне- и длинноцепочечные жирные кислоты со спиртом – глицеролом или холестеролом. Это ликвидирует их детергентное действие на мембраны и позволяет переносить по крови в ткани. Активация жирной кислоты Поступившая в энтероцит (как и в любую другую клетку) жирная кислота обязательно активируется через присоединение коэнзима А. Образовавшийся ацил-SКоА участвует в реакциях синтеза эфиров холестерола, триацилглицеролов и фосфолипидов. 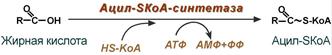 Реакция активации жирной кислоты Ресинтез эфиров холестерола Холестерол этерифицируется с использованием ацил-SКоА и фермента ацил-SКоА:холестерол-ацилтрансферазы (АХАТ). Реэтерификация холестерола напрямую влияет на его всасывание в кровь. В настоящее время ищутся возможности подавления этой реакции для снижения концентрации ХС в крови. 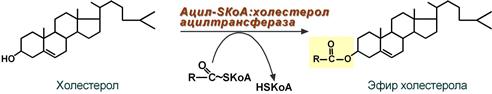 Реакция ресинтеза холестерола Ресинтез триацилглицеролов Для ресинтеза ТАГ есть два пути: Первый путь, основной – 2-моноацилглицеридный – происходит при участии экзогенных 2-МАГ и ЖК в гладком эндоплазматическом ретикулуме энтероцитов: мультиферментный комплекс триацилглицерол-синтазы формирует ТАГ. 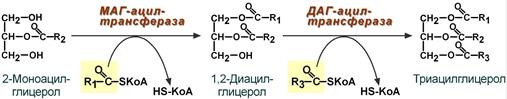 Моноацилглицеридный путь образования ТАГ Поскольку 1/4 часть ТАГ в кишечнике полностью гидролизуется, а глицерол в энтероцитах не задерживается и быстро переходит в кровь, то возникает относительный избыток жирных кислот для которых не хватает глицерола. Поэтому существует второй, глицеролфосфатный, путь в шероховатом эндоплазматическом ретикулуме. Источником глицерол-3-фосфата служит окисление глюкозы. Здесь можно выделить следующие реакции: Образование глицерол-3-фосфата из глюкозы. Превращение глицерол-3-фосфата в фосфатидную кислоту. Превращение фосфатидной кислоты в 1,2-ДАГ. Синтез ТАГ. 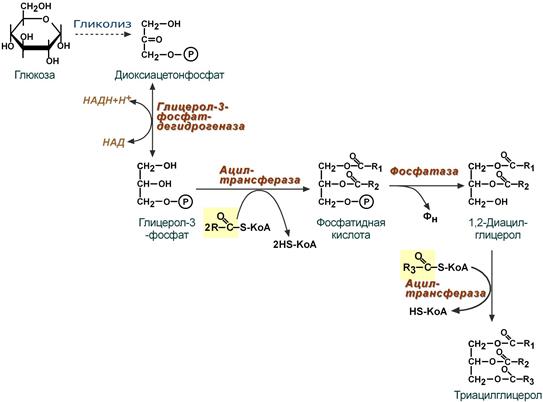 Глицеролфосфатный путь образования ТАГ Ресинтез фосфолипидов Фосфолипиды синтезируются также, как и в остальных клетках организма (см "Cинтез фосфолипидов"). Для этого есть два способа: Первый путь – с использованием 1,2-ДАГ и активных форм холина и этаноламина для синтеза фосфатидилхолина или фосфатидилэтаноламина. 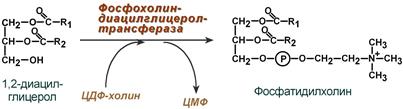 Ресинтез фосфолипидов из ДАГ на примере фосфатидилхолина Второй путь – на основе синтезируемой in situ фосфатидной кислоты. 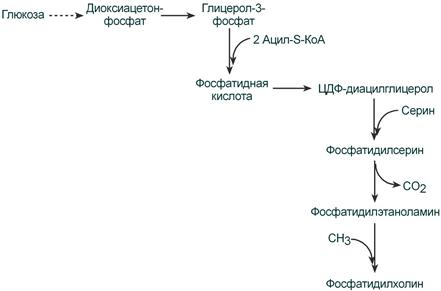 Схема ресинтеза фосфолипидов из фосфатидной кислоты После ресинтеза фосфолипиды, триацилглицеролы, холестерол и его эфиры упаковываются в особые транспортные формы липидов – липопротеины и только в такой форме они способны покинуть энтероцит и транспортироваться в крови. В кишечнике формируются два вида липопротеинов – хиломикроны и липопротеины высокой плотности (ЛПВП), другие типы липопротеинов здесь не образуются. 16. Роль липидов в структурной организации и функционировании мембран. Изменение физико-химических свойств липидного компонента. Роль холестерола. Функции мембранных липидов. Фосфо- и гликолипиды мембран, помимо участия в формировании липидного бислоя, выполняют ряд других функций. Липиды мембран формируют среду для функционирования мембранных белков, принимающих в ней нативную конформацию. Некоторые мембранные липиды – предшественники вторичных посредников при передаче гормональных сигналов. Так фосфатидилинозитолдифосфат под действием фосфолипазы С гидролизируется до диацилглицерола и инозитолтрифосфата, являющихся вторичными посредниками гормонов. Ряд липидов участвует в фиксации заякоренных белков. Примером заякоренного белка является ацетилхолинэстераза, которая фиксируется на постсинаптической мембране к фосфатитилинозитолу. 17. Основные липиды мембраны клетки и их функции. Жидко-кристаллическая мозаичная теория строения биологических мембран. Фосфолипиды составляют основу билипидного слоя клеточных мембран, холестерин — регулятор текучести мембран. ЖИДКОСТНО-МОЗАИЧНАЯ МОДЕЛЬ МЕМБРАН Функционирующие мембраны представляют собой двумерный раствор глобулярных интегральных белков, диспергированных в жидком фосфолипидном матриксе. Жидкостно-мозаичная модель мембранной структуры была предложена в 1972 г. Сингером и Николсоном (рис. 42.9). Первые данные об адекватности этой модели были получены при искусственно индуцированном слиянии двух разных родительских клеток. Оказалось, что при образовании межвидовой гибридной клетки в плазматической мембране происходит быстрое стохастическое перераспределение видоспецифичных белков. Впоследствии  Рис. 42.9. Жидкостно-мозаичная модель мембранной структуры. Основой мембраны является липидный бислой; с ним связаны белки, либо погруженные в бислой, либо присоединенные к цитоплазматической поверхности. Интегральные мембранные белки жестко закреплены в липидном бислое. Некоторые из этих белков пронизывают бислой и называются трансмембранными, другие погружены либо в наружный, либо во внутренний слой. Белки, слабо связанные с внутренней поверхностью мембраны, называются периферическими. Многие белки и липиды несут олигосахаридные цепочки, выступающие во внешнюю среду. было показано, что фосфолипиды тоже способны быстро перераспределяться в плоскости мембраны. Такая диффузия в плоскости мембраны, называемая латеральной, может осуществляться довольно быстро: одна молекула фосфолипида перемещается за 1 с на расстояние несколько микрометров. Фазовые переходы и, следовательно, текучесть мембран сильно зависят от липидного состава мембран. В липидном бислое гидрофобные цепочки жирных кислот ориентированы практически параллельно друг другу, в результате чего образуется достаточно жесткая структура. При повышении температуры гидрофобный слой переходит из упорядоченного состояния в неупорядоченное, и образуется более жидкая, текучая система. Температура, при которой вся структура претерпевает переход из упорядоченного состояния в беспорядочное, называется температурой перехода. Более длинные и более насыщенные жирнокислотные цепи обладают более высокой температурой перехода, т.е. для повышения текучести образованной ими структуры необходима более высокая температура. Наличие ненасыщенных связей в Холестерол играет роль молекулярного модификатора мембран, включение которого приводит к образованию состояний с промежуточной текучестью. Если ацильные боковые цепи находятся в неупорядоченном состоянии, то холестерол вызывает их конденсацию; если же они образуют какую-то кристаллоподобную структуру, то холестерол переводит ее в неупорядоченное состояние. При высоком отношении холестерол/липид фазовый переход вообще не происходит. Текучесть мембраны сильно влияет на ее функционирование. При увеличении текучести мембрана становится более проницаемой для воды и других малых гидрофильных молекул, растет скорость латеральной диффузии интегральных белков. Если активный центр интегрального белка, осуществляющий некую функцию, располагается исключительно в гидрофильной его части, то изменение текучести липидов, вероятно, не скажется слишком сильно на активности белка. Но если белок выполняет транспортную функцию и транспортный компонент пересекает мембрану, то изменения свойств липидной фазы могут привести к значительному изменению скорости транспорта. Превосходным примером является зависимость функционирования инсулинового рецептора от текучести мембран (гл. 51). Когда концентрация ненасыщенных жирных кислот в мембране растет (при культивировании клеток в среде, богатой этими соединениями), увеличивается текучесть, а это приводит к тому, что рецептор связывает больше инсулина. 18. Метаболизм мембран. Активные формы кислорода — активаторы ПОЛ мембран. Показатели ПОЛ. 19. Регуляторы перекисного окисления липидов в клетках. Прооксиданты и антиоксиданты. 20. Механизм переноса веществ через мембраны: простая диффузия, активный транспорт: первичный (Na+/К+-АТФаза), вторичный; экзо- и эндоцитоз. 21. Схема взаимосвязи углеводного и липидного обмена. Образование жиров из глюкозы. Роль пентозофосфатного пути. Печень перекрещивает метаболизм углеводов, липидов и белков Печень, являясь центральным органом метаболизма, участвует в поддержании метаболического гомеостаза и способна осуществлять взаимодействие реакций обмена белков, жиров и углеводов. Местами "соединения" обмена углеводов и белков является пировиноградная кислота, щавелевоуксусная и α-кетоглутаровая кислоты из цикла трикарбоновых кислот, способных в реакциях трансаминирования превращаться, соответственно, в аланин, аспартат и глутамат. Аналогично протекает процесс превращения аминокислот в кетокислоты. С обменом липидов углеводы связаны еще более тесно: образуемые в пентозофосфатном пути молекулы НАДФН используются для синтеза жирных кислот и холестерола, глицеральдегидфосфат, также образуемый в пентозофосфатном пути, включается в гликолиз и превращается в диоксиацетонфосфат, глицерол-3-фосфат, образуемый из диоксиацетонфосфата гликолиза, направляется для синтеза триацилглицеролов. Также для этой цели может быть использован глицеральдегид-3-фосфат, синтезированный в этапе структурных перестроек пентозофосфатного пути, "глюкозный" и "аминокислотный" ацетил-SКоА способен участвовать в синтезе жирных кислот и холестерола.  Взаимосвязь обмена белков, жиров и углеводов Углеводный обмен В гепатоцитах активно протекают процессы углеводного обмена. Благодаря синтезу и распаду гликогена печень поддерживает концентрацию глюкозы в крови. Активный синтез гликогена происходит после приема пищи, когда концентрация глюкозы в крови воротной вены достигает 20 ммоль/л. Запасы гликогена в печени составляют от 30 до 100 г. При кратковременном голодании происходит гликогенолиз, в случае длительного голодания основным источником глюкозы крови является глюконеогенез из аминокислот и глицерина. Печень осуществляет взаимопревращение сахаров, т.е. превращение гексоз (фруктозы, галактозы) в глюкозу. Активные реакции пентозофосфатного пути обеспечивают наработку НАДФН, необходимого для микросомального окисления и синтеза жирных кислот и холестерола из глюкозы. |
