Вирусология. Вирусология ответы. Вопросы к экзамену по дисциплине Вирусология
 Скачать 0.58 Mb. Скачать 0.58 Mb.
|
|
Аденовирусы. Общая характеристика (биологические особенности, классификации). Особенности репликации и важнейшие представители. Adenoviridae(греч. аdenos– железа) – вирусы, выделенные из железистой ткани носоглотки и поражающие у человека верхние дыхательные пути, а нередко и кишечник. Аденовирусы организованы по принципу кубической симметрии и не имеют суперкапсида. Геном представлен линейной молекулой двухнитевой ДНК. Средний диаметр вириона равен 6090 нм. Капсид состоит из 252 капсомеров, 240 из них (гексоны) образуют его грани, 12 (пентоны) полигональные основания и прикреплённые к нему нити. Вирус репродуцируется в ядре, образуя там скопления. Вирус обладает плюрализмом и гемагглютинирующими свойствами. 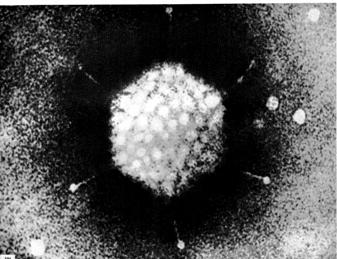 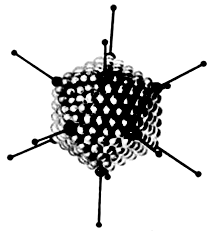 Вид аденовируса при электронной микроскопии (А) (ув. 600000 раз) и его модель (Б) Семейство включает 2 рода: а) Mastadenovirus (греч. mastos- грудь) – вирусы млекопитающих (31 вирус человека и 11 вирусов животных). б) Aviadenovirus (лат. avis- птица) птичьи вирусы (2 вируса кур, 2 – индеек, вирусы уток, гусей и фазанов). Резервуаром и источником инфекции являются больные как с явной, так и со скрытой, а также здоровые носители. Наибольшую опасность представляют больные в остром периоде заболевания, когда аденовирусы в большой концентрации обнаруживаются в носоглоточных смывах, в крови и фекалиях, соскобах пораженной конъюнктивы. Возбудитель выделяется из организма с секретом верхних дыхательных путей или с фекалиями. Восприимчивость людей высокая, особенно у детей раннего возраста. Перенесенная болезнь оставляет типоспецифический иммунитет; возможно повторное заболевание. Аденовирусная инфекция распространена повсеместно, составляет 5– 10% всех вирусных болезней. Заболеваемость регистрируется в течение всего года с подъемом в холодное время. Аденовирусы могут вызывать спорадические случаи заболевания, эпидемические вспышки и даже эпидемии. Возникновение случаев конъюнктивита связывают с перенесенной аденовирусной инфекцией или с заражением вирусом через воду в бассейнах или открытых водоемах. Заболевания у новорожденных и детей раннего возраста протекает по типу кератоконъюнктивита или поражения нижних отделов дыхательных путей. К редким аденовирусным поражениям у детей старшего возраста относят менингоэнцефалиты и геморрагические циститы. Для эпидемических вспышек воздушно-капельной инфекции в Северном полушарии характерна сезонность – зима или ранняя весна, а для фарингоконъюнктивальной лихорадки – лето. Механизм передачи инфекции – воздушно-капельный, но возможен и алиментарный путь заражения – по типу кишечных инфекций. В некоторых случаях передача возбудителя осуществляется через контаминированные предметы внешней среды. Лечение: не существует специфической антивирусной терапии для лечения аденовирусной инфекции, и лечение в основном направлено на устранение симптомов. Методы культивирования вирусов: использование лабораторных животных. Для культивирования вирусов используют культуры клеток, куриные эмбрионы и чувствительных лабораторных животных. Эти же методы используют и для культивирования риккетсий и хламидий — облигатных внутриклеточных бактерий, которые не растут на искусственных питательных средах. Выбор экспериментальных животных определяется целью работы и видовой чувствительностью к изучаемому вирусу. Для заражения используют обезьян, кроликов, морских свинок, хомячков, белых крыс и мышей. Лабораторных животных заражают различными способами в зависимости от тропизма вируса к определенным тканям. Так, например, для культивирования нейротропных вирусов заражение производят преимущественно в мозг (вирусы бешенства, клещевого энцефалита и др.), культивирование респираторных вирусов осуществляется при интраназальном инфицировании животных (вирусы гриппа), дерматотропных (вирус оспы) - путем накожного и внутрикожного заражения. Наиболее часто используются накожное, внутрикожное, внутримышечное, внутрибрюшинное и внутримозговое заражение. При первичном заражении животные могут не заболеть, поэтому через 5-7 дней внешне здоровых животных выводят из эксперимента, а из их органов готовят суспензии, которыми заражают следующие партии животных. Эти последовательные заражения называются «пассажами». Индикацию, т.е. обнаружение факта репликации вируса, устанавливают на основании развития типичных признаков заболевания, патоморфологических изменений органов и тканей животных или положительной реакции гемагглютинации (РГА). РГА основана на способности некоторых вирусов вызывать агглютинацию (склеивание) эритроцитов различных видов животных, птиц и человека за счет поверхностного вирусного белка - гемагглютинина. В настоящее время использование животных для культивирования вирусов ограничено, в соответствии с Европейской конвенцией о защите позвоночных животных, используемых в экспериментальных научных целях. Методы культивирования вирусов: использование куриных эмбрионов. Куриные эмбрионы по сравнению с культурами клеток значительно реже бывают контаминированы вирусами и микоплазмами, а также обладают сравнительно высокой жизнеспособностью и устойчивостью к различным воздействиям. Для получения чистых культур риккетсий, хламидий и ряда вирусов в диагностических целях, а также для приготовления разнообразных препаратов (вакцины, диагностикумы) используют 8—12-дневные куриные эмбрионы. О размножении упомянутых микроорганизмов судят по морфологическим изменениям, выявляемым после вскрытия эмбриона на его оболочках. О репродукции некоторых вирусов, например гриппа, оспы, можно судить по реакции гемагглютинации (РГА) с куриными или другими эритроцитами. К недостаткам данного метода относятся невозможность обнаружения исследуемого микроорганизма без предварительного вскрытия эмбриона, а также наличие в нем большого количества белков и других соединений, затрудняющих последующую очистку риккетсий или вирусов при изготовлении различных препаратов. Медленные вирусные инфекции. Медленные инфекции – это группа инфекционных заболеваний, характеризующиеся длительным инкубационным периодом с последующим прогрессирующим развитием заболевания вплоть до летального исхода. Для медленных вирусных инфекций характерны следующие особенности: длительный инкубационный периодот нескольких месяцев до нескольких лет и даже десятилетий; медленное, прогрессирующее развитие заболевания (без ремиссий); преимущественное поражение ЦНС, приводящее к дегенерации и тяжелому нарушению деятельности мозга; неизбежный смертельный исход. Различают две группы медленных инфекций, отличающихся по этиологии. Возбудителями первой группы заболеваний являются обычные, «канонические» вирусы, а второй группы инфекционные белки, называемые прионами (или же «неканоническими» вирусами). Медленные инфекции, вызываемые при определенных условиях обычными, «каноническими» вирусами, могут развиваться после перенесенных вирусных инфекций, таких как корь, краснуха, клещевой энцефалит, цитомегалия, аденовирусная инфекция, ВИЧ-инфекция и др. Развитию этой группы медленных инфекций способствует внутриутробное инфицирование вирусами и длительное персистирование вирусов в организме, особенно в нейронах и клетках нейроглии. Благодаря особенностям этих клеток, репродукция в них вирусов приобретает искаженный характер, что в конечном итоге приводит к дегенерации и массовой гибели нервных клеток и развитию глубокой патологии мозга. Например, через несколько лет после перенесения кори у детей и подростков может развиться подострый склерозирующий панэнцефалит. Следствием других вирусных инфекций могут явиться подострые энцефалиты, панэнцефалиты и другие тяжелые энцефалопатии. Во всех случаях эти инфекции заканчиваются гибелью больных. Прионные медленные инфекции обнаружены у людей и некоторых видов животных, от которых они могут передаваться алиментарным путем другим животным и, в редких случаях, людям. У животных это болезнь скрепи овец и коз, «бешенство» коров, болезнь норок и др. У людей обнаружено всего пять нозологических форм прионных медленных инфекций, по-видимому их вызывают разные типы прионов. Наиболее известны болезнь Крейцфельда-Якоба и куру. Другие заболевания это фатальная бессонница, синдром Герстмана-Штраусслера-Шейнкера и прогрессирующая энцефалопатия детского возраста (синдром Альперса). Прионные болезни могут быть инфекционными и/или наследственными с аутосомно-доминантным типом передачи. Прион – это нормальный белок наших нервных клеток. Но при мутации в его гене, он становится нейротоксичным, т.е. «ядовитым» для нервных клеток, убивающим их. В норме протеин-прион PrPC находятся в наружных мембранах клеток организма, их особенно много в нейронах. Эти белки принимают участие в межклеточном узнавании, осуществлении синапсов, возможно, в регуляции сна (функции PrPC выяснены не до конца). Инфекционный прионовый белок PrPSc (от англ. scrapie – скрепи) вызывает мутацию гена, кодирующего синтез нормального прионового белка PrPC (от англ. cell – клетка), в результате синтезируется инфекционный прионовый белок PrPSc, отличающийся нарушенной пространственной конфигурацией молекулы(третичной и четвертичной), т.е. являются их изомерами. Прионы обладают чрезвычайной устойчивостью к действию физических и химических факторов. Для их уничтожения необходимо автоклавирование при 134°С в течение 1 часа или обработка 90% раствором фенола. Патогенез прионных инфекций (особенности взаимодействия прионов с клетками). Проникнув в нейрон или глиальную клетку, молекула приона PrPSc контактирует с молекулой нормального белка PrPC и изменяет его конфигурацию, передавая ему свое патогенное состояние. Таким образом, нормальный белок превращается в патологический прион. Этот процесс нарастает в геометрической прогрессии. Патологические прионные белки устойчивы к действию клеточных протеаз, нечувствительны к интерферону. Для прионных болезней характерно образование в нервной ткани вакуолей (окруженных мембраной пузырьков) и амилоидных бляшек (скоплений аномального прионного белка); в итоге постепенно формируется своеобразное губчатое строение ткани мозга («губчатая дегенерация»). Эти изменения постоянно сопровождаются уменьшением числа нейронов различных отделов коры. Характерными клиническими проявлениями прионных медленных инфекций являются: - расстройства чувствительной сферы с выпадением функций органов чувств; - нарушение двигательной сферы вплоть до развития параличей; - различные нарушения психики, такие как депрессия, сонливость, снижение интеллекта с развитием деменции. При развитии клинических проявлений нет ни признаков воспаления, ни биологических аномалий в крови или в энцефалоарахноидальной жидкости, ни тестов, прямых или косвенных, позволяющих уверенно поставить диагноз. Электроэнцефалограмма сомнительна. Клинический диагноз подтверждается только при гистологическом изучении центральной нервной системы. Особенности реакции иммунной системы. Прионные инфекции не индуцируют образование интерферона, не вызывают иммунного ответа организма ни клеточного, ни гуморального. Диагностируют прионную инфекцию на основании клинических симптомов и результатов аутопсии. Разрабатываются лабораторные методы диагностики прионных болезней (ПЦР). К настоящему времени установлено прионное происхождение по крайней мере трех неврологических заболеваний человека. Все они относятся к редким: болезнь Крейтцфельда-Якоба; синдром «фатальной семейной бессонницы»; болезнь Куру. Болезнь Крейтцфельда-Якоба характеризуется медленной прогрессирующей гибелью нейронов. Болезнь проявляется обычно у взрослых и характеризуется быстрым развитием деменции. В мозге пораженных наиболее часто наблюдается атрофия коры головного мозга с губкоподобными изменениями. Заражение происходит при употреблении в пищу мяса коров, больных аналогичным заболеванием. Случаи передачи от человека к человеку были описаны при имплантации внутричерепных электродов, пересадке роговицы и, наиболее часто, при введении гормонов роста, экстрагированных из гипофиза человека. Средний уровень регистрируемой в мире заболеваемости составляет около 0,5-1,0% на 1 млн. жителей. Средняя продолжительность жизни от начала болезни – шесть месяцев. Болезнь Куру – это неврологическое заболевание, которое встречается исключительно среди жителей племен острова Папуа-Новая Гвинея, среди которых до недавнего времени существовал ритуал каннибализма. С момента первого описания этой болезни Гайдузеком и Зигасом в 1957 году до настоящего времени от болезни Куру погибло более 2 500 человек (почти 10% популяции некоторых деревень). Болезнь фактически исчезла с прекращением ритуального каннибализма. Фатальная семейная бессонница – это наследственно обусловленная, неизлечимая болезнь, описана в 1986 году. Встречается очень редко. Имеет аутосомно-доминантный тип наследования. Больной неизбежно умирает от бессонницы. Известно всего 40 семей, поражённых этой болезнью. Болезнь начинается в возрасте от 30 до 60 лет, чаще всего в 50−52. Болезнь продолжается от 7 до 36 месяцев, после чего больной умирает. Выделяют 4 стадии развития болезни. 1. Пациент страдает от всё более тяжёлой бессонницы, панических атак и фобий. Эта стадия длится в среднем 4 месяца. 2. Панические атаки становятся серьёзной проблемой, и к ним присоединяются галлюцинации. Эта стадия длится в среднем 5 месяцев. 3. Полная неспособность спать, сопровождаемая быстрой потерей веса. Эта стадия длится в среднем 3 месяца. 4. Пациент перестаёт говорить и не реагирует на окружающее. Это последняя стадия болезни, длящаяся в среднем 6 месяцев, после чего пациент умирает. К прионным болезням у животных относятся почесуха (скрейпи) у овец и коз, губчатые энцефалопатии у коров («бешенство коров»). Очень важный аспект, связанный с эпидемиологией прионовых инфекций – это безопасность групп риска, соприкасающихся с зараженным материалом животных или больными людьми. К этой группе относятся ветеринарные и медицинские хирурги, патологоанатомы, ветсанэксперты, работники мясоперерабатывающей промышленности и некоторые другие категории лиц, контактирующие с потенциально возможными источниками инфекционного приона. Интерфероны: определение, свойства интерферонов. Интерфероны – вещества, вырабатываемые зараженными клетками-хозяевами в ответ на вирусные или другие чужеродные антигены. Существует множество различных интерферонов, которые имеют многочисленные эффекты, такие как блокировка трансляции и транскрипции вирусной РНК и остановка репликации вируса без нарушения нормальной функции клетки-хозяина. Иногда интерфероны прикрепляются к гликолю полиэтилена (пегилированные соединения), что дает медленное и длительное высвобождение интерферона. Вирусные заболевания, которые можно лечить интерфероном: Хронический гепатит B и хронический гепатитC Генитальные бородавки (остроконечные кондиломы) Саркома Капоши Побочные эффекты от воздействия интерферонов включают лихорадку, озноб, слабость и миалгию, типично начинающиеся спустя 7–12 ч после первой инъекции и длящиеся до 12 ч. Депрессия, а при применении больших доз супрессия костного мозга, также возможны. Наиболее изученным свойством интерферона является его способность препятствовать размножению вирусов. Он образуется в клетках млекопитающих и птиц в ответ на вирусную инфекцию. Методы культивирования вирусов: использование культур клеток. Клеточная культура– система клеток, получаемая из ткани, находящаяся в виде слоя клеток, прикрепленных к стеклу, или в виде суспензии. Наиболее практическое применение получили однослойные культуры первично-трипсинизированных и перевиваемых линий клеток. Сущность методов при приготовлении первичных культур тканей заключается в разрушении межклеточной ткани и разобщения клеток для последующего получения монослоя. Разобщение клеток проводится путём воздействия на ткань протеолитических ферментов (трипсина). Для культивирования культуры клеток применяют синтетические питательные среды – 199, Игла, Хенкса, Эрла (эти среды имеют аминокислоты, витамины, глюкозу, минеральные соли). Смена питательной среды проводится через 2-3 дня. первичные (трипсинизированные) культуры клеток – у которых межклеточные связи разрушают ферментами (трипсином, панкреатином) и получают монослой клеток на стекле. Перевиваемые (стабильные): а) нормальные (ПКБ – почки барана; СОЦ – сердце обезьяны циномольгус); б) опухолевые – Hela– рак шейки матки;Hep–1 – эпидермоидный рак гортани; Дейтройт 6 – костный мозг больного раком легкого. |
