Закон сохранения массы. Закон сохранения массы. Масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции
 Скачать 1.02 Mb. Скачать 1.02 Mb.
|
106 раз больше, чем в химических реакциях, m следует учитывать.Закон сохранения массы. Масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции. Закон сохранения массы является частным случаем общего закона природы – закона сохранения материи и энергии. На основании этого закона химические реакции можно отобразить с помощью химических уравнений, используя химические формулы веществ и стехиометрические коэффициенты, отражающие относительные количества (число молей) участвующих в реакции веществ. Например, реакция горения метана записывается следующим образом: 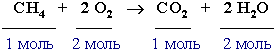 Закон сохранения массы веществ (М.В.Ломоносов, 1748 г.; А.Лавуазье, 1789 г.) Масса всех веществ, вступивших в химическую реакцию, равна массе всех продуктов реакции. Атомно-молекулярное учение этот закон объясняет следующим образом: в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка (т.е. химическое превращение- это процесс разрыва одних связей между атомами и образование других, в результате чего из молекул исходных веществ получаются молекулы продуктов реакции). Поскольку число атомов до и после реакции остается неизменным, то их общая масса также изменяться не должна. Под массой понимали величину, характеризующую количество материи. В начале 20 века формулировка закона сохранения массы подверглась пересмотру в связи с появлением теории относительности (А.Эйнштейн, 1905 г.), согласно которой масса тела зависит от его скорости и, следовательно, характеризует не только количество материи, но и ее движение. Полученная телом энергия E связана с увеличением его массы mсоотношением E = m • c2 , где с - скорость света. Это соотношение не используется в химических реакциях, т.к. 1 кДж энергии соответствует изменению массы на |
| ЗАКОН ПОСТОЯНСТВА СОСТАВА |
| Согласно закону постоянства состава, всякое чистое вещество имеет постоянный состав независимо от способа его получения. Так, оксид кальция можно получить следующими способами: 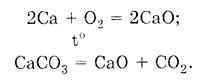 Независимо от того, каким способом получено вещество СаО, оно имеет постоянный состав: один атом кальция и один атом кислорода образуют молекулу оксида кальция СаО. Определяем молярную массу СаО: 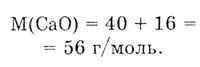 Определяем массовую долю Са по формуле: 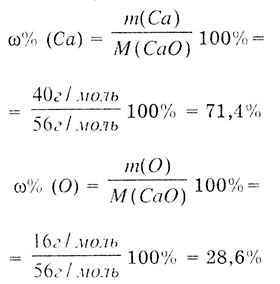 Вывод: В химически чистом оксиде массовая доля кальция всегда составляет 71,4% и кислорода 28,6%. |
Закон кратных отношений
Закон кратных отношений — один из стехиометрических законов химии: если два вещества (простых или сложных) образуют друг с другом более одного соединения, то массы одного вещества, приходящиеся на одну и ту же массу другого вещества, относятся как целые числа, обычно небольшие.
Примеры
1) Состав оксидов азота (в процентах по массе) выражается следующими числами:
| | Закись азота N2O | Окись азота NO | Азотистый ангидрид N2O3 | Двуокись азота NO2 | Азотный ангидрид N2O5 |
| N | 63.7 | 46.7 | 36.8 | 30.4 | 25.9 |
| O | 36.3 | 53.3 | 63.2 | 69.6 | 74.1 |
| Частное O/N | 0.57 | 1.14 | 1.71 | 2.28 | 2.85 |
Разделив числа нижней строки на 0,57, видим, что они относятся как 1:2:3:4:5.
2) Хлористый кальций образует с водой 4 кристаллогидрата, состав которых выражается формулами: CaCl2·H2O, CaCl2·2H2O, CaCl2·4H2O, CaCl2·6H2O, т. е. во всех этих соединениях массы воды, приходящиеся на одну молекулу CaCl2, относятся как 1: 2: 4: 6.
Закон объемных отношений
(Гей-Люссак, 1808 г.)
"Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа".
Следствие. Стехиометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объемных отношениях реагируют или получаются газообразные вещества.
Примеры.
a)
2CO + O2 2CO2
При окислении двух объемов оксида углерода (II) одним объемом кислорода образуется 2 объема углекислого газа, т.е. объем исходной реакционной смеси уменьшается на 1 объем.
b) При синтезе аммиака из элементов:
n2 + 3h2 2nh3
Один объем азота реагирует с тремя объемами водорода; образуется при этом 2 объема аммиака - объем исходной газообразной реакционной массы уменьшится в 2 раза.
Уравнение Клайперона-Менделеева
Если записать объединенный газовый закон для любой массы любого газа, то получается уравнение Клайперона-Менделеева:
pV= (m / M) RT
где m - масса газа; M - молекулярная масса; p - давление; V - объем; T - абсолютная температура (°К); R - универсальная газовая постоянная (8,314 Дж/(моль • К) или 0,082 л атм/(моль • К)).
Для данной массы конкретного газа отношение m / M постоянно, поэтому из уравнения Клайперона-Менделеева получается объединенный газовый закон.
Пример.
Какой объем займет при температуре 17°C и давлении 250 кПа оксид углерода (II) массой 84 г?
Решение.
Количество моль CO равно:
(CO) = m(CO) / M(CO) = 84 / 28 = 3 моль
Объем CO при н.у. составляет
3 • 22,4 л = 67,2 л
Из объединенного газового закона Бойля-Мариотта и Гей-Люссака:
(P • V) / T = (P0 • V0) / T2
Следует
V(CO) = (P0 • T • V0) / (P • T0) = (101,3 • (273 + 17) • 67,2) / (250 • 273) = 28,93 л
Относительная плотность газов показывает, во сколько раз 1 моль одного газа тяжелее (или легче) 1 моля другого газа.
DA(B)=(B)(A) = M(B) / M(A)
Средняя молекулярная масса смеси газов равна общей массе смеси, деленной на общее число молей:
Mср = (m1 +.... + mn) / (1 +.... + n) = (M1 • V1 + .... Mn • Vn) / (1 +.... + n)
ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ: в изолир. системе энергия системы остается постоянной, возможны лишь переходы одного вида энергии в другой. В термодинамике сохранения энергии закону соответствует первое начало термодинамики, к-рое выражается ур-нием Q = DU + W, где Q-кол-во сообщенной системе теплоты, DU-изменение внутр. энергии системы, W - совершенная системой работа. Частный случай сохранения энергии закона-Гесса закон.
Понятие энергии подверглось пересмотру в связи с появлением теории относительности (А. Эйнштейн, 1905): полная энергия E пропорциональна массе т и связана с ней соотношением Е = тс2, где с-скорость света. Поэтому массу можно выражать в единицах энергии и сформулировать более общий закон сохранения массы и энергии: в изо-лир. системе сумма масс и энергии постоянна и возможны лишь превращения в строго эквивалентных соотношениях одних форм энергии в другие и эквивалентно связанные друг с другом изменения массы и энергии.
Закон эквивалентов
вещества взаимодействуют друг с другом в количествах, пропорциональных их эквивалентам. При решении некоторых задач удобнее пользоваться другой формулировкой этого закона: массы (объемы) реагирующих друг с другом веществ пропорциональны их эквивалентным массам (объемам).
эквивалентов: химические элементы соединяются друг с другом в строго определенных количествах, соответствующих их эквивалентам. Математическое выражение закона эквивалентов имеет следующий вид:
Например: некоторое количество металла, эквивалентная масса которого равна 28г/моль, вытесняет из кислоты 0,7 л водорода, измеренного при нормальных условиях. Определить массу металла.
Решение: зная, что эквивалентный объем водорода равен 11,2 л/моль, составляет пропорцию:
28 г металла эквивалентны 11,2 л водорода
х г металла эквивалентны 0,7 л водорода.
Тогда х=0,7*28/11,2= 1,75 г.
Для определения эквивалента или эквивалентной массы необязательно исходить из его соединения с водородом. Их можно определить по составу соединения данного элемента с любым другим, эквивалент которого известен.
Например: при соединении 5,6 г железа с серой образовалось 8,8 г сульфида железа. Нужно найти эквивалентную массу железа и его эквивалент, если известно, что эквивалентная масса серы равна 16 г/моль.
Решение: из условия задачи следует, что в сульфиде железа на 5,6 г железа приходится 8,8-5,6=3,2 г серы. Согласно закону эквивалентов, массы взаимодействующих веществ пропорциональны их эквивалентным массам, то есть
5,6 г железа эквивалентны 3,2 г серы
mэкв (Fе) эквивалентна 16 г/моль серы.
Отсюда следует, что m3KB(Fe) = 5,6*16/3,2=28 г/моль. Эквивалент железа равен: 3=mэкв(Fe)/M(Fe)=28 г/моль:56 г/моль=1/2. Следовательно, эквивалент железа равен 1/2 моля, то есть в 1 моле железа содержится 2 эквивалента.
Закон Авогадро
Следствия закона
Первое следствие из закона Авогадро: один моль любого газа при одинаковых условиях занимает одинаковый объём.
В частности, при нормальных условиях, т. е. при 0 °C (273К) и 101,3 кПа, объём 1 моля газа, равен 22,4 л. Этот объём называют молярным объёмом газа Vm. Пересчитать эту величину на другие температуру и давление можно с помощью уравнения Менделеева-Клапейрона:
Второе следствие из закона Авогадро: молярная масса первого газа равна произведению молярной массы второго газа на относительную плотность первого газа по второму.
Положение это имело громадное значение для развития химии, так как оно дает возможность определять частичный вес тел, способных переходить в газообразное или парообразное состояние. Если через m мы обозначим частичный вес тела, и через d — удельный вес его в парообразном состоянии, то отношение m / d должно быть постоянным для всех тел. Опыт показал, что для всех изученных тел, переходящих в пар без разложения, эта постоянная равна 28,9, если при определении частичного веса исходить из удельного веса воздуха, принимаемого за единицу, но эта постоянная будет равняться 2, если принять за единицу удельный вес водорода. Обозначив эту постоянную, или, что то же, общий всем парам и газам частичный объём через С, мы из формулы имеем с другой стороны m = dC. Так как удельный вес пара определяется легко, то, подставляя значение d в формулу, выводится и неизвестный частичный вес данного тела.
Термохимия
Тепловой эффект химической реакции
Материал из Википедии — свободной энциклопедии
Тепловой эффект химической реакции или изменение энтальпии системы вследствие протекания химической реакции — отнесенное к изменению химической переменной количество теплоты, полученное системой, в которой прошла химическая реакция и продукты реакции приняли температуру реагентов.
Чтобы тепловой эффект являлся величиной, зависящей только от характера протекающей химической реакции, необходимо соблюдение следующих условий:
Реакция должна протекать либо при постоянном объёме Qv(изохорный процесс), либо при постоянном давлении Qp(изобарный процесс).
В системе не совершается никакой работы, кроме возможной при P = const работы расширения.
Если реакцию проводят при стандартных условиях при Т = 298,15 К = 25 ˚С и Р = 1 атм = 101325 Па, тепловой эффект называют стандартным тепловым эффектом реакции или стандартной энтальпией реакции ΔHr
Стандартная энтальпия образования (стандартная теплота образования)
Под стандартной теплотой образования понимают тепловой эффект реакции образования одного моля вещества из простых веществ, его составляющих, находящихся в устойчивыхстандартных состояниях.
Например, стандартная энтальпия образования 1 моль метана из углерода и водорода равна тепловому эффекту реакции:
С(тв) + 2H2(г) = CH4(г) + 76 кДж/моль.
Стандартная энтальпия образования обозначается ΔHf
Энтальпия образования простых веществ принимается равной нулю, причем нулевое значение энтальпии образования относится к агрегатному состоянию, устойчивому при T = 298 K. Например, для йода в кристаллическом состоянии ΔHI2(тв)
Тепловой эффект любой реакции находится как разность между суммой теплот образования всех продуктов и суммой теплот образования всех реагентов в данной реакции (следствиезакона Гесса):
ΔHреакции
Термохимические эффекты можно включать в химические реакции. Химические уравнения в которых указано количество выделившейся или поглощенной теплоты, называются термохимическими уравнениями. Реакции, сопровождающиеcя выделением тепла в окружающую среду имеют отрицательный тепловой эффект и называются экзотермическими. Реакции, сопровождающиеся поглощением тепла имеют положительный тепловой эффект и называются эндотермическими. Тепловой эффект обычно относится к одному молю прореагировавшего исходного вещества, стехиометрический коэффициент которого максимален.
