Значение биохимии в подготовке врача. Биологическая химия
 Скачать 8.33 Mb. Скачать 8.33 Mb.
|
Часть ЦМФ может превращаться в УМФ под действием цитидиндезаминазы и пополнять запасы уридиловых нуклеотидов. 1,2 г у мужчин и 0,6 г у женщин. При подагре без образования тофусов (т.е. подагрических узлов, в которых накапливаются ураты натрия и мочевая кислота) количество уратов возрастает до 2-4 г, а у пациентов с тяжёлой формой болезни, сопровождающейся ростом тофусов, может достигать 30 г.Подагра - распространённое заболевание, в разных странах ею страдают от 0,3 до 1,7% населения. А поскольку сывороточный фонд уратов у мужчин в 2 раза больше, чем у женщин, то они и болеют в 20 раз чаще, чем женщины. Как правило, подагра генетически детерминирована и носит семейный характер. Она вызвана нарушениями в работе ФРДФ синтетазы или ферментов "запасного" пути: гипоксантин-гуанин- или аденинфосфорибозилтрансфераз. К другим характерным проявлениям подагры относят нефропатию, при которой наблюдают образование уратных камней в мочевыводящих путях. 25. Синтез дезоксирибонуклеотидов. Рибонуклеотидредуктазный комплекс. Биосинтез тимидиловых нуклеотидов, роль фолиевой кислоты и фолатредуктазы. Регуляция. Противоопухолевые, антивирусные и антибактериальные препараты как ингибиторы синтеза рибо- и дезоксирибонуклеотидов. Синтез дезоксирибонуклеотидов идёт с заметной скоростью только в тех клетках, которые вступают в S-фазу клеточного цикла и готовятся к синтезу ДНК и делению. В покоящихся клетках дезоксинуклеотиды практически отсутствуют. Все дезоксинуклеотиды, кроме тимидиловых, образуются из рибонуклеотидов путём прямого восстановления ОН-группы у второго углеродного атома рибозы в составе рибонуклеозиддифосфатов до дезоксирибозы. Тимидиловые нуклеотиды синтезируются из dУМФ особым путём с участием N5,N10-метилен-Н4-фолата. Рибонуклеотидредуктазный комплекс Реакцию восстановления НДФ в дезоксипроизводные катализирует рибонуклеотидредук-тазный комплекс, в состав которого входят: собственно рибонуклеотидредуктаза (РНР), белок тиоредоксин и фермент тиоредоксинредуктаза, обеспечивающий регенерацию восстановленной формы тиоредоксина. Рибонуклеотидредуктаза - олигомерный белок, состоящий из двух В1- и двух В2-субъединиц, и содержит негеминовое железо в качестве кофактора. Непосредственным донором водорода в реакции восстановления рибозы служит низкомолекулярный белок тиоредоксин. В рабочую часть этого белка входят 2 SH-группы, которые, отдавая водород, окисляются с образованием дисульфидного мостика. Второй фермент комплекса - тиоредоксинредуктаза - катализирует гидрирование окисленного тиоредоксина с использованием NADPH. При участии комплекса РНР образуются: dАДФ, dГДФ, dУДФ и dЦДФ, которые с помощью НДФ-киназ превращаются в дНТФ, 3 из которых (кроме дУДФ) непосредственно используются в синтезе ДНК. дНДФ + АТФ → дНТФ + АДФ Биосинтез тимидиловых нуклеотидов Тимидин-5'-монофосфат (дТМФ) образуется из дУМФ в реакции, катализируемой тимиди-латсинтазой. Донором метильной группы, появляющейся в 5-положении пиримидинового кольца в молекуле дТМФ, служит кофермент тимидилатсинтазы - N5,N10-метилен-Н4-фолат. С помощью этого кофермента в молекулу дУМФ включается метиленовая группа и восстанавливается в метальную, используя 2 атома водорода от Н4-фолата. Образование субстрата тимидилатсинтазной реакции - дУМФ осуществляется двумя путями: -дефосфорилированием дУДФ; -гидролитическим дезаминированием дЦМФ с помощью дЦМФ дезаминазы. дЦМФ получается при дефосфорилировании дЦДФ - одного из продуктов рибонуклеотидредуктаз-ной реакции. В организме человека это основной путь образования дУМФ. Скорость синтеза дТМФ зависит также от количества второго субстрата тимидилатсинтазной реакции - N5,N10-метилен-Н4-фолата, пополнение запасов которого осуществляется при участии 2 ферментов: дигидрофолатредуктазы, которая с участием NADPH восстанавливает Н2-фолат в Н4-фолат, и серии гидроксиметилтрансферазы, осуществляющей перенос β-гидроксиметиленовой группы серина на Н4-фолат. У человека дТМФ образуется, главным образом, из дЦДФ. Противоопухолевые препараты Синтезировано очень много аналогов дНТФ, которые включаются ДНК полимеразами в ДНК и ингибируют репликацию. К числу мощных противоопухолевых препаратов принадлежит 5-фторурацил (5-FU) - аналог урацила. 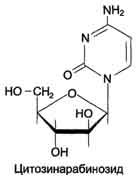 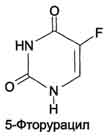 В организме по "запасным" путям 5-FU превращается в 5-Р-УМФ либо в реакции, катализируемой оротатфосфорибозилтрансферазой, либо через промежуточное образование нуклеозида и последующее фосфорилирование. Превращаясь в нуклеозиддифосфат, 5-FU может участвовать в реакции, катализируемой РНР, и восстанавливаться в соответствующее дезоксипроизводное. Под действием фосфатазы 5-Р-дУДФ снова теряет фосфат, и образующийся 5-Р-дУМФ связывается с тимидилатсинтазой и N5, N10-метилен-Н4-фолатом, образуя комплекс, напоминающий промежуточное соединение в реакции превращения дУМФ в дТМФ. Тимидилатсинтаза оказывается полностью блокированной, и синтез дТМФ прекращается: Цитозинарабинозид (или цитарабин)представляет собой соединение, в котором остаток ри-бозы замещён на стериоизомер - арабинозу. Оно используется в химиотерапии рака, в частности, при острой миелоцитарной лейкемии. В организме препарат может превращаться в дНТФ, ингибировать ДНК полимеразы и снижать скорость репликации. Аналоги фолиевой кислоты.В обмене нуклеотидов производные Н4-фолата как доноры од-ноуглеродных групп участвуют в формировании пуринового гетероциклического кольца и в ключевой реакции синтеза дТМФ из дУМФ, катализируемой тимидилатсинтазой. В последнем случае N5,N10-метилен-Н4-фолат служит донором метальной группы и в ходе реакции превращается в Н2-фолат. Для активного синтеза тимидиловых нуклеотидов Н2-фолат должен повторно использоваться, проходя стадию восстановления в Н4-фолат (см. формулу ниже). Метотрексат и аминоптерин - структурные аналоги фолиевой кислоты - ингибируют дигидрофолатредуктазу и таким образом нарушают синтез пуриновых нуклеотидов и превращение дУМФ в дТМФ, снижая внутриклеточную концентрацию субстратов синтеза ДНК и РНК. Препараты широко используют в химиотерапии опухолей. Антивирусные и антибактериальные препараты Азидотимидин (AZT, или зидовидин) представляет собой мощный противовирусный препарат, применяющийся в лечении инфекций, которые сопровождают приобретённые формы иммунодефицита. Будучи структурным аналогом тимиди-на, препарат имеет в З'-положении дезоксирибозы азидогруппу. AZT может фосфорилироваться и с помощью ДНК-полимераз включаться в растущую молекулу ДНК. Однако присутствие в 3'-положении дезоксирибозы азидогруппы делает синтезирующиеся молекулы ДНК не способными к последующему удлинению. В результате образование новых молекул ДНК прекращается. Важно, что фосфорилированные производные AZT утилизируются более эффективно вирусной ДНК-полимеразой или так называемой обратной транскриптазой, чем ДНК-полимеразами эукариотов, поэтому препарат наиболее эффективно влияет на размножение вирусов и, в частности, ретровируса, вызывающего ВИЧ-инфекцию. 5-йоддезоксиуридиниспользуют в терапии кератитов и поражений роговицы глаза вирусом герпеса. Азатиоприн в организме превращается в 6-меркаптопурин, который оказывает мощное иммуносупрессорное действие. Препарат широко используют в трансплантологии для предотвращения развития иммунологических реакций, вызывающих отторжение трансплантата. 26. Первичная структура нуклеиновых кислот. ДНК и РНК – черты сходства и различия состава, локализация в клетке, функции. Вторичная структура ДНК (модель Уотсана и Крика). Связи, стабилизирующие вторичную структуру ДНК. Комплементарность. Правило Чаргаффа. Полярность. Антипараллельность. Первичная структура ДНК - порядок чередования дезоксирибонуклеозидмонофосфатов (дНМФ) в полинукпеотидной цепи. Каждая фосфатная группа в полинукпеотидной цепи, за исключением фосфорного остатка на 5'-конце молекулы, участвует в образовании двух эфирных связей с участием 3'- и 5'-углеродных атомов двух соседних дезоксирибоз, поэтому связь между мономерами обозначают 3', 5'-фосфодиэфирной. Концевые нуклеотиды ДНК различают по структуре: на 5'-конце находится фосфатная группа, а на 3'-конце цепи - свободная ОН-группа. Эти концы называют 5'- и 3'-концами. Линейная последовательность дезоксирибонуклеотидов в полимерной цепи ДНК обычно сокращённо записывают с помощью однобуквенного кода, например -A-G-C-T-T-A-C-A- от 5'- к 3'-концу. В каждом мономере нуклеиновой кислоты присутствует остаток фосфорной кислоты. При рН 7 фосфатная группа полностью ионизирована, поэтому in vivo нуклеиновые кислоты существуют в виде полианионов (имеют множественный отрицательный заряд). Остатки пентоз тоже проявляют гидрофильные свойства. Азотистые основания почти нерастворимы в воде, но некоторые атомы пуринового и пиримидинового циклов способны образовывать водородные связи. Первичная структура РНК - порядок чередования рибонуклеозидмонофосфатов (НМФ) в полинуклеотидной цепи. В РНК, как и в ДНК, нуклеотиды связаны между собой 3',5'-фосфодиэфирными связями. Концы полинуклеотидных цепей РНК неодинаковы. На одном конце находится фосфорилированная ОН-группа 5'-углеродного атома, на другом конце - ОН-группа 3'-углеродного атома рибозы, поэтому концы называют 5'- и 3'-концами цепи РНК. Гидроксильная группа у 2'-углеродного атома рибозы делает молекулу РНК нестабильной. Так, в слабощелочной среде молекулы РНК гидролизуются даже при нормальной температуре, тогда как структура цепи ДНК не изменяется. Сходства: 1.Содержат остатки фосфорной кислоты; 2.Углеводы (рибоза и дезоксирибоза ) находятся в бета-Д-рибофуранозной форме; 3.Биополимеры мономерами, которых являются мононуклеотиды; 4.Содержат по 2 пиримидиновых и по 2 пуриновых оснований. Различия: 1.ДНК-дезоксирибоза, РНК-рибоза; 2.ДНК-тимин, РНК-урацил (Нуклеотид, комплементарный аденину, в РНК не тимин, как в ДНК, а урацил — неметилированная форма тимина) ; 3.ДНК-2 цепочная молекула, РНК- 1 цепочная; 4.Молярная масса молекулы ДНК больше чем РНК. ДНК содержится преимущественно в ядре, но небольшое ее кол-во содер. в митохондриях и пластидах. РНК содер. в ядре и цитоплазме. ДНК содержит генетическую информацию и определяет особенность белков. С помощью ДНК осуществляется передача наследственных особенностей клетки. РНК непосредственно участвует в биосинтезе белка. |
