Значение биохимии в подготовке врача. Биологическая химия
 Скачать 8.33 Mb. Скачать 8.33 Mb.
|
|
Вторичная структура ДНК. В 1953 г. Дж. Уотсоном и Ф. Криком была предложена модель пространственной структуры ДНК. Согласно этой модели, молекула ДНК имеет форму спирали, образованную двумя полинуклеотидными цепями, закрученными относительно друг друга и вокруг общей оси. Двойная спираль правозакрученная, полинуклеотидньхе цепи в ней антипараллельны(рис. 4-6), т.е. если одна из них ориентирована в направлении 3'→5', то вторая - в направлении 5'→3'. Поэтому на каждом из концов молекулы ДНК расположены 5'-конец одной цепи и 3'-конец другой цепи. Молекулы ДНК состоят из двух антипараллельных цепей с комплементарной последовательностью нукпеотидов. Цепи закручены относительно друг друга в правозакрученную спираль так, что на один виток приходится примерно 10 пар нуклеотидов. Все основания цепей ДНК расположены внутри двойной спирали, а пентозофосфатный остов - снаружи. Полинуклеотидные цепи удерживаются относительно друг друга за счёт водородных связей между комплементарными пуриновыми и пиримидиновыми азотистыми основаниями А и Т (две связи) и между G и С (три связи) (рис. 4-7). При таком сочетании каждая пара содержит по три кольца, поэтому общий размер этих пар оснований одинаков по всей длине молекулы. Водородные связи при других сочетаниях оснований в паре возможны, но они значительно слабее. Последовательность нуклеотидов одной цепи полностью комплементарна последовательности нуклеотидов второй цепи. Поэтому, согласно правилу Чаргаффа (Эрвин Чаргафф в 1951 г. установил закономерности в соотношении пуриновых и пиримидиновых оснований в молекуле ДНК), число пуриновых оснований (А + G) равно числу пиримидиновых оснований (Т + С). Комплементарые основания уложены в стопку в сердцевине спирали. Между основаниями двухцепочечной молекулы в стопке возникают гидрофобные взаимодействия, стабилизирующие двойную спираль. Такая структура исключает контакт азотистых остатков с водой, но стопка оснований не может быть абсолютно вертикальной. Пары оснований слегка смещены относительно друг друга. В образованной структуре различают две бороздки - большую, шириной 2,2 нм, и малую, шириной 1,2 нм. Азотистые основания в области большой и малой бороздок взаимодействуют со специфическими белками, участвующими в организации структуры хроматина. Антипараллельность (antiparallel) цепей ДНК: противоположная направленность двух нитей двойной спирали ДНК; одна нить имеет направление от 5' к 3', другая - от 3' к 5'. Каждая цепь ДНК имеет определенную ориентацию. Один конец несет гидроксильную группу (- ОН), присоединенную к 3'-углероду в сахаре дезоксирибозе, на другом конце цепи находится остаток фосфорной кислоты в 5'-положении сахара. Две комплементарные цепи в молекуле ДНК расположены в противоположных направлениях - антипараллельно: одна нить имеет направление от 5' к 3', другая - от 3' к 5'(рис. 43 ). При параллельной ориентации напротив 3'-конца одной цепи находился бы З'-конец другой. Ферменты, синтезирующие новые нити ДНК и называемые ДНК-полимеразами, могут передвигаться вдоль матричных цепей лишь в одном направлении от 3'-конца к 5'-концу. Поэтому в процессе репликации одновременный синтез новых цепей идет антипараллельно. Обе цепи в молекуле ДНК имеют противоположную полярность. Это означает, что межнуклеотидная связь в одной цепи имеет направление 5'–>3', а в другой – 3'–>5'. Подобная направленность цепей имеет важное биологическое значение при репликации и транскрипции молекулы ДНК. Полярность цепи играет важную роль при синтезе ДНК (удлинение цепи возможно только путём присоединения новых нуклеотидов к свободному 3'-концу). 27. Гибридизация нуклеиновых кислот. Денатурация и ренативация ДНК. Гибридизация (ДНК-ДНК, ДНК-РНК). Методы лабораторной диагностики, основанные на гибридизации нуклеиновых кислот. Гибридизация нуклеиновых кислот Вторичная структура нуклеиновых кислот образуется за счёт слабых взаимодействий - водородных и гидрофобных. Поэтому если водный раствор ДНК нагреть до 100 °С, то связи, удерживающие две цепи двойной спирали вместе, разрушаются. В результате разрыва водородных и гидрофобных связей цепи ДНК расходятся. Этот процесс называют "денатурация".Однако если раствор, содержащий денатурированную ДНК, очень медленно охлаждать, то могут получиться двухспиральные структуры, идентичные исходным. Такой процесс получил название "ренативация". На явлении денатурации и ренативации основан метод, называемый "молекулярная гибридизация".Процесс гибридизации может осуществляться между двумя любыми цепями нуклеиновых кислот (ДНК-ДНК, ДНК-РНК) при условии, что они содержат комплементарные последовательности нуклеотидов. Такие гибридные структуры можно выделить центрифугированием в градиенте плотности сахарозы или наблюдать в электронном микроскопе. Если раствор, содержащий образцы ДНК 1 и 2, выделенные из организмов разных видов, денатурировать, а затем провести ренатива-цию, то образуются двухспиральные структуры. Но наряду с исходными ДНК 1 и ДНК 2 образуются гибридные двойные спирали, содержащие цепь ДНК образца 1 и цепь ДНК образца 2, где присутствуют как спирализо-ванные, так и неспирализованные участки. В неспирализованных участках фрагменты цепей ДНК не комплементарны, т.е. в ходе гибридизации получаются несовершенные гибриды. Методом молекулярной гибридизации можно установить: сходство и различие первичной структуры разных образцов нуклеиновых кислот; различие ДНК, выделенных из организмов разных видов; идентичность ДНК всех органов и тканей одного организма. При проведении гибридизации ДНК-РНК были выделены гибридные молекулы, содержащие одну цепь ДНК и одну цепь РНК. Если для эксперимента были взяты ДНК и РНК (первичный транскрипт), выделенные из одного организма, то образовывались совершенные гибриды, потому что молекула РНК комплементарна цепи ДНК. Гибридизацией ДНК-РНК было впервые установлено, что все виды РНК клетки имеют на молекуле ДНК комплементарные участки. 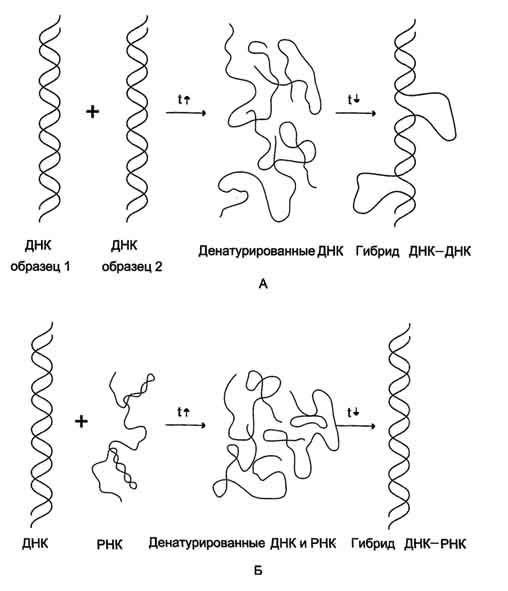 Рис. 4-13. Гибридизация нуклеиновых кислот. А - гибридизация ДНК-ДНК; Б - гибридизация ДНК-РНК. Первоначально классическим методом выявления вирусного генома считался высокоспецифичный метод гибридизации НК, но в настоящее время все шире используется выделение геномов вируса с помощью полимеразной цепной реакции (ПЦР). Молекулярная гибридизация нуклеиновых кислот. Метод основан на гибридизации комплементарных нитей ДНК или РНК с образованием двунитевых структур и на выявлении их с помощью метки. Для этой цели используются специальные ДНК- или РНК-зонды, меченные изотопом (32Р) или биотином, обнаруживающие комплементарные нити ДНК или РНК. Существуют несколько вариантов метода: – точечная гибридизация – выделенную и денатурированную НК наносят на фильтры и затем добавляют меченый зонд; индикация результатов – авторадиография при использовании 32Р или окраска – при авидин-биотине; – блот-гибридизация – метод выделения фрагментов НК, нарезанных рестрикционными эндонуклеазами из суммарной ДНК и перенесенных на нитроцеллюлозные фильтры и тестируемые мечеными зондами; используется как подтверждающий тест при ВИЧ инфекции; – гибридизация in situ – позволяет определять НК в инфицированных клетках [7]. ПЦР основана на принципе естественной репликации ДНК. Суть метода заключается в многократном повторении циклов синтеза (амплификации) вирусспецифической последовательности ДНК с помощью термостабильной Taq ДНК-полимеразы и двух специфических затравок – так называемых праймеров. Каждый цикл состоит из трех стадий с различным температурным режимом. В каждом цикле удваивается число копий синтезируемого участка. Вновь синтезированные фрагменты ДНК служат в качестве матрицы для синтеза новых нитей в следующем цикле амплификации, что позволяет за 25–35 циклов наработать достаточное число копий выбранного участка ДНК для ее определения, как правило, с помощью электрофореза в агарозном геле. Метод высокоспецифичен и очень чувствителен. Он позволяет обнаружить несколько копий вирусной ДНК в исследуемом материале. В последние годы ПЦР находит все более широкое применение для диагностики и мониторинга вирусных инфекций (вирусы гепатитов, герпеса, цитомегалии, папилломы и др.) [8, 9]. Разработан вариант количественной ПЦР, позволяющий определять число копий амплифицированного сайта ДНК. Методика проведения сложна, дорогостояща и пока недостаточно унифицирована для рутинного применения. 28. Третичная структура ДНК. Роль гистоновых и негистоновых белков в компактизации ДНК. Организация хроматина. Ковалентная модификация гистонов и ее роль в регуляции структуры и активности хроматина. Каждая молекула ДНК упакована в отдельную хромосому. В диплоидных клетках человека содержится 46 хромосом.Общая длина ДНК всех хромосом клетки составляет 1,74 м, но она упакована в ядре, диаметр которого в миллионы раз меньше. Чтобы расположить ДНК в ядре клетки, должна быть сформирована очень компактная структура. Компактизация и суперспирализация ДНК осуществляются с помощью разнообразных белков, взаимодействующих с определёнными последовательностями в структуре ДНК. Все связывающиеся с ДНК эукариотов белки можно разделить на 2 группы: гисгоновые и негистоновые белки.Комплекс белков с ядерной ДНК клеток называют хроматином. Гистоны- белки с молекулярной массой 11-21 кД, содержащие много остатков аргинина и лизина. Благодаря положительному заряду гистоны образуют ионные связи с отрицательно заряженными фосфатными группами, расположенными на внешней стороне двойной спирали ДНК. Существует 5 типов гистонов. Четыре гистона Н2А, Н2В, НЗ и Н4 образуют октамерный белковый комплекс (Н2А, Н2В, НЗ, Н4)2, который называют "нуклеосомный кор"(от англ. nucleosome core). Молекула ДНК "накручивается" на поверхность гистонового октамера, совершая 1,75 оборота (около 146 пар нуклеоти-дов). Такой комплекс гистоновых белков с ДНК служит основной структурной единицей хроматина, её называют "нуклеосома".ДНК, связывающую нуклеосомные частицы, называют линкерной ДНК. В среднем линкерная ДНК составляет 60 пар нуклеотидных остатков. Молекулы гистона H1 связываются с ДНК в межнуклеосомных участках (линкерных последовательностях) и защищают эти участки от действия нуклеаз. В ядре каждой клетки присутствует около 60 млн молекул каждого типа гистонов, а общая масса гистонов примерно равна содержанию ДНК. Аминокислотные остатки лизина, аргинина и концевые аминогруппы гистонов могут модифицироваться: ацетилироваться, фосфорилироваться, метилироваться или взаимодействовать с белком убиквитином (негистоновый белок). Модификации бывают обратимыми и необратимыми, они изменяют заряд и конформацию гистонов, а это влияет на взаимодействие гистонов между собой и с ДНК. Активность ферментов, ответственных за модификации, регулируется и зависит от стадии клеточного цикла. Модификации делают возможными конформационные перестройки хроматина. Негистоновые белки хроматина В ядре эукариотической клетки присутствуют сотни самых разнообразных ДНК-связывающих негистоновых белков. Каждый белок комплементарен определённой последовательности нуклео-тидов ДНК (сайт ДНК).К этой группе относят семейство сайт-специфических белков типа "цинковые пальцы. Каждый "цинковый палец" узнаёт определённый сайт, состоящий из 5 нуклеотидных пар. Другое семейство сайт-специфических белков - гомодимеры. Фрагмент такого белка, контактирующий с ДНК, имеет структуру "спираль-поворот-спираль". К группе структурных и регуляторных белков, которые постоянно ассоциированы с хроматином, относят белки высокой подвижности (HMG-белки- от англ, high mobility gel proteins). Они имеют молекулярную массу менее 30 кД и характеризуются высоким содержанием заряженных аминокислот. Благодаря небольшой молекулярной массе HMG-белки обладают высокой подвижностью при электрофорезе в полиакриламидном геле. К негистоновым белкам принадлежат также ферменты репликации, транскрипции и репарации. При участии структурных, регуляторных белков и ферментов, участвующих в синтезе ДНК и РНК, нить нуклео-сом преобразуется в высококонденсированный комплекс белков и ДНК. Образованная структура в 10 000 раз короче исходной молекулы ДНК. 29. Репликация. Принципы репликации ДНК. Стадии репликации. Инициация. Белки и ферменты, принимающие участие в формировании репликативной вилки. Живые организмы в течение S-фазы клеточного цикла, которая предшествует делению клетки, удваивают содержание ДНК таким образом, что каждая дочерняя клетка после деления получает набор хромосом, идентичный родительской клетке. Процесс удвоения хромосом называют репликацией (редупликацией). Хромосома содержит одну непрерывную двухцепочечную молекулу ДНК. При репликации каждая цепь родительской двухцепочеч-ной ДНК служит матрицей для синтеза новой комплементарной цепи. Вновь образованная двойная спираль имеет одну исходную (родительскую) и одну вновь синтезированную (дочернюю) цепь. Такой механизм удвоения ДНК получил название"полуконсервативная репликация". Репликацию можно разделить на 4 этапа: образование репликативной вилки (инициация), синтез новых цепей (элонгация), исключение праймеров, завершение синтеза двух дочерних цепей ДНК (терминация). Инициация репликации Синтез ДНК у эукариотов происходит в S-фазу клеточного цикла. Инициацию репликации регулируют специфические сигнальные белковые молекулы - факторы роста.Факторы роста связываются рецепторами мембран клеток, которые передают сигнал, побуждающий клетку к началу репликации. В определённом сайте (точка начала репликации)происходит локальная денатурация ДНК, цепи расходятся и образуются две репликативные вилки,движущиеся в противоположных направлениях. В образовании репликативной вилки принимает участие ряд белков и ферментов. Так, семейство ДНК-топоизомераз (I, II и III), обладая нуклеазной активностью, участвует в регуляции суперспирализации ДНК. Например, ДНК-топоизомераза I разрывает фосфоэфирную связь в одной из цепей двойной спирали и ковалентно присоединяется к 5'-концу в точке разрыва. По окончании формирования репликативной вилки фермент ликвидирует разрыв в цепи и отделяется от ДНК. Разрыв водородных связей в двухцепочечной молекуле ДНК осуществляет ДНК-хеликаза. Фермент ДНК-хеликаза использует энергию АТФ для расплетения двойной спирали ДНК. В результате происходит раскручивание участка суперспирализованной молекулы ДНК. В поддержании этого участка ДНК в раскрученном состоянии участвуют SSB-белки. SSB-белки, не закрывая азотистых оснований, связываются с одноцепочечной ДНК по всей длине разделившихся цепей и таким образом предотвращают их комплементарное скручивание и образование "шпилек". Они обладают большим сродством к одноцепочечным участкам ДНК, независимо от первичной структуры цепей. 30. Элонгация и терминация репликации. Ферменты. Асимметричный синтез ДНК. Фрагменты Оказаки. Роль ДНК-лигазы в формировании непрерывной и отстающей цепи. синтез новых цепей (элонгация), исключение праймеров, завершение синтеза двух дочерних цепей ДНК (терминация). Репликация ДНК осуществляется ДНК-зависимыми ДНК-полимеразами Субстратами и источниками энергии для синтеза продукта служат 4 макроэргических соединения - дезоксирибонуклеозидтрифосфаты дАТФ, дГТФ, дЦТФ и дТТФ, для активации которых необходимы ионы магния. Нейтрализуя отрицательный заряд нуклеотидов, они повышают их реакционную способность. Ферменты проявляют каталитическую активность только в присутствии предварительно раскрученной матричной двухцепочечной ДНК. Синтез цепей ДНК происходит в направлении 5'→3' растущей цепи, т.е. очередной нуклеотид присоединяется к свободному 3'-ОН-концу предшествующего нуклеотид-ного остатка. Синтезируемая цепь всегда антипараллельна матричной цепи. В ходе репликации образуются 2 дочерние цепи, представляющие собой копии матричных цепей. 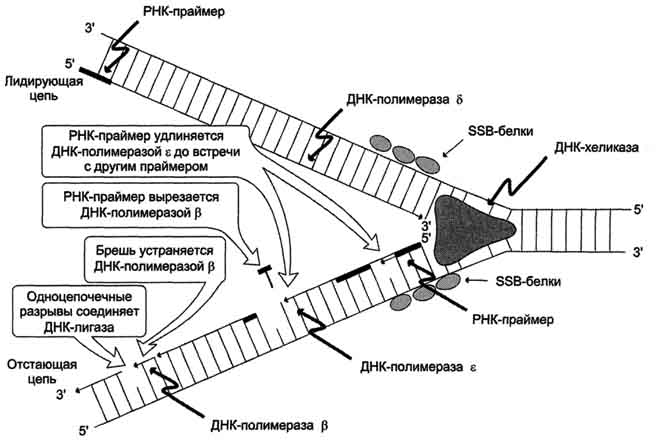 В синтезе эукариотических ДНК принимают участие 5 ДНК-полимераз (α, β, γ, δ, ε). ДНК-полимеразы α, β, δ, ε участвуют в синтезе ДНК в ядре клеток, ДНК-полимераза γ - в репликации митохондриальной ДНК. ДНК-полимеразы β, δ, ε не могут инициировать образование дочерних цепей, так как не имеют сродства к одиночной нити ДНК. Инициирует репликацию ДНК-полимераза α, которая комплементарна определённому сайту одноцепо-чечной ДНК. Присоединяясь к нему, ДНК-полимераза а синтезирует небольшой фрагмент РНК – праймер. ДНК-полимераза а состоит из четырёх субъединиц. Каждая из субъединиц фермента выполняет определённую функцию: "узнавание" сайта репликации, синтез праймера (8-10 рибо-нуклеотидов), синтез фрагмента цепи ДНК, около 50 дезоксирибонуклеотидов. Таким образом, ДНК-полимераза α синтезирует олигонуклеотид, содержащий примерно 60 нуклеотидных остатков; первые 8-10 представлены рибонуклеотида-ми (праймер), а остальные - дезоксирибонуклеотидами. ДНК-полимераза δ – олигонуклеотид, синтезированный ДНК-полимеразой α и образующий небольшой двухцепочечный фрагмент с матрицей, позволяет присоединиться ДНК-полимеразе δ и продолжить синтез новой цепи в направлении от 5'- к 3'-концу по ходу раскручивания репликативной вилки. ДНК-полимераза δ последовательно наращивает цепь, шаг за шагом присоединяя к ней соответствующие дезоксинуклеотиды. Выбор ДНК-полимеразой δ очередного нуклеотида определяется матрицей. Включение дезоксирибонуклеозидмонофосфатов в растущую цепь ДНК сопровождается гидролизом макроэргических связей соответствующих нуклеозидтрифосфатов и отщеплением пирофосфата (Н4Р2О7). Энергия макроэргических связей расходуется на образование 3',5'-фосфодиэфирной связи между последним нуклеотидом растущей цепи ДНК и присоединяемым нуклеотидом. В каждой репликативной вилке идёт одновременно синтез двух новых (дочерних) цепей. Направление синтеза цепи ДНК совпадает с направлением движения репликативной вилки лишь для одной из вновь синтезируемых цепей (лидирующая цепь). На второй матричной цепи синтез дочерней ДНК осуществляется двумя ферментами: ДНК-полимеразой α и ДНК-полимеразой ε в направлении 5'→3', но против движения репликативной вилки. Поэтому вторая цепь синтезируется прерывисто, короткими фрагментами, которые называют "фрагменты Оказаки" (по имени открывшего их исследователя). Дочерняя цепь ДНК, синтез которой происходит фрагментами, называют отстающей цепью. Каждый фрагмент Оказаки, примерно 100 нуклеотидных остатков, содержит праймер. Праймеры удаляет ДНК-полимераза β, постепенно отщепляя с 3'-конца фрагмента по одному ри-бонуклеотиду. К ОН-группе на 3'-конце предыдущего фрагмента ДНК-полимераза β присоединяет дезоксирибонуклеотиды в количестве, равном вырезанному праймеру и таким образом заполняет брешь, возникающую при удалении рибонуклеотидов. Фермент ДНК-лигаза катализирует образование фосфодиэфирной связи между 3'-ОН-группой дезоксирибозы одного фрагмента цепи ДНК и 5'-фосфатом следующего фрагмента. Реакция протекает с затратой энергии АТФ. Таким образом, из множества фрагментов Оказаки образуется непрерывная цепь ДНК. |
