науч менд. Перечень экзаменационных вопросов по дисциплине Менеджмент научных исследований
 Скачать 311.61 Kb. Скачать 311.61 Kb.
|
|
Перечень экзаменационных вопросов по дисциплине «Менеджмент научных исследований» Основы национального и международного права в области научных исследований. Принцип свободы научных исследований нашел свое подтверждение в различных по своей юридической силе источниках международного права, относящихся к тем или иным его отраслям - космическому, морскому, экологическому, информационному. Международно-правовое закрепление свободы научных исследований придает рассматриваемому принципу универсальное значение. Свобода как принципиальная константа научных исследований имеет многообразные измерения - правовое и этическое, субъективное и объективное. Как представляется, прогресс науки и технологии предполагает прогресс в свободе деятельности, представляющей собой осуществление научных исследований и технических разработок. Именно в условиях свободы возможна реализация планов исследователей, а также выработка новых знаний. Порядок и принципы этического регулирования исследований в области здравоохранения. Принципы этической оценки клинических исследований. Основные принципы этической экспертизы, реализуемой этическим комитетом, научных исследований на людях включают в себя: • оценку и минимизацию рисков; • оценку ожидаемой пользы, • анализ соотношения риска и пользы; • рассмотрение информированного согласия и процесса его получения, подбора испытуемых и их стимулирования к участию в исследованиях Этические принципы проведения медицинских исследований с участием человека в качестве субъекта. (Этические принципы- совокупность требований, нравственно орентирующих деятельность в области здоровья человека. Право пациента на выбор (Autonomy) - больной имеет право выбирать лечение или отказываться от него. Польза для больного (Beneficence)- врач действует только в интересах больного. Главный принцип - не навредить (Non-maleficence)Справедливое распределение медицинских ресурсов Соблюдение достоинства пациента Правдивость и честность (Truthfulness and honesty) информированное согласие пациента. Основные принципы Хельсинкской Декларации. - Долг врачей, участвующих в медицинских исследованиях, — защита жизни, здоровья, достоинства, целостности, права на самоопределение, права на личную жизнь и конфиденциальности личной информации участника исследования. -Медицинские исследования с участием человека должны соответствовать общепринятым научным принципам и основываться на максимальном знании научной литературы, других соответствующих источников информации, на результатах соответствующим образом проведенных лабораторных исследований, а также, где применимо, исследований на животных. Необходимо также проявлять гуманность в отношении животных, используемых в исследовании. -Особое внимание необходимо уделять при проведении исследований, которые могут негативно воздействовать на окружающую среду. -Долг врачей, участвующих в медицинских исследованиях, — защита жизни, здоровья, достоинства, целостности, права на самоопределение, права на личную жизнь и конфиденциальности личной информации участника исследования. - Медицинские исследования с участием человека должны соответствовать общепринятым научным принципам и основываться на максимальном знании научной литературы, других соответствующих источников информации, на результатах соответствующим образом проведенных лабораторных исследований, а также, где применимо, исследований на животных. Необходимо также проявлять гуманность в отношении животных, используемых в исследовании. - Особое внимание необходимо уделять при проведении исследований, которые могут негативно воздействовать на окружающую среду. Базовые принципы клинических исследований в Belmont report. 3 базовых принципа медицинских исследований – Автономия (уважение к личности) – Благодеяние («не навреди») – Справедливость (равное распределение затрат и выгод) Автономность – Уважение к решению человека относительно участия в испытании – Исследователи должны предоставить потенциальному участнику полную информацию об исследовании, чтобы помочь принять информированное решение • Благодеяние – Субъект должен получить пользу, или, хотя бы, не получить вред – Польза должна превышать риск • Справедливость – Защита подгрупп пациентов, особенно уязвимые популяции, от несправедливого таргетирования или взятия на себя бремени исследования, которое будет преимуществом для других – Равенство и справедливый отбор субъектов Стандарт GCP РК. Надлежащая клиническая практика (Good Clinical Practice (GCP)) - стандарт клинических исследований/испытаний с участием человека в качестве испытуемого, охватывающий планирование, проведение, завершение, проверку, анализ результатов, составление отчетов и ведение документации. Данный стандарт обеспечивает научную значимость исследований/испытаний, их этическую приемлемость и полную документированность клинических характеристик изучаемого лекарственного средства, доверие к полученным результатам, а также их признаваемость уполномоченными органами других стран. Международные стандарты при проведении научных исследований в сфере здравоохранения (GCP); Надлежащая клиническая практика . «Надлежащая клиническая практика» (Good Сlinical Рractice, GCP) понимают стандарт клинических исследований, охватывающий планирование, проведение, завершение, проверку, анализ результатов, составление отчетов и ведение документации, который обеспечивает научную значимость исследований, их этическую приемлемость и полную документированность клинических характеристик изучаемого лекарственного препарата. Международные стандарты при проведении научных исследований в сфере здравоохранения (GLP); Надлежащая лабораторная практика. Надлежащая лабораторная практика, GLP (англ. good laboratory practice) — система норм, правил и указаний, направленных на обеспечение согласованности и достоверности результатов лабораторных исследований. Главная задача GLP — обеспечить возможность полного прослеживания и восстановления всего хода исследования. GLP устанавливает очень строгие требования к ведению и хранению документации — значительно более жесткие, чем европейские стандарты Сферы применения норм GLP устанавливаются законодательно. В первую очередь это относится к разработке новых химических веществ, получению и использованию токсичных веществ и к здравоохранению. Международные стандарты при проведении научных исследований в сфере здравоохранения (GMP); Надлежащая производственная практика. Надлежащая производственная практика, GMP (англ. good manufacturing practice) — правила, которые устанавливают требования к организации производства и контроля качества лекарственных средств для медицинского и ветеринарного применения. Правила не распространяются на вопросы охраны труда персонала, занятого в производстве, на обеспечение промышленной безопасности, пожарной безопасности, взрывобезопасности, химической безопасности, санитарно-гигиенической безопасности и иной безопасности при производстве лекарственных средств, а также не затрагивают вопросы охраны окружающей среды Комиссия по вопросам этики. Состав. Функции. . Комиссия осуществляет свою деятельность в соответствии с Положением о комиссии, стандартными операционными процедурами, соблюдает требования настоящего стандарта и законодательства Республики Казахстан. Состав комиссии и Положение о комиссии утверждаются первым руководителем клинической базы. - Комиссия по вопросам этики защищает права, безопасность и здоровье испытуемых, при этом особое внимание уделяется уязвимым испытуемым. -Комиссия оценивает соответствие квалификации исследователя на основании его научной биографии и/или другой соответствующей документации. - Комиссия, в случаях, когда согласие на участие испытуемого в исследовании/испытании, дает его законный представитель, требует, чтобы предоставленный протокол и/или другая документация соответствовали этическим нормам и законодательству Республики Казахстан требованиям для таких исследований/испытаний. -Комиссия рассматривает размер и порядок выплат испытуемому. Размер выплат испытуемому определяется до начала исследования/испытания и не зависит от того, завершил испытуемый исследование/испытание полностью или нет. 11. Клинические исследования: Роль и обязанности исследовательской команды. Клинические исследования (КИ) ранних фаз заслуженно считаются исследованиями повышенного риска, а научная ценность получаемых данных о профиле безопасности и фармакологических свойствах исследуемого препарата (ИП) особенно высока, так как определяется дальнейшая судьба новой молекулы.Исследователь занимается научными, методологическими и методическими вопросами исследования, разрабатывает его план, набирает команду, анализирует результаты и готовит отчет. При большом объеме работы исследователь может делегировать часть своих функций ассистенту.Модератор проводит беседу, его задача — ознакомить участников с целями проведения фокус-групп и постоянно направлять обсуждение в нужное русло. Если респондент неверно истолковал цель своего присутствия, это затрудняет формулировку его собственного мнения, провоцирует к искажению мнения, подталкивает к достижению взаимного согласования точек зрения. Некоторые исследователи рекомендуют учитывать пол модератора при комплектовании команды, поручая женщинам проводить дискуссии в женских группах, а мужчинам — в мужских. Ассистент модератора концентрируется на мероприятиях, не связанных с исследованием напрямую: подготовкой помещения для дискуссии, табличек с именами участников, необходимого оборудования, обеспечением прохладительными напитками, подготовкой рекламных материалов, размещением респондентов, сменой кассет, вручением сувениров или денежного вознаграждения и др. Рекрутер в соответствии с заданными исследователем критериями занимается набором респондентов для участия в дискуссии. В ходе подготовки команды проводится ее тренинг с учетом специфики изучаемого целевого рынка. Формулировка вопросов должна отражать специфические задачи организации обсуждения; соответствующие группы вопросов: 1 . Ознакомительные помогают представиться респондентам и получить предварительную информацию насчет их осведомленности о предмете обсуждения. 2. Вводные позволяют участникам взглянуть на обсуждаемую тему более широко, выясняют отношение участников к данной теме. 3. Основные касаются поведения, мотивации людей и являются предметом анализа. 4. Уточняющие позволяют вернуться к обсуждаемой теме, проверить правильность высказывания, конкретизировать высказывания с помощью фактов (например, вопросы-воспоминания помогают вернуть респондента к определенным событиям, пережитому опыту). 5. Заключительные обобщают мнения о теме дискуссии, о характере обсуждения и о незатронутых аспектах проблемы. Формулировки вопросов проверяются по критериям восприятия их на слух: • длина, количество слов; • однозначность восприятия слов различными участниками. Формулировки вопросов не должны содержать ответов на них или предварительных оценок поведения. Процедура получения информированного согласия. Информированное согласие - это документ, подробно оговаривающий все аспекты лечения и диагностики, который подписывается пациентом и гарантирует добровольное согласие пациента на получение конкретного метода лечения и диагностики. Правило информированного согласия призвано обеспечить уважительное отношение к пациентам или испытуемым в биомедицинских экспериментах как к личностям, а также, разумеется, минимизировать угрозу их здоровью, социально-психологическому благополучию и моральным ценностям вследствие недобросовестных или безответственных действий специалистов. Каковы цели применения в медицинской практике и биомедицинских исследованиях правила информированного согласия? Согласно Бичампу и Чилдресу, их три: 1. Обеспечить уважительное отношение к пациенту или испытуемому в биомедицинском исследовании как к автономной личности, которая вправе осуществлять свободный выбор и контролировать все процедуры или действия, осуществляемые в процессе лечения или научного исследования с его телом 2. Минимизировать возможность морального или материального ущерба, который может быть причинен пациенту вследствие недобросовестного лечения или экспериментирования. 3. Создать условия, способствующие повышению чувства ответственности медицинских работников и исследователей за моральное и физическое благополучие пациентов и испытуемых. Для обстоятельного обсуждения правила информированного согласия удобно использовать предложенное Бичампом и Чилдресом теоретическое разложение данного принципа на составляющие элементы. С этой точки зрения структура правила имеет следующий вид: 1. "Пороговые" элементы (предварительные условия):а) компетентность пациента (в смысле понимания и принятия решения), б) добровольность принятия решения". 2. Информационные элементы:а) процедура передачи существенной информации, б) предложение рекомендаций (планов действия), в) акт понимания. 3. Элементы согласия:а) принятие решения (в пользу некоторого плана), б) авторизация (определенного плана). Формы информированного согласия. Требования к ИС. Общие требования к информированному согласию При обращении за информированным согласием каждому участнику исследования следует предоставить следующую информацию. 1. Объяснение содержащейся в исследовании научной части и целей исследования. Ожидаемая продолжительность участия в исследовании. Описание последующих процедур; и указание всех процедур, которые являются экспериментальными. 2. Описание всех предсказуемых рисков и неудобств, которым могут подвергнуться участники исследования. 3. Описание пользы для участников исследования или для кого-либо еще, получение которой можно ожидать из исследования. 4. Раскрытие информации о процедурах, соответствующих альтернативным курсам лечения, если таковые имеются, которые могут оказаться полезными для участников исследования. 5. Объяснение, описывающее степень, если таковая имеется, с которой будет поддерживаться конфиденциальность записи информации об участнике исследования. 6. Для исследований, несущих риски выше минимального, разъяснения о возможном предоставлении какой-либо компенсации и о возможном проведении каких-либо медицинских процедур, в случае, если будет нанесен ущерб, и, если да, то в чем они будут состоять и где можно получить дополнительную информацию. 7. Объяснение, к кому обратиться за ответами на соответствующие вопросы об исследовании и правах участников исследования и к кому обратиться в случае нанесения ущерба в ходе исследования. 8. Объяснение того, что участие является добровольным, отказ от участия не будет приводить к штрафным санкциям или потере выгод, на которые участник исследования имеет право, а также объяснение того, что участник исследования может прекратить участие в любое время без штрафных санкций или потери выгод, на которые он имеет право Защита прав уязвимых групп населения. Помимо удовлетворения основных потребностей в медицинской помощи особое внимание следует уделять защите и просвещению уязвимых групп населения, в частности детей, молодежи, женщин, коренных народов и беднейших слоев населения, что является необходимым условием для обеспечения устойчивого развития. Особое внимание необходимо уделить потребностям пожилых людей и инвалидов в медицинском обслуживании. Общая цель защиты уязвимых групп населения заключается в том, чтобы каждый представитель такой группы имел возможность полностью развить свои возможности (включая здоровое физическое, умственное и духовное развитие); обеспечить, чтобы молодежь могла вести здоровый образ жизни; позволить женщинам играть ключевую роль в обществе и оказывать поддержку коренным народам, предоставив им возможности в области образования и экономического и технического развития. Требования к исследованиям на животных. Существует ряд международных документов, регламентирующих проведение исследований и экспериментов на животных. Одним из основных такого рода документов являются «Международные рекомендации по проведению биомедицинских исследований с использованием животных», разработанные и принятые Международным Советом Медицинских Научных Обществ (CIOMS). Основные положения: 2)необходимо использовать минимально возможное количество животных; 3)следование таким этическим нормам, как должная забота о животных и избегание или минимизация дискомфорта, дистресса, боли; 4)если после эксперимента животное обречено на страдания, хронические боли или тяжелые увечья, то его следует безболезненно умертвить. 5)необходимо использование анестетических, анальгетических и седативных болеутоляющих средств; 6)если по условиям эксперимента требуется обходиться без таких средств, то эксперимент можно проводить только после обязательного одобрения этического комитета; Поиск и привлечение грантов отечественных и зарубежных фондов грантодателей Глава 2. Порядок привлечения грантов 7. Мероприятия по подготовке, оценке, предварительному отбору проектов осуществляются исполнительными агентствами. 8. Уполномоченный орган осуществляет методическое руководство, координацию работ по отбору, оценке и мониторингу реализации проектов, а также обращается в установленном порядке к донорам по вопросам привлечения грантов. 9. Уполномоченный орган осуществляет переговорный процесс с донорами по вопросам предоставления грантов, проводит работу в установленном порядке по подготовке, согласованию и подписанию рамочных соглашений о финансовом и техническом сотрудничестве между Правительством Республики Казахстан и донорами. 12. Для принятия уполномоченным органом заявки на рассмотрение необходимо: 1) соответствие заявленных проектов приоритетам социально- экономического развития Республики Казахстан, отраженным в индикативном плане социально-экономического развития Республики Казахстан; 2) наличие логического обоснования проекта и документации по проекту в соответствии с требованиями уполномоченного органа; 3) наличие отраслевого заключения соответствующего центрального исполнительного органа в случае предоставления заявки местным исполнительным органом; 4) в случае подачи исполнительным агентством нескольких заявок на соответствующий период, ранжирование заявляемых проектов по приоритетности. 14. Уполномоченный орган проводит отбор и оценку заявленных проектов, на основании которой формирует список приоритетных на соответствующий период проектов для направления на рассмотрение донорам, а в случае связанных грантов - в Республиканскую бюджетную комиссию (далее - Бюджетная комиссия). 16. При одобрении заявки на предоставление связанного гранта Бюджетной комиссией уполномоченный орган направляет соответствующий запрос донору. 17. В случае одобрения проекта донором уполномоченный орган извещает исполнительное агентство о необходимости проведения работ по подготовке и согласованию соглашения о гранте. 18. Привлечение связанных грантов осуществляется на основании решения Правительства Республики Казахстан по каждому отдельному соглашению о гранте с указанием суммы гранта и необходимых объемов софинансирования из республиканского бюджета. Научные и исследовательские программы по источникам финансирования. Для развития фундаментальных и приоритетных прикладных исследований, сохранения и развития научного потенциала предусматривается выделение средств республиканского бюджета. Финансирование научных исследований осуществляется на основе программно-целевого принципа. Государственный заказ на проведение приоритетных научных исследований может размещаться в государственных и негосударственных научных учреждениях, прошедших соответственно аттестацию либо аккредитацию, на конкурсной основе согласно программно- целевому принципу. Программно-целевое финансирование осуществляется для: фундаментальных научных исследований; приоритетных прикладных научных исследований; стратегических направлений исследований, отвечающих интересам национальной безопасности и независимости республики; государственных целевых научно-технических программ по приоритетным направлениям развития науки, техники и технологии; проведения исследований в рамках международных программ. Государство осуществляет развитие государственной научной инфраструктуры и сохранение уникальных научно-технических объектов и может субсидировать приобретение научного оборудования для научных организаций. Программно-целевое финансирование научных исследований и научно-технических программ осуществляется на конкурсной основе с обязательным проведением государственной научной и научно-технической экспертизы предлагаемых программ и результатов научных исследований. Финансирование прикладных научных исследований может осуществляться за счет заемных средств. Написание научных проектов и грантовых заявок. Переход отечественной науки на рыночные отношения и развитие конкурентной среды в сфере научных исследований заставляет научные организации и самих ученых менять свое отношение к процессу привлечения бюджетных и внебюджетных средств и значительно повышает ответственность всех заинтересованных лиц за качество реализуемых научных программ. Для привлечения финансирования на научные исследования все субъекты научной деятельности должны постоянно осуществлять поиск и привлечение средств. При этом основным инструментом получения финансовых средств на воплощение научных идей и замыслов является написание научных проектов и подача заявок в уполномоченные органы и фонды - грантодатели. В этой связи, наиболее важной компетенцией для научного работника в современных условиях становится умение написания проектов и подготовки заявок на конкурсы идей и проектов различного уровня (международный, национальный) и характера (научные, инновационные). При этом качество научных проектов напрямую определяет успешность прохождения заявки через конкурсные процедуры. Формальное отношение к процедуре подачи заявок на выделение бюджетных средств как это было раньше - в бытность государственного содержания организаций науки - в современных условиях становится неприемлемым. Выведенные в самостоятельное плавание (получив статус коммерческих организаций - предприятий на праве хозяйственного ведения и акционерных обществ) организации науки вынуждены конкурировать и выживать, и именно выигрышность заявок на реализацию научных проектов напрямую определяет возможность стабильного существования организаций науки и реализации всех творческих замыслов и идей научных сотрудников. Классификация клинических исследований. Клинические исследования — это исследования, организованные для оценки различных вмешательств, условия проведения которых направлены на устранение влияния систематических ошибок на результаты. 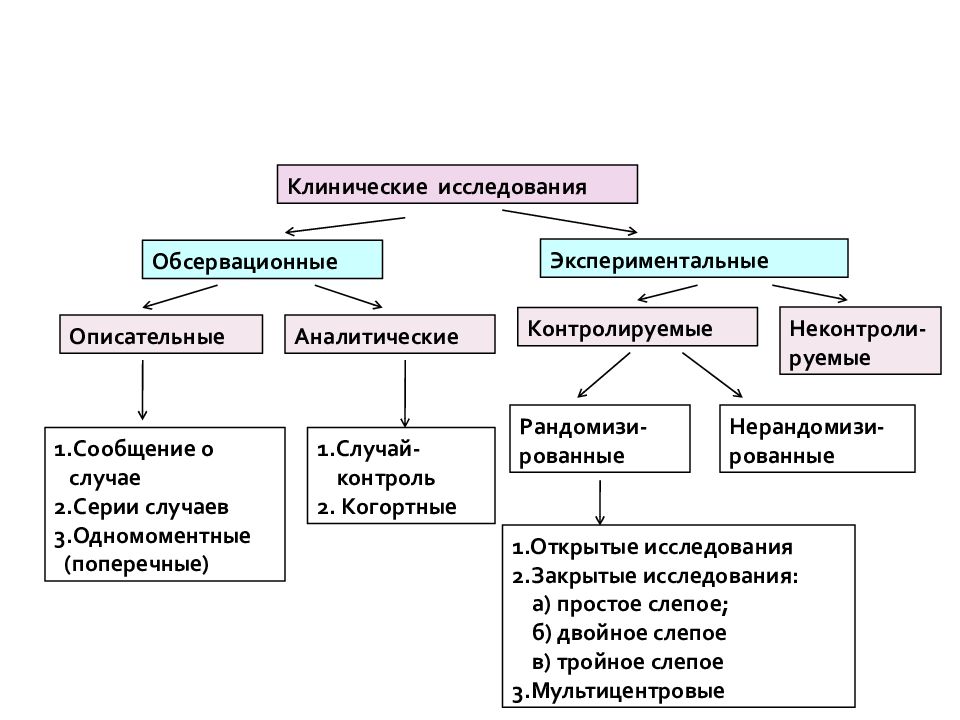 Методология исследований. Исследования в медицинском образовании. Методология науки — это учение о методах и процедурах научной деятель‐ ности. Методология делится на содержательную и формальную. Содержательная методология включает изучение законов, теорий, структуры научного знания, критериев научности и системы используемых методов исследования. Формаль‐ ная методология связана с анализом методов исследования с точки зрения логи‐ ческой структуры и формализованных подходов к построению теоретического знания, его истинности и аргументированности. В методологии выделяют следующую структуру: основания методологии (философия, логика, системология, психология, ин‐ форматика, системный анализ, этика); характеристики деятельности (особенности, принципы, условия, нормы); логическая структура деятельности (субъект, объект, предмет, формы, сред‐ ства, методы, результат деятельности, решение задач); временная структура деятельности (фазы, стадии, этапы). технология выполнения работ и решения задач (средства, методы, способы, приемы). Методология исследований включает: выбор темы исследования, формулирование проблемы, целей и задач; разработку теоретической основы исследования; формулировку гипотезы исследования; разработку дизайна и плана исследования; определение исследуемой генеральной совокупности, формирование выборки из нее; определение методов сбора данных; анализ полученных результатов. 21.Методология исследований. Описательные исследования. Методология - это логическая организация деятельности человека состоящая в определении цели и предмета исследования, подходов и ориентиров в его ведении, выборе средств и методов, определяющих наилучший результат. Любая деятельность человека характеризуется методологией. Но в исследовательской деятельности методология играет решающую роль в успехе. Цель исследования заключается в поиске наиболее эффективных вариантов строения системы управления и организации ее функционирования и развития. Исследования делятся на наблюдения(описательные, аналитические) и экспериментальные(клинич. испытания) Описательное исследование — маркетинговое исследование, направленное на описание маркетинговых проблем, ситуаций, рынков, например демографической ситуации, отношения потребителей к продукции компании. При проведении данного вида исследований обычно ищутся ответы на вопросы, начинающиеся со слов: Кто, Что, Где, Когда и Как. Как правило, такая информация содержится во вторичных данных или собирается путем проведения наблюдений и опросов, постановки экспериментов. Например, исследуется, кто является потребителем продукции фирмы. Что рассматривается как продукты, поставляемые фирмой на рынок. Где рассматривается как места, где потребители приобретают эти продукты. Когда характеризует время, когда потребители наиболее активно покупают эти продукты. Как характеризует способ использования приобретенного продукта. Заметим, что данные исследования не дают ответа на вопросы, начинающиеся со слова «почему». (Почему возрос объем продаж после проведения рекламной кампании?) Ответы на подобные вопросы получают при проведении казуальных исследований. 22.Методология исследований. Аналитические исследования. Аналитические эпидемиологические исследования применяют с целью установить причинные связи между заболеваниями и различными факторами риска (профессиональными, социально-бытовыми, окружающей среды, генетическими и др.), а также для оценки эффективности профилактических и лечебных вмешательств. Аналитическое исследование – это «самый углубленный вид социологического анализа, ставящего своей целью не только описание структурных элементов изучаемого явления, но и выяснение причин, которые лежат в его основе и обуславливают характер, распространенность, остроту и другие свойственные ему черты». Этот вид исследований очень часто используется на практике. Если в ходе описательного исследования устанавливается связь между характеристиками изучаемого явления, то в ходе аналитического исследования определяется, имеет ли обнаруженная связь причинный характер. При проведении аналитического исследования обычно используется комплекс методов сбора информации. Так, дополняя друг друга, применяются различные формы опроса, анализа документов, наблюдения. 23.Методология исследований. Экспериментальные исследования. Наиболее важной составной частью научных исследований являются эксперименты. Это один из основных способов получить новые научные знания. Более 2/3 всех трудовых ресурсов науки затрачивается на эксперименты. В основе экспериментального исследования лежит эксперимент, представляющий собой научно поставленный опыт или наблюдение явления в точно учитываемых условиях, позволяющих следить за его ходом, управлять им, воссоздавать его каждый раз при повторении этих условий. От обычного, обыденного, пассивного наблюдения эксперимент отличается активным воздействием исследователя на изучаемое явление. Основной целью эксперимента является проверка теоретических положений (подтверждение рабочей гипотезы), а также более широкое и глубокое изучение темы научного исследования. Эксперимент должен быть проведен по возможности в кратчайший срок с минимальными затратами при самом высоком качестве полученных результатов. Различают эксперименты естественные и искусственные. Естественные эксперименты характерны при изучении социальных явлений (социальный эксперимент) в обстановке, например, производства, быта и т. п. Искусственные эксперименты широко применяются во многих естественнонаучных исследованиях. В этом случае изучают явления, изолированные до требуемой степени, чтобы оценить их в количественном и качественном отношениях. 24.Виды исследования в медицине. Панельные исследования в медицине и общественном здравоохранении. Панельные исследования (панель) — это форма опроса, предполагающая повторяющийся сбор данных в одной и той же группе людей на одну и ту же тему через равные промежутки времени с целью контроля происходящих изменений в поведении потребителей под воздействием внешней среды. Частота повторяемости опроса, а также общая продолжительность исследования могут быть различными и зависят от сущности исследуемых процессов. Данный метод сбора информации достаточно точен благодаря опросу большого числа респондентов. Накопление данных — дорогостоящий процесс, поэтому исследования целесообразны только при условии, что их результаты востребованы на коммерческой основе широким кругом клиентов. Собственно «панелью» является группа респондентов, которая представляет собой репрезентативную выборку объектов генеральной совокупности и регулярно (за вознаграждение) заполняет опросные листы о своих покупках. На основе изучения поведения этой группы пытаются выяснить покупательские привычки, правила совершения покупок, основные тенденции в предпочтениях потребителей. Панельные исследования классифицируются по нескольким признакам: продолжительность, предмет исследования, используемые методы коммуникации. Панельные исследования классифицируются по нескольким признакам: По продолжительности:краткосрочные; долгосрочные По характеру предмета исследования:общие;специализированные По используемым методам коммуникации:почта;интервью;анкетирование Краткосрочные панели работают в течение полугода-года. Долгосрочные панели рассчитаны на срок до пяти лет. 25.Виды исследования в медицине. Исследования тренда в медицине и общественном здравоохранении. Исследование тренда (trend study, от англ. trend – тенденция) – эпидемиологическое обсервационное продольное исследование, осуществляемое в рамках единой генеральной совокупности (популяции) в течение некоторого периода времени и имеющее целью выявление и анализ изменений, происходящих в изучаемой совокупности. Для оценки изменений во времени данное исследование должно состоять из нескольких (минимум двух) одномоментных исследований, проведенных в различных временных точках. При этом обследованию подлежит одна и та же популяция, но необязательно одна и та же выборка. Можно представить исследование тренда на примере оценки заболеваемости. При этом целью исследования может быть оценка характера распределения заболеваемости внутри года (по месяцам, дням) или оценка многолетней заболеваемости. При этом можно оценивать, существует ли тенденция изменения заболеваемости, направление изменения заболеваемости, равномерно ли распределены показатели заболеваемости за изучаемый период (например, по месяцам), есть ли цикличность заболеваемости, а при дополнительной оценке распространенности фактора риска – существует ли его связь с выявленным распределением заболеваемости. 26.Применение экологических исследований в медицине и общественном здравоохранении. Экологическое исследование (ecological study, корреляционное исследование, correlation study) – это эпидемиологическое обсервационное исследование. Экологические исследования являются несколько обособленным типом эпидемиологических исследований, что связано с рядом их отличительных признаков: 1. Единицей анализа в исследовании являются не индивиды, как в большинстве других типов исследований, а группы людей, так как в анализ включаются групповые значения показателей изучаемых переменных. Очень целесообразно применение экологических исследований в тех случаях, когда популяционные (межгрупповые) различия интересует нас больше, чем внутрипопуляционные (внутригрупповые) различия. 2. Объединение интересующих индивидов в группы чаще всего происходит по территориальному принципу (страна, регион, район), но может происходить и по временому принципу (день, неделя, месяц наблюдения). Нет основной и контрольной групп. 4. Для анализа используются вторичные данные – официальная информация о социально-демографических показателях, показателях здоровья (заболеваемость, распространенность, смертность и др.), информация о воздействии (распространенность или уровень фактора риска, например, концентрация каких-либо веществ в воздухе на изучаемой территории). Основной задачей экологических исследований является формирование гипотез о наличии связей между изучаемым воздействием и исходом, которые в дальнейшем можно проверить при проведении других типов исследований с более высокой доказательной способностью. 27.Применение исследований «случай-контроль» в медицине и общественном здравоохранении. Исследование типа "случай-контроль" является одной из разновидностей медицинского исследования, и часто используется с целью определения причины заболевания, особенно при расследовании вспышек инфекционных заболеваний, или изучении редких болезней. Когда медицинским исследователям необходим относительно быстрый и простой способ узнать этиологию нового заболевания, например при вспышке неизвестной инфекции, они могут сравнить две группы людей: Тех, кто уже имеют заболевание - "случай" Тех, кто находился аналогичных условиях, но не имел заболевания - "контроль". Исследование "случай-контроль" всегда является ретроспективным, то есть исследователи используют данные, собранные в прошлом, с целью проверки наличия связи между конкретным полученным результатом и подозреваемым фактором риска. Для проверки конкретной причины, ученые должны сформулировать научную гипотезу о том, что, по их мнению, приводит к этой инфекционной вспышке или этому заболеванию. Затем они сравнивают, как часто в группе "случай" встречалась предполагаемая причина (фактор риска), и как часто эта причина встречалась в группе "контроль". Если искомый фактор риска имеет большую распространенность в группе "случай", то есть некоторые основания полагать, что он и является причиной заболевания. В ходе одного исследования может быть проанализирован только один фактор риска. Например, можно провести исследование "случай-контроль" чтобы проанализировать, как часто люди болеют раком легких, если у них есть стаж курения, сравнив их с группой пациентов без стажа курения. 28.Применение «поперечных» исследований в медицине и общественном здравоохранении. Поперечное исследование-исследование соотношений между заболеваниями (или иными признаками, относящимися к здоровью) и другими переменными в определенной популяции в определенный момент времени. Наличие или отсутствие болезни и наличие или отсутствие других признаков (или, если они количественные, степень их выраженности) определяется у каждого члена популяции или в репрезентативной выборке в один момент времени. Соотношение между переменной и заболеванием может быть изучено в терминах распространенности заболевания в различных подгруппах популяции в зависимости от наличия или отсутствия (или уровня) переменных и в терминах наличия или отсутствия (или уровня) переменных у больных и лиц, у которых нет заболевания. Заметьте, что определяется превалентность болезни, но не инцидентность. Временная последовательность событий, позволяющая различить причины и следствия, в поперечном исследовании заболевания определяется не всегда. 29.Когортные исследования. Правила организации. Преимущества. Недостатки. Когортные исследования – это такой тип медицинских исследований, который используется для выявления причин заболевания, установления связей между факторами риска и их последствий для здоровья. Такие исследования, как правило, являются прогнозными, или "перспективными" – то есть они планируются заранее и проводятся в течение определенного отрезка будущего периода времени.В ходе исследования ставится вопрос, формируется гипотеза о потенциальных причинах болезни. После этого исследователи наблюдают за группой людей, набранных в когорту, в течение определенного периода времени (нередко – очень долгого), стараясь обнаружить любые изменения в состоянии их здоровья, связанные с интересующими исследователей факторами риска. Например, ученые могут попросить участников записывать свои факторы риска и определенные моменты образа жизни в течение длительного времени, а затем проанализировать, как эти факторы коррелируют с изучаемым заболеванием. Такие исследования используются эпидемиологами, изучающими факторы, влияющие на здоровье и заболеваемость населения. Когортные исследования по-другому еще называют: инцидентные, продольные, наблюдательные, сопутствующие или перспективные. Преимущества Лучший дизайн для изучения причин состояний, заболеваний,факторов риска и результатов. Достаточно времени для получения строгих доказательств Многих систематических ошибок можно избежать (возникают ,если исход известен заранее) Позволяет оценить связь между воздействием фактора риска и несколькими заболеваниями. Недостатки Лонгитудинальное Дорогое (исследования большего числа людей) Позволяет оценить связь между заболеванием и воздействием относительно небольшого числа факторов (тех, что были определены в начале исследования) Не могут использоваться для редких заболеваний (размер выборки должен быть больше, чем число лиц с изучаемым заболеванием) |
