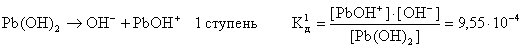Ответы на вопросы по химии 1 курс. Экзамен ХИМИЯ. 1 билет
 Скачать 2.97 Mb. Скачать 2.97 Mb.
|
50 билет 51 билетMgCl2 -> Mg(2+) + 2Cl(-) n=3 (число ионов) Возьмем 1 л (1000 мл) раствора MgCl2, тогда mр-ра(MgCl2) = V*p = 1000*1=1000 г m(MgCl2)=mр-ра*w/100 = 1000*0,5/100 = 5 См(MgCl2) = m/M*V = 5/95*1 =0,053 моль/л = 53 моль/м3 Изотонический коэффициент равен: i = Pосм/См*R*T =3,2*10^ (5) / 53*8,314*291 =2,5 α = i - 1 / n -1 = 2,5-1 / 3 - 1 = 1,5/2 = 0,75 https://vk.com/wall-27835604_3459 52 билетпо 2 закону Рауля можно рассчитать dT=К*м м=20/1,86=10,75 моль/кг молярня масса этиленгликоля Mr=62г/моль n=m/Mr => m=10,75*62=666,7 г при 20°С уд. вес этиленгликоля 1,1138 V=666,7/1,1138=599мл (примерно 600мл) , а воды 1000 мл, т. к. уд. вес воды=1 Вот и получается э/г : Н2О=600 : 1000 = 3 :5 53 билет^t = Cm*K . Cm = 25 / 1.86 = 13.44 моль/кг - моляльная концентрация этиленгликоля . V э-г = 13.44*62 / 1.116 = 747 см3 Объёмные отношения этиленгликоля и воды 0,747 /1 или 3 : 4
| |||||||||||||||||||||||||||||||||||||||
| | (при 25 С) |
| HCN H+ + CN- | 7·10-5 (или 0,007%) |
| | 0,013 (или 1,3%) |
Степень электролитической диссоциации зависит от:
природы электролита и растворителя;
концентрации раствора;
температуры
и возрастает при увеличении разбавления раствора:
| C(CH3COOH) , моль/л | 0,2 | 0,1 | 0,05 | 0,01 | 0,005 | 0,001 | |
| , % (при 25° С) | 0,05 | 1,4 | 1,9 | 4,2 | 6,0 | 12,4 | |
| | слабый электролит | электролит средней силы | |||||
Степень диссоциации возрастает при увеличении температуры раствора. Увеличение кинетической энергии растворенных частиц способствует распаду молекул на ионы, что приводит к возрастанию степени диссоциации при нагревании растворов.
Если в растворе слабой кислоты или слабого основания увеличить концентрацию одноименного иона введением соответствующей соли, то наблюдается резкое изменение степени диссоциации слабого электролита. Рассмотрим, например, как изменится уксусной кислоты (CH3COOH) при введении в раствор ацетата натрия (введение одноименных ионов CH3COO-).
Согласно принципу Ле Шателье равновесие процесса диссоциации
сместится влево в результате увеличения концентрации ацетат-ионов CH3COO-, образующихся при диссоциации ацетата натрия:
CH3COONa CH3COO- + Na+.
Такое смещение равновесия в сторону образования CH3COOH означает уменьшение степени ее диссоциации и приводит к уменьшению концентрации ионов водорода, например:
| C(CH3COOH), моль/л | 0,01 | 0,01 |
| C(CH3COONa), моль/л | | 0,01 |
| [H+], моль/л | 4,32·0-4 | 1,86·10-5 |
Таким образом, в результате введения в 1 л 0,01 М раствора CH3COOH 0,01 моль CH3COONa концентрация ионов водорода уменьшилась в
С точки зрения теории электролитической диссоциации амфотерные гидроксиды (амфолиты) - это вещества, диссоциирующие в водном растворе как по типу кислот, так и по типу оснований. К ним относят Be(OH)2, Zn(OH)2, Pb(OH)2, Sn(OH)2, Al(OH)3, Cr(OH)3, и др. Например, уравнения электролитической диссоциации Be(OH)2:
1) диссоциация по типу основания:
Be(OH)2 + 3H2O OH- + [BeOH(H2O)3]
[BeOH(H2O)3] + H2O OH- + [Be(H2O)4]
2) диссоциация по типу кислоты:
Be(OH)2 + 2H2O H+ + [Be(OH)3H2O]
[Be(OH)2H2O] H+ + [Be(OH)3]
Закон разведения Оствальда

Вильгельм Фридрих Оствальд (2.09.1853,—4.04.1932)— балтийский немец, физико-химик и философ-идеалист, лауреат Нобелевской премии по химии 1909 года. Член-корреспондент Петербургской АН (1895).
Между константой и степенью диссоциации существует определенная закономерность, которую в 1888г.обнаружил В.Оствальд и сумел ее объяснить. Эта закономерность впоследствии была названа законом разведения Оствальда.
Экспериментальное установление правильности закона разбавления Оствальда имело большое значение для обоснования теории электролитической диссоциации.
Kдсвязана спростой зависимостью. Если общую молярную концентрацию электролита в растворе обозначить СКА, то для бинарных электролитов концентрации ионов Ky+и Ax-будут равны·CKA. Очевидно, что
[Ky+] = [Ax-] = ·CKA ,
[KA] = CKA - ·CKA = CKA·(1- ), тогда
Для слабых электролитов 0 и (1 - ) 1. Следовательно,
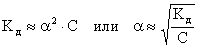 (7.6.7.)
(7.6.7.)Полученная зависимость является математическим выражением закона разбавления Оствальда:
степень диссоциации слабого электролита увеличивается при разбавлении раствора обратно пропорционально корню квадратному из его молярной концентрации.