микроциркуляция. микроциркуляция патфиз. 1. Классификация основных форм нарушений микроциркуляции
 Скачать 1.26 Mb. Скачать 1.26 Mb.
|
|
23.Особенности гемоциркуляции и лимфообращения в ишемизированном участке ткани. Микроциркуляция при ишемии Увеличение сопротивления в приводящих артериях создает условия для их сужения и понижает внутрисосудистое давление в микрососудах органа. Прежде всего давление падает в мелких артериях и артериолах к периферии от места сужения или закупорки, из-за чего артериовенозная разность давлений на протяжении микроциркуляторного русла уменьшается, вызывая замедление линейной и объемной скоростей кровотока в капиллярах. Из-за сужения артерий в области ишемии наступает перераспределение эритроцитов: в капилляры поступает кровь, бедная форменными элементами (низкий гематокрит). Понижение внутрикапиллярного давления способствует закрытию капилляров. Из-за этого количество функционирующих капилляров в ишемизированном участке ткани уменьшается. Ослабление микроциркуляции при ишемии вызывает нарушение питания тканей: уменьшается доставка кислорода (возникает циркуляторная гипоксия) и энергетических материалов. Одновременно в тканях накапливаются продукты обмена веществ. Вследствие понижения давления внутри капилляров интенсивность фильтрации жидкости из сосудов в ткани падает, создаются условия для усиленной резорбции жидкости из ткани в капилляры. Количество тканевой жидкости в межклеточных пространствах значительно уменьшается и лимфоотток из области ишемии ослабляется вплоть до полной остановки. Зависимость разных параметров микроциркуляции при ишемии показана на рис. 9-3. 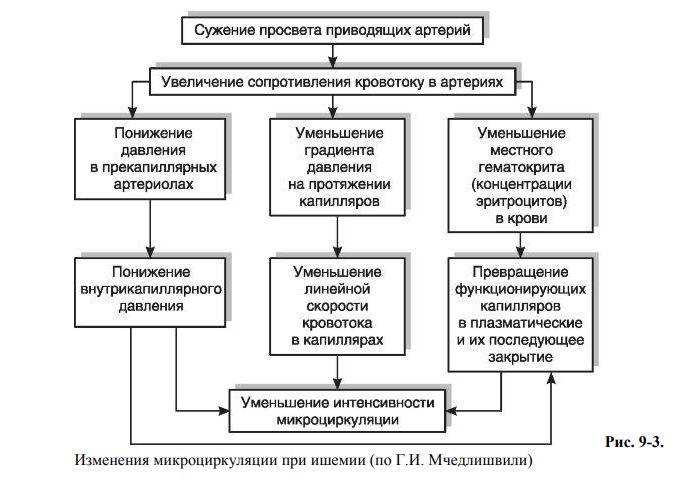 24.Факторы, определяющие степень тяжести ишемических повреждений в тканях. Ближайшие последствия и исходы ишемии зависят от следующих факторов: Скорость развития ишемии. Быстро развивающаяся ишемия более патогенна для клеток, чем медленно прогрессирующая, поскольку последняя оставляет определенное время для адаптации и компенсации. Достаточность развития коллатерального кровообращения. Существуют органы с достаточным коллатеральным кровообращением (тонкий кишечник, печень, нижние конечности, легкие), с относительно достаточным кровообращением (сердце), и абсолютно недостаточным магистральным кровоснабжением (почки, сетчатка, селезенка, спинной мозг). Чувствительность клеток к гипоксии. Наиболее чувствительны к гипоксии кортикальные нейроны, эпителиальные клетки проксимальных канальцев нефронов. Наименее чувствительны к гипоксии клетки мезенхимального происхождения. Функциональное состояние органа на момент развития ишемии, что определяет величину функционального запроса кислорода и нутриентов (биологически значимых элементов). Качество крови как кислородпереносящего агента. Например, у больных с серповидноклеточной анемией риск инфаркта миокарда и других органов значительно увеличен. 25.Клинические проявления и обмен веществ при ишемии. Симптомы ишемии Симптомы ишемии зависят главным образом от уменьшения интенсивности кровоснабжения ткани и соответствующих изменений микроциркуляции. Уменьшение диаметра и количества видимых артериальных сосудов в связи с их сужением и уменьшением кровенаполнения Цвет органа становится бледным в результате: сужения поверхностно расположенных сосудов снижения количества функционирующих капилляров уменьшения содержания эритроцитов в крови (понижение местного гематокрита). Объем органа при ишемии уменьшается в результате: ослабления кровенаполнения органа снижения количества тканевой жидкости снижения тургора ткани. Температура поверхностно расположенных органов понижается, т.к.: вследствие уменьшения интенсивности кровотока через орган нарушается баланс между доставкой тепла кровью и его отдачей в окружающую среду отдача тепла начинает превалировать над его доставкой к органу. Температура при ишемии, естественно, не понижается во внутренних органах, с поверхности которых теплоотдача не происходит. Снижение лимфообразования в результате понижения перфузионного давления в тканевых микрососудах (Перфузия – процесс прохождение крови через ткань или орган). Изменения в тканях при ишемии Разные ткани неодинаково чувствительны к изменениям кровоснабжения, поэтому нарушения в них при ишемии наступают соответственно неодинаково быстро. в ЦНС недостаточность кровоснабжения сразу же приводит к расстройствам функции соответствующих областей мозга (при поражении двигательных областей довольно быстро наступают парезы, параличи и т.д.) Следующее место по чувствительности к ишемии занимают сердечная мышца, почки и другие внутренние органы. Ишемия в конечностях сопровождается болями, ощущением онемения, «бегания мурашек» и дисфункцией скелетных мышц, проявляющейся, например, в виде перемежающейся хромоты при ходьбе. В случаях, когда кровоток в области ишемии в течение соответствующего времени не восстанавливается, возникает омертвение тканей - инфаркт. Белый инфаркт: в процессе омертвения кровь в область ишемии не поступает и суженные сосуды остаются заполненными лишь плазмой крови без эритроцитов. Наблюдаются в тех органах, в которых коллатеральные пути развиты слабо, например в селезенке, сердце и почках. Белый инфаркт с красной (геморрагической) каемкой: развивается в сердце, почках. Геморрагический венчик образуется в результате того, что спазм сосудов по периферии инфаркта сменяется паралитическим их расширением и развитием кровоизлияний. Красный (геморрагический) инфаркт: стенки сосудов разрушены и эритроциты как бы «нафаршировывают» всю ткань, окрашивая ее в красный цвет (тромбоэмболия мелких ветвей легочной артерии вызывает развитие геморрагического красного инфаркта легкого) Возникновению инфарктов при ишемии способствуют общие расстройства кровообращения, вызываемые сердечной недостаточностью, а также атеросклеротические изменения артерий, препятствующие коллатеральному притоку крови, склонность к спазмам артерий в области ишемии, повышение вязкости крови и т.д. Все это препятствует коллатеральному притоку крови и нормализации микроциркуляции. Обмен веществ при ишемии (на примере миокарда) В условиях ишемии миокард переходит на питание глюкозой, т.к: Клеткам миокарда для получения необходимого количества энергии путем окисления глюкозы нужно меньшее количество кислорода, чем при окислении жирных кислот = при одинаковом потреблении кислорода в условиях окисления глюкозы образуется на 14% АТФ больше, чем при окислении жирных кислот. При ишемии происходит дефицит поступления кислорода к клеткам, поэтому они начинают использовать для своего энергообеспечения гликоген, который содержится в ограниченном количестве в кардиомиоцитах. Такой «кислород-сберегающий» метаболизм является спасительным и сохраняет энергетический обмен на максимально возможном в данных условиях уровне. При дефиците кислорода в сердце происходит высвобождение катехоламинов из нервных окончаний, что приводит к активации фосфорилазы и фосфофруктокиназы и усилению анаэробного гликолиза. Образующаяся в процессе гликолиза энергия составляет всего 7% от необходимого количества и не позволяет длительно сохранять жизнеспособность миокарда. Запасы АТФ при ишемии начинают уменьшаться уже через несколько сокращений сердца; через 15 минут содержание АТФ составляет лишь около 35% от нормы, а через 40 минут – около 10%. 26.Определение понятия «стаз», классификация, этиология, патогенез, клинические проявления и последствия. Стаз — это остановка тока крови и/или лимфы в капиллярах, мелких артериях и венулах. Виды стаза: 1. Венозный (застойный). В этом случае происходит прогрессирующее нарастание давления в венозных сосудах вплоть до уравнивания его с артериальным. Причины его развития те же, что и венозной гиперемии. (лимфоток возрастает) 2. Постишемический. При этом артериальное давление падает до уровня венозного. Причины развития те же, что ишемии. (лимфоток уменьшается) 3. Истинный капиллярный стаз. Этот вид развивается в результате препятствия кровотоку в капиллярах при нарушении реологических свойств крови. Артериоло-венулярная разница по давлению при истинном стазе сохраняется, значительно повышается капиллярное сопротивление. Данный вид стаза обратим только в самом начале. Причины: 1.Ишемия и венозная гиперемия, При замедлении тока крови образование или активация веществ, обусловливающих склеивание ФЭК, формирование агрегатов и тромбов. 2.Проагреганты (тромбоксан А2, Пг F, Пг Е, аденозиндифосфат, катехоламины, АТ к ФЭК) – факторы, вызывающие агрегацию и агглютинацию ФЭК с их лизисом и высвобождением БАВ. 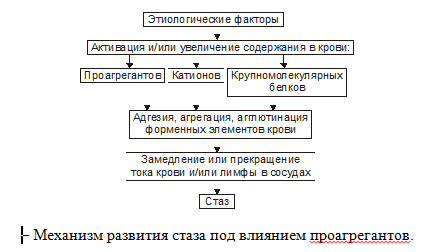 Основные причины: - дегидратация - гиперлейкоцитоз - повышение гематокрита - криогобулинемия и макроглобулинемия - анемии с агрегацией эритроцитов - снижение деформируемости эритроцитов - адгезия форменных элементов на стенке сосудов - понижение альбумин-глобулинового коэффициента - повышение концентрации фибриногена в плазме Проявления стаза Изменения в сосудах микроциркуляторного русла: – уменьшение внутреннего диаметра микрососудов при ишемическом стазе; – увеличение просвета сосудов микроциркуляторного русла при венознозастойном стазе; – формирование большого количества агрегатов форменных элементов крови в просвете сосудов микроциркуляторного русла и на их стенках; – образование микрокровоизлияний (при венознозастойном стазе). - отличительная особенность истинного стаза при микроскопии – гомогенный характер кровяных масс в микрососудах и сгущение крови. Последствия стаза При быстром устранении причины стаза происходит восстановление тока крови в сосудах микроциркуляторного русла и в тканях не развивается каких-либо существенных изменений. Длительный стаз (особенно ишемический) приводит к развитию дистрофических изменений в тканях и нередко к инфаркту. Патогенное значение стаза крови в капиллярах в значительной степени зависит от того, в каком органе он возник. Так, особенно опасен стаз крови в микрососудах головного мозга, сердца и почек. КЛАССИФИКАЦИЯ НАРУШЕНИЙ МИКРОЦИРКУЛЯЦИИ МЕТОДА I. Внутрисосудистые нарушения: Расстройства реологических свойств крови, связанные с изменением суспензионной стабильности форменных элементов и вязкости крови. Нарушение коагуляции крови и тромбоэмболизм. 3. Изменение скорости кровотока, т.е. нарушения перфузии крови через микроциркуляторное русло II. Нарушения самих сосудов (сосудистые нарушения): 1. Повреждение и изменение формы и местонахождения эндотелиальных клеток в стенках микрососудов. 2. Изменения проницаемости капиллярной и венулярной стенок. 3. Прилипание (адгезия) лейкоцитов, тромбоцитов и чужеродных частиц к эндотелию. 4. Диапедез форменных элементов крови через стенки капилляров и венул. 5. Микрокровоизлияния. III. Внесосудистые нарушения: Влияние поврежденной окружающей микрососуды соединительной ткани и паренхиматозных клеток органов. Реакция тучных клеток на патологические стимулы. Нарушения (затруднения) лимфообращения. Вовлечение микрососудистого ложа в нейродистрофический процесс. Классификация «сладж»-синдрома Различают несколько видов сладжа в зависимости от структурных особенностей агрегата Размер, плотность, характер края агрегата). Классический тип. Характеризуется сравнительно крупными агрегатами и плотной упаковкой эритроцитов и с неровными очертаниями контуров. Этот вид сладжа развивается, когда какое-либо препятствие (например, лигатура) мешает свободному движению крови через сосуд. Декстрановый тип. Агрегаты имеют различную величину, плотную упаковку, округлые очертания, свободные пространства в агрегатах в виде полостей. Этот вид сладжа развивается при введении в кровь декстрана с молекулярным весом 250-500 и выше КДн. Аморфный тип. Для этого типа характерно наличие огромного количества мелких агрегатов, похожих на гранулы. В этом случае кровь приобретает вид крупнодисперсной жидкости. Аморфный тип сладжа развивается при введении в кровь этилового, АДФ и АТФ, тромбина, серотонина, норадреналина. В образовании агрегата при аморфном типе сладжа участвует всего несколько эритроцитов. Малые размеры агрегатов могут представлять не меньшую, а даже большую опасность для микроциркуляции, так как их величина позволяет им проникнуть в мельчайшие сосуды до капилляров включительно. Синдром повышенной вязкости крови. Под синдромом повышенной вязкости крови понимают комплекс изменений ее реологических свойств: Повышение вязкости цельной крови и плазмы (вискоземетрия). Уменьшение деформируемости Er. Увеличение гематокритного числа. Увеличение концентрации фибриногена. Усиление агрегации эритроцитов. Недостаточность лимфообращения – состояние, при котором лимфатические сосуды не выполняют свою основную функцию – осуществление постоянного и эффективного дренажа интерстиция. Различают следующие формы недостаточности лимфатической системы: Механическая недостаточность, при которой течение лимфы затрудняется в связи с наличием органических (сдавление опухолью, рубцом, экстирпация лимфатических узлов и сосудов, облитерация лимфатических сосудов при их воспалении) или функциональных причин (повышение давления в магистральных венозных сосудах, спазм лимфатических сосудов). Филяриоз (личинки передаются комарами кровь лимфаузелфиброз). Динамическая недостаточность, при которой объем транссудации межтканевой жидкости превышает возможности лимфатической системы обеспечить эффективный дренаж ткани. Резорбционная недостаточность, обусловленная морфофункциональными изменениями межуточной ткани, накоплением белков и осаждением их в интерстиции. Артериальная гиперемия – динамическое увеличение кровенаполнения органа или ткани вследствие увеличения притока крови через его сосуды. По значению для организма различают физиологическую и патологическую артериальную гиперемию. Основным звеном патогенеза артериальной гиперемии является расширение мелких артерий и артериол и открытие прекапиллярных сфинктеров, что приводит к увеличению притока крови к органу и числа функционирующих капилляров. Основное звено патогенеза артериальной гиперемии может быть реализовано посредством различных механизмов. Миопаралитический механизм. Связан со снижением миогенного тонуса сосудов под влиянием метаболитов, медиаторов, внеклеточного увеличения концентрации калия, водорода и других ионов, уменьшения содержания кислорода. Это самый частый механизм развития артериальной гиперемии. Он лежит в основе развития физиологической рабочей гиперемии, при воспалении, постишемическом полнокровии и в других ситуациях. 2. Реактивная (реперфузионная, постокклюзионная) артериальная гиперемия развивается после ограничения кровоснабжения органа или ткани. В основе ее лежат накопление в обескровленной ткани пуринов, лактата, двуокиси углерода, калия и других метаболитов и снижение концентрации кислорода, что приводит к реализации миопаралитического механизма. Разновидностью реактивной является коллатеральная гиперемия при перекрытии магистральной артерии. К реактивной относится также и посткомпрессионная гиперемия после сдавления ткани. 3. Рабочая артериальная гиперемия. Механизм этого процесса связан с теми же метаболическими факторами, в избытке образующимися в активно функционирующем органе. 4. Гуморальная гиперемия обусловлена главным образом действием медиаторов воспаления на миогенный компонент сосудистого тонуса, хотя в данном случае присоединяются и другие механизмы. 5. Нейропаралитический механизм. Он состоит в уменьшении нейрогенного констрикторного влияния на сосуды и падении нейрогенного тонуса. Такая гиперемия возникает при перерезке, параличе или повреждении вазоконстрикторных нервов или их центров (огнестрельные раны, травмы, оперативные вмешательства). Проявлением нейропаралитического действия электротока считаются так называемые «знаки молнии» - мгновенно возникающие зоны артериальной гиперемии по ходу прохождения тока при поражении молнией. При понижении температуры кожи ее сосуды вначале претерпевают нейрогенный спазм. Однако, когда кожная температура падает ниже 15 С, вследствие холодового паралича нервно – мышечной возбудимости и проводимости, кожные сосуды начинают расширяться. Таким образом, морозный румянец на щеках – проявление артериальной гиперемии нейропаралитического типа. При некоторых инфекциях (сыпной тиф, дифтерия) бактериальные токсины могут оказывать паралитическое действие на вегетативные центры. Данный механизм может способствовать развитию коллапса при инфекциях. Нейротонический механизм. Он предусматривает повышение нейрогенной сосудорасширяющей активности или понижение тонуса вазоконстрикторов в результате истинного рефлекса или аксон – рефлекса. Этот механизм наблюдается только в некоторых тканях: в поджелудочной и слюнных железах, языке, коже, кавернозных телах. Примером этого типа гиперемии является односторонняя эритема у больных невритом тройничного нерва, у страдающих зубной болью и крупозной пневмонией. Классическим примером нейротонической артериальной гиперемии является краска стыда (гнева) на щеках, особенно выраженная у психастенических индивидов, страдающих эритрофобией – навязчивый боязнью приковать общее внимание. |
