1. Определение понятия фермент
 Скачать 0.71 Mb. Скачать 0.71 Mb.
|
|
2. Лекарственные препараты на основе коферментов и витаминов. Коферментные препараты: кокарбоксилаза, рибофлавина мононуклеотид, флавинат, пиридоксальфосфат, кобамамид используют для усиления активности ряда ферментов. 3. Лекарственные препараты на основе ингибиторов и активаторов ферментов.
16. Биологическое окисление (БО) совокупность окислительно-восстановительных реакций, которые протекают во всех живых клетках. Субстрат БО – вещество, способное отдавать электрон. (Любые вещества, способные вступать в реакции окисления). Биохимик В.И. Палладин создал теорию дыхания, как совокупности ферментативных процессов. Он предположил, что окисление субстратов может происходить в 2 фазы: 1). Анаэробная фаза. В этой фазе особые вещества хромогены (R) отщепляют Н от субстратов и восстанавливаются (RH2). 2). Аэробная фаза. Восстановленные хромогены RH2 передают Н на О2. 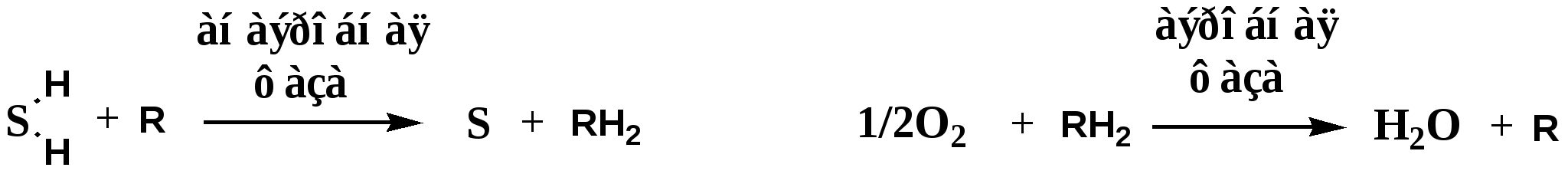 Субстрат БО - в-во, способное отдавать электроны (в-ва, способные вступать в реакции окисления). Пути использования кислорода в клетке В настоящее время выделено 4 основные пути использования кислорода в организме: 1. Оксидазный путь - окислительное фосфорилирование. Протекает в митохондриях, является основным источником АТФ в аэробных тканях. Потребляет 90% кислорода. 2. Монооксигеназный путь. Обеспечивает включение 1 атома кислорода в молекулу субстрата. Используется для синтеза новых веществ (стероидные гормоны), обезвреживания ксенобиотиков и токсических продуктов обмена в митохондриях и ЭПР. 3. Диоксигеназный путь. Обеспечивает включение молекулы кислорода в молекулу субстрата. Используется для деградации АК и синтеза новых веществ. 4. Пероксидазный и радикальный пути. Кислород участвует в образовании перекисей и активных радикалов, которые необходимы в пероксисомах для внутриклеточного пищеварения, разрушения макрофагами бактерий, вирусов, регуляции метаболизма и т.д. Перекиси и активные кислородные радикалы оказывают также повреждающее воздействие на структуры клеток и тканей, активируя ПОЛ. Разрушение перекисей и инактивация свободных радикалов осуществляется с помощью ферментативной и неферментативной антиокидантной системы. 17. Оксидазный путь потребления кислорода протекает в митохондриях, потребляет 90% О2 и обеспечивает процесс окислительного фосфорилирования. Окислительным фосфорилированием называют синтез АТФ из АДФ и Н3РО4 за счет энергии движении электронов по дыхательной цепи. Окислительное фосфорилирование является основным источником АТФ в аэробных клетках. МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ Окислительное фосфорилирование состоит из процессов окисления и фосфорилирования, которые между собой сопряжены. Процесс окисления происходит при движении электронов по дыхательной цепи от субстратов тканевого дыхания на кислород. Дыхательная цепь окислительного фосфорилирования состоит из 4 белковых комплексов, встроенных во внутреннюю мембрану митохондрий и небольших подвижных молекул убихинона и цитохрома С, которые циркулируют в липидном слое мембраны между белковыми комплексами. Комплекс I – НАДН2 дегидрогеназный комплекс Комплекс II – СДГ. Комплекс III – Комплекс b Комплекс IV – Цитохромоксидазный комплекс Коэнзим Q (убихинон Компоненты дыхательной цепи располагаются в мембране в порядке повышения их редокс-потенциала. При переходе е- от комплекса с низким редокс-потенциалом к комплексу с более высоким редокс-потенциалом происходит выделение свободной энергии. При окислении 1 НАДН2 выделяется 220 кДж/моль свободной энергии. I, III и IV комплексы дыхательной цепи используют 65-70% этой свободной энергии для переноса Н+ из матрикса митохондрий в межмембранное пространство, 30-35% свободной энергии рассеивается в виде тепла. 18. Этапы унифицирования энергии пищевых веществ и образования субстратов тканевого дыхания Образование субстратов тканевого дыхания осуществляется в несколько этапов:
19. Митохондрии - органеллы клеток. Они имеют 2 мембраны наружную гладкую и внутреннюю с многочисленными складками – кристами, внутреннее пространство митохондрий заполнено матриксом. Метаболические и гомеостатические функции митохондрий В митохондриях происходит: синтез АТФ и теплопродукция в реакция окислительного фосфорилирования; β-окисления жирных кислот; реакции ЦТК, через ЦТК протекают некоторые реакции глюконеогенеза, переаминирования, дезаминирования, липогенеза и синтеза гема, осуществляется интеграция белкового, липидного и углеводного обмена. Митохондрии имеют наружную мембрану, проницаемую для большинства метаболитов, и избирательно проницаемую внутреннюю мембрану с множеством складок (крист), выступающих в сторону матрикса (внутреннего пространства митохондрий). Наружная мембрана может быть удалена путем обработки дигитонином; она характеризуется наличием моноаминоксидазы и некоторых других ферментов (например, ацил-КоА-синтетазы, глицерофосфат- ацилтрансферазы, моноацилглицерофосфат-ацилтрансферазы, фосфолипазы А2). В межмембранном пространстве находятся аденилаткиназа и креатинкиназа. Во внутренней мембране локализован фосфолипид кардиолипин. В матриксе находятся растворимые ферменты цикла лимонной кислоты и ферменты (-окисления жирных кислот, в связи с этим возникает необходимость в механизмах транспорта метаболитов и нуклеотидов через внутреннюю мембрану. Сукцинатдегидрогеназа локализована на внутренней поверхности внутренней митохондриальной мембраны, где она передает восстановительные эквиваленты дыхательной цепи на уровне убихинона (минуя первую окислительно- восстановительную петлю). 3-гидроксибутиратдегид рогеназа локализована на матриксной стороне внутренней митохондриальной мембраны. Глицерол-3-фосфат- дегидрогеназа находится на наружной поверхности внутренней мембраны, где она участвует в функционировании глицерофосфатного челночного механизма. 20. Цикл Кребса ЦТК является процессом окисления АцетилКоА - универсального продукта катаболизма углеводов, жиров и белков. ЦТК протекает в митохондриях с участием 8 ферментов, которые локализованы в матриксе в свободном состоянии, или на внутренней поверхности внутренней мембраны. В ЦТК участвуют 5 витаминов В1, В2, РР, пантотеновая кислота и липоевая кислота в виде коферментов тиаминпирофосфата, ФАД, НАД+, КоА и липоата. Основной функции ЦТК является образование водородных эквивалентов, которые в цепи окислительного фосфорилирования обеспечивают синтез макроэргических соединений. Кроме того, ЦТК выполняет ведущую роль в процессах глюконеогенеза, переаминирования, дезаминирования АК, липогенеза и синтеза гема. Интегрирует все виды обмена веществ. Регуляция ЦТК. Осуществляется с участием 4 регуляторных ферментов: цитратсинтазы, изоцитрат ДГ, α-КГ ДГ и СДГ. ЦТК ингибируется в основном НАДН2 и АТФ, которые являются продуктами ЦТК и цепи окислительного фосфорилирования. Активируют ЦТК в основном НАД+ и АДФ. Реакции ЦТК 1). Цитратсинтаза локализуется в матриксе митохондрий, ее активируют ЩУК, НАД+; ингибируют АТФ, НАДН2, Сукцинил-КоА, цитрат.  2). Аконитаза локализуется в матриксе митохондрий.  3). Окислительно-восстановительная реакция, самая медленная в ЦТК. Изоцитратдегидрогеназа локализуется в матриксе митохондрий, ее активируют АМФ, Са2+, АДФ, НАД+; ингибируют АТФ, НАДН2. 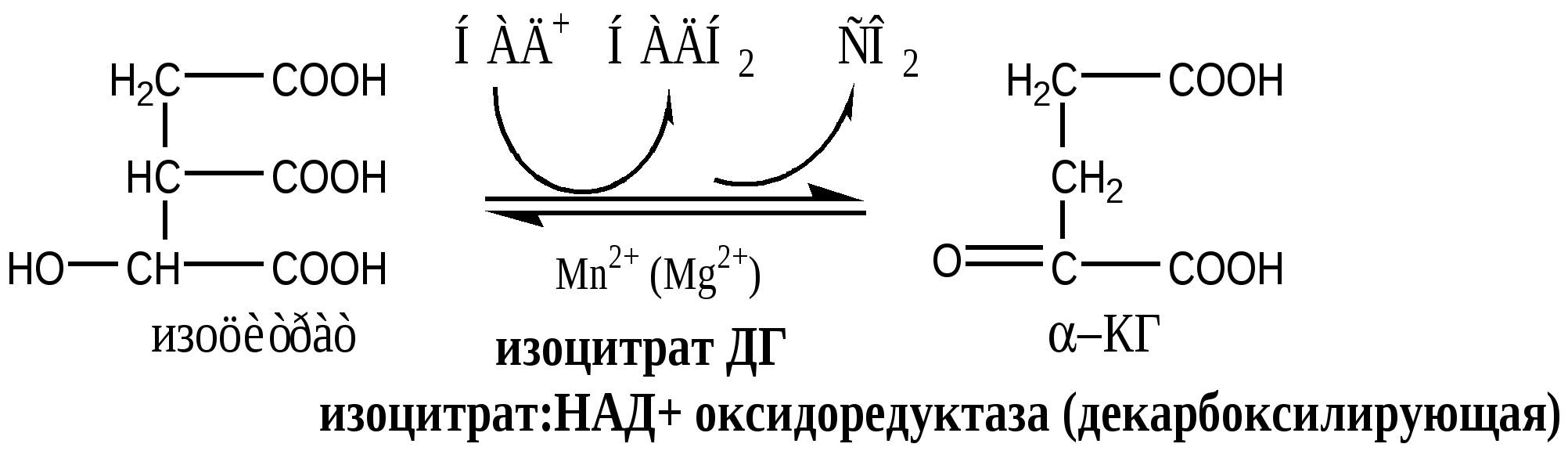 4). Окислительно-восстановительная реакция. α-кетоглутаратдегидрогеназный комплекс состоит из 3 ферментов и содержит 5 коферментов: тиаминдифосфат, кофермент А, липоевая кислота, НАД+, ФАД. α-КГ ДГ активируется Са2+, ингибируется сукцинил-КоА, АТФ, НАДН2.  5). Реакция субстратного фосфорилирования 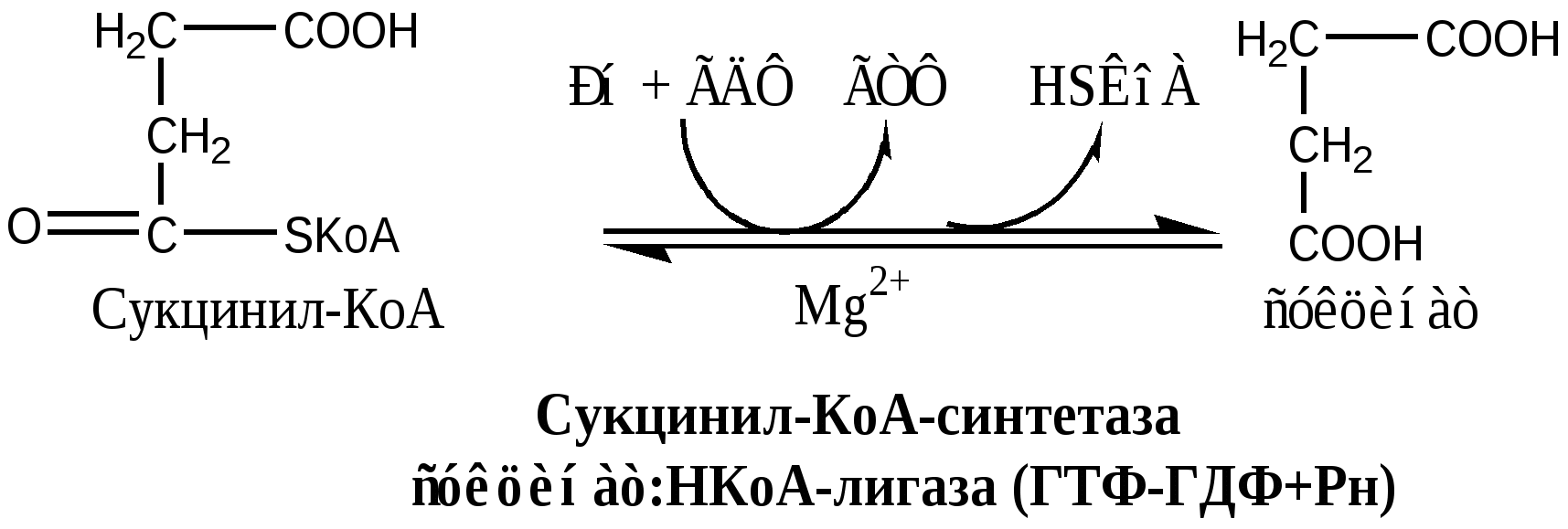 6). Окислительно-восстановительная реакция. Сукцинатдегидрогеназа, флавопротеин содержащий Fe2S2, связана с внутренней мембраной митохондрии. СДГ ингибирует ЩУК и Сукцинил-КоА,  7). Фумараза локализуется в матриксе митохондрий. 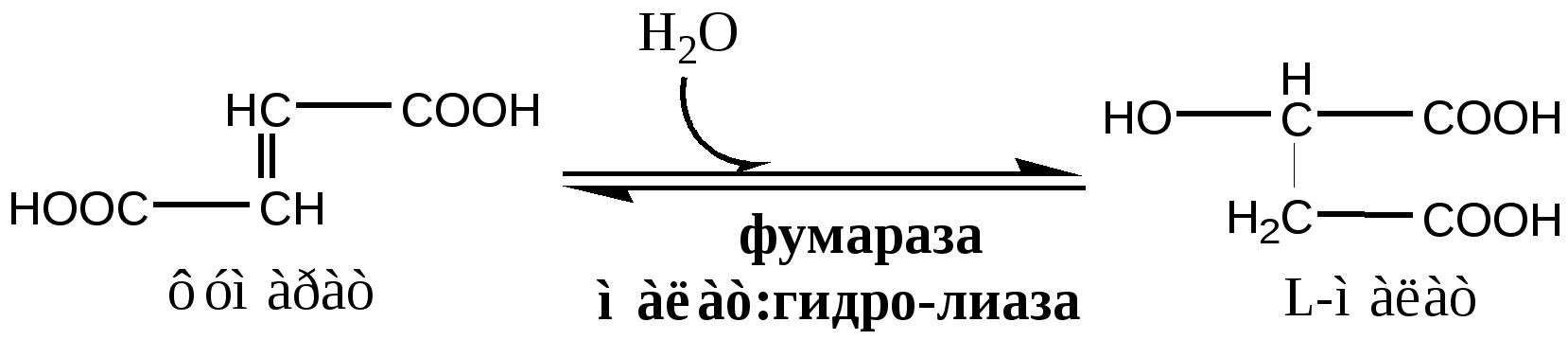 8). Окислительно-восстановительная реакция. Малат ДГ локализуется в матриксе митохондрий. 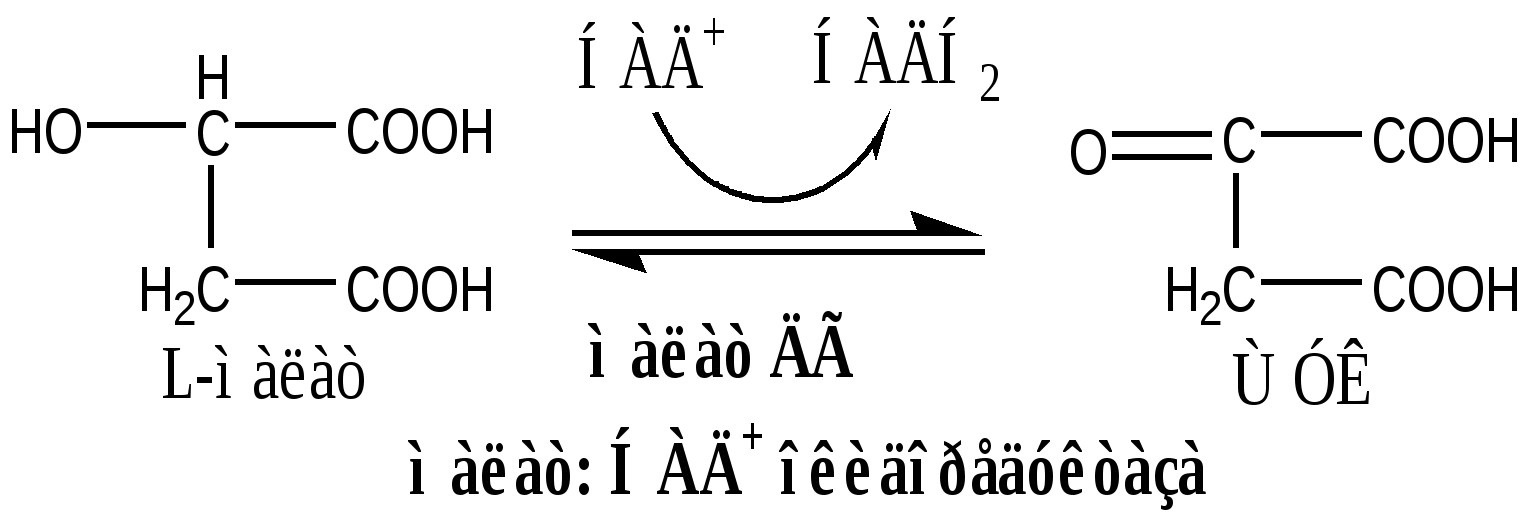 Образовавшиеся молекулы ЩУК реагируют с новой молекулой Ацетил-КоА и цикл повторяется вновь. Энергетический баланс одного оборота ЦТК В 4 окислительно-восстановительных реакциях ЦТК образуются 3 НАДН2 и 1 ФАДН2, которые направляются далее в дыхательную цепь окислительного фосфорилирования. В процессе окислительного фосфорилирования ДЦ из 1 НАДН2 образуется 3 АТФ, из 1 ФАДН2 - 2 АТФ. Из 1 ГТФ, образующейся в ЦТК за счет субстратного фосфорилирования, синтезируется 1 АТФ. Таким образом, за 1 цикл ЦТК из 3 НАДН2, 1 ФАДН2 и 1 ГТФ получается 12 АТФ. Коферменты и субстраты цикла Кребса – лекарственные препараты метаболической терапии. Препарат «Коэнзим композитум». Показания: Коррекция энергетического метаболизма при: длительной поддерживающей терапии больных: ─ тяжелыми острыми воспалительными заболеваниями; ─ хроническими воспалительными заболеваниями; 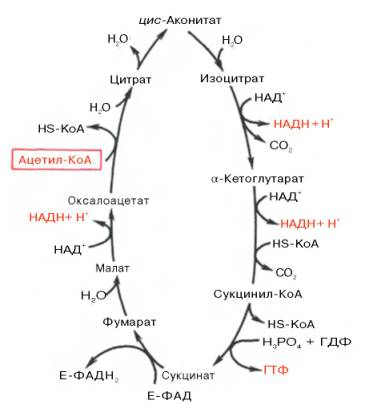 Фармакологические свойства: - энерготропное (регуляционное действие на работу внутриклеточных ферментных систем на уровне цикла Кребса и электронно-транспортной цепи, что сопровождается синтезом основного количества АТФ); - антигипоксическое; - антиоксидантное; - оптимизация витаминного и минерального обмена. Компоненты: - витамины: С, В1, В2, В6, РР - промежуточные катализаторы цикла Кребса: аконитовая, лимонная, яблочная, янтарная, фумаровая кислоты -субстраты -коферменты, растительные и минеральные компоненты 21. Состав, локализацию, последовательность расположения дыхательных комплексов в электронтранспортной цепи (ЭТЦ). Хемиосмотическую теорию Митчелла Дыхательная цепь окислительного фосфорилирования состоит из 4 белковых комплексов, встроенных во внутреннюю мембрану митохондрий и небольших подвижных молекул убихинона и цитохрома С, которые циркулируют в липидном слое мембраны между белковыми комплексами. Комплекс I – НАДН2 дегидрогеназный комплекс – самый большой из дыхательных ферментных комплексов –в качестве коферментов содержит ФМН и 5 железо-серных (Fe2S2 и Fe4S4) белков. Комплекс II – СДГ. В качестве коферментов содержит ФАД и железо-серный белок. Комплекс III – Комплекс b-c1 (фермент QH2 ДГ), существует в виде димера. Каждый мономер содержит 3 гема, связанных с цитохромами b562, b566, с1, и железо-серный белок. Комплекс IV – Цитохромоксидазный комплекс существует в виде димера. Каждый мономер содержит 2 цитохрома (а и а3) и 2 атома меди. Коэнзим Q (убихинон). Липид, радикал которого у млекопитающих образован 10 изопреноидными единицами (Q10). Убихинон переносит по 2Н+ и 2е-. убихинон ↔ семихинон ↔ гидрохинон Цитохром с. Периферический водорастворимый мембранный белок с молекулой гема. Хемиосмотическая теория Митчелла Для объяснения механизма окислительного фосфорилирования в 1961 году Митчеллом была предложена хемиосмотическая теория, которая включала четыре независимых постулата, касавшиеся функции митохондрий:
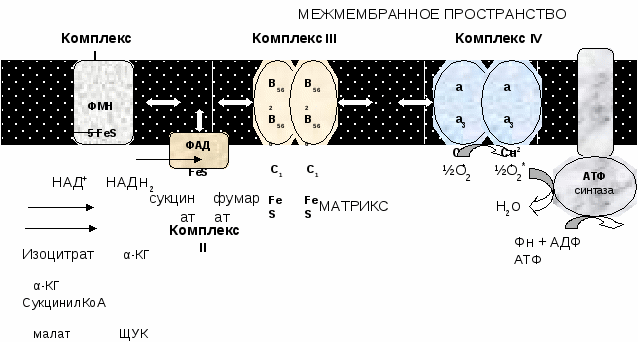 22. Механизмы сопряжения и разобщения окисления и фосфорилирования. Коэффициент Р/0. Понятие - дыхательный контроль. Эндогенные и экзогенные разобщители. электрохимический потенциал обеспечивает сопряжение (связывание) процессов окисления и фосфорилирования (окислительного фосфорилирования). Так как необходимый для сопряжения электрохимический потенциал создают I, III и IV комплексы дыхательной цепи, их называют пунктами сопряжения окисления и фосфорилирования. Повреждение внутренней мембраны митохондрий или увеличение ее проницаемости под действием разобщителей вызывает исчезновение электрохимического потенциала, разобщение процессов окисления и фосфорилирования, и прекращение синтеза АТФ. Разобщение дыхания и фосфорилирования называют явление исчезновения на мембране электрохимического потенциала под действием разобщителей и прекращение синтеза АТФ. Разобщителями являются вещества, которые могут переносить протоны (протонофоры) или другие ионы (ионофоры) через мембрану минуя каналы АТФ-синтетазы. В результате разобщения количество АТФ снижается, АДФ увеличивается, возрастает скорость потребления О2, окисления НАДН2, ФАДН2, а образовавшаяся свободная энергия выделяется в виде теплоты. Как правило, разобщители — липофильные вещества, легко проходящие через мембраны. Например, вещество 2,4-динитрофенол (переносит Н+), лекарство - дикумарол, метаболит - билирубин, гормон щитовидной железы - тироксин, антибиотики - валиномицин и грамицидин. Дыхательный контроль В норме субстраты тканевого дыхания и О2 находятся в достаточном количестве и не лимитируют окислительное фосфорилирование. Активность окислительного фосфорилирования ограничивает только концентрация АДФ, которая обратно пропорциональна концентрации АТФ. При нагрузке концентрация АТФ снижается, а АДФ увеличивается, что ускоряет дыхание и фосфорилирование. В состоянии покоя количество АТФ увеличивается, а АДФ снижается, что тормозит дыхание и фосфорилирование. Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30—50 г, но каждая молекула АТФ в клетке «живёт» меньше минуты. В сутки у человека синтезируется 40—60 кг АТФ и столько же распадается. Коэффициент окислительного фосфорилирования Для оценки эффективности окислительного фосфорилирования используют коэффициент окислительного фосфорилирования (Р/О). Коэффициентом окислительного фосфорилирования называют отношение количества фосфорной кислоты (Р), использованной на фосфорилирование АДФ, к атому кислорода (О), поглощённого в процессе дыхания. При окисление молекулы НАДН2, е- по дыхательной цепи проходят 3 пункта сопряжения, что обеспечивает синтез 3 АТФ при затрате 3 Н3РО4 и 3 АДФ на 1 атом кислорода. Соответственно для НАДН2 Р/О=3. При окисление молекулы ФАДН2, е- по дыхательной цепи проходят только 2 пункта сопряжения, что обеспечивает синтез 2 АТФ при затрате 2 Н3РО4 и 2 АДФ на 1 атом кислорода. Соответственно для ФАДН2 Р/О=2. Эти величины Р/О отражают теоретический максимум синтеза АТФ, фактически эта величина меньше из-за затрат на транспорт. |
