Органика. 1. Предмет орг химии. Этапы развития. Сырьевые источники. Функциональная группа. Классификация и номенклатура
 Скачать 410.1 Kb. Скачать 410.1 Kb.
|
1. Нитрование: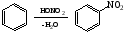 Нитрующие агенты: HNO3, HNO3/H2SO4, HNO3/CH3COOH, HNO3/(CH3CO)2O, NO2BF4 и др. 2. Галогенирование: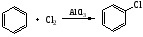 Сульфирование. Для сульфирования часто применяется серная кислота, содержащая избыток SO3 (олеум). Алкилирование по Фриделю – Крафтсу. Принято два возможных механизма протекания реакции. В первом случае электрофильной частицей является карбокатион, образующийся в результате взаимодействия галогеналкана с хлоридом алюминия (кислотой Льюиса): 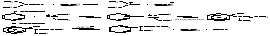 Во втором случае можно предполагать, что электрофилом служит алкильная группа полярного комплекса AlCl3 с алкилгалогенидом. 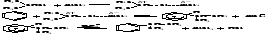 Алкилирование бензола (реакция Фриделя-Крафтса) C6H6 + C2H5Cl → С6H5-C2H5 + HCl Ацитилирование: 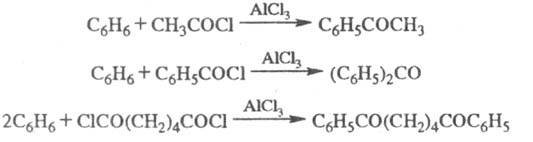 Механизм реакции. Механизм р-ции алкилирования предполагает, что сначала алкилгалогенид и катализатор образуют реагент (быстрая стадия), представляющий собой комплекс с переносом заряда или ионную пару , к-рый затем реагирует с ареном (медленная стадия), давая соединение; перенос протона к р-ри-телю приводит к продукту р-ции. Понятие о сигма- и пи-комплексах Образование пи-комплекса идет за счет пи-связи в соединении, а сигма-комплекса - за счет сигма-связи. Образование π-комплекса. Образовавшийся электрофил Х+(например, ион Br+) атакует богатое электронной плотностью бензольное ядро, образуя π-комплекс. Превращение π-комплекса в σ-комплекс. Электрофил отбирает 2 электрона у π-системы, образуя σ−связь с одним из атомов углерода бензольного кольца. Разница между пи- и сигма-связью: Сигма связь более крепкая, сигма связь образуется гибридными орбиталями Пи связь, которая образована негибридизованными пи-орбиталями. Пи-связь более удалены от центров, соединяемых атомов, поэтому она менее крепкая и её легче разорвать. 28. Правила ориентации в ароматическом ряду: активирующие и дезактивирующие заместители, их влияние на направление и скорость реакций электрофильного замещения. Факторы, определяющие соотношение изомеров. Примеры и механизмы реакций. Правила ориентации, в органической химии определяют порядок замещения в ароматическом кольце при наличии в нём заместителя (ориентанта). 1. Заместители, имеющиеся в бензольном ядре, направляют вновь поступающую группу в определенные положения, т.е. оказываются ориентирующее действие. 2. Заместители, уже имеющиеся в бензольном кольце, по своему ориентирующему действию на вновь входящие заместители делятся на две группы: заместители первого рода(активирующие) и заместители второго рода(дезактивирующие). Заместители (ориентанты) первого рода – это группировки атомов, способные отдавать электроны. К ним относятся – R, – ОН, ,–SH, – SR, – NH2, – NHR, – NHCOR, –N=N–, – CH3, , – Hal (F, Cl,Br, I). Эти заместители смещают электронную плотность в сторону бензольного кольца, т.е. обладают электродонорными свойствами. Они активируют бензольное кольцо (за исключением галогенов). Облегчая вхождение электрофильных реагентов в бензольное кольцо, они ориентируют новый заместитель в орто- и пара-положения. Такие заместители называют орто- и пара-ориентантами. При действии нуклеофильных реагентов реакция замещения протекает с большим трудом (при этом реагент должен быть ориентирован в метаположение). Заместители (ориентанты) второго рода – это атомные группировки, способные оттягивать (принимать) электроны от бензольного ядра.К ним относятся – SO3H, – NO2, – СНО, – COR, – СООН, – COOR, – CN, –CCl3, – NH3+, – NR+3 и т.д. Эти заместители смещают электронную плотность от бензольного кольца, т.е. они обладают электроноакцепторными свойствами. Эти заместители дезактивируют бензольное кольцо, затрудняя вхождение электрофильных реагентов. При этом вновь входящий заместитель ориентируют в мета–положение. Такие заместители называют мета-ориентантами. В то же время заместители второго рода облегчают реакциис нуклеофильными реагентами, способствуя в этом случае орто- и пара –ориентации. 29. Химические свойства ароматических углеводородов. Реакции присоединения. Окисление аренов. Реакции радикального замещения и окисления алкильных групп в алкилбензолах. Реакции присоединения Эти реакции характеризуют бензол и арены как непредельные соединения. Протекают они только в жестких условиях - высокой температуре, при наличии катализаторов, облучения и т.д. Воду, галогеноводороды бензол не присоединяет. Гидрирование: C6H6 + 3H2 → С6H12 циклогексан 2. Галогенирование: С6H6 + 3Сl2 → C6H6Cl6 гексахлорциклогексан (гексахлоран) – инсектицид Окисление Бензол очень стоек к обычным окислителям. На воздухе он горит с выделением сажи (при недостатке кислорода) или углекислого газа. 2C6H6 + 3O2 = 12C + 6H2O 2C6H6 + 15O2 = 12CO2 + 6H2O Гомологи бензола окисляются гораздо легче. Гомологи с более длинной боковой цепью окисляются с укорочением цепи. C6H5CH3 + 3O = C6H5COOH + H2O; C6H5CH3 + 2KMnO4 = C6H5COOK + 2MnO2 + KOH + H2O C6H5C2H5 + 4KMnO4 = C6H5COOK + K2CO3 + 4MnO2 + KOH + 2H2O Реакции радикального замещения и окисления алкильных групп в алкилбензолах - http://www.chemistry.ssu.samara.ru/chem2/u732.htm |
