все вопросы бх. А) Химическая природа ферментов Ферменты(энзимы) биологические катализаторы
 Скачать 6.2 Mb. Скачать 6.2 Mb.
|
ПереизбытокГипервитаминоз витамина D может вызывать нарушения метаболизма кальция, приводящие к гиперкальциемии и гиперкальциурии. При длительном лечении эргокальциферолом или холекальциферолом гиперкальциемия обычно обусловлена накоплением провитамина D3, но может быть вызвана одновременным избыточным потреблением пищевых продуктов, содержащих много кальция, например молочных продуктов[11]. Вит. F( арахидоновая, линолевая, линоленовая к-ты)Незаменимые жирные кислоты важны для сердечно-сосудистой системы: препятствует развитию атеросклероза, улучшает кровообращение, обладает кардиопротекторным и антиаритмическим действием. Полиненасыщенные жирные кислоты уменьшают воспалительные процессы в организме, улучшают питание тканей[13]. Суточная потребность человека оценивается в 5-10 грамм[9]. Витамин F в организме требуется для следующих процессов. Формирование мембран и стенок клеток Из полиненасыщенных жирных кислот в организме образуется эндогенный «хороший» холестерин, являющийся основой всех клеточных стенок и оболочек любых тканей. При его недостатке развивается ломкость кровеносных сосудов, возникают геморрагические явления, ухудшается работа нервной системы. Синтез жиров Многие липиды, необходимые для синтетических и энергетических процессов в организме, образуются именно из витамина F, поэтому без него немыслимы процессы регенерации тканей, запасание полезных веществ, работа печени, поддержание нормального состояния кожи и волос. Производство простагландинов Посредством простагландинов витамин F оказывает поддержку все нервной системе, ведь именно эти вещества являются медиаторами в различных реакциях возбуждения и торможения мускулов и нервных центров. Усвоение кальция и фосфора И как следствие — поддержка развития и функционирования костной ткани. Поддержка сперматогенеза И семенная жидкость, и сами сперматозоиды для производства требуют разных жирных кислот. При их недостатке синтез половых продуктов замедляется, и могут развиваться различные нарушения в половой сфере. Помощь иммунной системе При участии витамина F происходит производство некоторых антител. К тому же, жирные кислоты позволяют бороться с воспалениями и уменьшать их влияние на общее состояние всего тела. При воспалениях витамин F способствует уменьшению количества гистамина в крови, что уменьшает очаг воспаления и ускоряет его снятие. Восстановление повреждённых тканей Особенно это заметно при открытых ранах и других повреждениях наружных покровов тела. При достаточном количестве витамина F в организме их заживление происходит значительно быстрее. Связи же витамина F с другими веществами в организме так широки, что его недостаток отражается обычно организованно на всех системах органов. Наиболее явными проявлениями недостатка витамина F являются различные повреждения кожных покровов. Это может быть экзема, перхоть, шелушение кожи, различные высыпания, прыщи, утолщение эпидермиса. При этом же развивается ломкость ногтей и волос, может начаться облысение. Маленькие дети при недостатке витамина F в рационе сильно отстают в росте и психическом развитии. Параллельно у них увеличивается потребность в воде, но при этом увеличения количества выделяемой мочи не происходит, зато становится жидким стул. У мужчин при недостатке витамина F начинаются различные сексуальные расстройства и понижается выработка спермы. Хронический дефицит витамина F в рационе приводит к развитию нервных расстройств. Появляется депрессия, головные боли, возможно нарушение координации движений. И главным последствием постоянного недостатка витамина являются нарушения в работе кровеносных сосудов. Их стенки становятся тонкими и ломкими, часто возникают кровоизлияния разного масштаба, ухудшается их проницаемость. Вероятность развития атеросклероза при недостатке витамина F повышается в разы. Признаки гипервитаминоза витамина F у человека не выявляются даже при длительном поступлении избыточного количества его в организм. Чрезмерный прием может привести к увеличению веса тела. Не стоит злоупотреблять омега-3 жирными кислотами, т.к. у них есть свойство разжижать кровь и они могут быть причиной кровотечений. Гипервитаминоз витамина F проявляется болями в желудке, изжогой, кожно-аллергическими высыпаниями и связан с передозировкой ненасыщенных жирных кислот. 7. Процесс, начинающийся от пирувата, называется общим путем катаболизма и в свою очередь включает: окислительное декарбоксилирование пирувата цитратный цикл. Окислительное декарбоксилирование пировиноградной кислоты Суммарный результат многостадийной реакции выглядит следующим образом: 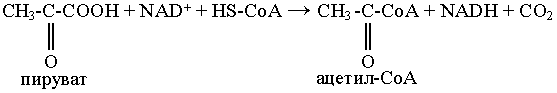 Реакция катализируется тремя ферментами, работающими в определенной последовательности и объединенными в пируватдегидрогеназный комплекс. Цитратный цикл Цитратный цикл (цикл Кребса, цикл трикарбоновых кислот) - это система реакций, приводящая к полному окислению двухуглеродного ацетильного фрагмента, имеющего различное происхождение. Цитратный цикл является общим конечным путем окисления белков, жиров и углеводов. Все реакции цитратного цикла, как и окислительного декарбоксилирования пирувата, локализованы в митохондриях. В ходе одного полного цикла происходит: полное окисление ацетильного остатка до двух молекул СО2; образование трех молекул восстановленного NAD+ и одной молекулы FADH2; образование одной молекулы GTP в результате субстратного фосфорилирования. Реакции цитратного цикла, ферменты и их характеристика приведена на рисунке: 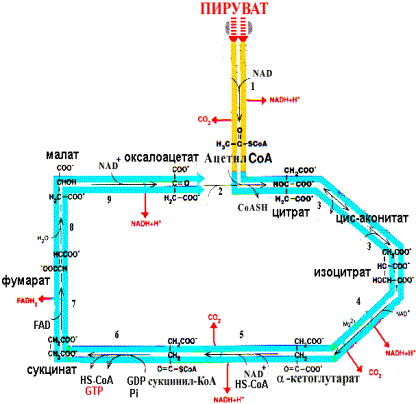 Схема цитратного цикла; ферменты: 1- пируватдегидрогеназный комплекс, 2- цитратсинтаза, 3- аконитаза, 4- изоцитратдегидрогеназа, 5- -кетоглутаратдегидрогеназный комплекс, 6- сукцинил-КоА-тиокиназа, 7- сукцинатдегидрогеназа, 8- фумараза, 9- малатдегидрогеназа Специфические пути катаболизма. Простые метаболиты подвергаются специфическим реакциям расщепления, в результате которых образуется либо пировиноградная кислота, либо ацетил - СоА. Причем ацетил - СоА может образоваться из пирувата в результате окислительного декарбоксилирования. Могут также образоваться другие соединения, непосредственно включающиеся в цитратный цикл.  Существует четыре этапа распада У, Ж, Б: I этап - Распад полимеров до мономеров: Белки до АК, Углеводы домоносахаров, Липиды до жирных кислот и глицерина. Процесс распада в основ гидролитический, освобождающаяся при этом в небольшом количестве энергия превращается в тепло. II этап - Мономеры подвергаются дальнейшему распаду по своим специфическим путям (1, 2, 3, 4, 5, 6) в результате чего все продукты переваривания пищи превращаются в ПВК и ацетил КоА. В ПВК превращаются все моносахара, глицерин, некоторые АК. Затем путем окислительного декарбоксилирования ПВК превращается в ацетил КоА. Минуя образование ПВК в ацетил КоА превращаются жирные кислоты и некоторые АК. Далее ацетил КоА вступает в реакции окисления в лимоннокислом цикле ( цикле трикарбоновых кислот (ЦТК)) Кребса. Образование ацетил КоА и реакции ЦТК (I и II этапы) относятся к общему пути катаболизма. Некоторы АК вступают в общий путь катаболизма на промежуточных стадиях ЦТК. III этап - Окисление ацетил КоА и др. метаболитов (α-кетоглутарат, щавелевоуксусная кислота (ЩУК)) в ЦТК. Этот этап сопровождается образованием восстановленных форм НАД ∙Н2 и ФАД∙Н2 IV этап - Через дыхательную цепь происходит перенос ℮‾ от восстановленных форм НАД ∙Н2 и ФАД∙Н2 на кислород. В результате образуется конечный продукт Н2О. 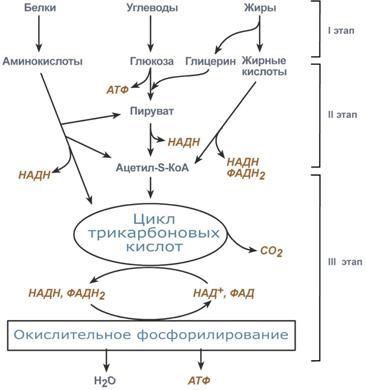 8 Вопрос Биологическое окисление - это совокупность реакций окисления, протекающих во всех живых клетках. Оно проходит 3 способами: 1.отщепление атомов Н+ 2.присоединение кислорода 3.перенос электронов Тканевое дыхание - это разновидность биологического окисления. В процессе тканевого дыхания в организме вырабатывается АТФ. Тканевое дыхание - это процесс расщепления органических веществ с выделением энергии в виде АТФ, что сопровождается поглощением кислорода, выделением СО2 и образованием воды. Расщепление органических веществ в организме проходит в 3 стадии: 1 и 2 стадия – это специфические пути превращения органических веществ, Ш стадия -–общая, объдиняет все пути превращения органических веществ. В ней образуется наибольшее количество энергии. Биологические виды энергии. Энергетические превращения в живой клетке подразделяют на две группы: локализованные в мембранах и протекающие в цитоплазме. В каждом случае для «оплаты» энергетических затрат используется своя «валюта»: в мембране это ΔμН+ или ΔμNa+, а в цитоплазме – АТФ, креатинфосфат и другие макроэргические соединения. Непосредственным источником АТФ являются процессы субстратного и окислительного фосфорилирования. Процессы субстратного фосфорилирования наблюдаются при гликолизе и на одной из стадий цикла трикарбоновых кислот (реакция сукцинил-КоА —> сукцинат). Генерация ΔμН+ и ΔμNa , используемых дляокислительного фосфорилирования, осуществляется в процессе транспорта электронов в дыхательной цепи энергосопрягающих мембран.Энергия разности потенциалов на сопрягающих мембранах может обратимо превращаться в энергию АТФ. Эти процессы катализируются Н+-АТФ-синтазой в мембранах, генерирующих протонный потенциал, или Na+-АТФ-синтазой (Na+-АТФазой) в «натриевых мембранах» алкалофиль-ных бактерий, поддерживающих ΔμNa+ [Скулачев В.П., 1989]. Cвет или энергия субстратов дыхания утилизируется ферментами фотосинтетической или дыхательной редокс-цепи (у галобактерий – бактериородопси-ном). Генерируемый потенциал используется для совершения полезной работы, в частности для образования АТФ. Будучи макроэргическим соединением, АТФ выполнняет функцию аккумулирования биологической энергии и ее последующего использования для выполнения клеточных функций. «Макроэргичность» АТФ объясняется рядом особенностей его молекулы. Это прежде всего высокая плотность зарядов, сконцентрированная в «хвосте» молекулы, обеспечивающая легкость диссоциациитерминального фосфата при водном гидролизе. Продукты этого гидролиза представляют собой АДФ и неорганический фосфат и далее – АМФ и неорганический фосфат. Это обеспечивает высокую величину свободной энергиигидролиза терминального фосфата АТФ в водной среде. Все окислительно-восстановительные реакции, протекающие в клетках катализируются ферментами класса- оксидоредуктаза. Типы реакций в процессах биологического окисления: Реакции связанные с передачей субстратом, который окисляется(SH2), АКЦЕПТОРУ (А), водорода (протонов и электронов): SH2 + A S + AH2 Реакции такого типа- дегидрирование, а ферменты которые их катализируют- дегидрогеназы. Коферменты дегидрогеназ, которые исполняют функцию акцепторов восстановительных эквивалентов: -никотинамид (пиридиновые) коферменты- нуклеотиды НАДФ+ и НАД+ -флавиновые коферменты- нуклеотиды ФАД и ФМН В зависимости от химической природы акцептора, с которым взаимодействуют дегидрогеназы, реакции дегидрирования делят на классы: Реакции дегидрирования, в которых акцептор- химическое соединение(R): SH2 + R S + RH2 Реакции дегидрирования, в которых как акцептор используется кислород: SH2 + O2 S + H2 O2 Ферменты, катализирующие эти реакции- аэробные дегидрогеназы, или оксидазы; в результате их образуется перекись водорода. Реакции, которые происходят с передачей от субстрата к акцептору электронов: Se– + A S + Ae– Реакции такого типа катализируются цитохромами дыхательной цепи митохондрий. Реакции, в основе которых – присоединение к субстрату, который окисляется, 1 или 2 атомов кислорода. Такие реакции- оксигеназные, ферменты- оксигеназы. В зависимости от количества атомов кислорода, оксигеназные реакции делят на: - монооксигеназные SH + 1/2 O2 ====S–OH - диоксигеназные S + O2===SO2 Монооксигеназные реакции катализируются цитохромом Р- 450 и лежат в основе окислительного гидроксилирования многих гидрофобных субстратов экзогенного и эндогенного происхождения ( микросомальное окисление). К диоксигеназным реакциям пренадлежат реакции переокисного окисления липидов. 10.вопрос Макроэргические соединения: А) Макроэргические соединения – органические соединения живых клеток, содержащие богатые энергией, или макроэргические связи. Эти соединения образуются в результате фото- и хемосинтеза и биологического окисления. К ним относятся, например, вещества, при гидролизе которых высвобождается энергии в 2—4 раза больше, чем при гидролизе других веществ. К макроэргическим соединениям относятся аденозинтрифосфорная кислота (АТФ), аденозиндифосфорная кислота (АДФ), а также пирофосфат (H4P2O7), полифосфаты (полимеры метафосфорной кислоты — (НРО3)n * Н2О) и ряд других соединений. Самое важное макроэргическое соединение — АТФ. Используя энергию, заключенную в макроэргических связях АТФ, при действии ферментов, переносящих фосфатные группы, можно получить другие макроэргические соединения, например, ГТФ (гуанозинтрифосфорная кислота), ФЕП (фосфоенолпировиноградная кислота) и др. Образуется АТФ в процессах биологического окисления и при фотосинтезе. Макроэргические связи — это ковалентные связи, которые гидролизуются с выделением значительного количества энергии: 30 кДж/моль и более (свободная энергия гидролиза).Вообще термин «макроэргическая связь» используется исключительно для связей, энергия которых используется в метаболизме и не указывает на истинную величину энергии связейОбычно это относится к макроэргическим молекулам — биологическим молекулам, которые способны накапливать и передавать энергию в ходе реакции. При гидролизе одной из связей высвобождается более 20 кДж/моль. По химическому строению макроэрги — чаще всего ангидриды карбоновой и фосфорной кислот, а также других слабых кислот. Примеры макроэргических соединений — молекулы АТФ, ГТФ и НАД. В АТФ имеются 2 макроэргические связи. Б) К макроэргическим соединениям относятся, главным образом, аденозинтрифосфорная кислота (АТФ) и вещества, способные образовывать АТФ в ферментативных реакциях переноса преимущественно фосфатных групп, а также нуклеозидтри- (или ди) -фосфорные кислоты, пирофосфорная и полифосфорная кислоты, креатинфосфорная, фосфопировиноградная, дифосфоглицериновая кислоты, ацетил- и сукцинилкоферменты А, аминоацильные производные адениловой и рибонуклеиновых кислот и другие.  Аденозинтрифосфорная кислота (АТФ) Аденозинтрифосфорная кислота (АТФ)Энергия, которая выделяется при распаде макроэргических соединений и за счет которой может быть совершена та или иная работа, используется не только для химического синтеза. Она может служить в организме для теплообразования, свечения, накопления электричества, выполнения механической работы и т. п. При этом химическая энергия преобразуется в тепловую, лучистую, электрическую, механическую и пр. Принципиально важно то, что преобразование химической энергии в другие ее виды протекает в организме при обязательном участии соединений с макроэргическими связями, в частности АТФ. В молекуле АТФ происходит трансформация стабильной энергии макроэргических межфосфатных химических связей в подвижную энергию возбуждения электронов пуриновой части молекулы; это и есть, вероятно, первый этап преобразования энергии в организме. Именно поэтому АТФ занимает центральное место в энергетическом обмене живой материи. В) В организме АТФ синтезируется путём фосфорилирования АДФ: АДФ + H3PO4 + энергия → АТФ + H2O. Фосфорилирование АДФ возможно тремя способами: субстратное фосфорилирование и окислительное фосфорилирование, (используя энергию окисляющихся веществ) и фотофосфорилирование в процессе фотосинтеза у растений. Основная масса АТФ образуется на мембранах митохондрий в ходе окислительного фосфорилирования H-зависимой АТФ-синтазой. Субстратное фосфорилирование АТФ не требует участия мембранных ферментов, оно происходит в цитоплазме в процессе гликолиза или путём переноса фосфатной группы с других макроэргических соединений. Реакции фосфорилирования АДФ и последующего использования АТФ в качестве источника энергии образуют циклический процесс, составляющий суть энергетического обмена. 11. ЦПЭ в митохондриях А) Дыхательная цепь переноса электронов (ЭТЦ)— система структурно и функционально связанных трансмембранных белков и переносчиков электронов. ЭТЦ запасает энергию, выделяющуюся в ходе окисления НАД∙Н и ФАДН2 молекулярным кислородом (в случае аэробного дыхания) или иными веществами (в случае анаэробного) в форме трансмембранного протонного потенциала за счёт последовательного переноса электрона по цепи, сопряжённого с перекачкой протонов через мембрану. Комплексы дыхательной цепи -Комплекс I (НАДН дегидрогеназа) окисляет НАД-Н, отбирая у него два электрона и перенося их на растворимый в липидах убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 2 протона и 2 электрона из матрикса в межмембранное пространство митохондрии. -Комплекс II (Сукцинат дегидрогеназа) не перекачивает протоны, но обеспечивает вход в цепь дополнительных электронов за счёт окисления сукцината. -Комплекс III (Цитохром bc1 комплекс) переносит электроны с убихинона на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии. Убихинон передаёт 2 электрона, а цитохромы за один цикл переносят по одному электрону. При этом туда также переходят 2 протона убихинона и перекачиваются комплексом. -Комплекс IV (Цитохромоксидаза) катализирует перенос 4 электронов с 4 молекул цитохрома на O2 и перекачивает при этом 4 протона в межмембранное пространство. Комплекс состоит из цитохромов a и a3, которые, помимо гема, содержат ионы меди. Кислород, поступающий в митохондрии из крови, связывается с атомом железа в геме цитохрома a3 в форме молекулы O2. Каждый из атомов кислорода присоединяет по два электрона и два протона и превращается в молекулу воды. Б) ЦПЭ локализуется на внутренней мембране митохондрий. 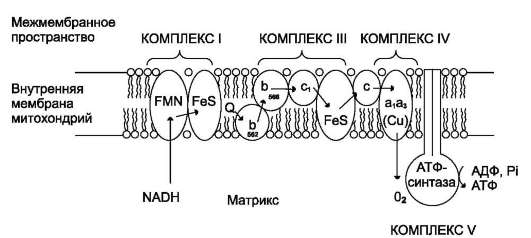 В) В интактной (неповрежденной) митохондриальной мембране перенос электронов в дыхательной цепи и фосфорилирование тесно сопряжены между собой. Так, например, выключение фосфорилирования по исчерпании АДФ либо неорганического фосфата сопровождается торможением дыхания (эффект дыхательного контроля). Большое число повреждающих митохондриальную мембрану воздействий нарушает сопряжение между окислением и фосфорилированием, разрешая идти переносу электронов и в отсутствие синтеза АТФ (эффект разобщения). В настоящее время наиболее признанной гипотезой, объясняющей синтез АТФ, является хемиосмотическая гипотеза. Хемиосмотическая гипотеза сформулированна английским биохимиком Питером Митчеллом. Согласно этой гипотезе, цепь переноса электронов можно представить себе как насос, перекачивающий ионы Н+. Энергия, высвобождаемая при переносе электронов, используется для перемещения ионов Н+ из митохондриального матрикса наружу, что приводит к возникновению электрохимического Н+ градиента с более высокой концентрацией ионов Н+ в наружной водной фазе. Этот же процесс ведет к появлению трансмембранного электрического потенциала - наружная сторона мембраны оказывается электроположительной. Ионы Н+ из окружающей Среды вновь устремляются внутрь, т.е. в митохондриальный матрикс, на этот раз по электрохимическому градиенту. Этот переход ионов Н+ из зоны с более высокой в зону с более низкой их концентрацией сопровождается выделением свободной энергии, за счет которой синтезируется АТФ. Электрохимический Н+ градиет с более высокой концентрацией Н+ на наружной мембране. Трансмембранный электрический потенциал - наружная мембрана заряжена положительно, а внутренняя - отрицательно. Ионы Н+ из окружающей среды по электрохимическому градиенту идут внутрь митохондрии и этот процесс сопровождается выделением свободной энергии, которая идет на синтез АТФ. 13. Ингибиторы можно разделить на 3 группы: ингибиторы собственно дыхательной цепи, ингибиторы окислительного фосфорилирования и разобщители окислительного фосфорилирования. Ингибиторы, блокирующие дыхательную цепь, по-видимому, действуют в трех местах. Одно из них ингибируется барбитуратами (например, амобарбиталом), а также антибиотиком пиерицидином А и ротеноном. Эти ингибиторы препятствуют окислению субстратов, которые поставляют восстановительные эквиваленты в дыхательную цепь при участии NAD-зависимых дегидрогеназ, — примером таких субстратов является гидроксибутират. Димеркапрол и антимицин А ингибируют дыхательную цепь на участке между цитохромом b и цитохромом с. Классические яды окись углерода и цианид — ингибируют цитохромоксидазу. Карбоксин и TTFA (теноилтрифторацегон) специфически ингибируют переход восстановительных эквивалентов от сукцинатдегидрогеназы на кофермент Q, а малонат является конкурентным ингибитором сукцинатдегидрогеназы. Антибиотик олигомицин полностью блокирует окисление и фосфорилирование в интактных митохондриях. Однако если вместе с олигомицином добавить к системе разобщитель динитрофенол, то окисление протекает, но без фосфорилирования. Это означает, что олигомицин не действует непосредственно на дыхательную цепь, а подавляет стадию фосфорилирования . Атрактилознд ингибирует окислительное фосфорилирование, блокируя транспорт адениновых нуклеотидов через внутреннюю митохондриальную мембрану. Он ингибирует транспорт ADP в митохондрии и выход АТР из митохондрий . Разобщители нарушают систему сопряжения процессов окисления в дыхательной цепи и фосфорилирования. В этих условиях процесс дыхания происходит неконтролируемым образом, поскольку концентрации ADP или Р, не являются лимитирующими. Чаще всего в качестве разобщителя используют 2,4-динитрофенол; аналогичное действие оказывает ряд других соединений: динитрокрезол, пентахлорфенол, СССР (карбонилцианид-л-хлорфенилгидразон). Последний по эффективности в 100 раз превосходит динитрофенол. Ингибиторы I комплекса — барбитураты, ротенон, пиерицидин Ингибитор II комплекса — малонат. Ингибитор III комплекса — антимицин А, миксотиазол, стигматтелин Ингибиторы IV комплекса — сероводород, цианиды, угарный газ, оксид азота. |
