биохимия хазипов. Биохимия животных Электронный дидактический комплекс (эдк)
 Скачать 14.38 Mb. Скачать 14.38 Mb.
|
|
Глава 1. ФИЗКОЛЛОИДНАЯ ХИМИЯ 1. Каким основным свойством обладает полупроницаемая мембрана: а) пропускает растворитель, но не пропускает дисперсную фазу золей; б) пропускает растворенное вещество, но не пропускает растворитель; в) пропускает только ионы. 2. Указать, какая смесь обладает буферным действием: а) СН3СООН+НСООН г) Н2СО3+ NаСl б) СН3СООН+NаСl д) СН3СООН+СН3СООNа в) NаОН+ СН3СООNа 3. Какое из указанных осмотических давлений наиболее близко соответствует осмотическому давлению крови животных? а) 4,9 атм г) 10,0 атм б) 7,8 атм д) 11,4 атм в) 8,9 атм 4. Дисперсная фаза золя при электофорезе смещается в сторону положительного электрода. Какой электролит наиболее эффективен для коагуляции этого золя? 1) НСI 4) MgCl2 2) NаСI 5) NaBr 3) Nа2SO4 5. Что определяет знак заряда коллоидной частицы? а) адсорбционный слой в) диффузный слой б) противоионы г) ядро 6. От чего зависит рН буферного раствора (кислого)? а) от константы диссоциации кислоты б) от объема растворителя соли в) от концентрации кислоты г) от соотношения между концентрациями кислоты и ее соли д) от концентрации соли 7. При определении рН жидкости, какая запись верна: а) водородный показатель равен 10-9 б) концентрация ионов водорода равна 9,0 в) рН = 10-9 г) сН = 10-9 д) рН = 9 8. Что понимают под активной реакцией среды? а) соотношение концентации ионов Н+ и ОН- б) концентрацию ионов Н+ в) концентрацию ионов ОН- г) произведение концентраций ионов Н+ и ОН- 9. Ионное произведение воды а) величина постоянная в) равно 1,8.10-16 б) равно 10-14 г) величина переменная 10. Буферные растворы способны сохранять определенное значение рН при: а) при нагревании раствора б) при повышенном осмотическом давлении в) при разбавлении раствора водой г) при добавлении определенных количеств кислот или оснований д) при добавлении любых количеств кислот или оснований 11. Количество компонентов буферных систем: а) два в) четыре б) три г) пять 12. От чего зависит рН буферных систем? а) от концентрации кислоты б) от концентрации ее соли в) от соотношения концентрации кислоты и ее соли 13. Что является фактором устойчивости золей? а) отсутствие заряда на поверхности частиц б) разноименные заряды на поверхности частиц в) наличие одноименного заряда на поверхности частиц г) гидратная оболочка частиц 14. Что такое изоэлектрическое состояние золя?
15. Факторы, способствующие коагуляции золей а) гидратная оболочка частиц б) заряд частиц в) отсутствие заряда частиц г) отсутствие гидратной оболочки частиц ГЛАВА 2. 2.1. БЕЛКИ
1) аргинин 4) аспарагиновая кислота 2) лизин 5) гистидин 3) валин 2. Биполярный ион моноаминомонокарбоновой аминокислоты заряжен: 1) отрицательно 2) электронейтрален 3) положительно 3. Приведенная аминокислота H2N—CН2—(CH2)3—CHNH2—COOH относится к группе аминокислот:
4.Установить соответствие: радикалы аминокислот аминокислоты 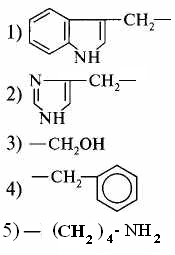 а) гистидин а) гистидин в) фенилаланин г) лизин д) триптофан 5. Иминокислотой является: 1) глицин 4) серин 2) цистеин 5) пролин 3) аргинин 6. Аминокислоты, входящие в состав белков, являются: 1) α-аминопроизводными карбоновых кислот 2) β-аминопроизводными карбоновых кислот 3) α-аминопроизводными ненасыщенных карбоновых кислот 7. Назвать аминокислоту: 
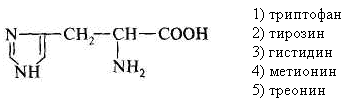 9.Установить соответствие: Аминокислота Группы
кислота 10. Серосодержащей аминокислотой является:
11. В состав белков не входят аминокислоты: 1) глутамин 3) аргинин
кислота 4) треонин 12. Гидроксигруппу содержат аминокислоты: 1) аланин 4) метионин 2) серин 5) треонин 3) цистеин 13. Установить соответствие: элементный химический содержание состав белка в процентах
14. В формировании третичной структуры белка не участвует связь: 1) водороданая 2) пептидная 3) дисульфидная 4) гидрофобное взаимодействие 15. Молекулярная масса белка варьирует в пределах: 1) 0,5-1,0 2) 1,0-5 3) 6-10 тысяч kДa 16. При денатурации белка не происходит: 1) нарушения третичной структуры 3) нарушения вторичной структуры 2) гидролиза пептидных связей 4) диссоциации субъединиц 17. Спектрофотометрический метод количественного определения белка основан на их свойстве поглощать свет в УФ-области при: 1) 280 нм 2) 190 нм 3) 210 нм 18. Аминокислоты аргинин и лизин составляют 20—30% аминокислотного состава белков: 1) альбуминов 4) гистонов 2) проламинов 5) протеиноидов 3) глобулинов 19. Белки волос кератины относятся к группе: 1) проламинов 4) глютелинов 2) протаминов 5) глобулинов 3) протеиноидов 20. 50% белков плазмы крови составляют: 1) α-глобулины 4) альбумин 2) β-глобулины 5) преальбумин 3) γ-глобулины 21. В ядрах клеток эукариот присутствуют главным образом:
2) гистоны 4) глобулины 22. К протеиноидам относятся: 1) зеин – белок семян кукурузы 4) фиброин – белок шелка 2) альбумин – белок яйца 5) коллаген – белок соеди- 3) гордеин – белок семян ячменя нительной ткани 23. Ортофосфорная кислота в фосфопротеинах обычно ковалентно связана:
24. К медьсодержащим белкам относится: 1) ферритин 4) церулоплазмин 2) ванадохром 5) лактоферрин 3) гемосидерин 25. Железосодержащими белками являются: 1) церулоплазмин 4) ферритин 2) карбоангидраза 5) пластоцианин 3) гемосидерин 26. В состав гема входит: 27. Гем представляет собой:
28. Трехвалентное железо содержится: 1) в дезоксигемоглобине 3) в метгемоглобине 2) в карбоксигемоглобине 4) в оксигемоглобине 29. Белки выполняют различные функции, кроме: 1) структурной 2) каталитической 3) регуляторной 4) генетической 5) рецепторной 30. Денатурация белков происходит в результате: 1) деградации первичной структуры 2) агрегации белковых глобул 3) изменений пространственных структур Глава 3. НУКЛЕИНОВЫЕ КИСЛОТЫ 1. К пиримидиновым основаниям относится: 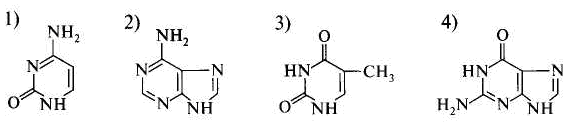 2. К пуриновым основаниям относится: 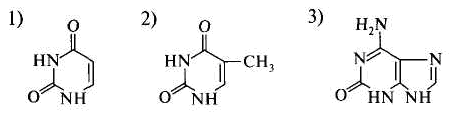 3. Входит в состав: 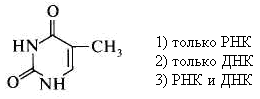 4. Входит в состав: 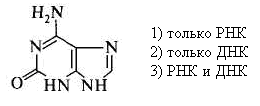 5. Является: 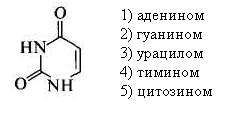 6. Является:  7. Установить соответствие: 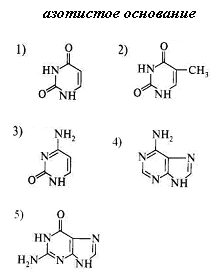 название а) аденин г) тимин б) гуанин д) урацил в) цитозин 8. В состав РНК не входит азотистое основание:
9. В состав нуклеозида входит:
кислоты 10. В состав нуклеотида входит:
11. В нуклеотидах азотистое основание и пентоза соединены связью: I) фосфоангидридными 4) 2',5'-фосфодиэфирными 2) 2',3'-фосфодиэфирными 5) N-гликозидными 3) 3',5'-фосфодиэфирными
1) Р.Митчелом и В.П.Скулачевым 2) Дж.Уотсоном и Ф.Криком 3) Ф.Жакобом и Ж.Моно 13. Согласно правилу комплементарности Чаргаффа водородные связи в молекуле ДНК замыкаются между: 1) аденином и гуанином 4) цитозином и тимином 2) аденином и тимином 5) цитозином и гуанином 3) урацилом и аденином 14. При формировании структур нуклеиновых кислот водородные свзи не возникают между: 1) аденином и гуанином 4) цитозином и тимином 2) аденином и тимином 5) цитозином и гуанином 3) урацилом и аденином 15. В молекуле ДНК число остатков аденина всегда равно числу остатков: 1) тимина 4) дегидроурацила 2) урацила 5) пиримидина 3) цитозина 16. В молекуле ДНК число остатков гуанина всегда равно числу остатков: 1) гуанин 4) цитозина 2) тимина 5) ксантина 3) урацила 17.Полинуклеотидные цепи в двухспиральной молекуле ДНК удерживаются: 1) коориднационными связями 3) ионными связями 2) водородными связями 4) гидрофобными взаимодействиями 18. В формировании третичной структуры ДНК у эукариот участвуют белки: 1) протамины 4) альбумины 2) глютелины 5) глобулины 3) гистоны 19. Вторичная структура тРНК имеет форму: 1) линейную 2) «клеверного листа» 3) «локтевого сгиба» 20. В продуктах полного гидролиза нуклеиновых кислот отсутствуют: 1) азотистые основания 3) гексозы 2) пентозы 5) фосфорные кислоты 21. При формировании структур нуклеиновых кислот водородные связи не возникают между:
22. В молекуле ДНК число остатков аденина всегда равно числу остатков: 1) гуанина 4) цитозина 2) тимина 5) ксантина 3) урацила 23. В молекуле ДНК число остатков гуанина всегда равно числу остатков:
24. Полинуклеотидные цепи в двухспиральной молекуле ДНК удерживаются: 1) координационными связями 3) ионными связями 2) водородными связями 4) гидрофобными взаимодей ствиями 25. В формировании третичной структуры ДНК у эукариот участвуют белки: 1) протамины 4) альбумины 2) глютелины 5) глобулины 3) гистоны 26. Вторичная структура тРНК имеет форму: 1) линейную 2) «клеверного листа» 3) «локтевого сгиба» Глава 4. ФЕРМЕНТЫ
2.Установить соответствие: ферменты катализируемая реакция
ные связи
3. Простые ферменты состоят из: 1) аминокислот 4) аминокислот и небел- 2) аминокислот и углеводов ковых компонентов 3) липидов 6) липидов и углеводов 4) углеводов 4. Скорость ферментативной реакции зависит от:
фермента 4) молекулярной гетерогенности фермента 5. К коферментам относятся:
6. Класс ферментов указывает на:
6. Установить соответствие: Класс фермента ферменты по классификации 1) 1 а) трансферазы 2) 2 б) лиазы 3) 3 в) оксидоредуктазы 4) 4 г) лигазы 5) 5 д) гидролазы 6) 6 е) изомераз 8. Активаторами ферментов являются: 1) ионы металлов 4) полипептиды 2) анионы 5) коферменты 3) аминокислоты 9. Ферменты необратимо ингибируются под действием: 1) липидов 3) ионов тяжелых металлов 2) аминокислот 4) углеводов 10. В состав фермента, катализирующего перенос электронов и протонов, входит: 1) биотин 4) НАД+ 2) глутатион 5) фолиевая кислота 3) пиридоксин 11. Аллостерическими эффекторами ферментов являются: 1) коферменты 4) углеводы 2) дипептиды 5) липиды 3) продукты превращения субстрата 12. Аллостерические ферменты могут иметь:
1) фермента 2) субстрата 3) фермента и субстрата
ферментативной реакции: 1) увеличивается 2) уменьшается 3) не изменяется 17. При иммобилизации ферментов на нерастворимых носителях появляется возможность:
белком; 3) уменьшить время протекания ферментативной реакции. 18. Для лечения вирусных инфекций наиболее эффективно применение фермента: 1)пепсина 3)трансаминазы 2) дезоксирибонуклеазы 4) каталазы 19. При заболеваниях поджелудочной железы наблюдается дефицит фермента: 1) альдолазы 3) липазы 2) пепсина 4) трансаминазы 20. Для очищения гнойных ран и удаления некротирующих тканей применяют фермент: I) липазу 3) амилазу 2) протеиназу 4) дегидрогеназу 21. Для определения глюкозы применяют фермент: 1) глюкозо-6-фосфатазу 3) гликозилтрансферазу 2) глюкозооксидазу 4) глюкокиназу ГЛАВА 5. ВИТАМИНЫ 1. В качестве структурных элементов изопреноидные фрагменты содержат витамины: 1) эргокальциферол 4) ретинол 2) токоферол 5) аскорбиновую кислоту 3) рутин 2. α-γ Диокси-β,β-диметил-β-аланинмасляной кислотой является: 1) пантотеновая кислота 4) биотин 2) пангамовая кислота 5) аскорбиновая кислота 3) карнитин 3. Производными стеролов являются: 1) цианкобаламин 4) холекальциферол 2) эргокальциферол 5) токоферол 3) ретинальацетат 4. Одним из наиболее эффективных природных антиоксидантов является: 1) филлохинон 4) ретинол 2) викасол 5) токоферол 3) холекальциферол 5. Для нормального световосприятия необходим: 1) ретинол 4) пиридоксаль 2) токоферол 5) биотин 3) рибофлавин 6. Антигеморрагическим действием обладает витамин: 1) эргокальциферол 4) рутин 2) ретинол 5) аскорбиновая кислота 3) филлохинон 7. Составной частью коэнзима А является: 1) п-аминобензойная кислота 4) оротовая кислота 2) пиридоксин 5) пантотеновая кислота 3) карнитин 8. Ксерофтальмию вызывает дефицит в организме витамина: 1) аскорбиновой кислоты 4) холекальциферола 2) тиамина 5) токоферола 3) ретинола 9. Повышение проницаемости и хрупкость сосудов возникают при недостаточности витамина: 1) тиамина 4) аскорбиновой кислоты 2) ниацина 5) токоферола 3) пиридоксина 10. Витамин B6 входит в состав следующих ферментов обмена аминокислот: 1) метилтрансфераз 3) глутаматдегидрогеназы 2) аминотрансфераз 4) декарбоксилаз 11. Витамин B3 входит в состав: 1) дегидрогеназ 3) мутаз 2) ацил-КоА-трансфераз 4) метилтрансфераз 12. В обмене липидов участвуют витамины: 1) тиамин 4) фолиевая кислота 2) рибофлавин 5) пантотеновая кислота 3) пиридоксин Глава 6. ГОРМОНЫ 1. Основной функцией гормонов является: 1) защитная 3) каталитическая 2) регуляторная 4) транспортная 2. Координирующим центром эндокринной системы является: 1) гипофиз 4) гипоталамус 2) спинной мозг 5) тимус 3) поджелудочная железа 3. Роль гормонов передней доли гипофиза заключается: 1) в регуляции функций периферических эндокринных желез; 2) в ингибировании секреции рилизинг-факторов; 3) в активации выработки статинов. 4. К гормонам белковой природы относятся: 1) трииодтиронин 4) адреналин 2) тироксин 5) альдостерон 3) паратгормон 5. Инсулин представляет собой: 1) производное ненасыщенных жирных кислот 2) производное аминокислоты тирозина 3) низкомолекулярный белок 4) гликопептид 6. Иод входит в состав: 1) глюкагона 3) кальцитонина 2) паратгормона 4) тироксина 7. К стероидным гормонам относятся: 1) кальцитонин 4) тестостерон 2) вазопрессин 5) адреналин 3) окситоцин 8. К гормонам, производным ароматических аминокислот, относятся: 1) эстрадиол 3) секретин 2) тироксин 4) норадреналин 9. В поджелудочной железе синтезируются: 1) тироксин 4)адреналин 2) глюкагон 5) инсулин 3) окситоцин 10. В регуляции обмена электролитов принимает участие: 1) инсулин 4) прогестерон 2) норадреналин 5) тиреотропин 3) альдостерон 11. Содержание кальция и фосфора в крови регулируют: 1) паратгормон 4) эстрадиол 2) кальцитонин 5) глюкагон 3)адренокортикотропин 12.Гормоны пептидной природы синтезируются: 1) в коре надпочечников 4) в гипофизе 2) в мозговом слое надпочечников 5) в яичниках 3) в семенниках 13. Стероидные гормоны синтезируются: 1) в поджелудочной железе 4) в коре надпочечников 2) в семенниках 5) в щитовидной железе 3) в мозговом слое надпочечников 14. В слизистой кишечника секретируется гормон: 1) инсулин 4) гастрин 2) секретин 5) кортикотропин 3) соматолиберин 15. Развитие вторичных половых признаков у особей мужского пола стимулирует: 1) тестостерон 4) прогестерон 2) андростерон 5) окситоцин 3) эстрадиол 16. Биосинтез кортикостероидов стимулирует: 1) адренокортикотропин 3) кортикостерон 2) кальцитонин 4) инсулин 17. Синтез гормонов щитовидной железы активирует: 1) кортикотропин 2) тиреотропин 3) соматотропин 18. Минералокортикоиды регулируют обмен: 1) углеводный 2) липидный 3) водно-солевой 19. Производными ненасыщенных жирных кислот являются: 1) пролактин 4) секретин 2) простагландины 5) тироксин 3) соматостатин 20. Дофамин вырабатывается: 1) в мозговом слое надпочечников 4) в семенниках 2) в коре надпочечников 5) в паращитовидной железе 3) в тимусе 21. Инсулин — гормон поджелудочной железы является: 1) стероидным гормоном; 2) производным аминокислот; 3) гормоном белково-пептидной природы. 22. Гормоны гипоталамуса являются:
3) производными высших жирных ненасыщенных кислот. 23. Установить соответствие: гормон тип рецепции 1) адреналин а) цитозольный 2) глюкагон б) мембрано-опосредованный 3) тироксин 4) прогестерон 24. Циклические нуклеотиды: 1) ингибируют фосфодиэстеразу; 2) активируют протеинкиназы, способные фосфорилиро вать белки; 3) активируют кальмодулин, входящий в состав некоторых протеинкиназ. 25. Вторичными посредниками гормонов в клетке являются: 1) ионы кальция 4) АТФ 2) цАМФ 5) кальмодулин 3) ГДФ Глава 7. ОБМЕН ВЕЩЕСТВ И ЭНЕРГИИ 1. Конечными продуктами обмена являются: 1) ацетил-КоА 4) H2O 2) мочевина 5) CO2 3) пируват 2. Центральную роль в энергообмене всех типов клеток осуществляет: 1) креатинфосфат 2) электрохимический потенциал сопрягающих мембран 3) ГТФ 4) система адениловых нуклеотидов 3. В молекуле АТФ макроэргической является связь: 1) гликозидная 2) фосфоэфирная 3) фосфоангидридная 4. Указать, какое соединение не относится к макроэргическим: 1) фосфоеноилпируват 4) аденозинтрифосфат 2) 1,3-дифосфоглицерат 5) цитидинтрифосфат 3) глюкозо-6-фосфат 5. Реакции биологического окисления, сопровождающиеся трансформацией энергии химических связей окисляемых субстратов в энергию АТФ, протекают путем: 1) активации молекулярного кислорода;
6. Синтез АТФ в клетках эукариот протекает на: 1) внутренней мембране митохондрий 3) мембранах ЭПР 2) наружной мембране митохондрий 4) плазматической мембране 7. Первичными акцепторами электронов от окисляемого субстрата к молекулярному кислороду являются: 1) коэнзим Q 4) трансферрин
8. Пиридинзависимые дегидрогеназы в качестве кофермента содержат: 1) гем 2) ФМН 3) НАД+ 4) ФАД 5) НАДФ+ 9. В состав НАД входят: 1) амид никотиновой кислоты 3) АМФ 2) изоаллоксазин 4) рибитол 10. Пиридинзависимые дегидрогеназы локализованы: 1) только в цитозоле 2) только в митохондриях 3) в цитозоле и в митохондриях 11. Простетической группой первичных акцепторов водорода флавиновых дегидрогеназ является: 1) НАДФ+ 2) ФАД 3) ФМН 12. В состав простетических групп флавиновых дегидрогеназ входит витамин: 1) В1 2) B2 3)В5 4) B3 5) B6 13. Активной частью молекулы ФАД или ФМН является:
3) изоаллоксазин 14.Синтез АТФ за счет энергии, выделяющейся при переносе электронов от окисляемого субстрата к молекулярному кислороду, называют:
15.Количество энергии, выделяющейся при переносе электронов от ФАДН2 к молекулярному кислороду, обеспечивает синтез АТФ: 1) 3 2) 2 3) 1 16. Установить соответствие: тип окисления роль кислорода 1) митохондриальное а) непосредственно внедряется в 2) микросомальное окисляемое вещество и исполь- зуется для образования воды б) является конечным акцептором электронов ииспользуется лишь для образования воды Глава 8. ХИМИЯ ОБМЕНА УГЛЕВОДОВ 1. Функцией углеводов не является: 1) защитная 4) энергетическая 2) резервная 5) каталитическая 3) структурная 2. Углеводы не входят в состав: 1) гликопротеинов 2) фосфолипидов 3) гликолипопротеинов 4) нуклеопротеинов 3. Моносахариды являются производными: 1) гидроксикарбоновых кислот 2) алифатических карбоновых кислот 3) многоатомных спиртов, содержащих карбонильную группу 4) ароматических карбоновых кислот циклических многоатомных спиртов 4. Природные моносахара относятся: 1) к L-ряду 2) к D-ряду 5.α- и β-Аномеры углеводов различаются конфигурацией при: 1) последнем хиральном атоме углерода 2) полуацетальном атоме углерода 3) втором атоме углерода, считая от альдегидной или ке- тогруппы 6. Назвать углевод: 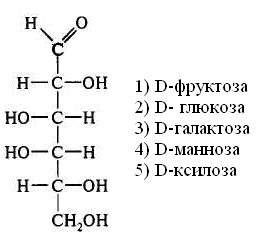 7. Назвать углевод: 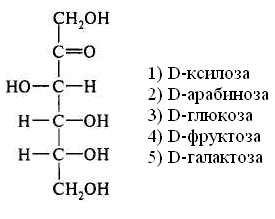 8. Назвать углевод: 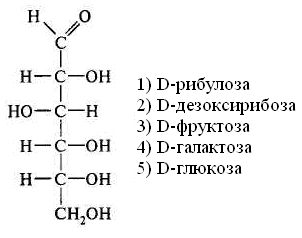 9. Назвать углевод: 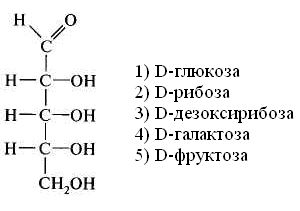 10. Назвать углевод: 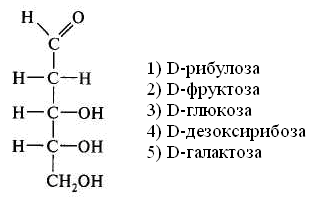 11. Назвать углевод: 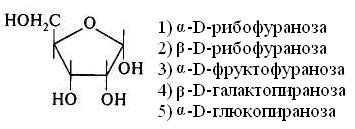 12. Назвать углевод: 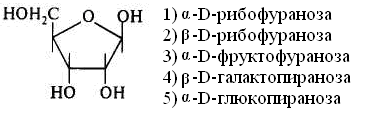 13. Назвать углевод: 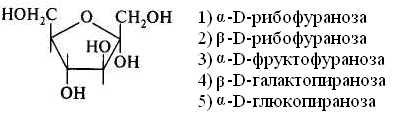 14. Установить соответствие: кислота название 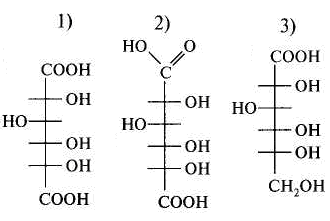 а) D-глюкуроновая б) D-глюконовая в) D-глюкаровая 15. Установить соответствие: спирт название 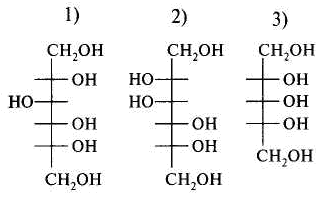 а) маннит б) рибит в) сорбит 16. Назвать углевод: 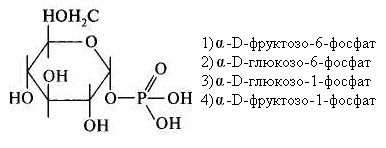 17. Назвать углевод: 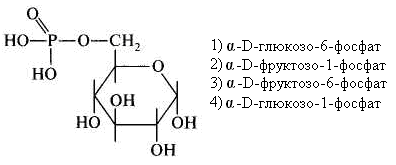 18. D-Фруктоза входит в состав: 1) мальтозы 2) сахарозы 3) лактозы 19. Назвать углевод: 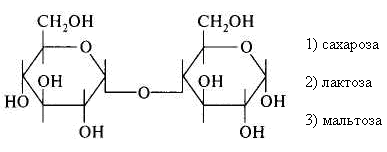 20. Назвать углевод: 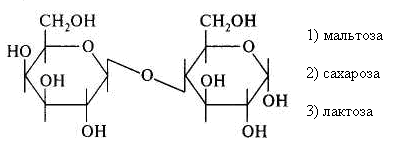 21. Назвать углевод: 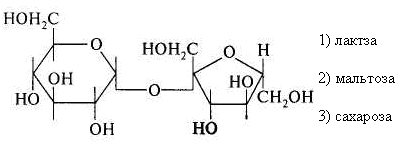 22. При гидролизе сахарозы образуются: 1) два остатка D-глюкозы 2) a-D-глюкоза и p-D-галактоза 3) D-глюкоза и D-фруктоза 4) D-глюкоза и D-манноза 5) два остатка a-D-маннозы 23. При кислотном гидролизе лактозы образуются: 1) два остатка α-D-глюкозы 4) α-D-глюкоза и α-D-манноза 2) α-D-глюкоза и β- D-галактоза 5) два остатка α-D-маннозы 3) α-D-глюкоза и α-D-фрутоза 24. Установить соответствие: дисахарид свойства дисахаридов 1) мальтоза а) восстанавливающие 2) сахароза б) невосстанавливающие 3) целлобиоза 4) лактоза 25. Отсток фруктозы входит в состав: 1) гликогена 3) инулина 2) крахмала 4) целлюлозы 26. К гетерополисахаридам относятся:
27. К готополисахаридам относятся: 1) крахмал, гликоген, целлюлоза 2) гликоген, гепарин, крахмал 3) гиалуроновая кислота, гликоген, гепарин 28. При полном гидролизе целлюлозы образуется: 1) β-D-глюкоза 3) α-D-фруктоза 2) α-D-глюкоза 4) α-D-фруктозо-6-фосфат 29. К линейным полисахаридам относится: 1) гликоген 2) амилоза 3) амилопектин 30. К структурным полисахаридам не относится:
ГЛАВА 8.1. КАТАБОЛИЗМ УГЛЕВОДОВ 1. Основными источниками в кормах являются 1) гликоген 4) коллаген 2) эластин 5) крахмал 3) целлюлоза 6) фибрины 2. Все известные амилазы ЖКТ осуществляют расщепление:
2) β-1,6-гликозидных связей 4) β-1,4-гликозидных связей 3. Расщепление а-(1→6)-гликозидной связи в полисахаридах катализируется ферментами: 1) гликогенфосфорилазы 3) α-(1—>6)-глюкозидазой 2) α-(1-6)-глюкантрансферазой 4) α-амилазой 4. Глюкозо-6-фосфат образуется в результате реакций:
5. Установить соответствие: фермент катализируемая реакция 1) гексокиназа а) расщепление фруктозо-1,6-фосфата на две триозы 2) гликогенфосфорилаза б) расщепление а-1,4-связи в молекуле гликогена 3) альдолаза в) фосфорилирование глюкозы 6. В процессе гликолиза АТФ расходуется в реакциях образования: 1) фруктозо-6-фосфата 4) 3-фосфоглицеральдегида 2) глюкозо-6-фосфата 5) 3-фосфоглицерата 3) фруктозо-1,6-дифосфата 7. В процессе гликолиза АТФ образуются в реакциях превращения: 1) 1,3-дифосфоглицерата 4) 3-фосфоглицеральдегида 2) 2-фосфоеноилпирувата 5) 2-фосфоглицерата 3) 3-фосфоглицерата 8. Для превращения фруктозо-6-фосфата во фруктозо-1,6-дифосфат под влиянием фосфофруктокиназы необходим: 1) НАДФН • H+ 4) НАД+ 2) коэнзим А 5) НАДН • H+ 3) АДФ 6 ) АТФ 9. Установить соответствие: гликолиз путь синтеза АТФ 1) аэробный а) окислительное фосфорилирование 2) анаэробный б) субстратное фосфорилирование в) оба пути 10.Образование этанола из пирувата при спиртовом брожении катализируют ферменты: 1) пируватдекарбоксилаза 2) фосфоеноилпируватгидратаза (енолаза) 3) глицеральдегидфосфатдегидрогеназа 4) фосфоглицераткиназа 5) алкогольдегидрогеназа 11. Гликогенфосфорилаза катализирует реакцию: I) образования свободной глюкозы
4) образования глюкозо-6-фосфата Глава 8.2 ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ 1. Коэнзим А выполняет функцию переносчика:
3) фосфатных групп 2. В цикле трикарбоновых кислот декарбоксилированию подвергаются субстраты: 1) пируват 4) фумарат 2) изоцитрат 5) цитрат 3) α-кетоглутарат 3. Дегидрирование в цикле трикарбоновых кислот происходит в реакциях образования: 1) изоцитрата 5) α-кетоглутарата 2) сукцинил-коэнзим А 6) цитрата 3) оксалоацетата 7) сукцината 4) фумарата 8) L-малата 4. Гидратация субстрата в цикле трикарбоновых кислот происходит в реакциях превращения: 1) цитрата в цисаконитат 4) оксалоацетата в цитрат 2) сукцинил-коэнзим А в сукцинат 5) цисаконитата в изоцитрат 3) фумарата в малат 5. При полном окислении D-глюкозы до CO2 и H2O образуется количество АТФ: 1) 12 4) 36 2) 24 5) 38 3) 30 6. Наибольшее количество АТФ образуется в процессе: 1) окислительного декарбоксилирования пирувата; 2) гликолиза; 3) цикла трикарбоновых кислот; 4) пентозомонофосфатного пути. 7. Установить соответствие: процессы количество синтезированных молекул АТФ 1) Сукцинат → Оксалоацетат а) 12 2) Ацетил-КоА → 2CO2 + 4H2O б) 15 3) Пируват →3CO2 + 5H2O в) 3 4) Пируват → Ацетил-КоА + CO2 + H2O г) 5 5) Сукцинат → Фумарат д) 2 Глава 9. ХИМИЯ И ОБМЕН ЛИПИДОВ 1. Липиды растворимы:
3) в кислоте 2. Ацилглицеролы относятся к группе: 1) глицерофосфолипидов 4) восков 2) нейтральных липидов 5) терпенов 3) гликолипидов 3. Сложные липиды наряду с остатками многоатомных спиртов и высших жирных кислот содержат:
3) азотсодержащие соединения, фосфорную кислоту, углеводы;
1) синтетазы высших жирных 4) вируса табачной мозаики кислот 5)мультиферментных комплексов 2) рибонуклеопротеидных комплексов 3) биомембран клетки 5. Мононенасыщенной жирной кислотой является: 1) линолевая 2) стеариновая 3) олеиновая 4) миристиновая 5) линоленовая 6. Установить соответствие: компонент фосфолипида название 1) неполярная часть фосфолипида а) фосфорная кислота 2) полярная часть фосфолипида б) диацилглицерол в) холин г) этаноламин д) инозитол 7. Наибольшее количество сфинголипидов содержится в мембранах клеток: 1) жировой ткани 3) селезенки 2) нервной ткани 4) легких 8. Стероиды являются производными: 1) фенантрена 4) пергидрофенантрена 2) циклопентана 5) протопорфирина 3) циклопентанпергидрофенатрена 9. Назвать стероид: 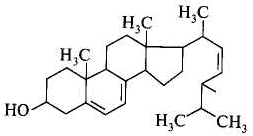 1) прогестерон 2) холестерол 3) тестостерон 4) эргостерол 5) альдостерон 10. Холестерол не является предшественником: 1) желчных кислот 4) половых гормонов 2) витамина D2 5) витамина D3 3) кортикостероидных гормонов 11. При окислении 1 г жира выделяется энергия в количестве (кДж): 1) 16,9 2) 220,0 3)39,0 4) 75,0 5) 34,5 12. Йодное число является показателем: 1) качества природного жира 2) содержания свободных жирных кислот
4) содержания в жире ненасыщенных жирных кислот 13. Регуляторную функцию выполняют: 1) фосфолипиды 4) стеролы 2) сфинголипиды 5) терпены 3) простагландины 14.Установить соответствие: кислота число атомов углерода: число двойных связей, Д - их положение 1) стеариновая а) 18: 1 (Д 9) 2) линолевая б) 16: 0
5) пальмитиновая д) 18: 0 15. Основными липидными компонентами (80—90%) плазматических биомембран являются: 1) нейтральные липиды 4) стероиды 2) гликолипиды 5) свободные жирные кислоты 3) фосфолипиды 16. Способность молекул фосфолипидов самопроизвольно формировать бислои в водных растворах обусловлена их: 1) гидрофобными свойствами 2) гидрофильными свойствами 3) амфифильными свойствами 17. Указать органеллу, имеющую внутреннюю и наружную мембраны: 1) рибосомы 4) митохондрии 2) ядро 5) лизосомы 3) аппарат Гольджи 18. В отличие от активного транспорта пассивный:
4) энергонезависим 19. Перечислить виды пассивного транспорта: 1) простая диффузия 4) фагоцитоз 2) Na+-, К+-насос 5) пиноцитоз 3) облегченная диффузия 20. Глюкоза может поступать в клетку путем:
3) облегченной диффузии и симпорта с ионами Na+ 4) антипорта с ионами Na+ 21. Работа Na+/ К+-насоса обеспечивает:
22. Na+/ К+-АТФ-аза выкачивает три иона Na+ в обмен на: 1) один ион K+ внутрь клетки 3) три иона K+ внутрь 2) два иона K+ внутрь клетки клетки 23. Роль Na+/ К+-АТФ-азы в клетке заключается:
24. Сложноэфирные связи в молекулах триацилглицеролов подвергаются ферментативному гидролизу при участии: 1) фосфолипазы 4) липазы 2) неспецифической эстеразы 5) ацетилхолинэстеразы 3) алилэстеразы 25. Первичные желчные кислоты образуются непосредственно из: 1) эргостерола 4) альдостерона 2) холановой кислоты 5) прегненалона 3) холестерола 26. В образовании парных желчных кислот участвуют: 1) таурин 4) глицин 2) серин 5) аланин 3) цистеин 27. С участием желчных кислот происходит: 1) всасывание глицерола 2) всасывание моносахаридов 3) эмульгирование липидов 4) активация липопротиенлипазы 5) всасывание высших жирных кислот 28. Гидролиз триацилглицеролов панкреатической липазой происходит:
4) постадийно, вначале 2 связь, затем 1 и 3 29. Образование хиломикронов локализовано: 1) в клетках эпителия кишечника 4) в печени 2) в крови 5) в селезенке 3) в лимфе 30. Установить соответствие: гидролитическое расщепление фосфолипида 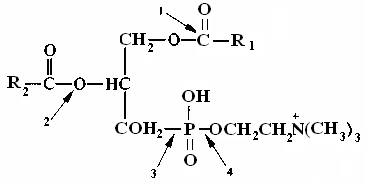 катализирует фермент: а) фосфолипаза A1 в) фосфолипаза D б) фосфолипаза С г) фосфолипаза A2 31. Основной путькатаболизма высших жирных кислот: 1) восстановление 4) β-окисление 2) w-окисление 5) декарбоксилирование 3) α-окисление 32. Окисление жирных кислот локализовано: 1) в цитозоле 2) в межмембранном пространстве митохондрий 3) в матриксе митохондрий 4) в эндоплазматическом ретикулуме 5) в пероксисомах 33. Указать фермент: 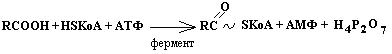 1) ацетилтрансфераза 3) ацил-КоА-трансфераза 2) ацил-КоА-синтетаза 4) ацетил-КоА-ацилтрансефраза 34. Транспорт активированных жирных кислот из цитозоля В митохондрии осуществляется главным образом с помощью: 1) карнитина 2) цитрата 3) малата 35. Установить последовательность реакций β-окисления жирных кислот: 1) тиолазная реакция 4) активация жирной кислоты 2) первое дегидирование 5) гидратация 3) второе дегидрирование 36. Каждая стадия β-окисления высших жирных кислот сопровождается образованием количества АТФ: 1) 3 2) 5 3) 2 4) 8 5) 7 37. Число стадий β-окисления жирной кислоты, содержащей число атомов углерода, равное n, составляет: 1) n 2) n/2 3) n/2 - 1 38. Количество АТФ, образующихся при полном окислении пальмитиновой кислоты до СО2 и Н2О: 1) 130 2)147 3)131 4)96 5) 105 39. К кетоновым телам относятся: 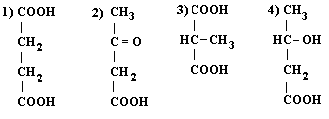 40. Предшественником для синтеза кетоновых тел является: 1) жирная кислота 4) малонил-КоА 2) глюкоза 5) сукцинил-КоА 3) ацетил-КоА 41. Структурным предшественником для синтеза жирных кислот служит: 1) малонил-КоА 4) оксалоацетат 2) цитрат 5) пируват 3) ацетил-КоА 42. Мультиферментный комплекс синтетаза высших жирных кислот локализован: 1) в матриксе митохондрий 3) в эндоплазматическом ретикулуме 2) в цитозоле 4) во внутренней мембране мито- хондрий 43. Особенно активно липогенез протекает: 1) в мышцах 4) в жировой ткани 2) в печени 5) в легких 3) в селезенке 44. Глицерол, образующийся при распде триацилглицеролов, независмо от пути его дальнейшего превращения в организме прежде всего: 1) окисляется 4) фосфоримлируется 2) восстанавливается 5) ацилируется 3) метилируется 45. Общим интермедиатом для синтеза триацилглицеролов и глицерофосфолипидов является: 1) диоксиацетон 4) 2-моноацилглицерол 2) 3-фосфоглицериновый альдегид 5) 1,2-диацилглицерол 3) фосфатидная кислота 46. Фосфатидная кислота синтезируется в процессе: 1) фосфорилирования глицерола 2) восстановления диоксиацетона 3) гидролиза сложных эфиров 4) расщепления фосфоангидридов высших жирных кислот 5) эстерификации глицерол-3-фосфата 47. Биосинтез глицеролфосфолипидов локализован: 1) в митохондриях 3) в аппрате Гольджи 2) в эндоплазматическом ретикуруме 4) в цитозоле |
