биохимия хазипов. Биохимия животных Электронный дидактический комплекс (эдк)
 Скачать 14.38 Mb. Скачать 14.38 Mb.
|
7. ОБМЕН ВЕЩЕСТВ И ЭНЕРГИИОбмен веществ и энергии являются главной сущностью жизнедеятельности любого организма. В процессе обмена веществ образуется энергия и используется для поддержания температуры тела, совершения работы, роста и развития организма, обеспечения структур и функций всех клеточных элементов. Обмен веществ и энергии неразрывно связаны между собой и включают два процесса – ассимиляцию (анаболизм) и диссимиляцию (катаболизм). Катаболизм – это процесс расщепления сложных органических молекул до более простых конечных продуктов. Углеводы, жиры и белки, поступившие извне с кормами и присутствующие в самой клетке в качестве запасных веществ, распадаются в последовательных реакциях до таких соединений, как молочная кислота, CO2 и аммиак. Катаболические процессы сопровождаются освобождением свободной энергии, заключенной в сложной структуре больших органических молекул. Эта энергия запасается в молекулах АТФ (аденозинтрифосфата) и частично в богатых энергией водородных атомах кофермента НАДФН2 -никотинамидадениндинуклеотидфосфата, находящегося в восстановленной форме. Ферментативное расщепление белков, углеводов, липидов происходит последовательно через ряд этапов. На первой стадии полисахариды распадаются до моносахаридов, жиры – до жирных кислот, глицерина и других компонентов, а белки – до аминокислот. Все эти компоненты на второй стадии катаболизма превращаются в еще более простые соединения: гексозы, пентозы и глицерин расщепляются до пировиноградной кислоты (пируват), затем до активированной уксусной кислоты – ацетил-коэнзима А. Расщепление жирных кислот и большинства аминокислот также завершается с образованием ацетил-КоА. На третьей стадии катаболизма ацетил-КоА вступает в цикл лимонной кислоты, где происходит его окисление до CO2 и H2O. Схематическое изображение стадии катаболизма представлено на рис.7.1. Анаболизм (ассимиляция) или биосинтез происходит одновременно с катаболизмом, при котором из малых молекул-предшественников синтезируются белки, нуклеиновые кислоты и другие макромолекулярные компоненты клетки, причем этот процесс требует затраты энергии. Источником энергии являются макроэргические молекулы АТФ, которые распадаются до АДФ и неорганического фосфата, а также НАДФН2. Биосинтез протекает также последовательно. 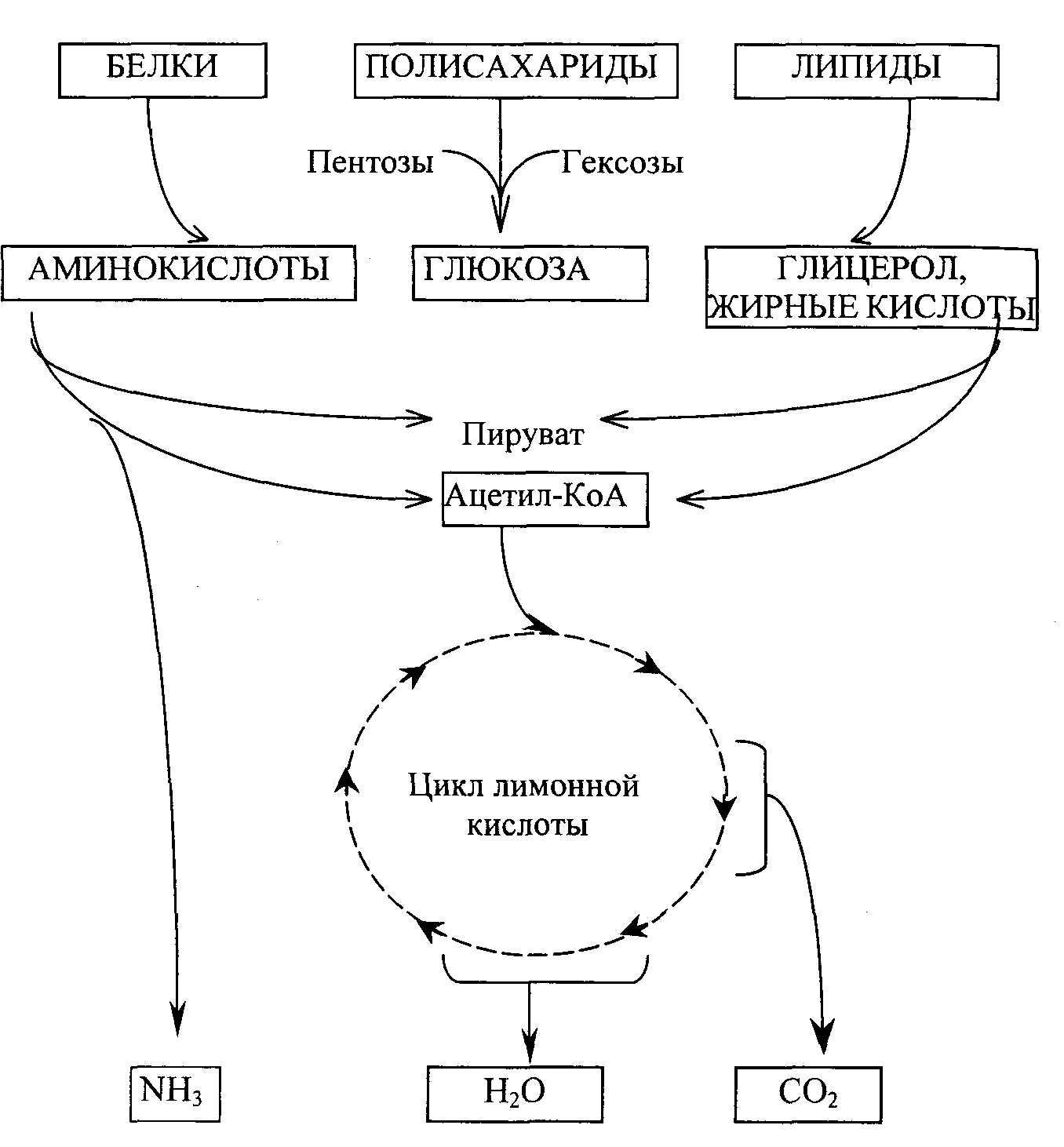 Рис. 7.1. Схематическое изображение стадий катаболизма (по Ленинджеру). Синтез белков начинается с образования α-кетокислот и других предшественников. На второй стадии происходит аминирование α-кетокислот – образуются α-аминокислоты. Затем из аминокислот строятся полипептидные цепи и образуются различные белки. Таким же образом синтезируются липиды. Клетка является основной единицей всех живых организмов, где происходит обмен веществ. В процессе эволюции возникли клеточные органеллы, которые обеспечивают последовательность основных химических реакций: ядро, митохондрии, эндоплазматический ретикулум, рибосомы, лизосомы, микросомы (рис.7.2.). Биохимические процессы происходят в клетке в определенной последовательности с участием ферментов. Ферменты локализованы в отдельных клеточных структурах, которые специализированы в обмене веществ. ОСНОВНЫЕ КЛЕТОЧНЫЕ СТРУКТУРЫ, В КОТОРЫХ ПРОИСХОДЯТ БИОХИМИЧЕСКИЕ РЕАКЦИИ: 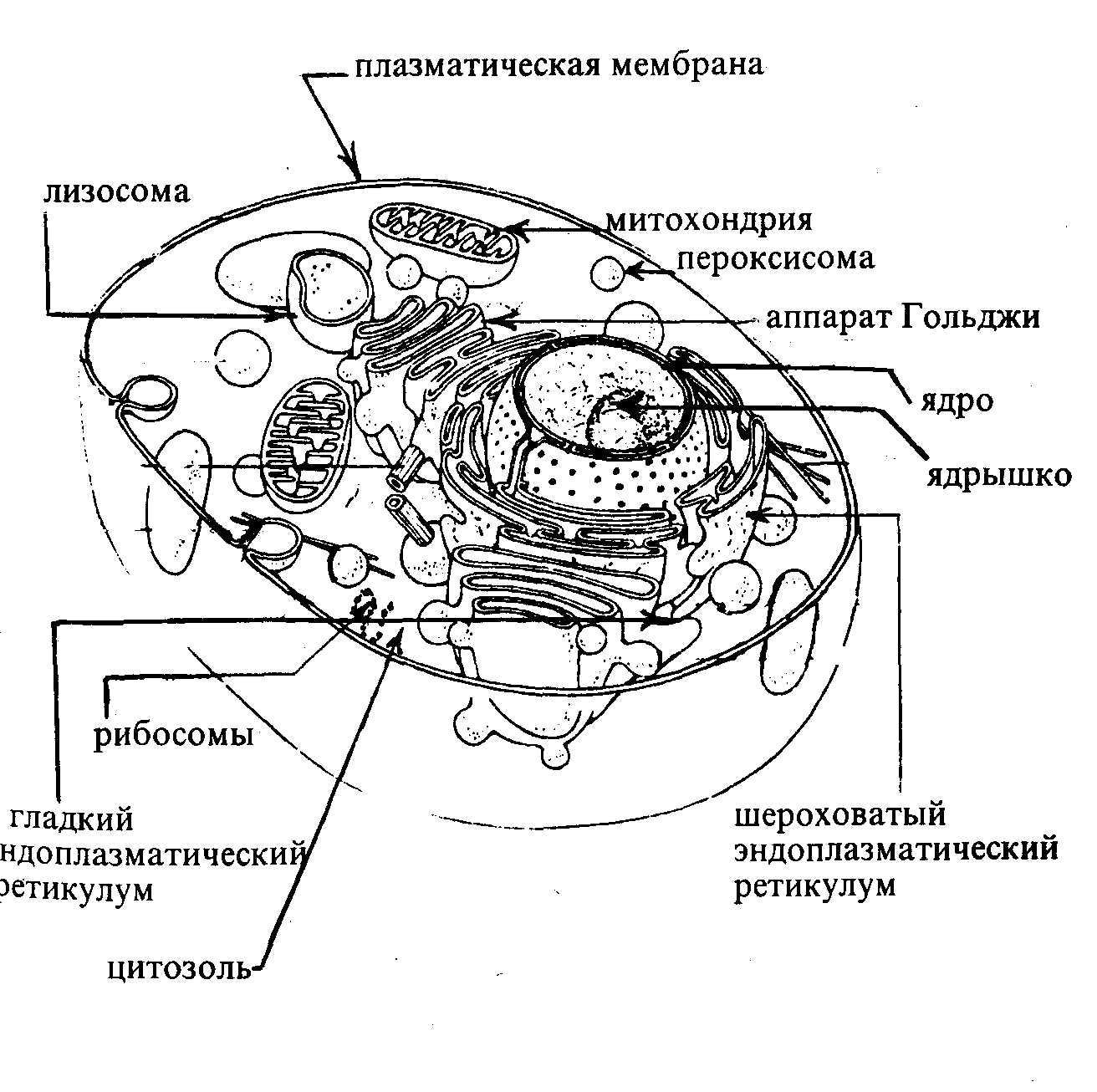 Рис.7.2. Строение эукариотической клетки Ядро локализовано в средней части клетки, окружено двойной мембраной, содержит хроматин (ДНК+белок) – носитель генетической информации. Внутри ядра находится ядрышко, где синтезируется рибосомальная РНК. Наружная мембрана ядра связана с аппаратом Гольджи, где происходит секреция метаболитов. Рибосомы расположены на поверхности эндоплазматической сети, где происходит синтез белковой молекулы. Митохондрии имеют внутреннюю и внешнюю мембраны, это «энергетические станции» клетки. В них происходят окислительно-восстановительные реакции и синтез АТФ. Лизосомы содержат гидролитические ферменты, где происходит расщепление белков, углеводов и других соединений, подлежащих лизису, а также веществ, поступивших путем пиноцитоза и фагоцитоза. Апоптоз – запрограммированная гибель клеток, лизис клеток, утративших свои функции, осуществляется с участием лизосомных ферментов. Микросомы (пероксисомы) содержат оксидазы, окисляющие чужеродные вещества (лекарственные вещества, ароматические соединения – ксенобионты). Цитозоль – цитоплазма - содержит ферменты различного назначения. Основные этапы обмена веществ Первый этап – пищеварение – процесс механической и химической обработки составных частей пищи в пищеварительных органах – распад углеводов до моносахаридов, белков – до аминокислот, липидов – до глицерина и жирных кислот и всасывание. Второй этап – промежуточный обмен. Тканевой обмен включает распад питательных веществ, образование различных промежуточных соединений и конечных продуктов обмена. Третий этап – образование и выделение конечных продуктов обмена из организма. В процессе обмена веществ в организме образуются метаболиты, которые принимают участие в химических реакциях обмена веществ и влияют на их течение: аминокислоты, жирные и ароматические кислоты, пуриновые и пиримидиновые основания, простые сахара, амины, гормоны, витамины и др. Одни и те же вещества могут быть метаболитами для одних организмов и конечным продуктом обмена для других. Например, СНзСНОНСООН – молочная кислота, у млекопитающих метаболит, окисляется до CO2 и H2O. У молочнокислых бактерий это конечный продукт обмена. Мочевая кислота – конечный продукт обмена пуринов (человека, птицы, рептилии). У других млекопитающих метаболит превращается в аллантоин и др. продукты. Выделение энергии из питательных веществ в процессе обмена веществ происходит ступенчато. На I-м этапе при гидролизе белков до аминокислот, углеводов – до глюкозы, жира – до жирных кислот и глицерина выделяется 0,6% энергии углеводов, 1% липидов. На II-м этапе при окислении до ацетил-КоА: СНз-СО-КоА выделяется 1/3, при окислении СНзСО-S-KoA до CO2 и H2O – 2/3 энергии. 40% энергии превращается в теплоту, а 60% используется для синтеза АТФ. В животноводстве различают основной обмен, обеспечивающий поддержание тела, и продуктивный обеспечивающий продуктивность. Например, корова с живой массой 500 кг и продуктивностью 20 кг молока затрачивает 15 кормовых единиц. В том числе на основной обмен 5 кормовых единиц и на продуктивный обмен 10 кормовых единиц. Методы изучения обмена веществ разнообразны. Общей характеристикой обмена веществ является дыхательный коэффициент (ДК), где учитывают количество кислорода, поглощаемого за определенный отрезок времени и количество углекислоты, выделяемое за это время ДК = СО2/О2. Дыхательный коэффициент для углеводов равен 1,0. Так, при окислении 1 молекулы глюкозы затрачивается 6 молекул кислорода и образуется 6 молекул углекислоты: C6H12O6 + 6O2 => 6CO2 + 6H2O Выделение энергии при окислении одного грамма вещества составляет: для углеводов (ДК = 1.0) – 4,1 ккал, жиров (ДК = 0,7) – 9,2 ккал, белков (ДК = 0,8) – 4,1 ккал. Как видно из представленных данных, при окислении липидов выделяется в два раза больше энергии, чем при окислении углеводов и белков (1 ккал = 4,2 кДж). Для изучения обмена веществ широко применяются балансовые опыты. При этом учитывают количество веществ, поступивших с кормом за определенный срок (за сутки) и выделившихся из организма – азота, углерода, фосфора, кальция и т.д. В результате анализа определяют баланс как положительный, если вещество откладывается в организме, баланс отрицательный, если вещества выделяется из организма больше, чем поступает с кормом. Метод меченых атомов позволяет проследить судьбу отдельных соединений в процессе обмена веществ, участие их в метаболизме и выделение из организма. Многие вопросы по обмену веществ можно изучать с использованием метода культуры клеток или же на изолированных органах. Биологическое окисление Биологическое окисление – это окислительно-восстановительные реакции, происходящие в клетках с участием ферментов, являющиеся источником энергии в организме. Химизм горения и биологического окисления, например, глюкозы происходят по общей схеме: C6H12O6 +6O2 -> 6CO2 + 6 H2O+ 686 ккал (на 1 грамм-молекулу) Но имеются отличия: а) горение происходит при высокой температуре, а тканевое окисление – при 37 0C; б) горение в воде невозможно, а тканевое окисление происходит в водной среде; в) при горении энергия освобождается моментально в виде тепла, а при биологическом окислении энергия освобождается ступенчато, аккумулируется в молекулах АТФ. Окисление в тканях может происходить: а) присоединением кислорода; б) потерей или отнятием от водорода электрона. Под окислением понимают все химические реакции, в основе которых лежит отдача электронов и увеличение положительных валентностей. Если одно вещество окисляется, то другое – восстанавливается, т.е. присоединяет электроны. Окислительно-восстановительные реакции – это перенос электронов, иногда и протонов. Биологическое окисление – это совокупность окислительно-восстановительных реакций переноса электронов, происходящих в клетках. Субстратное окисление – это отнятие электронов от промежуточных продуктов обмена углеводов, жиров и белков. Катализируется дегидрогеназами. Тканевое дыхание – разновидность биологического окисления, при котором акцептором электрона является кислород. Окисление в дыхательной цепи – это ферментативный перенос электронов от субстрата к кислороду по дыхательной цепи. Ферменты тканевого дыхания находятся в митохондриях, они строго упорядочены, обеспечивают передачу электронов и протонов от субстрата до кислорода, их называют метаболонами. Различают четыре группы ферментов: пиридинзависимые дегидрогеназы; флавиновые ферменты; убихинон (кофермент Q); цитохромная система.
НАДФ+ отличается от НАД+ тем, что у второго углеродного атома рибозы атом водорода гидроксильной группы замещен остатком фосфорной кислоты. 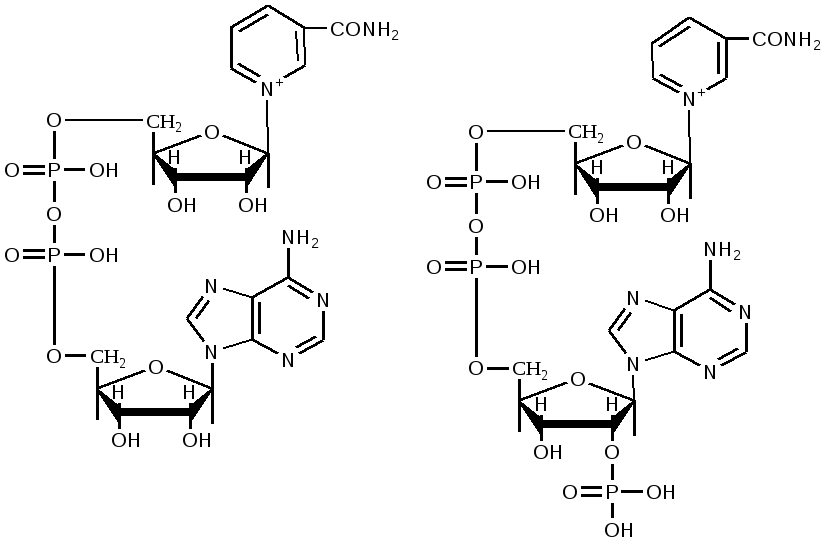 никотинамидадениндинуклеотид никотинамидадениндинуклео- (НАД+) тидфосфат (НАДФ+) Восстановление НАД происходит путем переноса гидрид-иона (: Н-) от субстрата RH2 в положение 4 никотинамидного кольца: 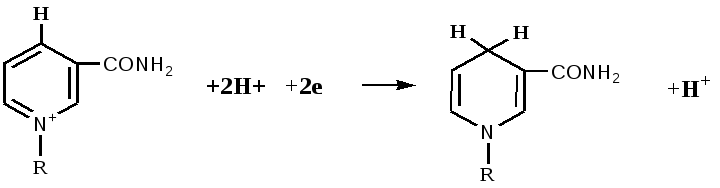 НАД+ НАДН
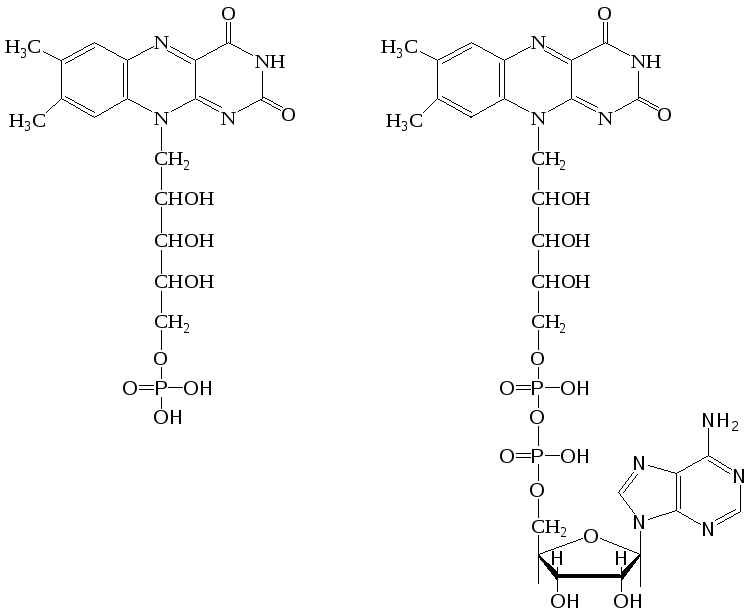 флавинмононуклеотид (ФМН) флавинадениндинук- леотид (ФАД) ФМН построен из молекулы витамина B2 и остатка фосфорной кислоты, а ФАД представляет собой ФМН, соединенный через фосфорную кислоту с АМФ. Восстановление ФАД (или ФМН) происходит путем переноса атомов водорода (и 2-х электронов) от субстрата RH2 в положение 1 и 10 молекулы рибофлавина: 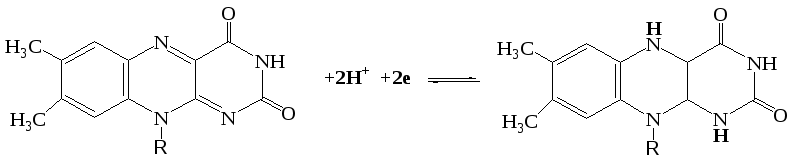
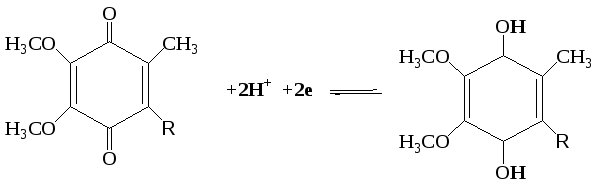 KoQ окисленный KoQ-H2 -восстановленный
Биологическое окисление субстрата начинается с отнятия водорода - дегидрирования. Это происходит с участием НАД (или НАДФ). Дегидрогеназы, отщепив водород от окисляемого вещества, передают его флавиновым ферментам (ФАД, ФМН). Активной группой НАД является витамин В5 – амид никотиновой кислоты, принимая водород, он превращается в восстановленную форму (НАДН2). Далее происходит восстановление ФАД (ФМН), где активной группой является витамин B2. В дальнейшем атом водорода передается на убихинон, образуется восстановленная форма его KoQ.H2. Следующие ферменты дыхательной цепи – цитохромоксидазы. Эти хромопротеиды содержат железо, способное изменять свою валентность Fe2+ ↔ Fe 3+. В ходе каталитического процесса валентность железа изменяется обратимо. Различают цитохромы в, cl, с и аа3 . Последовательность передачи электронов следующая: Цитохромы в - с1 - с являются промежуточными переносчиками, а цитохром ааЗ (цитохромоксидаза) – конечным ферментом, непосредственно взаимодействующим с кислородом. Окисленная форма Fe3+ принимает электроны от восстановленного цитохрома с, переходя в восстановленное Fe2+. Переносчиком электронов являются также белки, содержащие негеминовое железо. В этих белках несколько атомов железа связано с остатком цистеина. Указанные ферменты находятся в строгой последовательности в фиксированном состоянии на внутренней мембране митохондрий, их называют метаболонами (Рис. 7.2.). Окислительное фосфорилирование Окислительное фосфорилирование происходит в митохондриях в процессе биологического окисления в дыхательной цепи. Энергия, высвобождающаяся в дыхательной цепи, аккумулируется в макроэргических соединениях АТФ. Энергия, освобождающаяся в процессе биологического окисления только частично рассеивается в виде тепла (около 40%), а большая часть накапливается в форме макроэргических молекул АТФ (около 60%). Молекула АТФ – это универсальный акцептор и донор химической энергии в клетках. Гидролиз каждой макроэргической связи АТФ сопровождается выделением 7,3 килокалорий энергии на 1 грамм-молекулу. В дыхательной цепи при переносе каждой пары электронов на 1 атом кислорода образуется 3 молекулы АТФ, то есть отношение фосфора к кислороду равно трем: P / О = 3. Синтез молекулы АТФ происходит в определенных участках дыхательной цепи. На каждом этапе синтеза АТФ аккумулируется 8 ккал на каждую грамм-молекулу образовавшейся АТФ. 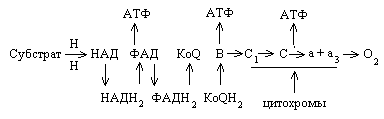 Рис.7.2. Схема дыхательной цепи. Свободное окисление происходит без фосфорилирования, то есть при этом АТФ не синтезезируется. Такое окисление происходит на наружной поверхности митохондрий с участием таких же ферментов, как внутри митохондрий, промежуточные и конечные продукты окисления также не отличаются от продуктов дыхательной цепи. Отличие только в том, что в этом случае не образуются макроэргические соединения (АТФ). Свободное окисление происходит также в пероксисомах цитоплазмы, где главным ферментом является пероксидаза (каталаза), окисляющая H2O2. Свободное окисление важно для поддержания температуры тела в условиях холода, так как энергия, выделяющаяся при этом, рассеивается в виде тепла. Микросомальное окисление происходит в микросомах. В мембранах клеток имеется окислительная система, которая катализирует гидроксилирование различных субстратов: R   H + O2 + НАДФН2 ROH + H2O + НАДФ H + O2 + НАДФН2 ROH + H2O + НАДФРеакция происходит с участием кислорода и восстановленной формы НАДФ. При этом один атом молекулярного кислорода включается в R-OH, другой идет на образование воды. Это так называемое монооксигеназное окисление. Фермент цитохром Р450 катализирует образование гидроксильных (-ОН) групп при синтезе желчных кислот, стероидных гормонов, катаболизме чужеродных соединений (ксенобионты). Токсичность кислорода Молекулярный кислород O2 в клетках может образовать супероксидный анион O2-, который действует как окислитель (акцептор электрона) и как восстановитель (донор электрона). Супероксид, пероксид водорода (H2O2), гидроксильный радикал (–ОН) имеют высокую химическую активность, реагируют со многими веществами организма, они оказывают повреждающее действие на липиды. Активные формы кислорода способны отнимать водород из CH2– групп, жирных кислот, превращая их в свободнорадикальные группы –CH–. Такой радикал жирной кислоты легко присоединяет молекулу кислорода и превращается в пероксидный радикал жирной кислоты. Такой радикал может отнимать водород от другой молекулы жирной кислоты. В результате возникает цепная реакция. Это пероксидное окисление липидов приводит к разрушению структуры мембран. Защита от перекисного окисления – окисление каталазой, глутатион-пероксидазой (фермент, соединенный с селеном). Витамин E совместно с микроэлементом селеном может предотвращать перекисное окисление липидов, так как токоферол может окисляться (отдавать электрон) с образованием малоактивного свободного радикала. |
