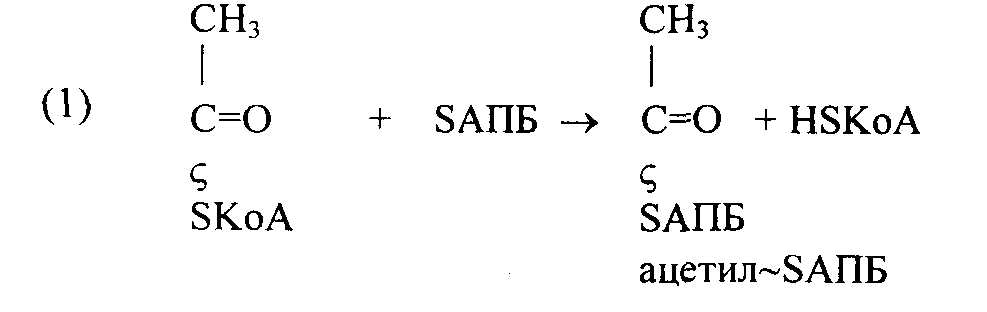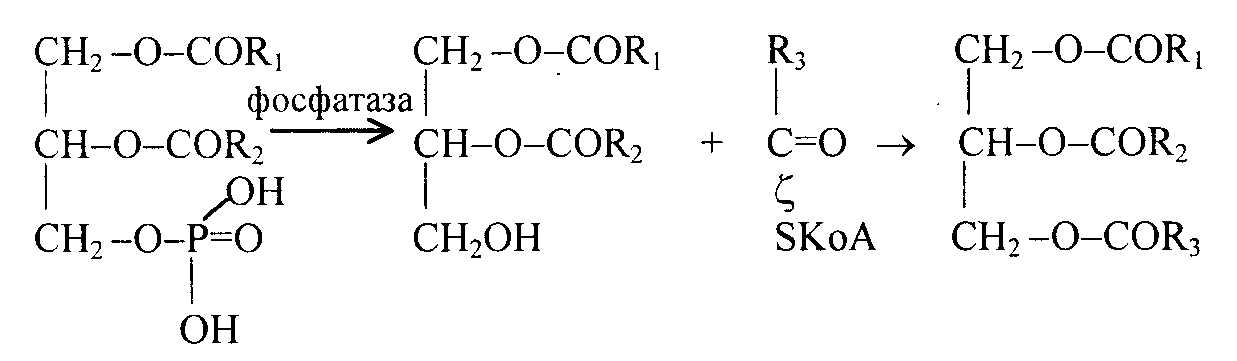К липидам относится большое число малополярных природных веществ, различающихся между собой по химической структуре и выполняющих в организме разнообразные функции – это свободные жирные кислоты, нейтральные глицериды, воски, фосфолипиды, в том числе гликосфинголипиды, стерины и т.д.
Функции липидов: а) липиды являются источником энергии. При окислении липидов освобождается в два раза больше энергии, чем при окислении белков и углеводов; б) липиды являются основным структурным компонентом клеточных мембран; в) являются хорошим растворителем для некоторых витаминов и обеспечивают их накопление в организме; г) играют роль защиты от холода и механических ударов; д) выполняют функцию важнейших биологических регуляторов и медиаторов, участвующих во всех важнейших физиологических процессах (иммунный ответ, передача нейрональной информации, регуляции сосудистого и мышечного тонуса, воспаление и т.д.), происходящих в организме и в биохимических реакциях, протекающих в клетках животных и человека.
Являясь вторичными мессенджерами (передатчиками, переносчиками), они передают внутрь клетки различные внешние сигналы, а также сами являются межклеточными медиаторами. Так, гликосфинголипиды участвуют в процессах роста, дифференцировки и распознавания клеток, в межклеточной передаче сигналов, являются антигенами и активными иммуномодуляторами.
Липиды являются биоэффекторами. Так, фосфолипиды (фосфоинозиты) стимулируют активность некоторых форм протеинкиназы С, мобилизуют Ca2+ из внутриклеточного депо; фосфатидилхолин регулирует многие биологические процессы в крови. Лизофосфатидилхолин (лизолецитин) усиливает клеточную пролиферацию, стимулирует дифференцировку лимфоидных клеток.
Полиненасыщенные жирные кислоты и их производные регулируют активность фосфолипаз, ионных каналов, АТФаз, протеинкиназ, перенос гормональной информации и информацию генов.
Церамиды регулируют рост и развитие нервных клеток, рост аксонов нейронов гиппокампа, играют роль в апоптозе, дифференцировке и старении клеток, а также в торможени клеточного цикла.
В тканях животных липиды находятся или в свободном состоянии, или в виде соединения с белками и углеводами. Различают две группы липидов: простые и сложные. Простые липиды состоят из остатков спиртов (глицерина высших и циклических) и высших жирных кислот: сюда относята нейтральные жиры, стериды и воски.
Сложные липиды состоят из остатков спиртов (глицерина сфингозина, инозита и др.), высших жирных кислот и други) веществ (азотистых оснований, Н3РО4, H2SO4, углеводов и т.д.). К ним относятся фосфатиды, гликолипиды, сульфатиды.
Количество жиров в тканях животных различно. В одни> тканях их очень мало, например, в мышечной ткани их не более 0,1%, а в сальнике - до 90%.
Распределение нейтрального жира (в %) в организме животных (среднее число, общее количество жира принято за 100%): жир подкожной клетчатки – 50; почек – 10; сальника - 20; мышц – 1-2; печени – 2-5; молока – 3-5.
Жир является важнейшим энергетическим материалом в организме животного. Установлено, что 1 г жира дает 9,3 ккал; 1 г белка или углевода – не более 4,1 ккал.
Подкожный жировой слой у животных северных широт защищает их от охлаждения. У кита, например, он достигает 50-70 см толщины. Большое значение в защите от охлаждения тела имеет подкожный жир у новорожденных животных.
Жиры откладываются вокруг жизненно важных органов толстым слоем и предохраняют их от механических повреждений (почки, кишечник, сердце и т.д.).
Распадаясь в организме, жиры дают не только энергию, но значительное количество эндогенной воды, что очень важно у зимнеспящих животных (медведь), верблюдов, у насекомых, находящихся в стадии куколки и т.д.
Известно, что 100 г жира при биохимическом сгорании дает 107,1 г воды, а крахмал – 55,5 г, белок – 41,3 г.
Установлено большое значение для нормального обмена веществ ненасыщенных жирных кислот: олеиновой, линолевой, линоленовой, арахидоновой. Исключение их из рациона питания приводит к тяжелым заболеваниям. В зависимости от происхождения различают жиры животных, растений, рыб, микробов и т.д.
Химическое строение нейтральных жиров
Нейтральные жиры представляют собой сложные эфиры глицерина и высших жирных кислот. Природные жиры (рыбий жир, сливочное масло) представляют собой смесь триглицеридов, состав которых зависит от условий кормления животных. При гидролизе нейтральных жиров всегда выделяется глицерин и жирные кислоты.
Насыщенные и ненасыщенные жирные кислоты широко распространены во всех жирах животного и растительного происхождения. Остальные встречаются редко и преимущественно в сложных липидах.
Все кислоты, выделенные из жиров, содержат четное число атомов углерода. В состав природных жиров могут входить как простые, так и смешанные триглицериды. Простые триглицериды содержат во всех трех положениях глицерина одинаковые жирные кислоты, например:
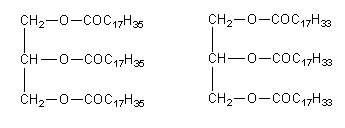
тристеарин триолеин
Смешанные триглицериды содержат различные жирные кислоты, например:
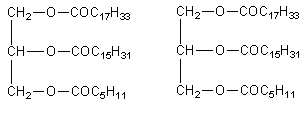
капронопальмитоолеин дистеаринопальмитин
Жирные кислоты.
Жирные кислоты являются структурными компонентами всех природных липидов.
Жирные кислоты - гидрофобные соединения, их молекулы -длинные углеводородные цепи с концевой карбоксильной группой. В составе липидов содержатся жирные кислоты с углеродным атомом от 4 до 30, часто 16 и 18 атомов углерода.
Природные жирные кислоты бывают насыщенные и ненасыщенные; с прямой цепью, с разветвленной цепью, с циклами в цепи, оксикислоты.
Насыщенные жирные кислоты.
Общая формула: СН3-(СН2)n -СООН.
Количество углеродных атомов чаще всего С4 (масляная кислота), C 14 (миристиновая кислота), C16 (пальмитиновая кислота), C18 (стеариновая кислота).
Насыщенные жирные кислоты довольно устойчивы к действию окислителей.
Ненасыщенные жирные кислоты – различаются числом и местом двойных связей, а также пространственной конфигурацией.
Известны кислоты, содержащие одну, две, три, четыре и более двойных связей.
Кислоты с тремя и более двойными связями называются полиненасыщенными жирными кислотами. В липидах тканей встречаются наиболее часто олеиновая, линолевая, линоленовая, арахидоновая кислоты.
Олеиновая кислота (C18) имеет одну двойную связь, содержится в оливковом масле 85% от общего количества кислот, в пальмовом масле – 74%, в других растительных маслах – 10-50%.
Линолевая кислота (C18) имеет две двойные связи, много в растительных маслах. Соевое, хлопковое, подсолнечное масла содержат более 50% линолевой кислоты. В животных жирах содержится в небольших количествах.
Линоленовая кислота (C18) имеет три двойные связи, много в льняном, конопляном маслах, в животных жирах встречается реже. Широко представлена в тканях животных (до 20%) в составе липидов (фосфолипидов) печени, почек, мозга и т.д.
Арахидоновая кислота (С20) имеет четыре двойные связи.
Полиненасыщенные жирные кислоты обладают высокой биологической активностью, являются источником образования простагландинов – внутриклеточных регуляторов обмена веществ.
В результате окислительного метаболизма арахидоновой кислоты образуются лейкотриены, которые являются биоэффекторами воспалительных реакций. Они активируют сокращение гладкой мускулатуры дыхательных путей и сосудов, вызывают секрецию слизи и усиливают экссудацию эндотелиальных клеток.
В бактериальных клетках содержатся ненасыщенные жирные кислоты с разветвленной цепью (туберкулостеариновая – в воске туберкулезных бацилл) и ненасыщенные разветвленные оксикислоты – миколевые кислоты (составные части микобактерий).
Ненасыщенные жирные кислоты в организме животных находятся в жидком состоянии; насыщенные, в основном, представляют собой твердые тела (кроме первых представителей).
Преобладание твердых жирных кислот делает жиры более тугоплавкими и наоборот. Следовательно, температура плавления жиров является важным физико-химическим фактором, отражающим состав входящих в них жирных кислот. В состав природных жиров могут входить одновременно многие жирные кислоты. Например, сливочное масло содержит 13 различных жирных кислот, в т.ч. олеиновая – 30%, пальмитиновая – 28,5%, стеариновая – 12%, миристиновая – 12,5%. (Афонский СИ.)
Свободные жирные кислоты реагируют со щелочами и образуют соли (мыла). Процесс расщепления жиров с последующим образованием мыла называется омылением жиров.
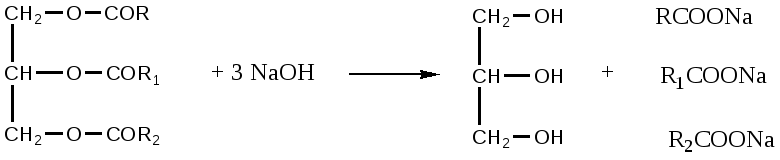
триглицерид глицерин соль жирной
кислоты
В организме животных расщепление жиров происходит под влиянием ферментов пищеварительного тракта и ферментов микроорганизмов. Бактериальное разложение жиров идет за счет их окисления. В результате жирные кислоты переходят в летучие продукты (альдегиды, кетоны, оксикислоты).
Для характеристики качества и чистоты животных и растительных жиров принято определять: удельный вес, температуру плавления и застывания, коэффициент рефракции. Особенно важно определить химические константы.
Число омыления соответствует количеству миллиграммов KOH, идущего на нейтрализацию кислот, образующихся при омылении 1 г жира; чем меньше их молекулярный вес, тем больше отдельных молекул жирных кислот возникает при расщеплении жира, тем больше число омыления.
При щелочном гидролизе (омылении) образуются глицерин и соответствующие соли жирных кислот – мыла.
Число Рейхерта-Мейсля свидетельствует о наличии низкомолекулярных летучих жирных кислот (масляной, каприновой, каприловой) в составе жира. Оно выражается количеством мг 0,1 н. NaOH, идущего на нейтрализацию кислот, отгоняющихся с водяным паром на 5 г жира после его гидролиза.
Йодное число характеризует степень ненасыщенности жирных кислот. Оно соответствует числу граммов йода, способного присоединяться к 100 г жира по месту разрыва двойных связей в непредельных (ненасыщенных) кислотах. Йодное число говяжьего жира – 32-47, бараньего – 35-46, свиного – 46-66.
Кислотное число – количество миллиграммов едкого калия, необходимое для нейтрализации 1 г жира. Это число указывает на количество имеющихся в жире свободных кислот (С.И.Афонский).
Нейтральные гликолипиды
Гликолипиды – сложные соединения, содержащие липидный и углеводный фрагменты, соединенные ковалентной связью. В последние годы к этим соединениям возрос интерес, т.к. они выполняют не только структурные, но и регуляторные функции. Они входят в состав плазматических мембран и мембранных систем клетки, обладают антигенными свойствами, определяют серологический тип бактерий. Различают нейтральные гликолипиды, гликофосфолипиды, серингликолипиды. Нейтральные гликолипиды были выделены из растений (зерно пшеницы, водоросли, зеленые листья растений), из животных тканей (головной мозг), из микроорганизмов, углеводным компонентом их является галактоза. Например, моногалактозилдиацилглицерин:
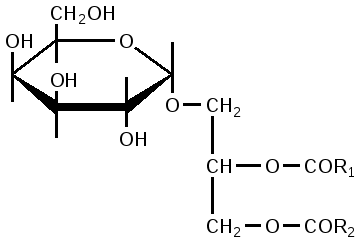
R1 и R2 – остатки жирных кислот. В составе нейтральных гликолипидов в значительных количествах присутствуют остатки ненасыщенных жирных кислот (олеиновая, линолевая и др.) Основным углеводным компонентом кислотоустойчивых бактерий является D-арабиноза, D-глюкоза, D-манноза. D-рамноза, O-метилированные дезоксигексозы, трегалоза; липидный компонент представлен высокомолекулярными разветвленными жирными кислотами.
Воска – сложные эфиры высших жирных кислот и первичных одноатомных высокомолекулярных спиртов. Общая формула воска: R1CH2-O-CO-R2, где R1CH2-O – остаток высокомолекулярного одноатомного первичного спирта, R2-CO – остаток жирной кислоты.
Воска животных, растений и насекомых различаются составом спирта и жирных кислот. В пчелином воске находятся спирты ряда с 24-34 атомами углерода в молекуле, наиболее широко представлен мирициловый спирт. Из жирных кислот обнаруживается пальмитиновая кислота и кислоты ряда CH3(CH2)n-COOH, где n=22-32.
Растительные воска (например, воск на листьях табака, капусты и др. растений) кроме указанных спиртов и жирных кислот содержат также большое количество свободных насыщенных углеводородов с 25-33 атомами углерода. Из головного мозга кашалота выделен воск спермацет, являющейся эфиром цетилового спирта и пальмитиновой кислоты.
Из ланолина (жира овечьей шерсти) выделены воска, содержащие спирты с числом углеродных атомов равным, 18-26.
Воска образуют защитную смазку на коже, шерсти, перьях листьях и плодах высших растений, а также содержатся в наружном скелете многих насекомых. Воска – химически устойчивые соединения, устойчивы к действию бактерий.
Фосфолипиды (фосфатиды)
Фосфолипиды содержатся во всех тканях животных и растений. Много фосфатидов найдено в нервной ткани и головном мозге животных, а также в желтке яиц птиц. Они содержат остаток глицерина, жирных кислот, фосфорной кислоты, азотистых оснований.
Различают: холинфосфатиды, коламинфосфатиды, серинфосфатиды, ацетальфосфатиды, инозитфосфатиды, сфингофосфатиды.
Фосфатиды нерастворимы в воде, но способны набухать в ней и образовывать водные эмульсии, хорошо растворяются в эфире, бензоле, хлороформе. В ацетоне, в отличие от нейтральных жиров и стеринов, фосфатиды не растворимы. Этим свойством пользуются для отделения фосфатидов от стеринов и жиров. Фосфатиды легко окисляются из-за наличия ненасыщенных жирных кислот.
Холинфосфатиды или лецитины – широко распространены в тканях животных, растений, микробов, являются компонентами большинства мембран животных клеток. Много лецитина в ткани мозга, надпочечниках, эритроцитах. В яичном желтке его до 8-10%.
Холинфосфатиды образованы путем взаимодействия глицерина с двумя молекулами жирных кислот и молекулой фосфорной кислоты, которая соединена эфирной связью с азотистым основанием холином.
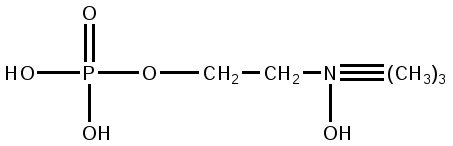
Соединение холина с фосфорной кислотой
Холинфосфатиды животного и растительного происхождения отличаются друг от друга главным образом природой входящих в них жирных кислот и положением остатка фосфорной кислоты. В зависимости от положения последнего различаются α-лецитины, если остаток H3PO4 расположен у первого углеродного атома глицерина, и β-лецитины. если в образовании эфирной связи с фосфорной кислотой участвует вторичный спиртовый гидроксил глицерина.
Как видно из формулы, в молекуле лецитина имеется кислотный гидроксил в остатке фосфорной кислоты и основной в остатке холина, поэтому лецитин может существовать в виде внутренней соли. Правильнее изображать формулу в следующем виде:
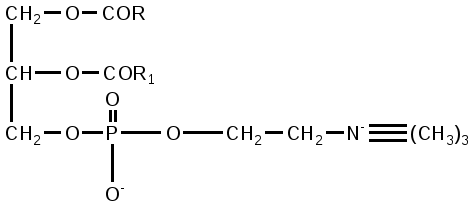
В состав лецитинов могут входить олеиновая, пальмитиновая, линолевая кислота, арахидоновая и другие кислоты. При гидролизе лецитинов получаются жирные кислоты, холин, глицерофосфорная кислота, которая затем может распадаться на свободную фосфорную кислоту и глицерин.
Составная часть лецитина – холин обнаруживается в тканях и жидкостях организма как в свободном состоянии, так и в связанном с белками тканей. Он образует соединение с уксусной кислотой по типу сложных эфиров, называемое ацетилхолином:
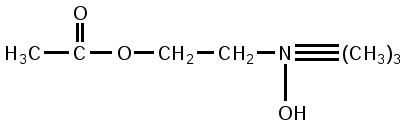
Ацетилхолин имеет важное значение в процессах нервной деятельности как переносчик нервного возбуждения (медиатор). Холин легко окисляется, превращаясь сначала в альдегид – мускарин (найден впервые в грибе мухомора), затем в кислоту-бетаин, встречающуюся в тканях животных и растений.
Коламинфосфатиды (кефалины) – построены также как и холинфосфатиды из глицерина, жирных кислот и фосфорной кислоты, но в качестве азотистого основания в них входит этаноламин (коламин): CH2(NH2 )СН2ОН
Кефалины широко распространены в природе. Впервые были найдены в составе головного мозга (Cephalus – голова), находятся в печени, почках, яичном желтке и др. Они растворимы в спирте и этим отличаются от лецитинов.
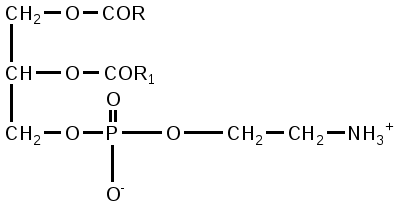
Кефалин
Серинфосфатиды. Структура серинфосфатида аналогична структуре лецитина и кефалина, но в качестве азотистого соединения в них входит аминокислота серии:
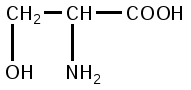
Серинфосфатиды впервые были найдены в составе мозга, имеют следующее строение:
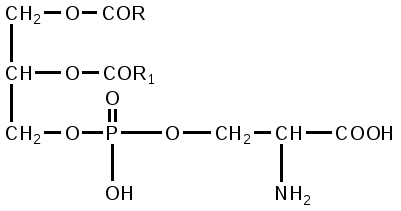
Серинфосфатиды различаются по характеру входящих в них кислот, обладают кислым характером, т.к. у них имеется свободная карбоксильная группа. Между холинфосфатидами, коламинфосфатидами и серинфосфатидами существует родство, азотистые соединения этих фосфатидов могут переходить друг в друга:
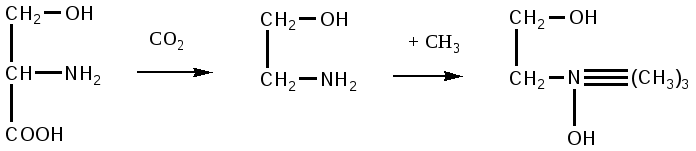
серии коламин холин
Превращение серина в коламин происходит путем декарбоксилирования, а коламина в холин – путем метилирования.
Инозитфосфатиды содержат в качестве замещающего полярного радикала производное циклогексана – инозит – шестиатомный циклический спирт.
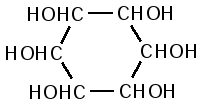
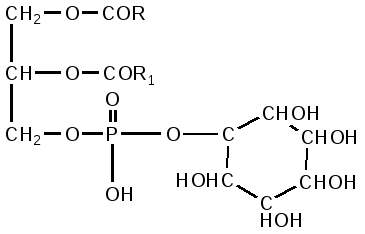
Впервые выделены из туберкулезных бацилл, а позже из растительных и животных тканей. Кроме обычных (глицерин, инозит, фосфорная кислота, жирные кислоты) компонентов обнаружены сложные инозитфосфатиды, содержащие амины, аминокислоты, углеводные остатки.
Гликофосфоглицериды – углеводсодержащие фосфолипиды – обнаружены в различных тканях. В них в качестве полярной группы выступает молекула углевода (их называют также фосфатидилсахара). Связь между фосфолипидом и углеводом может быть О-эфирной или N-гликозидной. Так, выделены производные фосфатидилглицерина, содержащие остаток глюкозамина в третьем положении (О-эфирная связь).
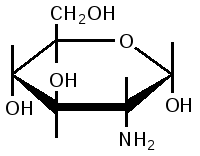
D - глюкозамин
Фосфоглицериды, содержащие группу -OCH=CH- (альдегидогенные) или фосфосодержащие плазмогены, присутствуют во всех тканях животного организма. Их особенно много в головном и спинном мозге, сердечной мышце, где они представлены в мембранах клетки.
Так, фосфолипиды составляют 25-30% сухой массы мозга, из которых на долю плазмогенов приходится до 90%. Фосфолипиды в качестве азотистого компонента чаще всего содержат этаноламин, холин, инозит.
Сфинголипиды
Это сложные эфиры сфингозина, являются компонентом нервных клеток, тканей мозга, мембранах эритроцитов, плазмы крови, печени и других органов и тканей. Сфинголипиды являются вторичными посредниками в передаче различных внешних сигналов в клетку, регулируют рост, дифференцировку, активацию и пролиферацию лимфоцитов, апоптоз клеток.
Сфингозин – алифатический двухатомный аминоспирт из 18 углеродных атомов:
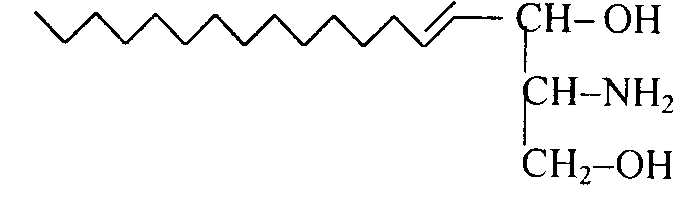
Сфингозин мобилизует ионы кальция из внутриклеточного депо и контролирует специфический Ca2+ канал, влияет на синтез ДНК, конкурируя с гистонами.
Сфингомиелин образуется из сфингозина, где атом водорода аминной группы замещен жирной кислотой и одна гидроксильная группа соединена через фосфорную кислоту с холином. Входит в состав нервных клеток.
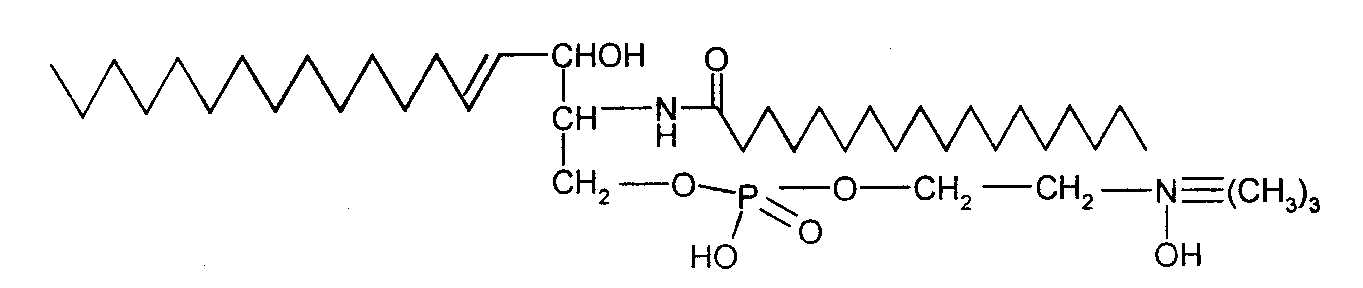
Цероброзиды состоят из сфингозиновых оснований, жирной кислоты и гексозы (галактозы). Жирные кислоты их содержат 24 атома углерода, чаще всего встречаются невроновая, оксиневроновая, цереброновая кислоты.
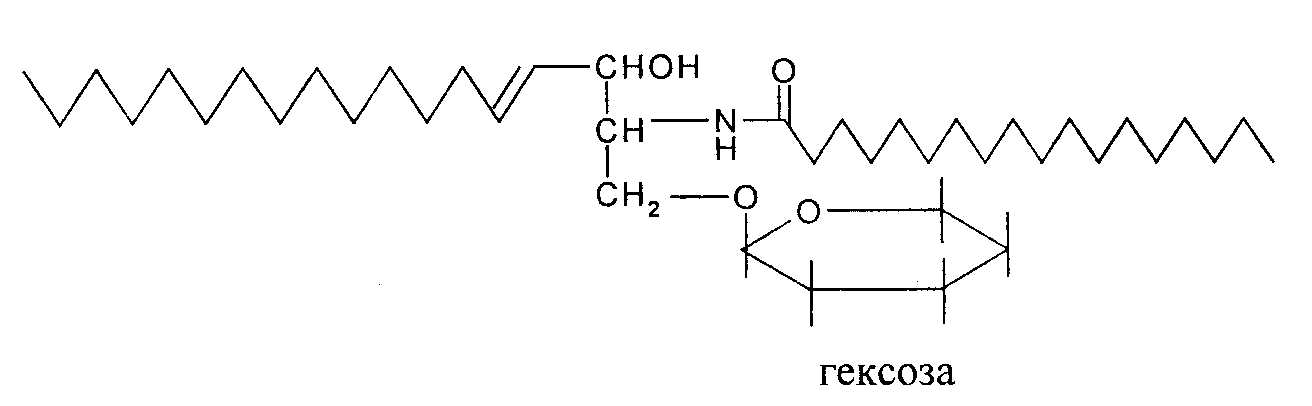
Сульфатиды отличаются от цереброзидов наличием остатка серной кислоты. Они обладают кислым характером, играют важную роль в ионном транспорте через мембраны.
Церамидогексозы: у них углеводным компонентом являются олигосахара (β-лактоза). Регулируют рост и развитие нервных клеток, рост аксонов нейронов гиппокампа, играют роль в апоптозе, дифференцировке и старении клеток, а также в торможении клеточного цикла.
Гематозиды – содержат сиаловую (нейраминовую) кислоту.
Ганглиозиды – сложные гликосфинголипиды, разнообразны по структуре, образуют гигантские молекулы (до 400 мономеров), принимают участие в передаче нервного импульса.
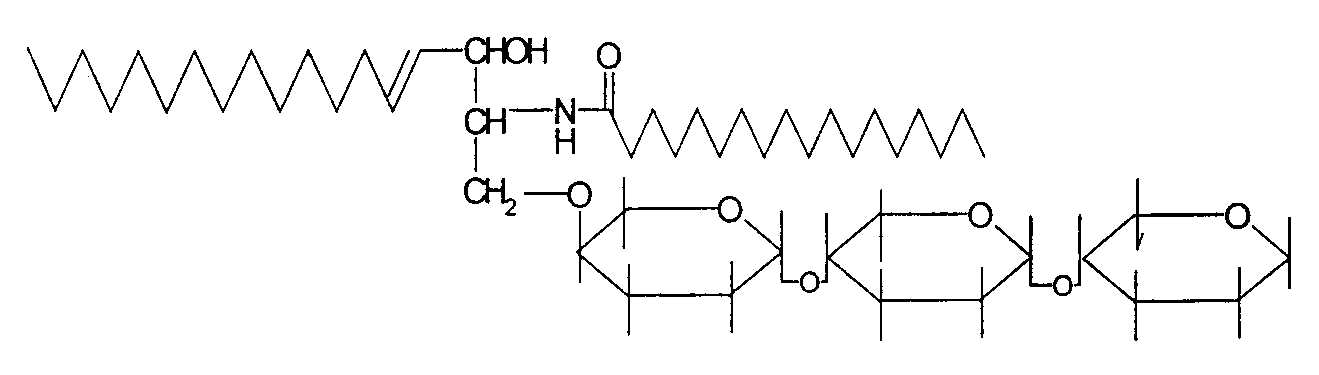
Стериды и стерины распространены в животных и растительных организмах. Стериды представляют сложные эфиры холестерина и жирных кислот. В основе молекулы холестерина лежит ядро циклопентанпергидрофенантрена. В ядро входят полностью гидрированный фенантрен и циклопентан. При конденсации циклопентана с фенантреном образуется циклопентанпергидрофенантрен.
Водород гидроксила C3 может замещаться различными радикалами, что лежит в основе многочисленных физиологически активных соединений – стероидов. К стероидам относятся стерины (греч. стереос – твердый), одноатомные вторичные предельные или ненасыщенные спирты, половые гормоны, гормоны коры надпочечников, желчные кислоты и т.д. К стероидам относятся также канцерогенные вещества, например, метилхолантрен. Стерины, выделенные из животных тканей – зоостерины, из растений – фитостерины, из грибов – микостерины.
Холестерин (холестерол) – одноатомный вторичный полициклический спирт, содержится во всех тканях:
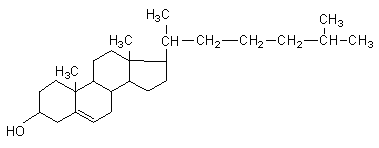
В тканях находится как в свободном состоянии, так и в виде сложных эфиров жирных кислот (этерифицирован спиртовой радикал при С-3). Много холестерина содержится в тканях нервной системы, в мембране эритроцитов. Впервые был выделен из желчных камней и отсюда получил название (chole – желчь, греч.). Желчные камни до 90% состоят из холестерина. Холестерин является ненасыщенным спиртом, производным холестана с двойной связью в кольце между 5 и 6 углеродными атомами. В коже млекопитающих содержится еще более ненасыщенное производное холестерола: 7-дегидрохолестерол, провитамин витамина D3.
Под действием солнечных лучей провитамин превращается в витамин D3 – антирахитический витамин (см. стр. 92-93).
При восстановлении холестерина образуется капростерин, этот процесс совершается в толстом отделе кишечника.
Эргостерин имеет 3 двойные связи между 5 и 6, 7 и 8, 22 и 23 атомами С, и дополнительный радикал CH3 у 24 С-атома. Эргостерин содержится в грибах, дрожжах, является провитамином D2.При облучении солнечными лучами кольцо раскрывается, образуется витамин D2.
Ланолин - жир овечьей шерсти представляет собой ланостерин, соединенный с жирной кислотой. Он широко применяется как основа для мазей и кремов в парфюмерии и фармацевтической промышленности.
Двойной липидный слой мембран
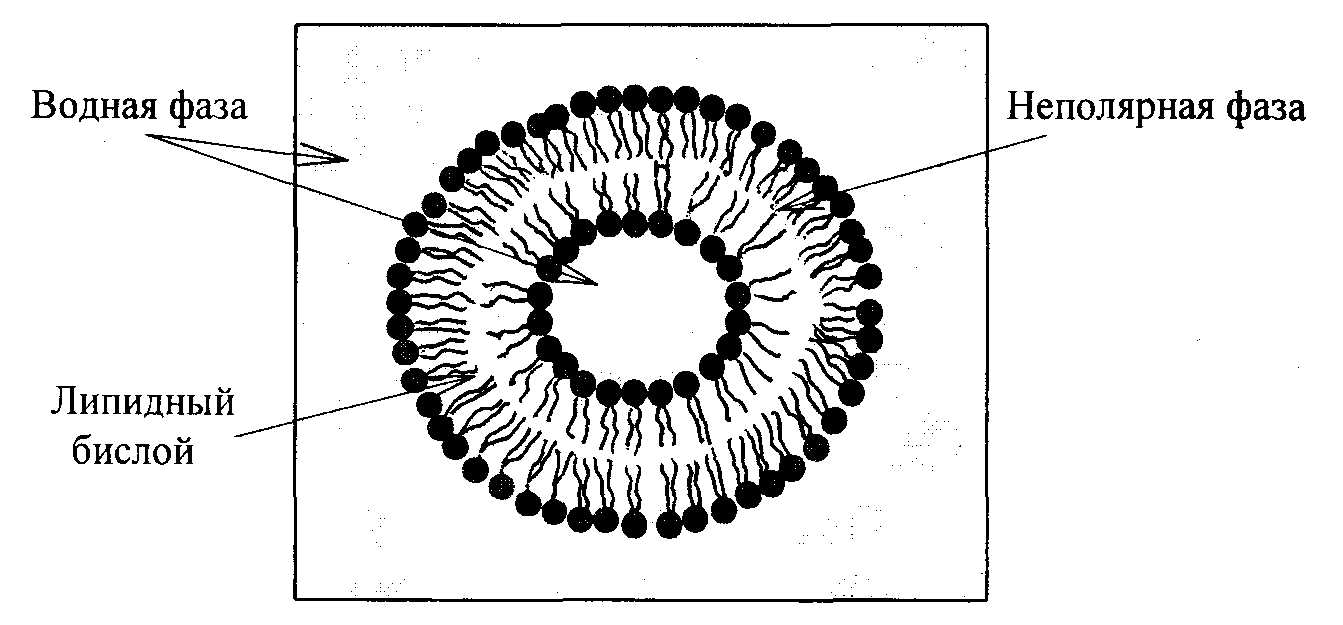
Молекулы фосфолипидов и гликолипидов амфифильны, то есть углеводородные радикалы жирных кислот и сфингозина являются гидрофобными, а другая часть молекулы, образованная из углеводов, остатка фосфорной кислоты с присоединенным к нему холином, серином, этаноламином – гидрофильна. В результате этого в водной среде гидрофобные участки молекулы фосфолипидов вытесняются из водной среды и взаимодействуют между собой, а гидрофильные участки контактируют с водой, в результате образуется двойной липидный слой клеточных мембран (рис.9.1.). Этот двойной слой мембраны пронизан белковыми молекулами – микротрубочками. На наружной стороне мембраны прикреплены олигосахариды. Количество белка и углеводов в различных мембранах неодинаково. Белки мембран могут выполнять структурные функции, могут быть ферментами, осуществлять трансмембранный перенос питательных веществ, могут выполнять различные регуляторные функции. Мембраны всегда существуют в виде замкнутых структур (см. рис.9.1). Липидный бислой обладает способностью к самосборке. Эту способность мембран используют для создания искусственных липидных пузырьков – липосом.
Липосомы широко применяются как капсулы для доставки различных лекарственных веществ, антигенов, ферментов в различные органы и ткани, так как липидные капсулы способны проникать через клеточные мембраны. Это позволяет направлять лекарственные вещества точно по адресу в пораженный орган.
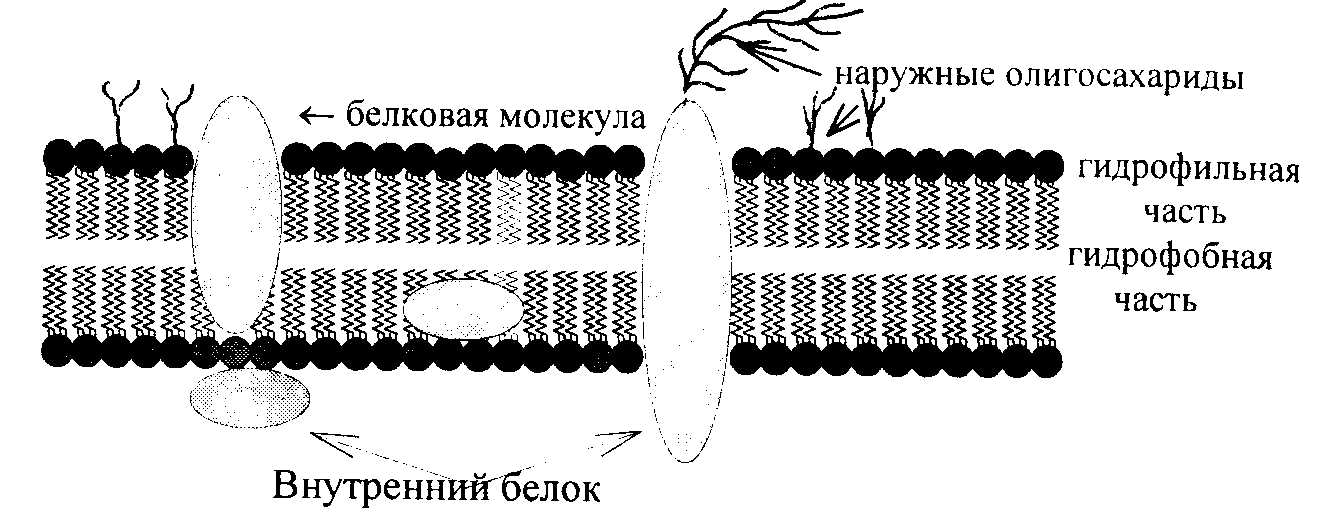
Рис.9.1. Схема клеточной мембраны из двойного липидного слоя. Гидрофобные участки молекулы липидов притягиваются между собой; гидрофильные участки молекулы находятся с наружной стороны. Молекулы белков пронизывают липидный бислой.
Обмен липидов
В организме нейтральные жиры находятся в 2-х формах: запасного жира и протоплазматического жира.
В состав протоплазматического жира входят фосфолипиды и липопротеиды. Они участвуют в формировании структурных компонентов клеток. Мембраны клеток, митохондрий и микросом состоят из липопротеидов и регулируют проницаемость отдельных веществ. Количество протоплазматического жира стабильно, и не изменяется в зависимости от голодания или ожирения.
Запасной (резервный) жир – в его состав входят триацилглицерины жирных кислот – находится в подкожной жировой клетчатке и в жировых депо внутренних органов.
Функции резервного жира заключаются в том, что это -запасной источник энергии, доступной для использования в период голодания; это – изоляционный материал от холода, от механических травм.
Важно также, что липиды, распадаясь, выделяют не только энергию, но и значительное количество воды:
При окислении 1 грамма белка выделяется – 0,4 г; углеводов – 0,5 г; липидов – 1 г воды. Это свойство липидов имеет большое значение для животных, обитающих в условиях пустыни (верблюды).
Переваривание липидов в желудочно-кишечном тракте
В полости рта липиды подвергаются лишь механической обработке. В желудке имеется небольшое количество липазы, которая гидролизует жиры. Малая активность липазы желудочного сока связана с кислой реакцией содержимого желудка. Кроме того, липаза может влиять только на эмульгированные жиры, в желудке отсутствуют условия для образования эмульсии жира. Только у детей и у моногастричных животных липаза желудочного сока играет важную роль в переваривании липидов.
Кишечник является основным местом переваривания липидов. В двенадцатиперстной кишке на липиды воздействует желчь печени и сок поджелудочной железы, одновременно происходит нейтрализация кишечного содержимого (химуса). Происходит эмульгирование жиров под действием желчных кислот. В состав желчи входят: холевая кислота, дезоксихолевая (3,12 дигидроксихолановая), хенодезоксихолевая (3,7 дигидроксихолановая) кислоты, натриевые соли парных желчных кислот: гликохолевая, гликодезоксихолевая, таурохолевая, тауродезоксихолевая. Они состоят из двух компонентов: холевой и дезоксихолевой кислот, а также глицина и таурина.
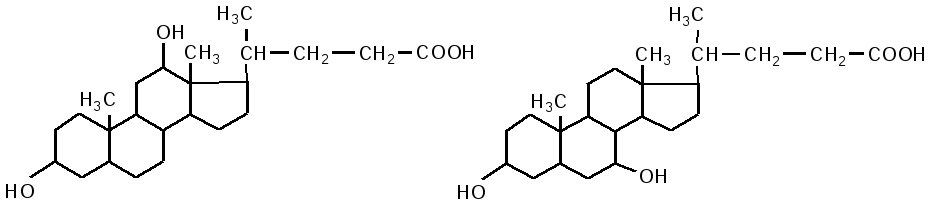
дезоксихолевая кислота хенодезоксихолевая кислота
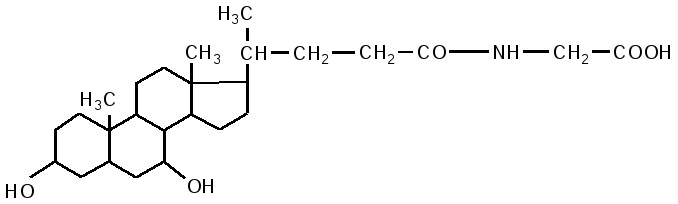
гликохолевая кислота
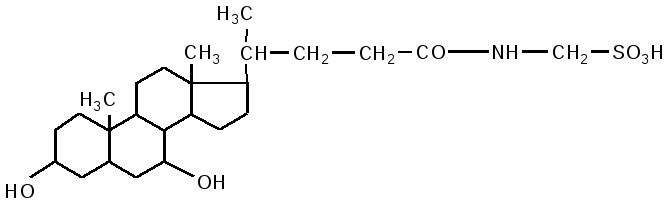
таурохолевая кислота
Соли желчных кислот хорошо эмульгируют жиры. При этом увеличивается площадь соприкосновения ферментов с жирами и увеличивается действие фермента. Недостаточность синтеза желчных кислот или задержка поступления нарушает эффективность действия ферментов. Жиры, как правило, всасываются после гидролиза, но часть тонко эмульгированных жиров всасывается через стенку кишечника и переходит в лимфу без гидролиза.
Эстеразы разрывают в жирах эфирную связь между, спиртовой группой и карбоксильной группой карбоновых кислот и неорганических кислот (липаза, фосфатазы).
Под действием липазы жиры гидролизуются на глицерин и высшие жирные кислоты. Активность липазы возрастает под действием желчи, т.е. желчь непосредственно активирует липазу. Кроме того, активность липазы увеличивают ионы Са++ вследствие того, что ионы Са++ образуют нерастворимые соли (мыла) с освободившимися жирными кислотами и предотвращают их подавляющее влияние на активность липазы.
Под действием липазы в начале гидролизуются эфирные связи у α и α1 (боковых) углеродных атомов глицерина, затем у β-углеродного атома:
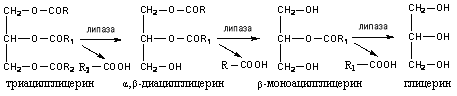
Под действием липазы до 40% триацилглицеридов расщепляются до глицерина и жирных кислот, 50-55% гидролизуется до 2-моноацилглицеринов и 3-10% не гидролизуется и всасываются в виде триацилглицеринов.
Стериды корма расщепляются ферментом холестеролэстеразой до холестерина и высших жирных кислот. Фосфатиды гидролизуются под влиянием фосфолипаз А, A2, С и D. Каждый фермент действует на определенную сложноэфирную связь липида. Точки приложения фосфолипаз представлены на схеме:
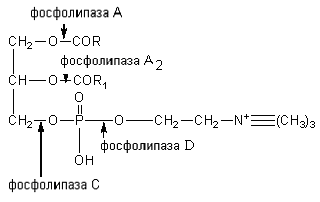
Фосфолипазы поджелудочной железы, тканевые фосфолипазы вырабатываются в виде проферментов и активируются трипсином. Фосфолипаза A2 змеиных ядов катализирует отщепление ненасыщенной жирной кислоты в положении 2 фосфоглицеридов. При этом образуются лизолецитины с гемолитическим действием.
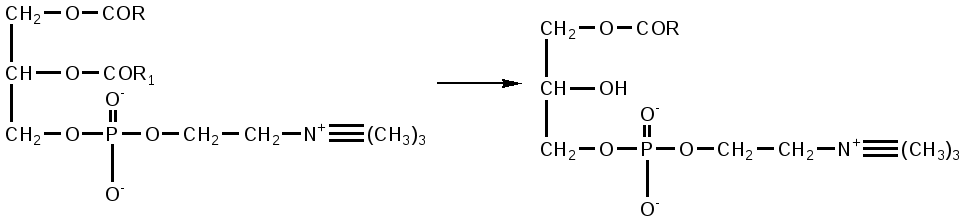
фосфотидилхолин лизолецитин
Поэтому при попадании этого яда в кровь происходит сильный гемолиз.. В кишечнике эта опасность устраняется действием фосфолипазы A1, быстро инактивирующей лизофосфатид в результате отщепления от него остатка насыщенной жирной кислоты с превращением его в неактивный глицерофосфохолин.
Лизолецитины в малых концентрациях стимулируют дифференцировку лимфоидных клеток, активность протеинкиназы С, усиливают клеточную пролиферацию.
Коламинфосфатиды и серинфосфатиды расщепляются фосфолипазой А до лизоколаминфосфатидов, лизосеринфосфатидов, которые далее расщепляются фосфолипазой A2. Фосфолипазы С и D гидролизуют связи холина; коламина и серина с фосфорной кислотой и остатка фосфорной кислоты с глицерином.
Всасывание липидов происходит в тонком отделе кишечника. Жирные кислоты с длиной цепи менее 10 углеродных атомов всасываются в неэтерифицированной форме. Для всасывания необходимо присутствие эмульгирующих веществ – желчных кислот и желчи.
Ресинтез жира, характерного для данного организма, происходит в кишечной стенке. Концентрация липидов в крови в течение 3-5 часов после приема корма высокая. Хиломикроны – мелкие частицы жира, образующиеся после всасывания в кишечной стенке, представляют собой липопротеиды, окруженные фосфолипидами и белковой оболочкой, внутри содержат молекулы жира и желчных кислот. Они поступают в печень, где липиды подвергаются промежуточному обмену, а желчные кислоты проходят в желчный пузырь и далее обратно в кишечник (см. рис.9.3 на стр.192). В результате такого кругооборота теряется малое количество желчных кислот. Считают, что молекула желчной кислоты в сутки совершает 4 кругооборота.
Промежуточный обмен липидов
Синтез и распад липидов происходит в течение 1-2 суток. Адипоциты жировых тканей играют основную роль в обмене триацилглицеринов, которые в них синтезируются, откладываются про запас и по мере необходимости расходуются. Липолиз – расщепление жира в жировой ткани осуществляется ферментами моно-, ди-, три-глицеридлипазами, которые расщепляют триацилглицериды на глицерин и жирные кислоты. Жирные кислоты и глицерин в клетках организма окисляются до углекислоты и воды, а энергия, образующаяся при этом аккумулируется в молекулах АТФ.
Окисление глицерина начинается с фосфорилирования с участием АТФ. В результате этой реакции образуется фосфоглицериновая кислота, которая при участии НАД подвергается дегидрированию с образованием 3-фосфоглицеринового альдегида:
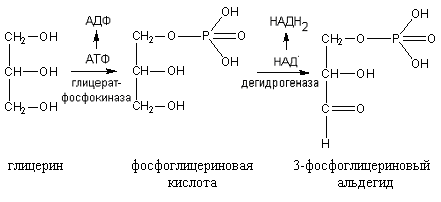
3-фосфоглицериновый альдегид далее окисляется как при гликолизе. Часть фосфоглицериновой кислоты используется для синтеза фосфатидов.
Окисление жирных кислот происходит по β-углеродному атому в матриксе митохондрий. Жирные кислоты с короткой углеродной цепью (4-10 атомов) проникают в митохондрии; а с более длинной цепью проникают в виде ацилкарнитинов:
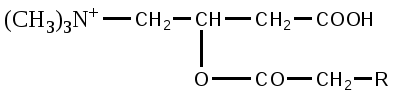
ж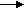 ирная кислота + АТФ + карнитин ацилкарнитин ирная кислота + АТФ + карнитин ацилкарнитин
При β-окислении жирных кислот в каждом цикле отделяется по 2 С в виде активированной уксусной кислоты (ацетил-КоА) – CH3-CO-SKoA. Например, при окислении пальмитиновой кислоты (C16) образуется 8 молекул CH3-CO-SKoA:
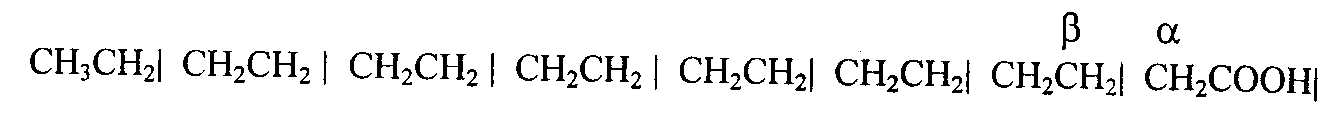
Последовательность реакции окисления жирной кислоты выглядит следующим образом: в начале жирная кислота активируется с участием HS-коэнзима А, в результате образуется ацил-КоА. В митохондриях ацил-КоА подвергается дегидрированию с участием фермента ацил-КоА-дегидрогеназы, при этом происходит восстановление ФАД в ФАДН2, образуется ненасыщенная активированная жирная кислота:
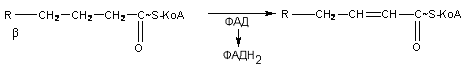
На следующем этапе происходит присоединение молекулы воды с участием фермента еноилгидратазы, в результате образуется β-гидроксиацил-КоА:
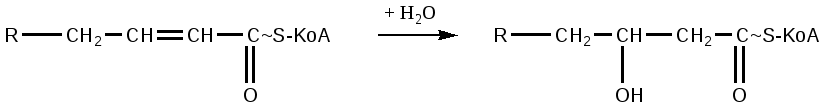
Далее происходит образование кетокислоты в результате дегидрирования β-гидроксиацил-КоА: реакция происходит с участием кофермента НАД, который восстанавливается в НАДН2:

Молекула кетоформы ацил-КоА под влиянием фермента и при наличии одной молекулы HS-KoA разрывается на 2 части: ацетил-КоА и ацил-КоА, который имеет на два атома углерода меньше исходной кислоты:
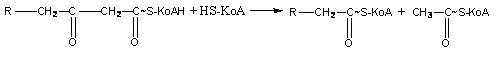 ацил-КоА ацетил-Коа ацил-КоА ацетил-Коа
Ацетил-КоА подвергается окислению в цикле Кребса, ацил-KoA - снова проходит путь β-окисления, при этом каждый раз цепь укорачивается на 2 атома углерода.
Окисление жирной кислоты, имеющий 2n атомов углерода происходит за n-1 циклов, так как, окисление бутирил-КоА (4C) завершается за один цикл.
Энергетический баланс β-окисления жирных кислот
При каждом цикле образуется ФАДН2, НАДН2 которые в дыхательной цепи дают:
ФАДН2 – 2 молекулы АТФ
НАДН2 – 3 молекулы АТФ.
Окисление 1 молекулы CH3-CO-KoA в цикле Кребса дает 12 молекул АТФ.
При полном окислении жирной кислоты (n/2)-1 циклов β-окисления, возникает n/2 молекул ацетил-КоА, следовательно, при окислении, например, пальмитиновой кислоты (C16) образуется 130 молекула АТФ.
Метаболизм ацетил-коэнзима А
Ацетил-КоА может окисляться в цикле трикарбоновых кислот. При этом обеспечивается 12 молекул АТФ на каждую молекулу ацетилкоэнзима А. Ацетил-КоА может использоваться для синтеза жирных кислот, при этом требуется достаточное количество энергии (АТФ). При недостатке энергии, при нарушении обмена углеводов и липидов синтез холестерина через мевалоновую кислоту нарушается и происходит образование кетоновых тел с их накоплением в тканях и выделением с мочой (кетозы). Мевалоновоя кислота является предшественником холестерина. Однако реакции биосинтеза холестерина почти полностью совпадают с реакциями биосинтеза кетоновых тел. При нормальной энергетической обеспеченности ацетоацетил-КоА полностью превращается в печени в мевалоновую кислоту, затем в холестерин. При уменьшении углеводов, сахарном диабете, нарушении обмена липидов происходит увеличение кетоновых тел, развиваются кетозы.
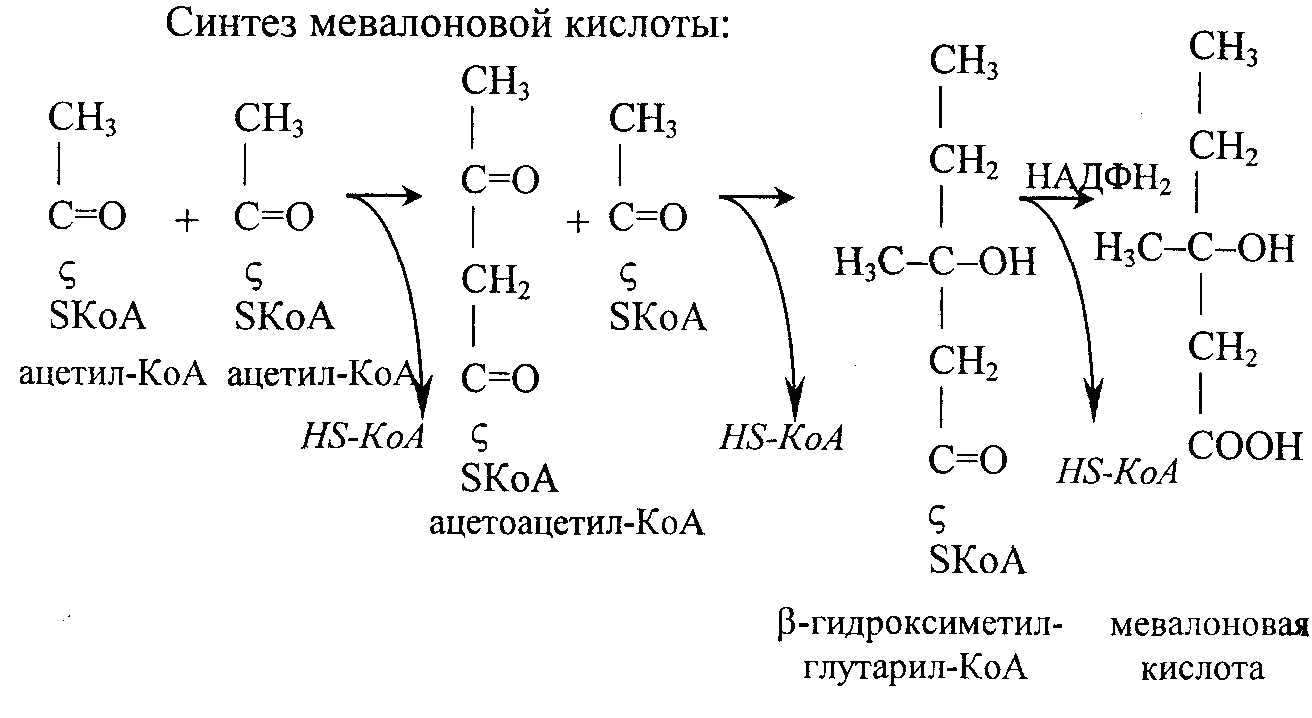
Пути образования кетоновых тел
1. Образование кетоновых тел происходит при углеводном голодании, уменьшении энергетических источников для синтеза жира, холестерина из активированной уксусной кислоты. При этом активированная мевалоновая кислота распадается на ацетоуксусную кислоту и ацетил-КоА:
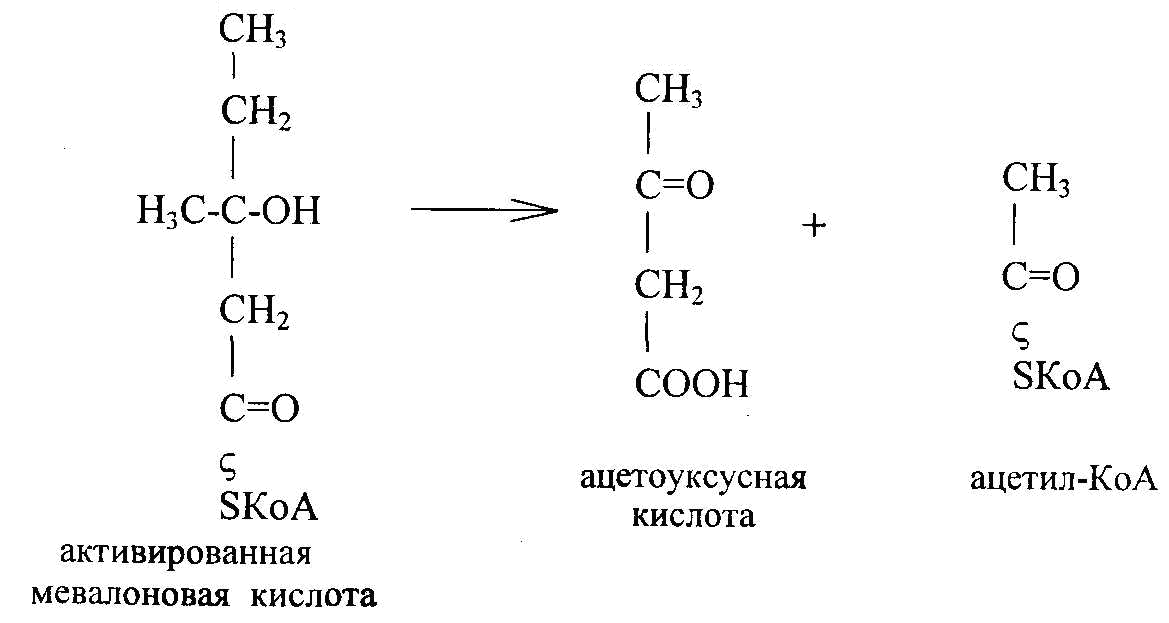
Ацетоуксусная кислота частично восстанавливается до (β-оксимасляной кислоты, а частично декарбоксилируется, образуя ацетон:
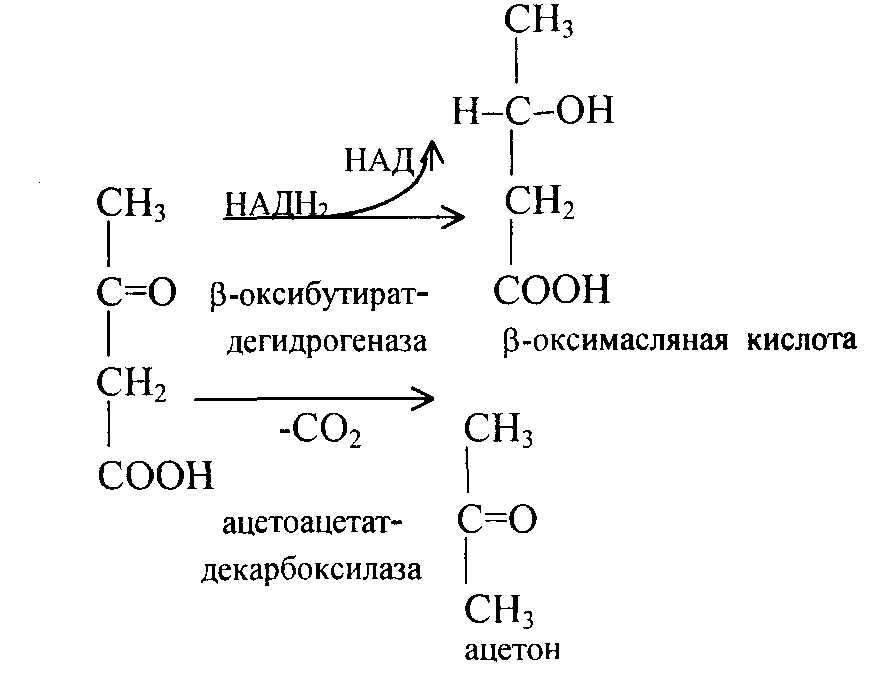
II. Если CH3-CO-KoA образуется много и недостаточно энергии для синтеза жира, то образуется активированная ацетоуксусная кислота:

Затем образуется свободная ацетоуксусная кислота:
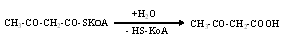
Образующаяся ацетоуксусная кислота может превращаться в β-оксимасляную кислоту или ацетон, как указано выше. Кетоновые тела синтезируются в печени и поступают в кровь. В нормальных условиях β-оксимасляная кислота, ацетоуксусная кислота окисляются в тканях мышц и являются источником энергии. Однако при нарушениях обмена (сахарный диабет), когда использование углеводов затруднено и усиливается окисление липидов, при длительном недостатке углеводов, происходит чрезмерный биосинтез кетоновых тел с образованием ацетона. При этом происходит кетонемия (ацидоз) и нарушение нормального функционирования организма.
Окисление ненасыщенных жирных кислот происходит после их превращения в соответствующую насыщенную жирную кислоту. Затем они окисляются по β-углеродному атому.
Окисление жирных кислот с нечетным числом углеродных атомов происходит так же, как и при окислении жирных кислот с четным числом атомов углерода. Отличие состоит в том, что в конечном итоге образуется пропионил-КоА, который вначале подвергается карбоксилированию, в результате образуется активированная янтарная кислота (сукцинил-КоА). Сукцинил-КоА окисляется в цикле трикарбоновых кислот.
Биосинтез липидов
Способность животных запасать полисахариды довольно ограничена; поэтому глюкоза, поступающая в организм в значительных количествах, используется для синтеза жирных кислот и глицерина. Важным процессом является также биосинтез холестерина, так как он является исходным продуктом для образования многочисленных биологически активных стероидов.
Синтез высших жирных кислот происходит из ацетил-KoA в цитозоле. Фермент ацетил-КоА-карбоксилаза, содержащий биотин, катализирует АТФ-зависимый синтез малонил-КоА из ацетил-КоА и СО2:
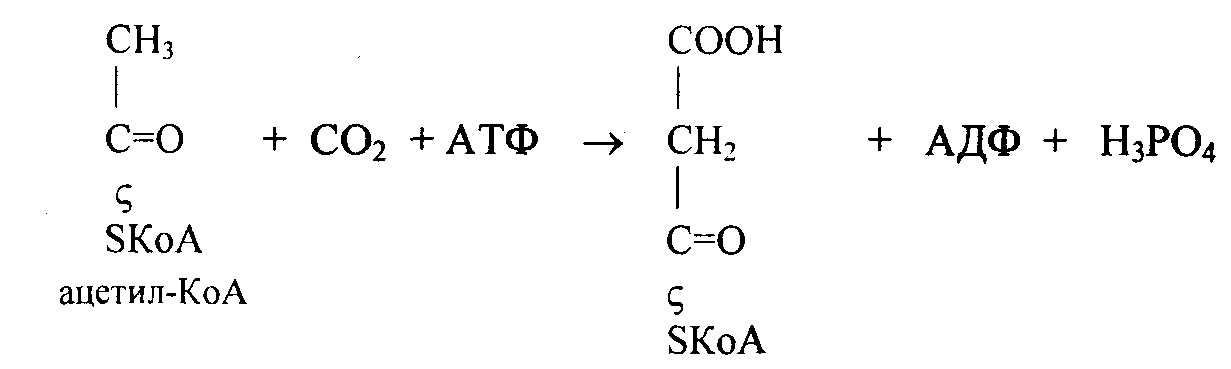
При участии ацилпереносящего белка (АПБ) Мм 10 Да происходит синтез ацетил-SАПБ и малонил-SАПБ:
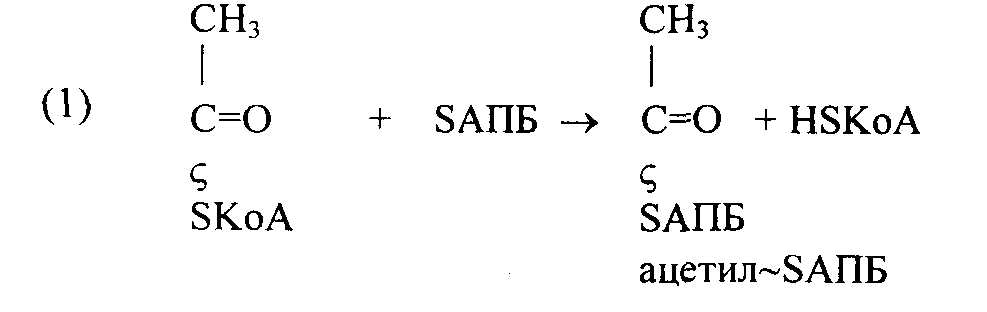
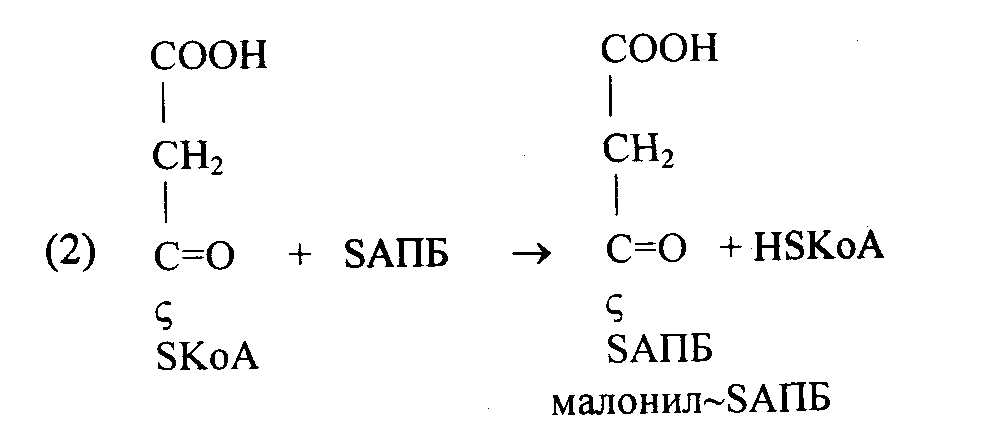
На следующем этапе ацетил-SАПБ и малонил-SАПБ взаимодействуют с образованием ацето-ацетил- SAПБ:
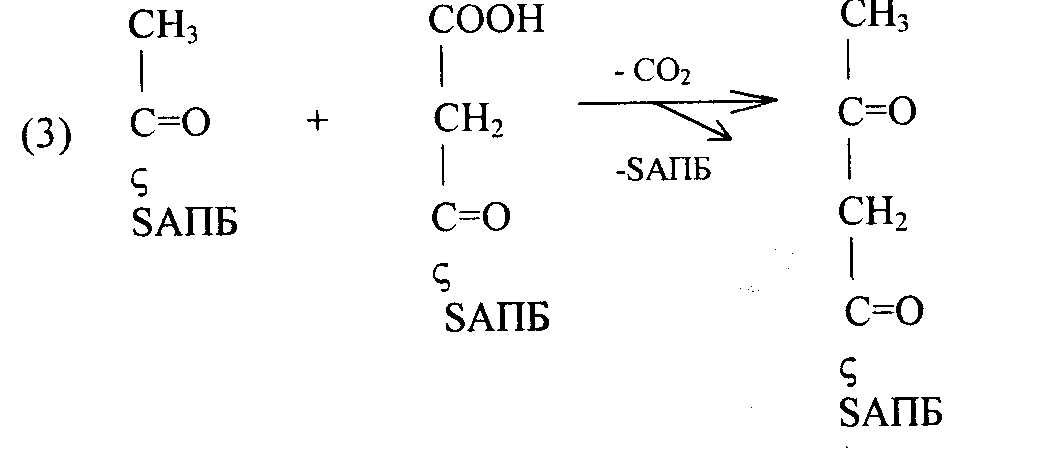
ацетоацетил-SАПБ
После этого ацетоацетил-SАПБ восстанавливается по β-углеродному атому с участием НАДФН2, в результате образуется β-гидроксибутирил-SAПБ. Затем происходит присоединение активированной уксусной кислоты и молонила к ацетилпереносящему белку (АПБ):
β-ГидроксибутирилSАПБ под действием фермента β-гидрокси-АПБ-дегидратазы теряет молекулу воды (5) и превращается в кротонил-SАПБ; последний с участием НАДФН2 восстанавливается в бутирил-SAПБ. Далее цикл реакции повторяется.
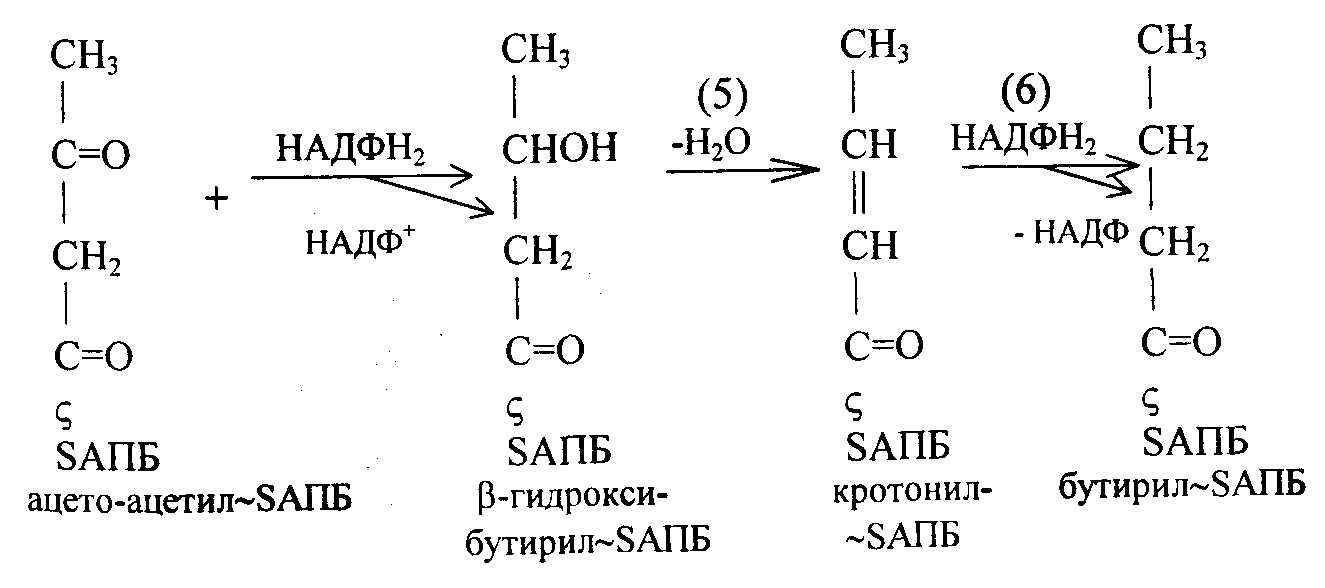
Если идет синтез пальмитиновой кислоты (C16), то к бутирил-SAПБ присоединяется последовательно еще 7 раз малонил
SАПБ, при этом отщепляется дистальная карбонильная группа малонил
SАПБ в виде CO2. Суммарный результат этих реакций следующий:
а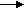 цетил-КоА + 7 малонил-КоА + 14 НАДФН2 цетил-КоА + 7 малонил-КоА + 14 НАДФН2
п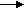 альмитиновая кислота + 7 CO2 + 8 HSKoA + 14 НАДФ + 7 H2O альмитиновая кислота + 7 CO2 + 8 HSKoA + 14 НАДФ + 7 H2O
В этом процессе 7 молекул CO2 образуется за счет свободных карбоксильных групп 7 молекул малонил-КоА. Из 16 углеродных атомов пальмитиновой кислоты 2 атома образуется за счет ацетил-КоА, а остальные за счет малонил-КоА.
В ходе синтеза 7 карбоксильных групп – С=О- восстанавливаются из семи групп -CH2 -, на это расходуется 14 НАДФН2: за счет 7 из них образуются водородные атомы групп -CH2 -, а за счет остальных семи – кислород карбонильных групп превращается в воду.
Биосинтез фосфатидных кислот и триглицеридов происходит в печени и жировой ткани при наличии глицерина и жирных кислот. Глицерин образуется при гидролизе липидов, затем под влиянием фермента глицерокиназы с участием АТФ синтезируется глицерофосфат:
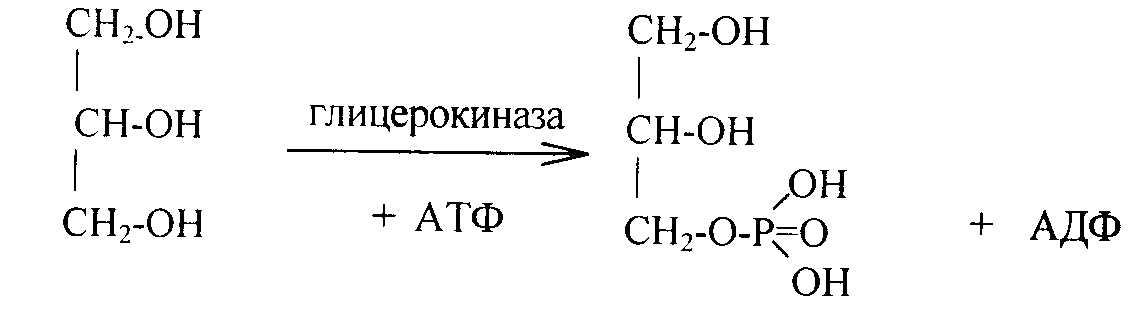
Глицерофосфат может образоваться также из диоксиацетонфосфата, возникшего при окислении глюкозы путем восстановления НАДН2.
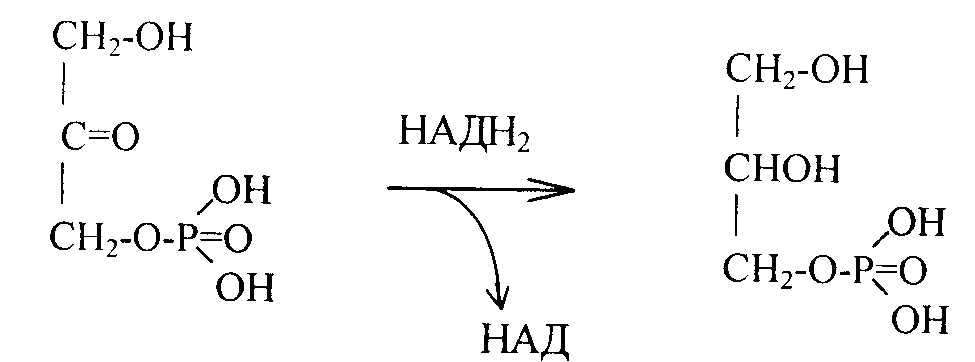
фосфодиоксиацетон глицерофосфат
Глицерофосфат далее используется для биосинтеза фосфатидной кислоты. Реакция катализируется фосфатидсинтетазой:
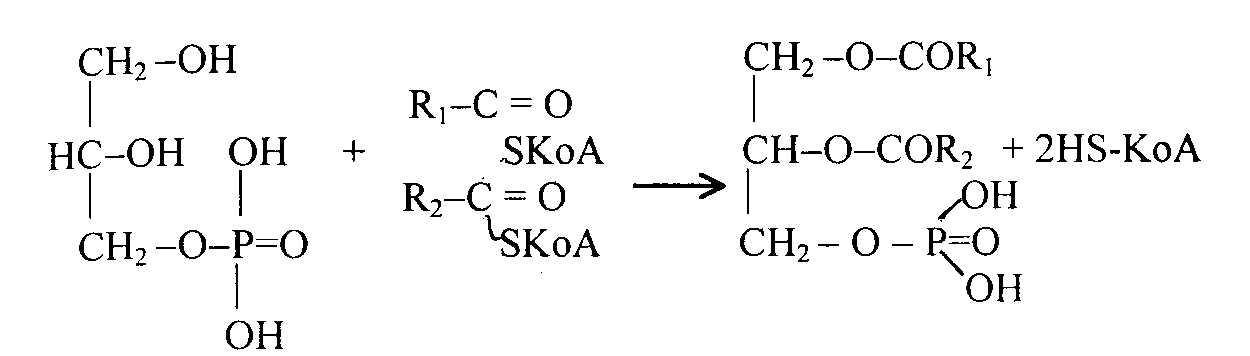
глицерофосфат ацил-КоА фосфатидная кислота
В фосфатидной кислоте в двух позициях спиртовые группы глицерина соединены сложноэфирной связью с остатками жирной кислоты (чаще всего с 16 и 18 углеродными атомами), а в одной позиции с фосфорной кислотой. Синтез триацилглицеринов осуществляется из фосфатидной кислоты. Вначале из фосфатидной кислоты отделяется фосфорная кислота, при этом образуется диацилглицерин. Далее диацилглицерин реагирует с третьей молекулой активированной жирной кислоты (ацил-КоА) и образуется триацилглицерин:
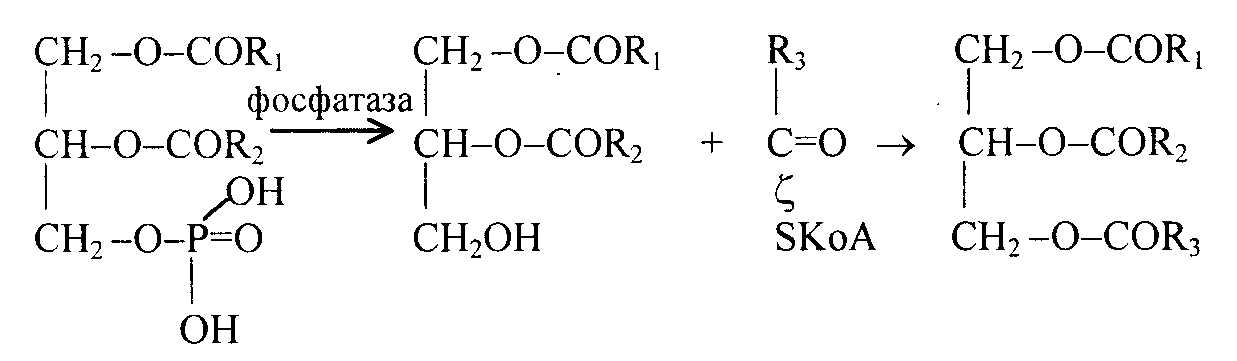
фосфатидная диацилглицерин ацил-КоА триацилглицерин
кислота
Биосинтез фосфоглицеридов происходит в эндо- плазматических мембранах клетки. Фосфатидилэтаноламин синтезируется в следующей последовательности: в начале этаноламин фосфорилируется с участием АТФ и фермента этаноламинкиназы:
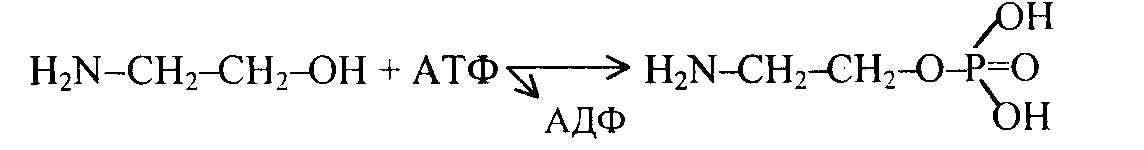
этаноламин фосфоэтаноламин
Затем фосфоэтаноламин реагирует с ЦТФ, в результате образуется цитидилдифосфатэтаноламин и пирофосфат:
фосфоэтаноламин + ЦТФ → ЦДФ-этаноламин.
Далее ЦДФ-этаноламин взаимодействуя с 1,2- диацилглице-ридом, превращается в фосфатидилэтаноламин:
ЦДФ-этаноламин + 1,2-диацилглицерид →
→ фосфатидилэтаноламин + ЦМФ.
Биосинтез фосфатидилхолина (лецитина) осуществляется следующим образом: синтезируется фосфатидилхолин из фосфатидилэтаноламина путем метилирования или же вначале холин взаимодействует с ЦТФ.
Затем ЦДФ-холин с 1,2- диацилглицерином образует дифосфатидилхолин:.
ЦДФ-холин + 1,2 - диацилглицерин →
→ фосфатидилхолин + ЦМФ
Биосинтез фосфатидилсерина происходит путем обмена этаноламина на серин:
Фосфатидилэтаноламин + L-серин →
→ фосфатидилсерин + этаноламин.
Метаболизм стеринов и стеридов
Стерины растительного происхождения – фитостерины в кишечнике животных не всасываются и выделяются с фекалиями. Холестерин и его эфиры имеют большое значение в обмене веществ, так как из холестерина образуются желчные кислоты, витамины D2 и Dз, стероидные гормоны. Холестерин, поступающий с кормом, всасывается из кишечника в виде комплексных соединений с желчными кислотами.
В организме животных холестерин синтезируется из ацетил-KoA. В начале образуется мевалоновая кислота, затем через ряд превращений возникает сквален-ланостерин-холестерин. Основные пути превращения жиров можно представить таким образом:
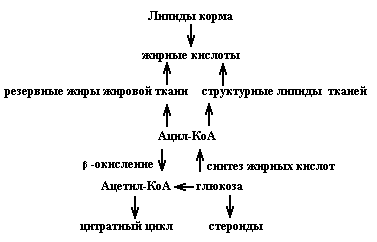
Регуляция липидного обмена осуществляется нейрогуморальным путем. Центральная нервная система влияет на обмен липидов через гипофиз, щитовидную железу и половые железы.
Нарушение липидного обмена может происходить в результате различных причин – голодания, низкого содержания легкоперевариваемых углеводов в кормах, нарушения переваривания липидов в желудочно-кишечном тракте, гиповитаминозов и т.д. Например, кетозы развиваются в результате нарушения синтеза холестерина из-за недостаточности в кормах источников энергии, при этом содержание кетоновых тел в крови повышается в десятки раз; при избыточном поступлении углеводов с кормом в организме резко возрастает синтез жиров и они усиленно откладываются в жировое депо. Нарушение обмена липидов может быть следствием малого поступления в кишечник желчных кислот, которые способствуют гидролизу жиров и их всасыванию. Нарушение всасывания липидов ведет к гиповитаминозу в связи со снижением всасывания жирорастворимых витаминов.
Часто встречаются нарушения холестеринового обмена в крови, во внутренних органах, в печени, наблюдается повышенное отложение холестерина. Появляется желчно-каменная болезнь, когда в желчных путях и желчном пузыре откладываются желчные камни, состоящие на 90-99 % из холестерина. На внутренней поверхности кровеносных сосудов образуются холестериновые бляшки, что приводит к снижению эластичности кровеносных сосудов, является причиной разрыва их, возникновения инфарктов и инсультов, обширных кровоизлияний.
Липосомы – это липидные пузырьки, состоящие из одного или нескольких фосфолипидных бислоев, разделенных водной фазой (рис.9.2.). Липосомы получают путем встряхивания или обработкой ультразвуком водных суспензий фосфолипидов.
Липосомы
Рис.9.2. Схематическое изображение небольшой сферической липосомы в поперечном разрезе; диаметр липосомы 25 нм. Внутренняя водная фаза липосом используется для доставки лекарственных препаратов, антител, ферментов в органы и ткани.
Они могут быть сформированы из индивидуальных фосфолипидов или же из их смеси. Липосомы можно применять как микроконтейнеры, которые способны доставлять различные лекарственные вещества в органы и ткани организма. В липосомы могут быть заключены лекарственные вещества, антигены, антитела, ферменты и т.д. Использование липосом для доставки к тканям определенных лекарственных веществ имеет большие преимущества, так как без липосомной оболочки многие из них не могут проходить через клеточные мембраны. Например, антитела в липосомах могут проникнуть в клеточное ядро; гормоны, ферменты в липосомах могут быть доставлены по определенному «адресу»; антигены в липосомах могут быть использованы более эффективно. Прохождение липосом через клеточную оболочку обеспечивается за счет эндоцитоза -
липосома захватывается клеткой, образуется вакуоль, которая сливается с липосомами. Ферменты лизосом гидролизуют фосфолипиды липосом, что обеспечивает выход препарата в цитоплазму клетки. Применение различных лекарственных веществ, антигенов, ферментов, витаминов, инкапсулированных в липосомах является очень перспективным и изучается интенсивно.
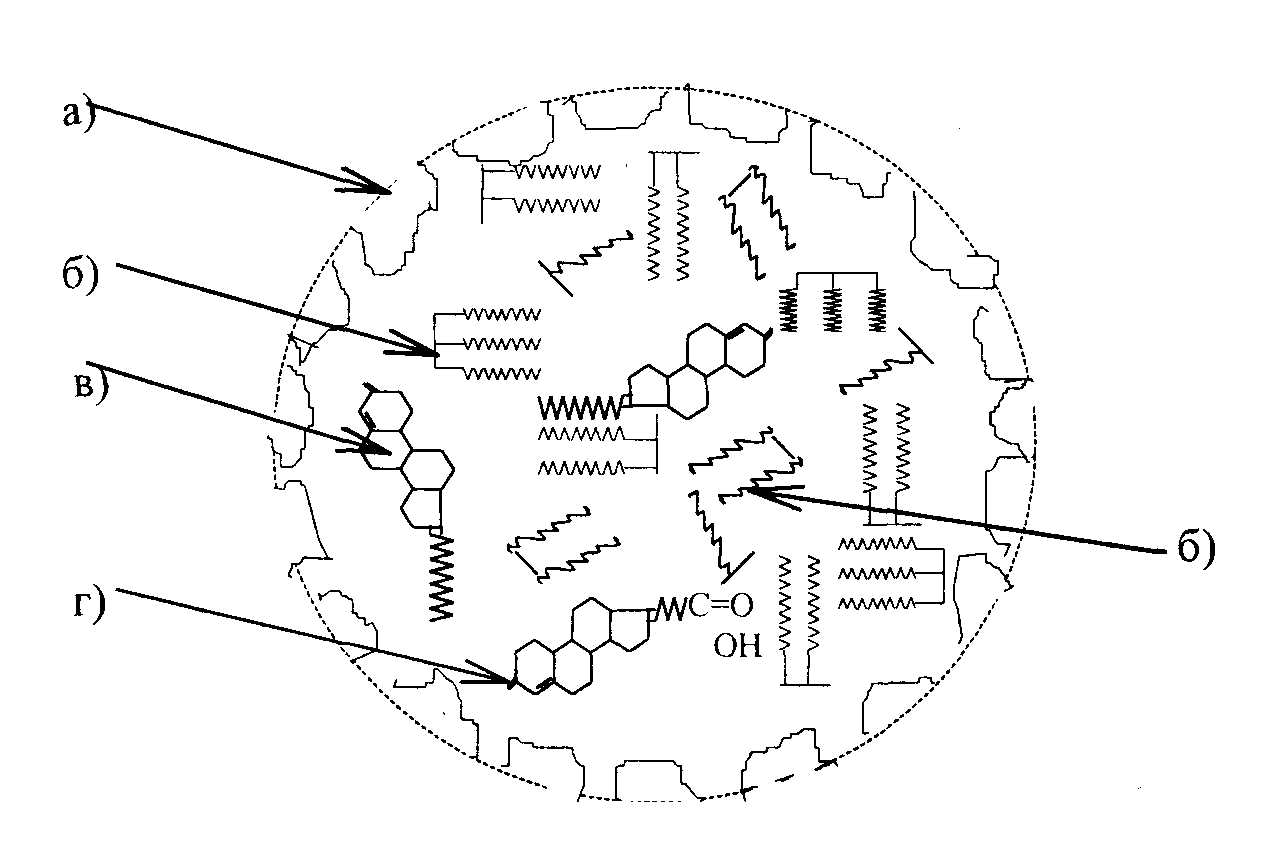
Рис.9.2. Хиломикроны - мелкие жировые частицы, образуются в кишечной стенке из липопротеидов (а), моно-, ди-, три- ацилглицеридов (б), стеридов (в) и желчных кислот (г).
|
 Скачать 14.38 Mb.
Скачать 14.38 Mb.



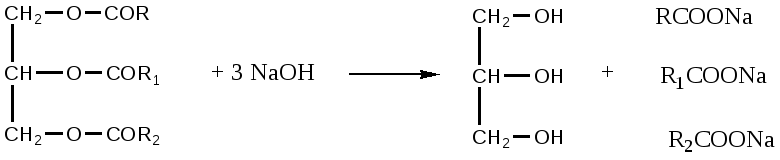







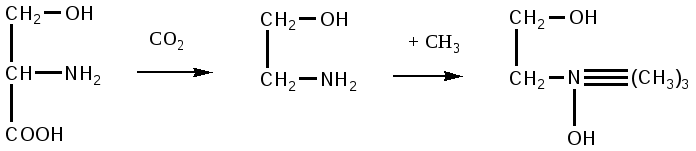

















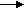 ирная кислота + АТФ + карнитин ацилкарнитин
ирная кислота + АТФ + карнитин ацилкарнитин
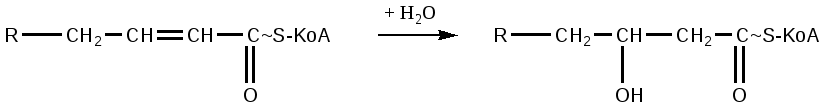

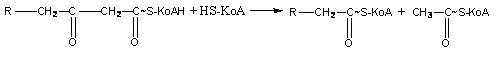 ацил-КоА ацетил-Коа
ацил-КоА ацетил-Коа