Патфиз ч.2. Патфиз ч. Гл. 11 Нарушения водного обмена Гл. 12 Нарушения ионного обмена
 Скачать 7.84 Mb. Скачать 7.84 Mb.
|
|
§ Гиперосмия тканей в связи с увеличением диссоциации органических и неорганических соединений (электролитов) в ксловиях ацидоза. § Гиперонкия тканей в результате повышения гидролиза и дисперсности белковых молекул при увеличении содержания ионов H+ в жидкостях. § Снижение реабсорбции жидкости в микрососудах в связи с венозным застоем, характерным для недостаточности кровообращения. § Повышение проницаемости стенок артериол и прекапилляров в условиях ацидоза. ‡ Потеря ионов Ca2+ костной тканью с развитием остеодистрофии. § Причина: расходование гидрокарбоната и фосфата кальция костной ткани на забуферивание избытка H+ в крови и других жидкостях организма. Этот процесс регулирует ПТГ. Стимулом для повышенного образования гормона является снижение концентрации Ca2+ в крови в связи с его включением в буферные системы. В результате развивается остеопороз, остеодистрофия, у детей — рахит. § Указанные изменения кальциевого обмена и состояния костной ткани получили название «феномена расплаты» за компенсацию негазового ацидоза. † Негазовые алкалозы При всем разнообразии вариантов негазовых алкалозов, они имеют ряд общих, закономерно развивающихся признаков. К числу основных относятся: ‡ Гипоксия. Причины. § Гиповентиляция лёгких, обусловленная снижением [Н+] в крови и как следствие — уменьшением функциональной активности инспираторных нейронов дыхательного центра. § Увеличение сродства Hb к кислороду вследствие уменьшения содержания H+ в крови. Это вызывает снижение aennioeaoee HbО2 и поставки кислорода тканям. ‡ Гипокалиемия Причины: § увеличение выведения K+ почками в условиях альдостеронизма, § активация обмена Na+ на K+ в дистальных отделах канальцев почек в связи с повышением в первичной моче [Na+], § потеря K+ (хотя и в ограниченном объёме) в связи со рвотой. Последствия: § транспорт H+ в клетку с развитием в ней ацидоза; § нарушения обмена веществ, особенно — торможение протеосинтеза; § ухудшение нервномышечной возбудимости. ‡ Недостаточность центрального и органнотканевого кровотока. Причины. § Снижение тонуса стенок артериол в связи с нарушением энергообеспечения и ионного обмена. § Артериальная гипотензия, развивающаяся при уменьшении тонуса артериол, сердечного выброса, а также вследствие гиповолемии. ‡ Нарушения микрогемоциркуляции, вплоть до признаков капиллярно-трофической недостаточности. Причины: § Расстройства центрального и органнотканевого кровотока. § Нарушение агрегатного состояния крови в связи с гемоконцентрацией (наиболее выражено при повторной рвоте и полиурии). ‡ Ухудшение нервномышечной возбудимости, проявляющееся мышечной слабостью, нарушением перистальтики желудка и кишечника. Причины: гипокалиемия и изменение содержания других ионов в крови и межклеточной жидкости, а также гипоксия клеток. ‡ Расстройства функций органов и тканей вплоть до их недостаточности. Причины: гипоксия, гипокалиемия и нарушения нервномышечной возбудимости. ТИПОВЫЕ ФОРМЫ НАРУШЕНИЙ КИСЛОТНО-ЩЕЛОЧНОГО РАВНОВЕСИЯ РЕСПИРАТОРНЫЙ АЦИДОЗ Респираторный ацидоз характеризуется снижением рН крови и гиперкапнией (повышением рСО2 крови более 40 мм рт.ст.). При этом линейной зависимости между степенью гиперкапнии и клиническими признаками респираторного ацидоза нет. Последние во многом определяются причиной гиперкапнии, особенностями основного заболевания и реактивностью организма пациента. ПРИЧИНЫ И ПРИЗНАКИ РЕСПИРАТОРНОГО АЦИДОЗА • Компенсированный ацидоз, как правило, существенных изменений в организме не вызывает. • Некомпенсированный ацидоз приводит к значительным нарушениям жизнедеятельности организма и развитию в нём комплекса характерных изменений. ПРИЧИНА И НАИБОЛЕЕ ЗНАЧИМЫЕ ПРИЗНАКИ РЕСПИРАТОРНОГО АЦИДОЗА Причина: нарастающая гиповентиляция лёгких. Она является главным фактором возникновения газового ацидоза (при спазме бронхиол или обтурации дыхательных путей). Механизм спазма бронхиол: повышение холинергических эффектов в условиях значительного ацидоза. Это является результатом: † Увеличенного высвобождения ацетилхолина из нервных терминалей. † Повышения чувствительности холинорецепторов к ацетилхолину. Проявления респираторного ацидоза. •Спазм мелких бронхов и бронхиол. Опасность бронхоспазма в условиях ацидоза заключается в возможности формирования порочного патогенетического круга «Бронхоспазм → нарастание pCO2 → быстрое снижение рН → усиление бронхоспазма → дальнейшее увеличение рCO2». • Расширение артериол мозга, развитие артериальной гиперемии ткани мозга, повышение внутричерепного давления. Причины: длительнaя значительная гиперкапния и гиперкалиемия. Механизм: снижение базального мышечного тонуса стенок артериол мозга в условиях продолжительно повышенного рCO2, рН и гиперкалиемии. Проявления повышенного внутричерепного давления: † сначала головная боль и психомоторное возбуждение, † затем сонливость и заторможенность. Сдавление вещества головного мозга приводит также к повышению активности нейронов блуждающего нерва. Это, в свою очередь вызывает: † артериальную гипотензию, † брадикардию, † иногда остановку сердца. • Спазм артериол и ишемия органов (кроме мозга!). Причины † Гиперкатехоламинемия, наблюдающаяся в условиях ацидоза. † Гиперсенситизация αадренорецепторов периферических артериол. Проявления Ишемия тканей и органов сопровождается полиорганной дисфункцией. Однако, как правило, доминируют признаки ишемии почек: при значительном повышении рCO2 снижается почечный кровоток и объём клубочковой фильтрации и увеличивается масса циркулирующей крови. Это значительно повышает нагрузку на сердце и при хроническом респираторном ацидозе (например, у пациентов с дыхательной недостаточностью) может привести к снижению сократительной функции сердца, т.е. к сердечной недостаточности. • Нарушение тока крови и лимфы в сосудах микроциркуляторного русла. Причины † Спазм артериол в тканях и органах (за исключением мозга!). † Сердечная недостаточность, ведущая к снижению перфузионного давления крови в артериолах и нарушению её оттока по венулам. Проявления. У многих пациентов расстройства микрогемоциркуляции становятся одним из главных патогенетическиo caaiuaa развития полиорганных расстройств. • Гипоксемия и гипоксия Причины † Гиповентиляция лёгких. † Нарушение перфузии лёгких в связи с сердечной недостаточностью. † Уменьшение сродства Hb к кислороду (является следствием гиперкапнии). † Нарушение процессов биологического окисления в тканях (обусловлено нарушением микрогемоциркуляции, гипоксемией, снижением активности ферментов тканевого дыхания, а при тяжёлом ацидозе и гликолиза). • Дисбаланс ионов: увеличение содержания ионов K+ в межклеточной жидкости, гиперкалиемия, гиперфосфатемия, гипохлоремия. Причины † Гипоксия и нарушения энергетического обеспечения клеток. † Увеличение концентрации H+ во внеклеточной жидкости. При этом вхождение H+ в клетки сопровождается выходом из них K+. Последствия. Значительная гиперкалиемия обусловливает снижение порога возбудимости клеток, в том числе кардиомиоцитов. Это нередко приводит к сердечным аритмиям, включая фибрилляцию. МЕХАНИЗМЫ КОМПЕНСАЦИИ РЕСПИРАТОРНОГО АЦИДОЗА Имеются срочные и долговременные механизмы компенсации респираторного ацидоза. Обе группы механизмов направлены на нейтрализацию избытка H+, образующихся при диссоциации угольной кислоты (рис. 13–3). СРОЧНАЯ КОМПЕНСАЦИЯ РЕСПИРАТОРНОГО АЦИДОЗА Механизм срочной компенсации респираторного ацидоза реализуется при участии химических буферных систем организма, а также Cl––HCO3–обменного механизма (антипорта) эритроцитов 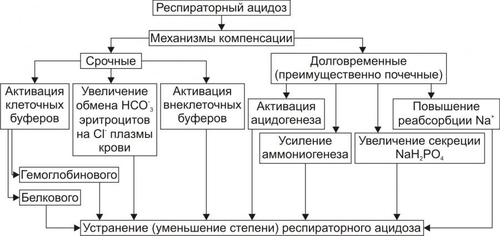 Рис. 13–3. Механизмы компенсации респираторного ацидоза. • Гемоглобиновый буфер эритроцитов является наиболее ёмким среди механизмов компенсации респираторного ацидоза. Избыток H+ связывается неоксигенированным Hb эритроцитов. • Белковая буферная система клеток снижает [H+] во внеклеточной жидкости в результате обмена на внутриклеточный K+, что может сопровождаться гиперкалиемией. • Белковый и фосфатный буферы костной ткани также активируются при значительном снижении рН. • Белковый буфер плазмы крови вносит определённый (хотя и не очень большой) вклад в нейтрализацию H+ в крови, акцептируя его анионными лигандами белков и высвобождая в плазму Na+ (с развитием гипернатриемии). • Анионы HCO3–_ выходят из эритроцитов в обмен на Cl– плазмы, восполняют её гидрокарбонатный буфер и тем самым способствуют устранению ацидоза. ДОЛГОВРЕМЕННАЯ КОМПЕНСАЦИЯ РЕСПИРАТОРНОГО АЦИДОЗА Механизм долговременной компенсации длительно сохраняющегося респираторного ацидоза реализуется почками. Для достижения эффекта требуется 3–4 сут (отсюда и название механизма). При респираторном ацидозе в почках активизируются: • ацидогенез, • аммониогенез, • секреция NaH2 PO4, • K+ — Na+ обмен. Указанные механизмы одновременно обеспечивают реабсорбцию в кровь гидрокарбоната и Na+, что восполняет расход гидрокарбонатной буферной системы. ТИПИЧНЫЕ ИЗМЕНЕНИЯ ПОКАЗАТЕЛЕЙ КЩР ПРИ РЕСПИРАТОРНОМ АЦИДОЗЕ Основной патогенетический фактор: увеличение рCO2 в крови. • Типичные изменения показателей КЩР при газовом ацидозе (капиллярная кровь):
• Пример изменения показателей КЩР (капиллярная кровь) при некомпенсированном газовом ацидозе.
У пациента приступ бронхиальной астмы. РЕСПИРАТОРНЫЙ АЛКАЛОЗ Респираторный алкалоз характеризуется увеличением рН и гипокапнией (снижением рСО2 крови до 35 мм рт.ст. и более). ПРИЧИНА И ОСНОВНЫЕ ПРИЗНАКИ РЕСПИРАТОРНОГО АЛКАЛОЗА Причина газового алкалоза: гипервентиляция лёгких. При этом объём альвеолярной вентиляции выше необходимого для выведения того количества СО2, которое образуется в процессе обмена веществ за определённый период времени. Основные признаки газового алкалоза • Нарушения центрального и органнотканевого кровообращения. Причины † Повышение тонуса стенок артериол головного мозга, ведущее к его ишемии. † Повышение тонуса стенок сосудов головного мозга, ведущее к его ишемии. † Снижение тонуса стенок артериол в органах и тканях (кроме мозга!). Это, в свою очередь приводит к: ‡ развитeю aртериальной гипотензии, ‡ депонированию крови в расширенных сосудах, ‡ уменьшению ОЦК, ‡ снижению венозного давления, ‡ уменьшению объёма крови, притекающей к сердцу, ‡ уменьшению ударного и сердечного выбросов. Указанная цепь изменений кровообращения уменьшает кровоснабжение тканей и органов, включая сердце. Это ещё более усугубляет системные расстройства кровообращения, что замыкает гемодинамический порочный круг при газовом алкалозе. • Гипоксия Причины † Недостаточность кровообращения. † Увеличение сродства Hb к кислороду, снижающее диссоциацию HbO2 в тканях. † Нарушение (в условиях респираторного алкалоза) карбоксилирования пировиноградной кислоты и превращения её в оксалоацетат, а также восстановления последнего в малат. Помимо усугубления энергодефицита, описанные расстройства создают условия для развития метаболического ацидоза. † Угнетение гликолиза в условиях гипоксии: снижение pСО2 до 15–18 мм рт.no. сопровождается торможением активности многих ферментов гликолиза. • Гипокалиемия, развивающаяся в значительной мере в связи с транспортом K+ из межклеточной жидкости в клетки в обмен на H+. • Мышечная слабость, проявляющаяся гиподинамией, парезом кишечника, параличами скелетной мускулатуры. Указанные расстройства являются в основном результатом гипокалиемии. • Нарушения ритма сердца — пароксизмы тахикардии, экстрасистолия — также обусловлены гипокалиемией. При снижении уровня K+ в плазме крови до 2 ммоль/л развивается гиперполяризация плазмолеммы кардиомиоцитов, нередко приводящая к остановке сердца в систоле. • Гипервентиляционная тетания вследствие: † Снижения [K+] в межклеточной жидкости в связи с повышенным связыванием K+ альбуминами. † Уменьшения концентрации H+ в межклеточной жидкости. рН плазмы крови является важным фактором, регулирующим связывание Ca2+ альбуминами: уменьшение [H+] (при алкалозе) активирует фиксацию Ca2+ белками. МЕХАНИЗМЫ КОМПЕНСАЦИИ РЕСПИРАТОРНОГО АЛКАЛОЗА Устранение респираторного алкалоза достигается при участии двух групп механизмов: срочных и долговременных. Как те, так и другие обеспечивают: 1) снижение в плазме крови и в других биологических жидкостях концентрации HCO–3 и 2) повышение рCO2 и как следствие — концентрации H2CO3 (рис. 13–4). 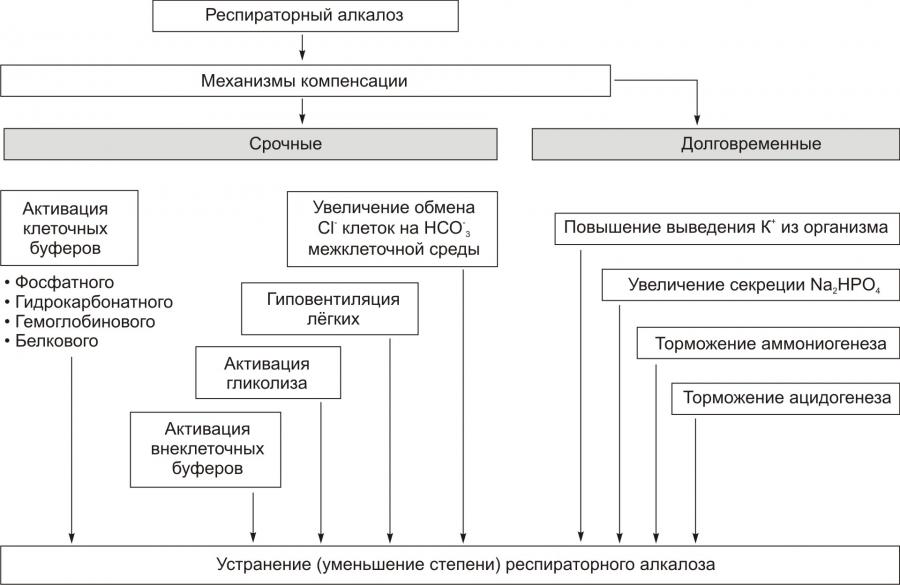 Рис. 13–4. Механизмы компенсации респираторного алкалоза. СРОЧНАЯ КОМПЕНСАЦИЯ РЕСПИРАТОРНОГО АЛКАЛОЗА • Снижение объёма альвеолярной вентиляции в связи с подавлением активности инспираторных нейронов при уменьшении рCO2 крови. Этот экстренный механизм включается при алкалозе, развивающемся в результате гипервентиляции и обусловливает восстановление уровня углекислоты в организме. • Активация внутриклеточных буферных систем: гидрокарбонатного, белкового, гемоглобинового, фосфатного. Это обеспечивает выход H+ из клетки в межклеточную жидкость и далее в кровь в обмен на K+ и Na+. • Активация гликолиза с интенсивным образованием молочной и пировиноградной кислот, что приводит к уменьшению рН крови (снижение концентрации H+ и увеличение HCO3 активирует гликолитические реакции). • Выход внутриклеточного Cl– в межклеточную жидкость в обмен на HCO3–. Это обеспечивает снижение концентрации гидрокарбоната как в интерстиции, так и в плазме крови и, как следствие — уменьшение рН. Активация внеклеточных буферных систем значимой роли в устранении газового алкалоза не имеет в связи с их малой ёмкостью по генерации H+. ДОЛГОВРЕМЕННЫЕ МЕХАНИЗМЫ КОМПЕНСАЦИИ РЕСПИРАТОРНОГО АЛКАЛОЗА Долговременные механизмы устранения респираторного алкалоза реализуется преимущественно почками: • Торможением ацидогенеза в связи с повышенной концентрацией НCO–3 в эпителии дистальных отделов нефронов. • Активацией калийуреза. • Увеличением выведения из крови в мочу Na2 HPO4. • Торможением аммониогенеза. Последнее происходит при угнетении в условиях алкалоза активности глутаминазы и снижения количества глутамата, поступающего в митохондрии. ТИПИЧНЫЕ ИЗМЕНЕНИЯ ПОКАЗАТЕЛЕЙ КЩР ПРИ РЕСПИРАТОРНОМ АЛКАЛОЗЕ Основной патогенетический фактор: снижение рCO2 в крови. • Типичные направления изменений показателей КЩР (капиллярная кровь) при газовом алкалозе
|
