Патфиз ч.2. Патфиз ч. Гл. 11 Нарушения водного обмена Гл. 12 Нарушения ионного обмена
 Скачать 7.84 Mb. Скачать 7.84 Mb.
|
|
Дендритные клетки происходят из костного мозга и образуют популяцию долгоживущих клеток, которые запускают и модулируют иммунный ответ. В костном мозге их предшественники образуют субпопуляцию CD34+-клеток, которые способны дифференцироваться в клетки Лангерханса для эпителия и дендритные клетки для внутренней среды. Незрелые и неделящиеся предшественники дендритных клеток заселяют многие ткани и органы. Дифференцировку дендритных клеток поддерживают колониестимулирующий фактор гранулоцитов и макрофагов GMCSF и ИЛ3. Дендритные клетки имеют звёздчатую форму и в состоянии покоя несут на поверхности относительно небольшое количество молекул МНС. В отличие от клеток Лангерханса, интерстициальные дендритные клетки способны стимулировать синтез Ig Влимфоцитами. Все дендритные клетки могут вначале поступать в тимус-зависимую зону периферических лимфоидных органов, где созревают в так называемые интердигитирующие клетки. ВЗАИМОДЕЙСТВИЕ КЛЕТОК ПРИ ИММУННОМ ОТВЕТЕ Иммунный ответ возможен в результате активации клонов лимфоцитов и состоит из двух фаз. В первой фазе Аг активирует те лимфоциты, которые его распознают. Во второй (эффекторной) фазе эти лимфоциты координируют иммунный ответ, направленный на устранение Аг. ГУМОРАЛЬНЫЙ ИММУННЫЙ ОТВЕТ В гуморальном иммунном ответе эффекторными клетками являются В-лимфоциты. Регуляцию антителообразования осуществляют Т-хелперы и Т-супрессоры. Вторгшийся в организм Аг поглощается макрофагом и подвергается процессингу — расщеплению на фрагменты. Фрагменты Аг выставляются на поверхности клетки вместе с молекулой MHC. Комплекс «Аг–молекула MHC класса II» предъявляется Tхелперу (рис. 164). 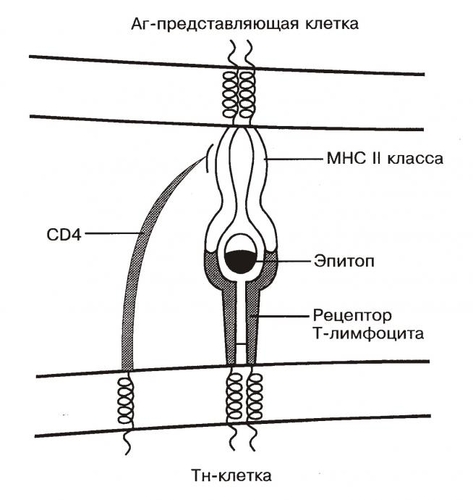 Рис. 164. Распознавание антигена рецептором Tлимфоцита. При помощи рецептора Т-лимфоцита Тклетка распознает Аг, но только находящийся в комплексе с молекулой MHC. В случае ТHклетки в процессе участвует её молекула — CD4, которая свободным концом связывается с молекулой MHC. Распознаваемый Тклеткой Аг имеет два участка: один взаимодействует с молекулой MHC, другой (эпитоп) связывается с рецептором Т-лимфоцита. Подобный тип взаимодействия, но с участием молекулы CD8, характерен для процесса распознавания TCлимфоцитом Аг, связанного с молекулой MHC класса I. TХЕЛПЕРЫ Tхелпер распознаёт комплекс «Аг–молекула MHC класса II» на поверхности антигенпредставляющей клетки (рис. 165). Для активации Тхелпера специфическое узнавание Тхелпером фрагмента Аг на поверхности антигенпредставляющей клетки оказывается недостаточным. Активацию Тхелперов обеспечивает взаимодействие молекулы В7 (расположена на поверхности антигенпредставляющей клетки) с молекулой CD28 на поверхности Тхелпера. Узнавание Тхелпером нужных молекул на поверхности антигенпредставляющей клетки стимулирует секрецию ИЛ1 (рис. 165). Активированный ИЛ1 Tхелпер синтезирует ИЛ2 и рецепторы ИЛ2, через которые агонист стимулирует пролиферацию Тхелперов и цитотоксических Tлимфоцитов. В случае Тхелпера речь идёт об аутокринной стимуляции, когда клетка реагирует на тот агент, который сама же синтезирует и секретирует. Таким образом, после взаимодействия с антигенпредставляющей клеткой Tхелпер приобретает способность отвечать на действие ИЛ2 всплеском пролиферации. Биологический смысл этого процесса состоит в накоплении такого количества Тхелперов, которое обеспечит образование в лимфоидных органах необходимого количества плазматических клеток, способных вырабатывать АТ против данного Аг. 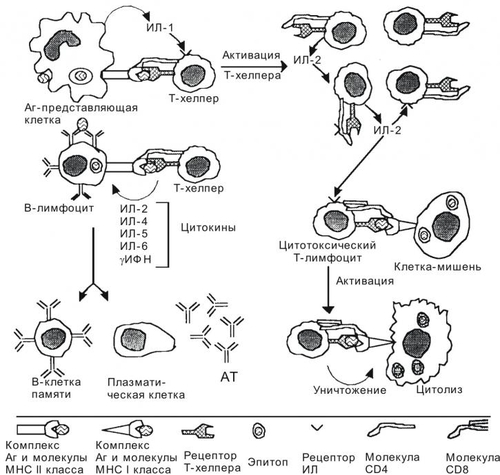 Рис. 165. Взаимодействие клеток при иммунном ответе. Рецептор Тхелпера распознаёт антигенную детерминанту (эпитоп) вместе с молекулой MHC класса II, выставленные на поверхности антигенпредставляющей клетки. В молекулярном взаимодействии участвует дифференцировочный Аг Тхелпера CD4. В результате подобного взаимодействия антигенпредставляющая клетка секретирует ИЛ1, стимулирующий в Тхелпере синтез и секрецию ИЛ2, а также синтез и встраивание в плазматическую мембрану того же Тхелпера рецепторов ИЛ2. ИЛ2 стимулирует пролиферацию Тхелперов и активирует цитотоксические Tлимфоциты. Отбор Влимфоцитов производится при взаимодействии Аг с Fabфрагментами IgM на поверхности этих клеток. Эпитоп этого Аг в комплексе с молекулой MHC класса II узнаёт рецептор Тхелпера, после чего из Tлимфоцита секретируются цитокины, стимулирующие пролиферацию Влимфоцитов и их дифференцировку в плазматические клетки, синтезирующие АТ против данного Аг. Рецептор цитотоксических Tлимфоцитов связывается с антигенной детерминантой в комплексе с молекулой MHC класса I на поверхности вирус-инфицированной или опухолевой клетки. В молекулярном взаимодействии участвует дифференцировочный Аг цитотоксического Tлимфоцита CD8. После связывания молекул взаимодействующих клеток цитотоксический Tлимфоцит убивает клетку–мишень. BЛИМФОЦИТЫ Активация Bлимфоцита (рис. 165) предполагает прямое взаимодействие Аг с Ig на поверхности Bклетки. В этом случае сам Bлимфоцит процессирует Аг и представляет его фрагмент в комплексе с молекулой MHC II на своей поверхности. Этот комплекс распознаёт Tхелпер, отобранный при помощи того же Аг. В активации Вклетки участвуют две пары молекул: с одной стороны, специфическое взаимодействие Аг с рецептором (IgM) на поверхности Влимфоцита, а с другой стороны, молекула CD40 на поверхности Вклетки взаимодействует с молекулой CD40L на поверхности Тхелпера, активирующего Вклетку. Узнавание рецептором Tхелпера комплекса «Аг–молекула MHC класса II» на поверхности Bлимфоцита приводит к секреции из Тхелпера ИЛ2, ИЛ4, ИЛ5 и ПЛАЗМАТИЧЕСКИЕ КЛЕТКИ Плазматическая клетка синтезирует Ig. ИЛ6, выделяемый активированными Тхелперами, стимулирует секрецию Ig. Часть зрелых Влимфоцитов после Аг-зависимой дифференцировки циркулирует в организме как клетки памяти. КЛЕТОЧНЫЙ ИММУННЫЙ ОТВЕТ В клеточном иммунном ответе эффекторными клетками являются цитотоксические Т-лимфоциты, активность которых регулируют Т-хелперы и Т-супрессоры. РЕАКЦИИ КЛЕТОЧНО-ОПОСРЕДОВАННОГО ЦИТОЛИЗА Эффекторные клетки при помощи своих рецепторов распознают клетку–мишень и уничтожают её. За клеточно-опосредованный цитолиз отвечают не только Т-лимфоциты, но и другие субпопуляции лимфоидных клеток, а в некоторых случаях миелоидные клетки. В процессе узнавания участвуют различные молекулы, выставленные на поверхности взаимодействующих клеточных партнеров: • специфические Аг (например, вирусные пептиды на поверхности инфицированных клеток) в комплексе с молекулой MHC распознаются рецепторами цитотоксических Тклеток, преимущественно CD8+-клеток и некоторыми субпопуляциями CD4+-клеток; • антигенные детерминанты опухолевых клеток распознаются NK-eлетками без участия молекулы MHC класса I; • связанные с Аг АТ на поверхности клеток–мишеней, распознаются рецепторами Fcфрагментов NK-eлеток (феномен АТ-зависимой цитотоксичности). ЦИТОТОКСИЧЕСКИЕ TЛИМФОЦИТЫ Предъявленный на поверхности клетки–мишени Аг в комплексе с молекулой MHC класса I связывается с рецептором цитотоксического Tлимфоцита (TC, рис. 165). В этом процессе участвует молекула CD8 клеточной мембраны TC. Секретируемый Tхелперами ИЛ2 стимулирует пролиферацию цитотоксических Tлимфоцитов. УНИЧТОЖЕНИЕ КЛЕТКИ–МИШЕНИ Цитотоксический Tлимфоцит раcпознаёт клетку–мишень и прикрепляетcя к ней. В цитоплазме активированного цитотоксического Tлимфоцита присутствуют мелкие тёмные органеллы, напоминающие запаcающие гранулы cекреторных клеток. Гранулы концентрируютcя в той чаcти Tкиллера, которая расположена ближе к меcту контакта c клеткой–мишенью. Параллельно проиcходят переориентация цитоcкелета и cмещение в эту облаcть комплекса Гольджи, в котором и формируютcя гранулы. В них содержится цитолитический белок перфорин. Выделяемые Tкиллером молекулы перфорина полимеризуютcя в мембране клетки–мишени в приcутcтвии Ca2+. Сформированные в плазматической мембране клетки–мишени перфориновые поры пропуcкают воду и cоли, но не молекулы белка. Еcли полимеризация перфорина произойдет во внеклеточном проcтранcтве или в крови, где в избытке имеетcя кальций, то полимер не cможет проникнуть в мембрану и уничтожить клетку. Cпецифическое дейcтвие Tкиллера проявляется только как результат тесного контакта между ним и клеткой–мишенью, который доcтигаетcя за cчёт взаимодейcтвия Аг на поверхноcти жертвы c рецепторами Tкиллера. Cам Tкиллер защищён от цитотокcичеcкого дейcтвия перфорина. НЕСПЕЦИФИЧЕСКАЯ ЗАЩИТА ОРГАНИЗМА Помимо иммунокомпетентных клеток, в реакциях обнаружения и устранения чужеродных молекулярных и клеточных структур участвуют также клеточные и гуморальные факторы (конституциональные факторы) системы неспецифической защиты организма (см. рис. 16–1). К ним относят фагоцитирующие клетки, факторы системы комплемента, кинины, ИФН, лизоцим, белки острой фазы и некоторые другие. Факторы неспецифической резистентности подразделяют на физические, химические и иммунобиологические. Основа первых — анатомические барьеры (кожа и слизистые оболочки). Они служат первой линией защиты против возбудителей инфекций. Строение, свойства, секреторные вещества физических и химических барьеров не позволяют микробам попасть во внутреннюю среду организма, часто убивая либо ингибируя их рост (табл. 16–1). Таблица 16–1. Некоторые конституциональные защитные барьеры
| |||||||||||||||||||||||||||||||||||||||||||||||||||
