Глик Молекулярная биотехнология. Глик Б., Пастернак Дж. Молекулярная биотехнология. Принципы и применение. Пер с англ. М. Мир, 2002. 589 с
 Скачать 9.74 Mb. Скачать 9.74 Mb.
|
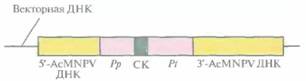
Системы экспрессии с использованием культур клеток насекомыхБакуловирусы инфицируют только беспозвоночных, в том числе многих насекомых. В ходе инфекционного процесса образуются две их формы. Одна представлена отдельными вирио-нами, которые высвобождаются из инфицированной клетки хозяина, как правило клетки средней кишки, и способны инфицировать другие клетки этого органа. Вторая состоит из множества вирионов, заключенных в белковый матрикс. Белок этого матрикса называется полиэдрином, а сама структура — полиэдроном. Синтез полиэдрина начинается через 36—48 ч после инфекции и продолжается 4—5 сут, пока зараженные клетки не лизируют и хозяйский организм не погибнет. После этого множество таких частиц высвобождается и попадает в среду, где от инактивации их защищает белковый 144 ГЛАВА 7 матрикс. Если восприимчивый хозяйский организм проглатывает такую частицу, то полиэдрин солюбилизируется и высвобождаются вирионы, способные инициировать новый инфекционный цикл. Промотор гена полиэдрина чрезвычайно сильный, а цикл развития вируса не зависит от наличия самого гена. Следовательно, замена последнего геном чужеродного белка с последующей инокуляцией полученным рекомбинантным бакуловирусом культуры клеток насекомого может привести к синтезу большого количества гетерологичного белка, который благодаря сходству систем внесения посттрансляционных модификаций у насекомых и млекопитающих будет близок (а возможно, и идентичен) к нативной форме того белка, который интересует исследователя. Исходя из этого на основе бакуловирусов были разработаны векторы для экспрессии генов, кодирующих белки млекопитающих и вирусов животных. Наиболее широко используется вирус множественного ядерного полиэдроза Autographacalifornica(AcMNPV). Этот бакуловирус инфицирует более 30 других видов насекомых, а также хорошо растет в культуре многих клеточных линий. Линии клеток, обычно использующиеся для работы с рекомбинантным AcMNPV, получают из гусениц Spodopterafrugiperda. Промотор полиэдрина в этих клетках чрезвычайно активен, и при их заражении бакуловирусом дикого типа синтезируются большие количества белка. Система экспрессирующих векторов на основе бакуловирусовПервый шаг в конструировании рекомбинантного бакуловируса AcMNPV состоит в создании транспортного вектора. Транспортный вектор - это производная плазмиды E. coli, содержащая фрагмент ДНК AcMNPV (рис. 7.8), который включает: 1) промоторную область и расположенную перед ней последовательность ДНК AcMNPV, необходимую для гомологичной рекомбинации с AcMNPV; 2) сайт для клонирования; 3) сайт терминации-полиаденилирования гена полиэдрина и прилегающую к нему последовательность ДНК AcMNPV — вторую область, обеспечивающую гомологичную рекомбинацию с AcMNPV (рис. 7.8). Кодирующая последовательность гена полиэдри-
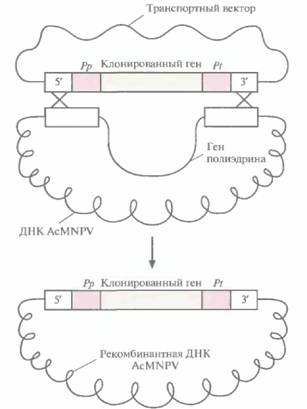
на из этого фрагмента удалена. Интересующий исследователя ген встраивают между промотором и сигналом терминации гена полиэдрина и вводят конструкцию в Е. соli. Культуру клеток насекомого, трансфицированную ДНК AcMNPV, трансфицируют затем транспортным вектором, несущим клонированный ген. В некоторых дважды трансфицированных клетках происходит двойной кроссинговер, в результате которого клонированный ген вместе с промотором и сигналом терминации транскрипции гена полиэдрина встраивается в ДНК AcMNPV (рис. 7.9), замещая ген полиэдрина. Вирионы, не содержащие этого гена, образуют зоны клеточного лизиса, из которых можно выделить рекомбинантный бакуловирус. Визуальная идентификация зон лизиса — утомительная и субъективная процедура. Вместо нее для обнаружения рекомбинантных бакуловирусов можно использовать ДНК-гибридизацию или полимеразную цепную реакцию (ПЦР). Кроме того, если под контроль промотора бакуловируса, активного с ранних и до поздних стадии литического цикла, поместить ген lacZ E. coli., кодирующий ß-галактозидазу, и такую конструкцию включить во фрагмент ДНК, встраивающийся в геном AcMNPV, то в присутствии хромогенного субстрата ß-галактозидазы зоны с рекомбинантными вирусами окрасятся в синий цвет. Гетерологичный белок, синтезируемый культурой клеток насекомого-хозяина, зараженной Получение рекомбинантных белков с помощью эукариотических систем 145
рекомбинантным бакуловирусом, можно выделять через 4—5 сут. С помощью системы экспрессирующих векторов на основе бакуловирусов уже получено более 500 различных гетерологичных белков, при этом более 95% из них имели правильные посттрансляционные модификации (рис. 7.10). Получение рекомбинантных бакуловирусовИсходная методика получения рекомбинантных бакуловирусов в дальнейшем была изменена по ряду причин. Во-первых, применение промотора гена полиэдрина имеет ограничения: белки, синтезирующиеся на поздней стадии литического цикла, часто оказываются модифицированными не до конца. Для решения этой проблемы промотор гена полиэдрина заменили одним из сильных промоторов AcMNPV, активно функционирующих с самого начала и до конца литического цикла. Во-вторых, линеаризация генома AcMNPV перед трансфекцией клеток насекомого увеличивает долю зон лизиса с реком-бинантными вирусами. Расщепление генома AcMNPV в одном сайте уменьшает число зон с нерекомбинантными вирусами, потому что линеаризованные геномы бакуловирусов обладают ограниченной инфицирующей способностью. В результате двойного кроссинговера между линеаризованной ДНК AcMNPV и кольцевым транспортным вектором образуется замкнутая кольцевая молекула, которая обладает инфицирующей способностью. Чтобы обеспечить стабильную линеаризацию в каждом эксперименте, в геном AcMNPV дикого типа в ген полиэдрина встроили уникальный сайт для рестриктазы Bsu361. В результате доля зон лизиса с рекомбинантными бакуловирусами увеличилась с <1% (когда использовались нерасщепленные кольцевые молекулы AcMNPV) до примерно 30%.
146 ГЛАВА 7
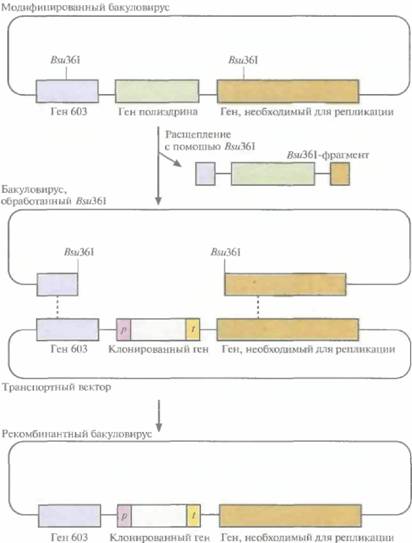
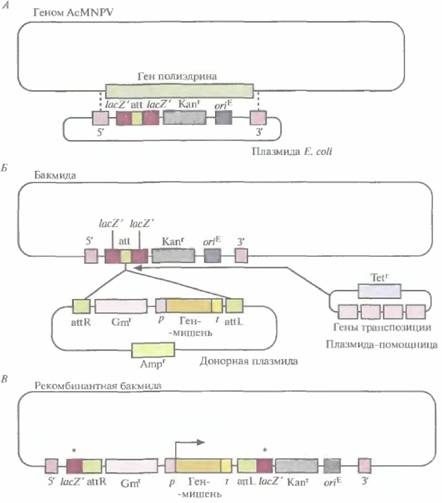
Bsu361-систему линеаризации далее модифицировали так, чтобы получить сверхвысокую частоту рекомбинантных бакуловирусов. Для этого в геном AcMNPV внесли два BsuЗб1-сайта, по одному с каждой стороны гена полиэдрина (рис. 7.11). Один сайт находился в гене 603 (открытая рамка считывания 603 [ORF603]), а второй — в одном из генов (ORF 1629), необходимых для репликации вирусной ДНК. При трансфек-ции клеток насекомого с помощью ДНК модифицированного бакуловируса, инкубированного с Bsu361, репликация вируса не происходила, поскольку отсутствовал фрагмент необходимого для этого гена (ORF1629). Далее был создан транспортный вектор, содержащий ген-мишень и, если это нужно, селективный маркерный ген между интактной копией гена 603 и необходимым для репликации геном. Таким вектором трансфицировали клетки насекомого, которые были предварительно трансфицированы линеаризованной ДНК AcMNPV с делецией участка между Bsu361-сайтами. В результате двойного кроссинювера постанавливалась функциональная форма ORF 1629 и происходило включение клонированного гена в геном AcMNPV (рис. 7.11). С помощью этой системы доля зон лизиса, содержащих рекомбинантные бакуловирусы, была увеличена до 99%. Создание челночного вектора на основе бакуловирусов для E. coli и клеток насекомыхРазработана система, позволяющая осуществлять все генноинженерные манипуляции по созданию экспрессирующего вектора на основе бакуловируса в Е. соli. При этом трансфекция клеток насекомого нужна только для синтеза рекомбинантного белка. В системе используется фрагмент небольшой плазмиды E. coli, фланкированный участками ДНК, расположенными с 5'- и 3’-концов гена полиэдрина. Он содержит ген устойчивости к канамицину, нуклеотидную последовательность, играющую роль сайта интеграции и встроенную в ген lacZ–без нарушения его функции, и сайт инициации репликации, активный в E. coli. Интеграция плазмиды в геном AcMNPV происходит в результате двойного кроссинговера и сопровождается элиминацией гена полиэдрина (рис. 7.12, А). При этом образуется кольцевая ДНК, способная сущест- Получение рекомбинантных белков с помощью эукариотических систем 147
вовать в E, coli как плазмида и ответственная за образование в трансфицированных клетках насекомого бакуловирусов. Челночные векторы на основе бакуловирусов для E. coli и клеток насекомых называют бакмидами. Система на основе бакмид позволяет создать еще одну плазмиду E. coli, в которой между промотором и сайтом терминации гена полиэдрина встроен ген-мишень (плазмида-донор). В донорной плазмиде ген устойчивости к гентамицину и единица экспрессии гена-мишени фланкированы нуклеотидными последовательностями, которые связываются с сайтом интеграции в бакмиде, а ген устойчивости к ампициллину находится вне двух сайтов встраивания (рис. 7.12, Б). Рекомбинация между соответствующими сайтами в донорной плазмиде и бакмиде может происходить только в присутствии специфичных белков (белков транспозиции), которые в этой системе кодируются третьей плазмидой E. coli (плазмидой-помощницей), несущей еще и ген устойчивости к тетрациклину (рис. 7.12, Б). Бактериальные клетки, несущие бакмиду, трансформируют одновременно плазмидой-по- 148 ГЛАВА 7 мощницей и донорной плазмидой. В некоторых двойных трансформантах фрагмент ДНК, ограниченный двумя сайтами интеграции, встраивается в сайт интеграции бакмиды (рис. 7.12, Б и В). Встраивание фрагмента донорной плазмиды с единицей экспрессии и геном устойчивости к гентамицину в сайт интеграции бакмиды нарушает рамку считывания гена lacZ'. В результате бактерии, несущие рекомбинантные (со встройкой) бакмиды, образуют белые колонии в присутствии изопропил-β-D-тиогалактопиранозида (ИПТГ) и 5-бром-4-хлор-3-индолил-β-D-галак-
Получение рекомбинантных белков с помощью эукариотических систем 149 топиранозида (X-Gal). Te из них, которые устойчивы к канамицину и чувствительны к ампициллину и тетрациклину, несут только рекомбинантную бакмиду, но не донорную плазмиду и плазмиду-помощницу. В наличии вставки клонированного гена после всех этих манипуляций можно убедиться при помощи ПЦР. Далее рекомбинантной бакмидой можно трансфицировать клетки насекомого, в которых произойдет транскрипция клонированного гена и синтез рекомбинантного белка. Для создания экспрессирующих векторов на основе бакуловирусов использовались и другие подходы. Один из них предполагал проведение всех генноинженерных манипуляций с геномом AcMNPV в дрожжевых клетках с использованием челночного вектора для дрожжей и клеток насекомых с последующим введением рекомбинантного бакуловируса в клетки насекомого. В другом для создания конструкции «клонированный ген—геном AcMNPV» использовали систему рекомбинации in vitro, основанную на вырезании—встраивании ДНК бактериофага Р1, после чего такой конструкцией напрямую трансфицировали клетки насекомого. Выделение рекомбинантного белка из клеток насекомых с помощью аффинного связыванияДля выделения специфических гетерологичных белков из клеточных экстрактов и из смесей секретируемых белков можно использовать разные подходы. Один из них основывается на присоединении к клонированному гену - без нарушения рамки считывания — сегмента ДНК, кодирующего короткую аминокислотную последовательность, которая специфически связывается с каким-либо химическим элементом, соединением или макромолекулой. Такую конструкцию встраивают в экспрессирующий вектор между промотором и сайтом терминации транскрипции. Короткая аминокислотная последовательность в составе рекомбинантного белка, синтезируемого в хозяйской клетке, играет роль аффинной метки. В одном случае перед клонированным геном был встроен - без нарушения рамки считывания -- сегмент ДНК, кодирующий шесть остатков гистидина (His6), спейсерный участок, кодирующий семь аминокислот, и сайт расщепления протеиназы из шести аминокислот; получившийся рекомбинантный белок выделяли хроматографией на колонке с никель-агарозой. Последовательность из шести остатков гистидина (гексагистидин) связывалась с ионами никеля, и рекомбинантный белок задерживался в колонке. Его элюировали добавлением конкурирующего соединения (например, имидазола), который вытеснял гексагистидин рекомбинантного белка из комплекса с ионами никеля, или понижением pH буфера для элюиии. Аффинную метку отщепляли с помощью протеолитического фермента (протеиназы) и очищали рекомбинантный белок от нее и от протеиназы хроматографи-ческими методами. Если рекомбинантный белок не предполагается использовать в медицинских целях, можно и не отщеплять гексагистидиновую последовательность, поскольку обычно она не влияет на структуру и функцию белка. Было разработано несколько аффинных меток. Среди них — глутатионтрансфераза, белок, связывающий мальтозу, и короткие аминокислотные последовательности — антигенные детерминанты, которые связываются соответственно с глутатионом, мальтозой и специфическими антителами. Использовали и разные сайты расщепления, специфичные для тромбина, энтерокина-зы и других протеиназ. Аффинная метка и сайт расщепления могут находиться как на N-, так и на С-конце рекомбинантного белка и использоваться в прокариотических системах экспрессии, а также в системах экспрессии на основе клеток насекомых, млекопитающих или грибов. Экспрессирующие векторы для работы с клетками млекопитающихВнехромосомные экспресс ирующие векторы млекопитающих используются для изучения функций и регуляции генов млекопитающих. Кроме того, с их помощью могут быть получены аутентичные рекомбинантные белки, которые потенциально могут использоваться в медицинских целях для лечения некоторых заболеваний человека. Уже сконструированные экспрессирующие векторы млекопитающих весьма многочисленны, но все они обладают сходными свойствами и похожи на другие эукариотические экспрессирующие векторы. 150 Глава 7
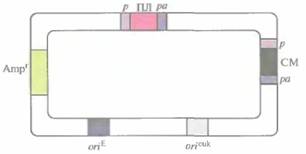
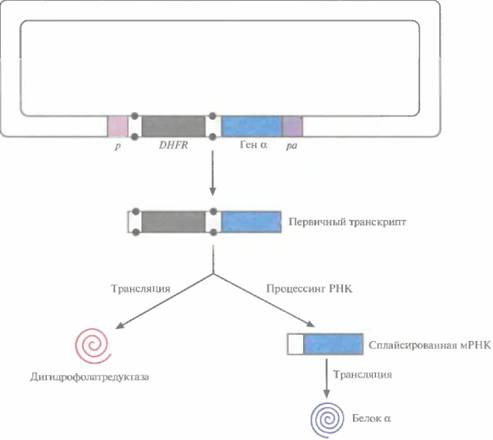
Вектор, представленный на рис. 7.13, содержит эукариотический сайт инициации репликации вируса животных (например, обезьяньего вируса 40 [SV40]). Промоторы клонированного и селективного маркерного генов, а также их сигналы терминации транскрипции (сигналы полиаденилирования) должны происходить из клеток эукариот; обычно используют регуляторные последовательности ДНК вирусов животных (например, цитомегаловируса человека, SV40 или HSV) или генов млекопитающих (например, гена ß-актина, металлотионеина, тимидинкиназы или бычьего гормона роста). При этом более предпочтительны сильные промоторы и эффективные сигналы полиаденилирования. Последовательности, необходимые для отбора и амплификации экспрессирующего вектора млекопитающих в E. coli, происходят из стандартного клонирующего вектора E. coli (например, плазмиды pBR322). Селективные маркерные геныДля отбора трансфицированных клеток млекопитающих часто используют бактериальный ген Neor, кодирующий неомицинфосфотрансферазу. В этой системе применяется токсичное соединение генетицин (G-418), блокирующее трансляцию в нетрансфицированных клетках млекопитающих. При этом в трансфицирован- ных клетках G-418 фосфорилируется неомицинфосфотрансферазой и инактивируется. Следовательно, выживают и пролиферируют только клетки, синтезирующие продукт гена Neor. Другая система отбора трансфицированных клеток млекопитающих основана на использовании гена, кодирующего фермент дигидрофолатредуктазу (DHFR). В этой системе используют клетки с дефектным геном DHFR, т. е. клетки, в которых функциональная DHFR не синтезируется. После трансфекции DНFR–-клеток экспрессирующим вектором млекопитающих с функционирующим DHFR-геномв среду добавляют метотрексат. Не трансфицированные клетки не растут в его присутствии, а клетки, синтезирующие дигидрофолатредуктазу, выживают. После предварительного отбора клеток с DHFR-геномконцентрацию метотрексата в среде увеличивают и отбирают клетки с большим числом копий вектора, синтезирующие в большом количестве рекомбинантный белок. Разработаны и другие схемы отбора с доминантным маркером, например с использованием фермента глутаминсинтетазы (GS), обеспечивающей устойчивость к цитотоксическому действию метионинсульфоксимина. В этой системе применяется вектор, несущий GS-ген. Его вводят в культуру клеток млекопитающих и для отбора клеток, несущих большое количество копий вектора, повышают концентрацию метионинсульфоксимина в среде. При этом в хозяйских клетках тоже должна присутствовать GS, поскольку только множественные копии GS-гена могут обеспечивать устойчивость к метионинсульфоксимину. Такая схема обладает определенными преимуществами перед описанной выше. В экспрессирующие векторы млекопитающих уже встроены гены самых разных белков и осуществлена их экспрессия в хозяйских клетках. Иногда выход продукта увеличивался, если между промотором и клонированным геном встраивали интрон. Механизм этого феномена неизвестен. Возможно, первичный транскрипт клонированного гена содержит скрытые сайты сплайсинга, по которым вырезается часть кодирующей области клонированного гена, а при наличии дополнительного интрона сплайсинг по ним происходит с меньшей вероятностью. Получение рекомбинантных белков с помощью эукариотических систем 151 Высокий уровень экспрессии клонированного гена достигался при ее координации с экспрессией селективного маркерного гена, Для этого, например, ген DHFRвстраивали поблизости от клонированного гена, так чтобы оба гена находились под контролем одного промотора и имели общий сигнал полиаденилирования, а ген DHFRбылфланкирован сайтами сплайсинга интрона. DHFR и рекомбинантный белок, транслировались с первичного транскрипта и сплайсированной мРНК соответственно (рис. 7.14). Экспрессия двух клонированных генов в одной клетке млекопитающихНекоторые ценные в коммерческом отношении белки в активной форме состоят из разных полипептидных цепей. Например, тиреотропный гормон человека — это гетеродимер, а гемоглобин — тетрамер, состоящий из двух субъединиц, по две копии каждая (α2β2). Чтобы получить активный мультимерный белок, можно попытаться клонировать ген или кДНК каждой из субъединиц, синтезировать и очистить
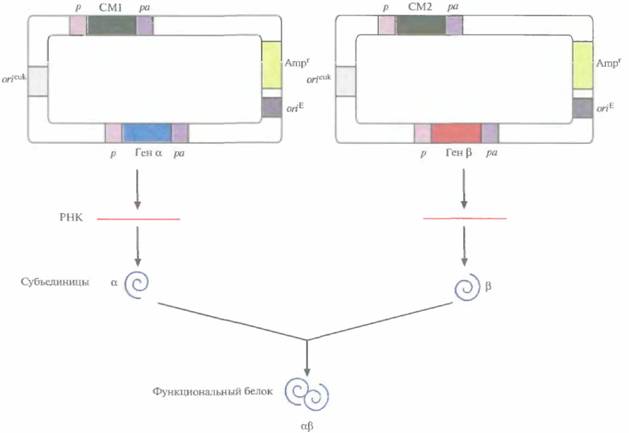
152 Глава 7 субъединицы, а затем смешать их в пробирке. Однако таким образом удается получить лишь немногие мультимерные белки, поскольку in vitro правильная укладка полипептидных цепей осуществляется редко. Сборка же димерных и тетрамерных белков in vivo протекает весьма эффективно. Поэтому были разработаны стратегии синтеза двух разных рекомбинантных белков в одной клетке. Для этого хозяйские клетки одновременно трансфицировали двумя экспрессирующими векторами млекопитающих, каждый из которых нес ген или кДНК одной из субъединиц и разные гены селективных маркеров (рис. 7.15). Трансфицированные клетки подвергали двойному отбору, соответственно и выжившие клетки несли оба вектора. Системы с двумя векторами успешно использовались для синтеза аутентичных димерных и тетрамерных рекомбинантных белков. К сожалению, дважды Трансфицированные клетки часто утрачивают один из двух векторов. Кроме того, число копий каждого из векторов не всегда одинаково, так что одна субъединица может синтезиро-
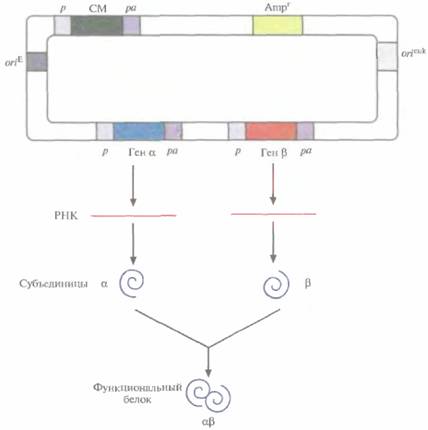
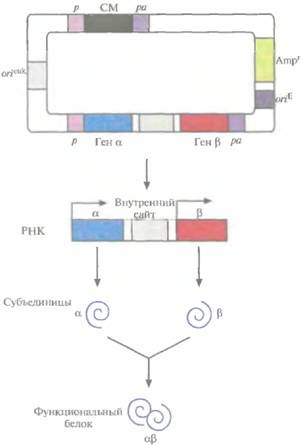
Получение рекомбинантных белков с помощью эукариотических систем 153 ваться в большем количестве, чем другая, и выход конечного продукта может снижаться. Чтобы решить эти проблемы, были сконструированы векторы, содержащие оба клонированных гена. В некоторых случаях они были помещены под контроль независимых промоторов и сигналов пол над енилирования (рис. 7.16). А для того чтобы гарантировать синтез рекомбинантных белков в одинаковом количестве, были созданы так называемые двухцистронные векторы, в которых клонированные гены разделялись сегментом ДНК, содержащим внутренний сайт связывания рибосом. Такие сайты были обнаружены в геномах вирусов млекопитающих; они обеспечивают одновременную трансляцию различных белков с полицистронной мРНК. Транскрипция конструкции «ген—внутренний сайт связывания рибосом—ген» регулируется одним промотором и одним сигналом полиаденилирования. Синтезируется один транскрипт с двумя генами, трансляция начинается с 5'-конца мРНК и с внутреннего сайта, в результате синтезируются субъединицы димерного белка α и β (рис. 7.17). Суммируя, можно сказать, что экспрессирующие векторы млекопитающих столь же универсальны и эффективны, как и векторы для других эукариотических систем экспрессии, если речь идет о получении аутентичных рекомбинантных белков для исследовательских и медицинских целей. Однако промышленный синтез рекомбинантных белков с использованием модифицированных клеток млекопитающих обходится слишком дорого. В этом случае предпочтительны менее дорогие системы экспрессии, за исключением тех ситуаций, когда
154 ГЛАВА 7 аутентичности рекомбинантного белка удается достичь только с помощью культуры клеток млекопитающих.
Прокариотические системы экспрессии успешно используются для синтеза многих белков. Однако некоторые белки для превращения в активную форму должны претерпеть специфические посттрансляционные модификации — гликозилирование, фосфорилирование или ацетилирование, а бактерии к этому не способны. Поэтому было решено попытаться экспрессировать клонированные гены в эукариотических клетках с помощью специально созданных эукариотических экспрессирующих векторов. Для синтеза разнообразных белков, кодируемых клонированными генами, использовались дрожжи S. cerevisiae. Их генетика хорошо изучена, а кроме того, их можно выращивать в больших ферментерах. Чтобы упростить очистку белков, были сконструированы векторы, обеспечивающие их секрецию. С помощью 5. cerevisiaeбыло получено множество самых разных аутентичных белков. Однако многие рекомбинантные белки в этой системе не подвергались посттрансляционной модификации, к тому же их выход зачастую был недостаточно высок. Поэтому были предприняты попытки разработать другие дрожжевые системы синтеза рекомбинантных белков. В поисках других эукариотических систем экспрессии, с помощью которых можно было бы получать биологически активные белки, исследователи сосредоточили усилия на создании экспрессирующих векторов на основе бакуловирусов, в частности бакуловируса AcMNPV, инфицирующего клетки многих насекомых. Исходная стратегия предполагала трансфекцию клеток насекомого, зараженных AcMNPV, транспортным вектором, который содержал клонированный ген, фланкированный AcMNPV-специфичными последовательностями. В результате двойного кроссинговера между вектором и геном AcMNPV клонированный ген встраивался в последний и попадал под контроль сильного промотора, функционирующего на последних стадиях логического цикла. Клетки насекомого, инфицированные рекомбинантным бакуловирусом, синтезировали гетерологичный белок. Получение рекомбинантных белков с помощью эукариотических систем 155 Частоту появления рекомбинантных бакуловирусов удалось повысить с менее чем 1% до 99%. Для этого ДНК AcMNPV обрабатывали эндонуклеазой рестрикции, которая расщепляла ДНК в двух специфичных сайтах с высвобождением фрагмента, несущего часть гена, необходимого для осуществления литического цикла. Клетки насекомого трансфицировали этим фрагментом, а затем — транспортным вектором, В результате двойного кроссинговера в некоторых клетках восстанавливался кольцевой геном AcMNPV, который содержал клонированный ген и функциональный ген, необходимый для осуществления литического цикла. В результате почти все вирулентные бакуловирусы оказывались рекомбинантными. Следующий шаг в усовершенствовании системы экспрессии на основе бакуловирусов состоял в создании бакмиды, челночного вектора Е. соli/клетки насекомого, позволяющего проводить все генноинженерные манипуляции в Е. coll. Клетки насекомого трансфицировали рекомбинантной бакмидой только с целью получения гетерологичного белка. Примерно 95% гетерологичных белков, синтезированных в системах экспрессии на основе бакуловирусов, имели соответствующие посттрансляционные модификации. Внехромосомные экспрессирующие векторы млекопитающих обычно применяют для синтеза гетерологичных белков, использующихся в научных или медицинских целях. Они представляют собой челночные векторы с сайтами инициации репликации вируса животных и Е. соli-плазмиды, Регуляторные элементы транскрипции обычно происходят из генома вируса животных или из геномов млекопитающих. Для отбора трансфицированных клеток используют доминантные селективные маркерные гены. Некоторые системы отбора основаны на введении в среду возрастающего количества цитотоксичного соединения и позволяют получать клетки, содержащие большое число копий вектора, что увеличивает выход чужеродного белка. Разработаны системы экспрессии млекопитающих, позволяющие получать белки, состоящие из двух разных субъединиц. Для этого хо- зяйские клетки трансфицировали сразу двумя векторами, каждый из которых нес ген одной из субъединиц. Альтернативный подход состоял в использовании одного вектора, который нес эти два гена в виде отдельных единиц транскрипции или в виде одного транскриптона, содержащего оба этих гена. ЛИТЕРАТУРАCockett M. I., С. R. Beddington, G. T. Yarranton. 1990. High level expression of tissue inhibitor or metalloproteinases in Chinese hamster ovary cells using glutamine synthetase gene amplification. Bio/Technology 8: 662-667. Cole E. S., K. Lee, K. Lau/iere, C. Kelton, S. Chappel, B. Weintraub, I). Ferrara, F. Peterson, R. Bernasconi, T. Edmunds, S. Richards, L. Dickrell, I. M. Kleeman, J. II. McPhersun, B. M. Pratt. 19УЗ. Recombinanl human thyroid stimulating hormone: development of a biotechnology product for detection of metasla tic lesions of thyroid carcinoma. Bio/Technology 11: 1014-1024. Cregg J. M., J. F. Tschopp, C. Stillman, R. Siegel, M. Akong, W. S. Craig, R. G. Buckhnl/, К. R. Madden, P. A. Kellaris, G. R. Davis, B. L. Smiley, J. Cruzc, R. Torregrossa, G. Veiicclebi, G. P. Thill. 1987. High-level expression and efficient assembly of hepatitis В surface antigen in the methylotrophic yeast, Pichla pastoris. Bio/Technology 5: 479-485. Davîes A. H. 1994, Current methods for manipulating baculovirus, Bio/Technology 12: 47—50. Digan M. E., S. V. Lair, R. A. Brieriey, R. S. Siegel, M. E. Williams, S. B. Ellis, P. A. Kellaris, S. A. Provow, W. S. Craig, G. Velicelebi, M. M. Harpold, G. P. ThiU. 1989. Continuous production of a novel lysozyme via secretion from the yeast, Pichia pastoris. Bio/Technology 7: 160-164. Dirks W., M. Wirth, H. Hauser. 1993. Dicistronic transcription units lor gent expression in mammalian cells. Gene 128: 247-24'λ Gellissen G., Z. A. Janowicz, U. Weydemann, K. Melber, A. W. M. Strasser, C. P. Hollenberg. 1992, High-level expression of foreign genes in 156 ГЛАВА 7 Hansenula polymorpha. Bioiechnol. Adv. 10: 179-189, Giga-Hama Y., H. Tohda, H. Okada, M. K. Owada, H. Okayama, II. Kumagai. 1994. High-level expression of human lipocortin I in the fission yeast Schizosaccharomyces pombe using a novel expression vector. Bio/Technology 12: 400-404. Gilbert S. C., H. van Urk, A. J. Greenfield, M. J. McAvoy, K. A. Denton, D. Coghlan, G. D. Jones, D. J. Mead. 1994. Increase in copy number of an integrated vector during continuous culture of Hansenula polymorpha expressing functional human hemoglobin. Yeast 10: 1569-1580. The Global Use of Strategies to Open Occluded Arteries (GUSTO) lib Investigators. 1996. A comparison of recombinant hirudin with heparin for the treatment of acute coronary syndromes. N. Engl. J. Med. 335: 775-782. Hallewell R. Α., R. Mills, P. Tekamp-OLson, R. Blacher, S. Rosenberg, F. Otting, F. R. Masiarz, C. J. Scandella. 1987. Amino terminal acetyla-tion of authentic human Cu, Zn Superoxide dis-mutase produced in yeast. Bio/Technology 5: 363-366. Kidd L M., V. C. Emery. 1993. The use of baculoviruses as expression vectors. Appl. Biochem. Biotechnol. 42: 137-159. Kitts P. A., R. D. Possee. 1993. A method for producing recombinant baculovirus expression vectors at high frequency. BioTechniques 14: 810-817. Laroche Y., V. Strome, J. DeMeutter, J. Messens, M. Lauwereys. 1994. High-level secretion and very efficient isotopic labeling of tick anticoagulant peptide (TAP) expressed in the methylotrophic yeast, Picftia postons. Bio/Technology 12: 1119-1124. Loison G., A. Findeli, S. Bernard, M. Nguyen-Juilleret, M. Marquet, N. Riehl-Bellon, D. Carvallo, L. Guerra-Santos, S. W. Brown, M. Courtney, C. Roitsch, Y. Lemoine. 1988. Expression and secretion in S. cerevisiae of biologically active leech hirudin. Bio/Technology 6: 72-77. Lucas B. K., L. M. Giere, R, A. DeMarco, A. Shen, V. Chisholm, C. W. Crowley. 1996. High-level production of recombinant proteins in CHO cells using a dicistronic DHFR intron expression vector. Nucleic Acids Res. 24: 1774-1779. Lucknow V. A., S. C. L«e, G. F. Barry, P. O. Olins. 1993, Efficient generation of infectious recombinant baculoviruses by site-specific transposon-mediated insertioin of foreign genes into a baculovirus genome propagated in Eschericia coli. J. VIrol. 67: 4566-4579. Peng S., M. SommtrFelt, J. Logan, Z. Huang, T. Jilling, K. Kirk, E. Hunter, E. Sorscher. 1993. One-step affinity isolation of recombinant protein using the baculovirus/insect expression system. Protein Expr. Purif. 4: 95-100. Robinson A. S., V. Hines, K. D. Wittrup. 1994. Protein disulfide isomerase overexpression increases secretion of foreign proteins in Saccharomyces cerevisiae. Bio/Technology 12: 381-384, Romanes Μ. Α., C. A. Scorer, J. J. Clare. 1992, Foreign gene expression in yeast: a review. Yeast 8: 423-488. Vozza L. A., L. Wittmer, D. R. Higgins, T. J. Purcell, M. Bergseid, L. A. Collins-Racie, E. R. LaVaUie, J. P. Hoeffler. 1996, Production of a recombi-rtant bovine enterokinase catalytic subunit in the methylotrophic yeast, Pichia pastoris. Bio/ Technology14: 77-81. КОНТРОЛЬНЫЕ ВОПРОСЫ1. Почему для получения белков, использующихся в медицине, лучше применять эукариотические, а не прокариотические системы? 2. Какие достоинства и недостатки имеют различные типы дрожжевых векторов, предназначенных для получения данного рекомбинантного продукта? 3. Опишите основные свойства интегративной векторной системы P. pastoris, обладающей высоким уровнем экспрессии, 4. Что такое бакуловирусы? Опишите исходную систему экспрессии на основе ба-куловирусов и ее последующие модификации. 5. Что такое бакмида? Для чего ее используют? Получение рекомбинантных белков с помощью эукариотических систем 157 6. Что такое аффинная метка? Для чего ее используют? 7. Опишите основные свойства внехромосомного экспрессирующего вектора млекопитающих. 8. Опишите как минимум две селективные системы, использующиеся в случае экспрессирующих векторов млекопитающих. 9. Опишите разные подходы к созданию систем синтеза двух рекомбинантных белков в одной клетке млекопитающего. 10. Какими критериями руководствуются при выборе системы экспрессии генов гетерологичных белков (дрожжи, система экспрессии на основе бакуловирусов, клетки млекопитающих)? | |||||||||||||||||||||||||||||