Глик Молекулярная биотехнология. Глик Б., Пастернак Дж. Молекулярная биотехнология. Принципы и применение. Пер с англ. М. Мир, 2002. 589 с
 Скачать 9.74 Mb. Скачать 9.74 Mb.
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
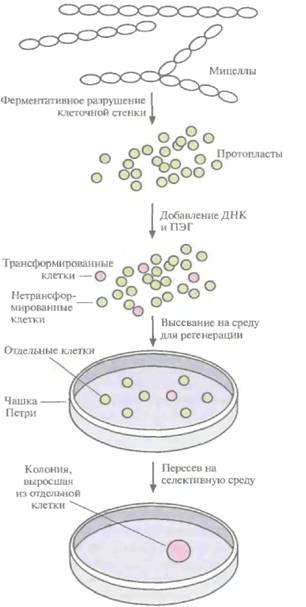 | Рис. 12.9. Схема трансформации и отбора рекомбинантных штаммов Sireptvmycea. Tрансформированные клетки обозначены розовыми кружками, нетрансформированные — зелеными. ПЭГ — полиэтиленгликоль. |
Использование рекомбинантных микроорганизмов для получения коммерческих продуктов 259
Клонирование генов биосинтеза антибиотиков
Процесс биосинтеза одного антибиотика может состоять из 10—30 ферментативных реакций, так что клонирование всех генов его биосинтеза -задача не из легких. Один из подходов к выделению полного набора таких генов основан на трансформации одного или нескольких мутантных штаммов, не способных синтезировать данный антибиотик, банком клонов, созданным из хромосомной ДНК. штамма дикого типа. После введения банка клонов в мутантные клетки проводят отбор трансформантов, способных синтезировать антибиотик. Затем выделяют плазмидную ДНК клона, содержащего функциональный экспрессируюшийся ген антибиотика [т. е. ген, восстанавливающий (комплементирующий) утраченную мутантным штаммом функцию], и используют ее в качестве зонда для скрининга другого банка клонов хромосомной ДНК штамма дикого типа, из которого отбирают клоны, содержащие нуклеотидные последовательности, которые перекрываются с последовательностью зонда. Таким образом идентифицируют, а затем клонируют элементы ДНК, примыкающие к комплементирующей последовательности, и воссоздают полный кластер генов биосинтеза антибиотика. Описанная процедура относится к случаю, когда эти гены сгруппированы в одном сайте хромосомной ДНК. Если же гены биосинтеза разбросаны в виде небольших кластеров по разным сайтам, то нужно иметь по крайней мере по одному мутанту на кластер, чтобы получить клоны ДНК, с помощью которых можно идентифицировать остальные гены кластеров.
Этот подход с успехом использовался для идентификации некоторых генов биосинтеза ундецилпродигиозина из StreptomycescoelicolorA3 (рис. 12.10), В этом случае комплементационный анализ основывается на сравнении цвета колоний: колонии микроорганизмов дикого типа имеют красный цвет, а колонии мутантных микроорганизмов — кремовый. Таким образом, в результате комплементации образуется красная колония.
Помимо комплементации, для идентификации генов биосинтеза антибиотиков могут использоваться и более прямые подходы. Так, с
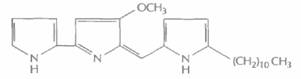 |
| Рис. 12.10. Структурная формула ундецилпродигиозина. |
помощью генетических или биохимических экспериментов можно идентифицировать, а затем выделить один или несколько ключевых ферментов биосинтеза, определить их N-концевые аминокислотные последовательности и, исходя из этих данных, синтезировать олигонуклеотидные зонды. Этот подход использовался для выделения из Pénicillium chrysogenutn гена синтетазы изопенициллина N. Этот фермент катализирует окислительную конденсацию δ-(L-α-аминоадипил)-L-цистеинил-D-валина в изопенициллин N, ключевое промежуточное звено в биосинтезе пенициллинов, цефалоспоринов и цефамицинов (рис. 12.11 ).
Синтез новых антибиотиков
Новые антибиотики с уникальными свойствами и специфичностью можно получить, проводя генноинженерные манипуляции с генами, участвующими в биосинтезе уже известных антибиотиков. Один из первых экспериментов, в ходе которого был получен новый антибиотик, состоял в объединении в одном микроорганизме двух немного различающихся путей биосинтеза антибиотика.
Одна из плазмид Streptomyces, рIJ2303, несущая фрагмент хромосомной ДНК S. coelicolor длиной 32,5 т.п.н., содержит все гены ферментов, ответственных за биосинтез из ацетата антибиотика актинородина, представителя семейства изохроманхиноновых антибиотиков (рис. 12.12). Целую плазмиду и различные субклоны, несущие части 32,5 т.п.н.-фрагмента (например, рIJ2315), вводили либо в штамм АМ-7161 Streptomyces sp., синтезиурующий родственный антибиотик медермицин, либо в штамм В1140 или Tü22 S. violaceoruber, синтезирующие родственные антибиотики гранатицин и дигидрогранатицин.
Все указанные антибиотики являются кислотно-щелочными индикаторами, которые при-
260 ГЛАВА 12
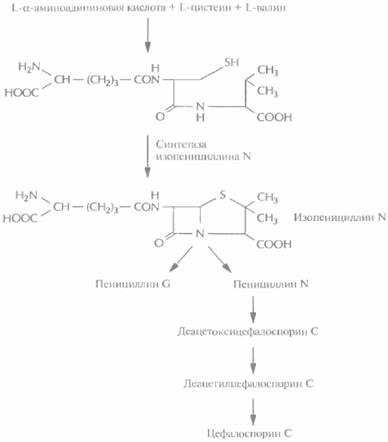 | Рис. 12.11. Биосинтез ленициллинов и цефалоспоринов в P. chrysogenum. Синтетаза изопенициллина N катализирует синтез из δ-(L-α-аминоалилил)-L-цистеинил-D-валина изопенициллина N — предшественника пенициллина G, пенициллина N и цефалоспорина С. |
дают растущей культуре характерный цвет, зависящий от pH среды (табл. 12.3). В свою очередь pH (и цвет) среды зависят от того, какое соединение синтезируется. Мутанты родительского штамма 5. coelicolor, не способные синтезировать актинородин, бесцветные. Появление окраски после трансформации штамма АМ-7161 Streptomycessp. либо штаммов В1140 или Tü22 S. violaсеоruber плазмидой, несущей все или несколько генов, кодирующих ферменты биосинтеза актинородина, свидетельствует о синтезе нового антибиотика (рис. 12.12, табл. 12.3), Трансформанты штамма АМ-7161 Streptomyces sp. и штамма В1140 S. violaceoruber, содержащие плазмиду p[J2303, синтезируют антибиотики, кодируемые и плазмидой, и хромосомной ДНК. Однако при трансформации штамма Tü22 5. violaceoruber плазмидой pIJ2303 наряду с актинородином синтезируется новый антибиотик — Дигидрогранатиродин, а при трансформации штамма АМ-7161 Sireptomuces sp. плазмидой pIJ2315 синтезируется еще один новый антибиотик — медерродин А.
В структурном отношении эти новые антибиотики мало отличаются от актинородина, медермицина, гранатицина и гидрогранатицина и, вероятно, образуются в том случае, когда промежуточный продукт одного пути биосинтеза служит субстратом для фермента другого пути. Когда будут детально изучены биохимические свойства различных путей биосинтеза антибиотиков, появится возможность создавать новые уникальные высокоспецифичные антибиотики, манипулируя генами, которые кодируют соответствующие ферменты.
Разработка новых методов получения поликетидных антибиотиков
Термин «поликетидные» относится к классу антибиотиков, которые образуются в результате
Использование рекомбинантных микроорганизмов для получения коммерческих продуктов 261
| Таблица 12.3. Антибиотики, синтезируемые различными штаммами Streptomyces, в том числе штаммами, трансформированными плазмидами pIJ2303 и pIJ23l51) | | |||
| Штамм/плазмида | Цвет культуры | Антибиотик(и) | | |
| | кислая среда | щелочная среда | | |
 | | |||
| | ||||
| | ||||
| | ||||
| | ||||
| | ||||
| | ||||
| | ||||
| | ||||
| | | | | |
последовательной ферментативной конденсации карбоновых кислот типа ацетата, пропионата и бутирата. Некоторые поликетидные антибиотики синтезируются растениями и грибами, но большая их часть образуется актиномицетами в виде вторичных метаболитов. Прежде чем. проводить манипуляции с генами, кодирующими ферменты биосинтеза поликетидных антибиотиков, необходимо выяснить механизм действия этих ферментов.
Поликетидные антибиотики синтезируются по тому же пути, что и длинноцепочечные жирные кислоты. В результате каждого цикла конденсации к растущей углеродной цепи добавляется ß-кетогруппа. Процесс состоит из ряда повторяющихся стадий, включающих восстановление кетогруппы, дегидратацию и восстановление ß-еноильных групп в растущей поликетидной цепи. Существуют два класса поликетидсинтаз — ферментных комплексов, ответственных за синтез поликетидных антибиотиков (рис. 12.13). Первый класс составляют синтазы, катализируюшие реакции биосинтеза ароматических поликетидов; каждая синтаза представляет собой один полипептид с одним активным центром, который последовательно катализирует биосинтетические реакции (рис. 12.13, А). Второй класс включает синтазы, образованные несколькими полипептидами (АЕ на рис. 12.13, Б); каждый из них имеет свой активный центр и обладает специфической ферментативной активностью, катализирующей определенную реакцию биосинтеза.
Если каждый домен субъединицы многофункциональной поликетидсинтазы, обладающий ферментативной активностью, катализирует определенную реакцию, то утрата любой из активностей затронет только одну реакцию биосинтеза, а изменение домена с известной функцией приведет к предсказуемым изменениям структуры синтезируемого антибиотика. Так, детально изучив генетические и биохимические составляющие биосинтеза эритромицина в клетках Saccharopolyspora erythraea, удалось внести специфические изменения в гены, ассоциированные с биосинтезом этого антибиотика, и синтезировать производные эритромицина с другими свойствами. Вначале была определена первичная структура фрагмента ДНК 5, erythraeaдлиной 56т. п. н., содержащего кластер генов ery, затем двумя разными способами модифицирована эритромицинполикетидсинтаза. Для этого 1) удаляли участок ДНК, кодирующий ß-кеторедуктазу, либо 2) вносили изменение в участок ДНК, кодирующий еноилредуктазу. Делеция ß-кеторедуктазного гена приводила к накоплению промежуточного продукта, у которого к С-5-атому кольца была присоединена карбонильная группа, а не гидроксильная (рис. 12,14), а мутация в гене еноилредуктазы — к образованию двойной связи между атомами С-6 и С-7 (рис. 12.14). Из этих экспериментов следует, что если идентифицировать и охарактеризовать кластер генов, кодирующих ферменты биосинтеза определенного поликетидного антибиотика, то, внося в
262 ГЛАВА 12
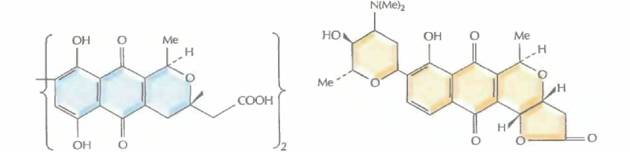 | |
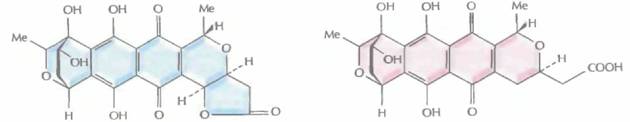
| Актинородин | Медермицин |
 | |
| Гранатицин | Дигидрогранатицин |
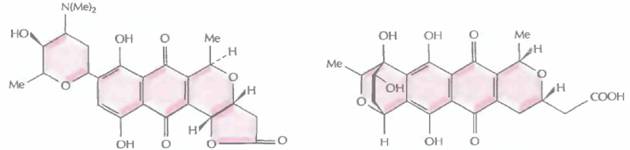 | |
| Медерродин А | Дигидрогранатиродин |
| Рис. 12.12. Структурные формулы различных изохроманхиноновых антибиотиков, синтезируемых штаммами Streptomyces. S. coelicolor дикого типа и плазмида рIJ2303 кодируют актинородин; Streptomyces sp. синтезирует медермицин, a S. violaceoruber — гранатицин и дигидрогранатицин. Синтезируемые гибридные антибиотики — это медерродин А и дигидрогранатиродин. | |
них специфические изменения, можно будет направленно изменять структуру антибиотика. Кроме того, вырезая и соединяя те или иные участки ДНК, можно перемещать домены поликетидсинтазы и получать новые поликетидные антибиотики.
Все кластеры генов ароматических поликетидов содержат три гена, кодирующих так называемую минимальную поликетидсинтазу. Этот ферментный комплекс включает кетосинтазу (с ацилтрансферазным доменом), фактор, определяющий длину цепи, и ацилпереносящий белок. Минимальная поликетидсинтаза отвечает за синтез ароматического поликетидного остова, а его модификации осуществляются другими ферментами, действующими согласо-
Использование рекомбинантных микроорганизмов для получения коммерческих продуктов 263
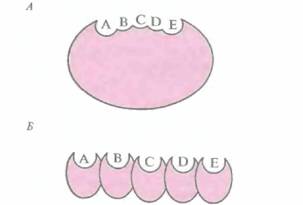 | Рис. 12.13. Схематическое изображение структуры поликетидсинтазы ароматических поликетидов, у которой активный центр находится в одном полипептиде (А), и поликетидсинтазы, представляющей собой комплекс нескольких полипептидов с разными активными центрами (Б). Ферменты обоих типов содержат несколько доменов (А— Е), каждый из которых обладает собственной ферментативной активностью. |
ванно с ней. Гены, кодирующие все эти ферменты, обычно организованы в один кластер (рис. 12.15). Каждый кластер генов кодирует синтез определенного антибиотика. С помощью обмена генами между кластерами были синтезированы два новых ароматических поликетидных антибиотика (рис. 12.16), что еще раз иллюстрирует возможности генной инженерии.
Усовершенствование производства антибиотиков
С помощью генной инженерии можно не только создавать новые антибиотики, но и увеличивать эффективность синтеза уже известных. Лимитирующим фактором в промышленном производстве антибиотиков с помощью Streptomycesspp. часто является количество доступного клеткам кислорода. Вследствие плохой растворимости кислорода в воде и высокой плотности культуры Sireptomycesего часто оказывается недостаточно, рост клеток замедляется и выход антибиотика снижается. Чтобы решить эту проблему, можно, во-первых, изменить конструкцию биореакторов, в которых выращивается культура Streptomyces, a во-вторых, используя методы генной инженерии, создать штаммы Streptomyces, более эффективно использующие имеющийся кислород. Эти два подхода не исключают друг друга.
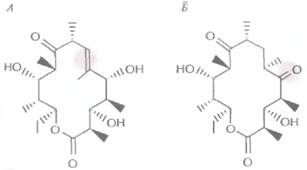 | Рис. 12.14. Производные эритромицина, полученные генноинженерными методами. А, В результате мутации в гене еноилредуктазы образуется продукт с двойной связью между атомами С-6 и С-7 (цветной кружок). Б. Делеция гена ß-кеторедуктазы сопровождается образованием производного с С-5-карбонильной, ане гидроксильной группой (цветной кружок). (По данным работы Kutz, Donadio, Annu. Rev. Microbiol. 47: 875-912, 1993.) |
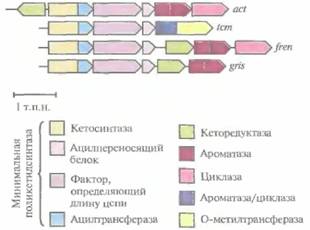 |
| Рис. 12.15. Кластер генов биосинтеза ароматических поликетидных антибиотиков актинородина (act), тетраценомицина (tcm), френолицина (fren) и гризеузина (gris). Каждый кластер содержит гены, кодирующие минимальную поликетидсинтазу, которая отвечает за синтез поликетидного остова. Ферменты, кодируемые другими генами, катализируют реакции его модификации. Сужающийся «конец» гена указывает направление его транскрипции. |
264 ГЛАВА 12
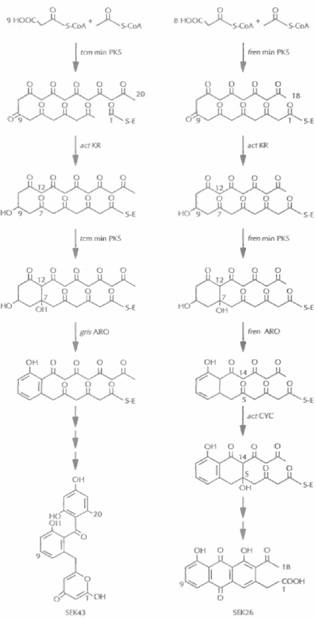 | Рис. 12.16. Искусственно созданные пути биосинтеза поликетидных антибиотиков SEK43 и SEK26- Обозначения: act — актинородин, tст — тетраценомицин, fren — френолицин, gris -гризеузин, min PKS — минимальная поликетидсинтаза, KR — ß-кеторедуктаза. ARO -ароматаза, CYC — цикл а за. |
