Глик Молекулярная биотехнология. Глик Б., Пастернак Дж. Молекулярная биотехнология. Принципы и применение. Пер с англ. М. Мир, 2002. 589 с
 Скачать 9.74 Mb. Скачать 9.74 Mb.
|
Растения, устойчивые к вирусамВирусы растений часто причиняют значительный ущерб растениям и существенно снижают урожай. Чтобы не прибегать к обработке культур химическими препаратами, селекционеры попытались перенести природные гены устойчивости к вирусам от одной линии растений к другой. Однако устойчивые растения часто вновь становятся чувствительными, а устойчивость к одному вирусу не гарантирует устойчивости к другим. Природный иммунитет к вирусным инфекциям обусловливается разными причинами: блокированием проникновения вируса в растение, предотвращением его распространения, подавлением симптомов вирусной инфекции. 396 ГЛАВА 18 Чтобы получить растения, устойчивые к вирусам, проводили их «иммунизацию» вирусными генами, кодирующими белки оболочки, другими вирусными генами или антисмысловыми последовательностями вирусного генома. Если в трансгенном растении экспрессирует-ся ген, кодирующий белок оболочки вируса, который обычно инфицирует это растение (а данный белок зачастую является основным белковым компонентом вируса), то способность вируса проникать в растение и распространяться в нем часто значительно уменьшается. Механизм ингибирования пролиферации вируса в присутствии генов белка оболочки точно не установлен, однако ясно, что противовирусное действие начинает проявляться на ранних стадиях репликации вируса, так что вирусные частицы не образуются. Это снижает вероятность возникновения спонтанных вирусных мутантов, способных к репликации в присутствии вирусного белка оболочки. С помощью этого подхода были получены устойчивые к различным вирусам трансгенные растения множества различных зерновых культур (табл. 18.3). И хотя абсолютной устойчивости при этом достичь не удавалось, ее уровень был весьма высок. Более того, обнаружилось, что ген белка оболочки одного вируса иногда обеспечивает устойчивость к широкому кругу неродственных вирусов. Ценность подхода повышается и благодаря тому, что грансгенные растения развиваются одинаково как в полевых условиях, так и в лаборатории. Молекула РНК, комплементарная транскрипту нормального гена (мРНК), называется антисмысловой, а сама мРНК, участвующая в трансляции, — смысловой. Антисмысловая РНК образует дуплекс с мРНК, блокируя тем самым трансляцию, так что в ее присутствии синтез белкового продукта соответствующего гена уменьшается. Кроме того, дуплекс антисмысловая РНК—мРНК быстро деградирует, что уменьшает содержание конкретной мРНК в клетке. Учитывая все сказанное выше, можно попытаться предотвратить репликацию растительных вирусов и защитить от них растения, введя в них ген, обеспечивающий синтез антисмысловых РНК, комплементарных мРНК вирусного белка оболочки.
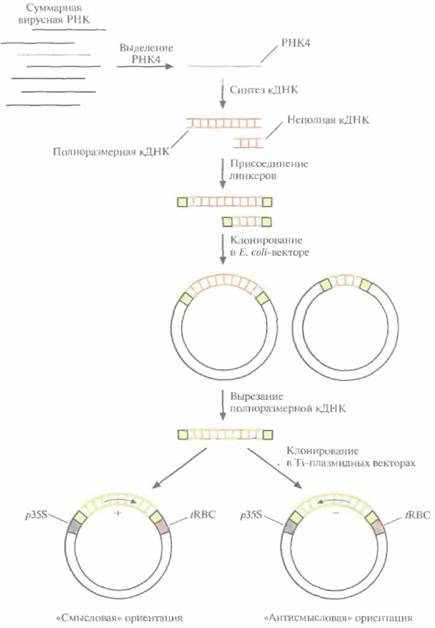
Для сравнения эффективности подходов, основанных на использовании вирусного гена белка оболочки, с одной стороны, и антисмысловой РНК - с другой, клонировали кДНК белка оболочки вируса мозаики огурца (CuMV) в растениях табака в двух ориентациях, «смысловой» и «антисмысловой» (в каждом конкретном растении — одна из этих ориентации), а затем определили чувствительность трансгенных растений к вирусной инфекции (рис. 18.6). Геном CuMV представлен тремя отдельными одноцепочечными молекулами РНК, каждая из которых кодирует определенный вирусный белок. In vivo одна из этих молекул — РНК3 — подвергается процессингу; часть ее последовательности удаляется и образуется РНК4, кодирующая вирусный белок оболочки. Создание трансгенных растений, которые синтезируют либо нормальную мРНК и вирусный белок оболочки, либо соответствующую антисмысловую РНК, включает следующие Генная инженерия растений; применение 397
1. Выделение РНК4. 2. Ферментативный синтез in vitro кДНК на РНК4. 3. Присоединение к кДНК линкерных последовательностей. 4. Встраивание полноразмерной кДHК в векторы для клонирования в обеих ориентациях, в каждой из которых она находится под контролем 35S-промотора вируса мозаики цветной капусты и регуляторных сигналов терминации транскрипции растительного гена малой субъединицы рибулозобисфосфаткарбоксилазы. 5. Регенерация отдельных трансгенных растений, в геном которых встроена кДНК в одной из двух возможных ориентации. Для введения кДНК, кодирующих смысловую (белок-кодирующую) и антисмысловую 398 ГЛАВА 18
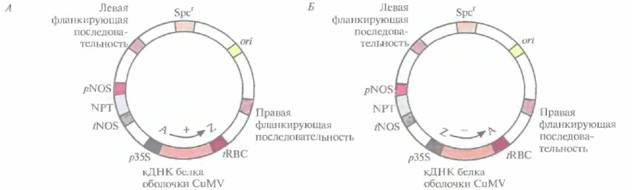
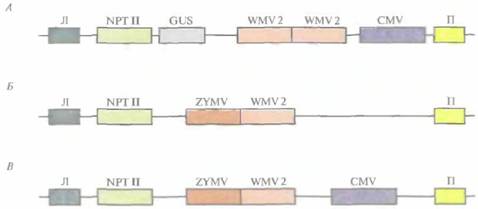
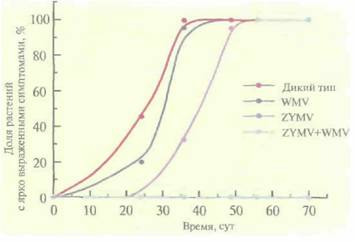
РНК, в отдельные клетки табака использовали бинарную векторную систему на основе Ti-плазмид (рис. 18.7). ß трансгенных растениях, синтезирующих белок оболочки вируса CuMV, вирусные частицы не накапливались и симптомы инфекции не проявлялись независимо от титра инокулята. В отличие от этого трансгенные растения, синтезирующие антисмысловую РНК белка оболочки CuMV, проявляли устойчивость только при малых концентрациях вирусных частиц в инокуляте. Сходные результаты были получены в других лабораториях, где были созданы трансгенные растения, синтезирующие антисмысловые РНК-копии генов вирусных белков оболочки, и проверено, смогут ли эти растения противостоять вирусной инфекции. Во всех случаях растения проявляли устойчивость к инфекции, только если титр используемого инокулята был мал, Общий вывод, который можно сделать из подобных экспериментов, состоит в следующем: антисмысловые РНК-копии генов вирусных белков оболочки обеспечивают гораздо худшую защиту трансгенных растений от вирусных инфекций, чем смысловые копии генов белков оболочки вируса. Возможно, не стоит совсем отказываться от стратегии защиты, основанной на использовании антисмысловой РНК, однако прежде чем внедрять эту методику, ее необходимо значительно усовершенствовать. Часто сельскохозяйственные культуры бывают подвержены нескольким вирусным инфекциям; любая из них может нанести ущерб растениям и снизить урожай. В идеале трансгенные растения должны быть устойчивы более чем к одному вирусу. Чтобы достичь этой цели, для трансформации растений желтой яйцевидной тыквы (Cucurbitapepo) использовали бинарные векторы на основе Ti-плазмид, несущие один или несколько генов белков оболочки CuMV, вируса желтой мозаики кабачков и вируса 2 мозаики арбуза (рис. 18.8). Трансгенные растения, в которых экспрессировались все три гена, в лабораторных условиях были устойчивы ко всем указанным вирусам. Растения, экспрессирую-щие гены белков оболочки вируса желтой мозаики кабачков и вируса 2 мозаики арбуза, были проверены в полевых условиях на устойчивость к тлям — насекомым, являющимся природным переносчиком этих вирусов в растущие растения. Если в растении экспрессировались оба гена белков оболочки, то они проявляли полную устойчивость к одновременной инфекции этими вирусами (рис, 18.9), а если наблюдалась экспрессия только одного из вирусных белков оболочки, то заражение происходило не сразу, Генная инженерия растений: применение 399
но в конце концов все симптомы вирусной инфекции проявлялись, и растение утрачивало коммерческую ценность. Итак, ясно, что наиболее эффективной стратегией при выведении трансгенных растений, устойчивых ко всем основным вирусам, замедляющим их рост и развитие, является введение в них нескольких генов, детерминирующих синтез белков оболочки вирусов. Имеются предварительные данные о том, что трансгенные растения, в которых экспрессируются вирусные гены, отличные от генов белков оболочки (например, ген вирусных сателлитных РНК или ген репликации вируса), также оказываются в какой-то мере защищенными от вирусных инфекций, но насколько эффективными и применимыми будут соответствующие подходы, пока неясно. Защита растений от патогенных вирусов может осуществляться не только их «иммунизацией» генами вирусных белков, но и при участии противовирусных белков, синтезируемых сами- 400 ГЛАВА 18 ми растениями. Например, в клеточной стенке фитолакки американской (Phytolaccaamericana) присутствуют три разных противовирусных белка: РАР, синтезируемый в листьях весной, РАРП, обнаруживаемый в листьях летом, и PAP-S, содержащийся в семенах. Эти белки легко выделить из водных экстрактов измельченных тканей растения. Если небольшое количество РАР нанести на листья других растений, то последние также окажутся устойчивыми к нескольким вирусам. Таким образом, ген белка РАР вполне можно использовать для получения трансгенных растений, устойчивых к широкому спектру вирусов растений. Выделенную кДНК РАР вводили в геном табака и картофеля с помощью бинарных векторов на основе Ti-плазмид. Трансформанты, синтезирующие РАР в большом количестве (> 10 нг на l мг суммарного белка), были чахлыми, пятнистыми и бесплодными, растения же с более низким содержанием РАР (1—5 нг на 1 мг белка) имели нормальный внешний вид и были фертильны. Эти данные говорят о том, что если концентрация РАР превышает некоторый пороговый уровень, то нормальное функционирование клетки нарушается. Противовирусный эффект белка РАР в трансгенных растениях проявляется в основном в уменьшении числа повреждений; однако, если уж повреждение возникало, то растение систематически инфицировалось. Отсюда следует, что РАР подавляет вирусную инфекцию на ранней стадии. Тем не менее, когда трансгенные растения табака и картофеля, экспрессирующие РАР в небольших количествах, инфицировали вирусами картофеля X или Y, на листьях обнаруживалось значительно меньше повреждений, чем в случае нетрансформированных контрольных растений. Поскольку противовирусное действие РАР проявляется при относительно небольших его концентрациях, можно попытаться создать транс-генные растения, синтезирующие этот белок в малом количестве, и параллельно использовать другие способы защиты растений от вирусов. Растения, устойчивые к гербицидамНесмотря на то что на производство более 100 различных химических гербицидов во всем мире ежегодно расходуется 10 млрд. долларов, примерно 10% урожая теряется из-за большого количества сорняков. Кроме того, многие гербициды оказывают одинаковое действие на сорняки и сельскохозяйственные культуры; нередко обработку полей необходимо проводить еще до появления сорняков, а некоторые гербициды накапливаются в окружающей среде. Чтобы решить хотя бы некоторые из этих задач, можно попытаться создать сельскохозяйственные культуры, устойчивые к гербицидам. Для этого можно • уменьшить поглощение гербицида растением • обеспечить синтез белка, чувствительного к гербициду, в таком количестве, чтобы его хватало на выполнение присущих ему функций в присутствии гербицида • уменьшить способность белка, чувствительного к гербициду, к связыванию с ним • обеспечить инактивацию гербицида в растении в ходе метаболизма. Из этих подходов были реализованы три последних. Выведенные с их помощью гербицидустойчивые трансгенные растения перечислены в табл. 18.4. Были получены растения, устойчивые к гли-фосфату - гербициду, быстро разлагающемуся в почве на нетоксичные составляющие и потому безопасному для окружающей среды. Глифос-фат является ингибитором 5-енолпирувилши-кимат-3-фосфатсинтазы (EPSPS) - фермента, играющего важную роль в синтезе ароматических аминокислот и у бактерий, и у растений. Из глифосфатустойчивого штамма E. coli был выделен ген, кодирующий EPSPS, помещен под контроль растительного промотора и сигналов терминации транскрипции/полиаденилирования и введен в растительные клетки. Трансгенные растения табака, петуньи, томата, картофеля и хлопка, синтезировавшие EPSPS в количестве, достаточном для замены ингибированного гербицидом растительного фермента, были устойчивы к глифосфату и при обработке, в отличие от сорняков, не погибали. Другой способ приобретения устойчивости — с помощью инактивации гербицида — был реализован для бромоксинила (3,5-дибром-4-гид- Генная инженерия растений: применение 401
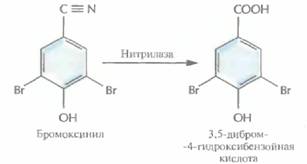
роксибензонитрила) — гербицида, который ингибирует фотосинтез. Устойчивые растения создавали путем введения в их геном бактериального гена, кодирующего нитрилазу, которая инактивирует бромоксинил еще до того, как он начинает действовать (рис. 18.10). Из почвенной бактерии Klebsiellaozaenaeбыл выделен ген нитрилазы, помещен под контроль светочувствительного промотора гена малой субъединицы
рибулозобисфосфат-карбоксилазы и встроен в геном табака. Трансгенные растения синтезировали активную нитрилазу и были устойчивы к бромоксинилу. Растения, устойчивые к грибам и бактериямФитопатогенные грибы наносят весьма ощутимый вред сельскохозяйственным культурам. По оценкам, убытки, которые терпят фермеры Юго-Восточной Азии, Японии и Филиппин в результате поражения грибом, вызывающим пирикуляриоз, одного из основных зерновых этого региона, риса, исчисляются примерно 5 млрд. долл. в год. Сейчас основной способ борьбы с фитопатогенными грибами состоит в обработке растений химическими веществами, которые накапливаются в окружающей среде и представляют опасность для животных, в том числе и для человека. Поэтому очень важно выработать другие, простые, недорогие, эффективные и безопасные для окружающей среды нехимические методы защиты сельскохозяйственных культур от грибов. 402 ГЛАВА 18
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||