тесты фармхимия. ФАРМХИМИЯ_1. Государственная фармакопея рф
 Скачать 1.43 Mb. Скачать 1.43 Mb.
|
Соединения кислорода.Препараты:Aqua purificataВода очищенная, H2O Описание Бесцветная прозрачная жидкость без вкуса и запаха. pH от 5 до 7. Недопустимые примеси: Восстанавливающие в-ва: 100 мл доводят до кипения, прибавляют 1 мл KMnO4 и 2 мл H2SO4 разведённой, кипятят 10 минут. Розовая окраска должна сохраняться. MnO4- + 6e + 8H+ Mn2+ + 4H2O Диоксид углерода: При взбалтывании с раствором известковой воды в течении 1ч. не должно быть помутнения. Известковая вода – это кальция гидроокиси раствор, который готовят из жженой извести, настаивая её в воде. Ca2+ + CO32- CaCO3 Нитраты и нитриты: к 5 мл. воды прибавляют 1 мл. раствора дифениламина: не должно появиться голубого окрашивания. 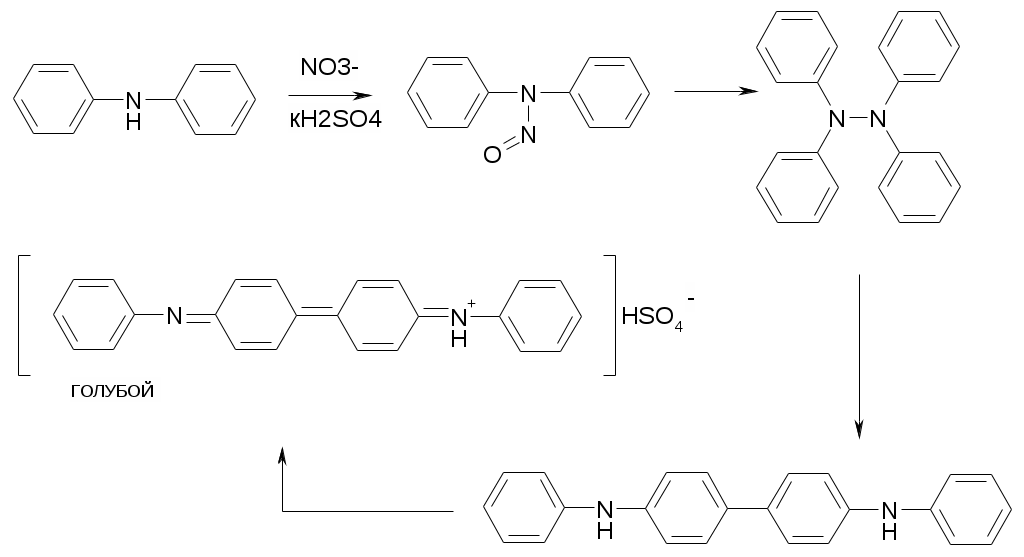 Хлориды, кальций, тяжёлые металлы, сульфаты. Допустимые примеси: Аммиак. Natrii hydrocarbonasНатрия гидрокарбонат, NaHCO3, M. в. 84,0 Описание. Белый кристаллический порошок без запаха, соленощелочного вкуса, устойчив в сухом воздухе, медленно разлагается во влажном. Водные растворы имеют щелочную реакцию. Растворимость. Растворим в воде, практически нерастворим в 95% спирте. Подлинность. Препарат дает характерные реакции на натрий и гидрокарбонаты. Na+ - смотри выше. Для отличия от карбонат-иона проводят реакцию взаимодействия с насыщенным раствором сульфата магния. Испытание основано на образовании магния карбоната основного: 4MgSO4 + 4Na2CO3 MgCO3•Mg(OH)2•3H2O + 4Na2SO4 +CO2 Гидрокарбонат-ион образует осадок только при кипячении смеси, а карбонат-ион при обычной температуре. Недопустимые примеси: тяжелые металлы, соли аммония. Допустимые примеси: хлориды, сульфаты, железо, кальций, мышьяк. Количественное определение. Около 1 г препарата (точная навеска) растворяют в 20 мл свежепрокипяченной и охлажденной воды и титруют 0,5 н раствором соляной кислоты (индикатор — метиловый оранжевый). NaHCO3 + HCl H2CO3 + NaCl f=1; 1 мл 0,5 н. раствора соляной кислоты соответствует 0,04200 г NaHCO3, которого в препарате должно быть не менее 99,0%. Натрия гидрокарбонат для инъекций, кроме перечисленных выше требований, должен выдерживать следующее испытание: 5% раствор препарата должен быть прозрачным и бесцветным. Хранение. В хорошо укупоренной таре. Применение: ацидоз, язвенная болезнь желудка и двенадцатиперстной кишки, интоксикации, диабет, воздушная болезнь, морская болезнь. Kalii permanganasKMnO4 Описание: темные или красно-фиолетовые кристаллы или мелкий кристаллический порошок с металлическим блеском. Растворимость: Растворим в воде, легко растворим в кипящей воде. Подлинность: 1. К раствору препарата прибавляют разведенную H2SO4 и раствор H2O2 происходит обесцвечивание раствора: 2KMnO4 + 5H2O2 + 3H2SO4 2MnSO4 + K2SO4 + 8H2O + 5O2 2. Препарат растворяют в воде, прибавляют спирт, кипятят до полного обесцвечивания, фильтруют; фильтрат дает реакции на К+ Примеси: хлориды не более 0,02%, сульфаты не более 0,05% Количественное определение: около 0,3 г препарата (т.н.) растворяют в мерной колбе на 100 мл, 25 мл полученного раствора помещают в склянку с притертой пробкой, содержащей 10 мл 20% KI и 5 мл H2SO4 разведенной, оставляют на 10 минут в темном месте, разводят водой до 100 мл и выделившийся йод титруют 0,1М Na2S2O3 до обесцв. с индикатором – крахмалом: 2MnO4-+ 10I-+ 16H+ 2Mn2+ + 5I2 + 8H20 S2O32- + I2 S4O62 -+ 2I- f=1/5; Хранение: хорошо укупоренные банки или запаянные жестянки, Применение: антисептическое средство Natrii thiosulfasNa2S2O3•5H2O Описание: бесцветные прозрачные кристаллы без запаха, солено-горького вкуса. Растворимость: легко растворим в воде, практически нерастворим в спирте. Подлинность: 1) 0,1 г растворяют в 2 мл H2O прибавляют несколько капель HCl и через некоторое время раствор мутнеет и появляется запах Na2S2O3 + HCl NaCl + S + SO2 + H2O 2) с избытком AgNO3 образуется осадок, который меняет свою окраску от белого через желтый и бурый к черному. Na2S2O3 + 2AgNO3 изб. Ag2S2O3 Ag2S2O3 Ag2SO3 + S Ag2SO3 + S + H2O Ag2S + H2SO4 3) Характерные реакции на натрий. Количественное определение: около 0,5 г препарата (т.н.) растворяют в 25 мл H2O и титруют 0,1М раствором I2 с индикатором крахмалом до обесцвечивания: 2Na2S2O3 + I2 Na2S4O6 + 2NaI f Na2S2O3=1; Вещества в препарате должно быть не менее 99,0% и не более 102,0% Хранение: хорошо укупоренная тара, т.к. в сух. теплом воздухе преп. выветривается, во влажном-расплывается,500С-плавится Применение: противотоксическое и десенсибилизирующее средство, используется при отравлении цианидами, при отравлении солями тяжелых металлов, при аллергических заболеваниях (внутривенно). Solutio Hydrogenii peroxydi dilutaСостав: Пергидроля – 10г, антифебрин – 0,5%, воды до 100 мл Описание: Бесцветная прозрачная жидкость без запаха Подлинность: к 1 мл препарата прибавляют 0,2 мл H2SO4 разведенной, 2 мл эфира, 0,2 мл раствора K2Cr2O7 и взбалтывают, эфирный слой окрашивается в синий цвет K2Cr2O7 + H2SO4 H2Cr2O7 + K2SO4 H2Cr2O7 + 4H2O2 H2Cr2O8 + H2O Количественное определение: 1. Безындикаторная перманганатометрия: 10мл раствора помещают в мерную колбу на 100 мл и доводят водой до метки, к 10 мл полученного раствора прибавляют 5мл H2SO4 разведенной и титруют 0,1М KMnO4 до устойчивой розовой окраски: 2KMnO4 + 5H2O2+3 H2SO4 2MnSO4 + K2SO4 + 8H2O + 5O2 f(H2O2) = ½ ; 2. Косвенная йодометрия: 2KI + H2O2 + H2SO4 р. I2 + K2SO4 + 8H2O I2 + 2Na2S2O3 2NaI + Na2S4O6 f(H2O2) = ½; 3. Прямая цериметрия 4. Фотоколориметрия 5. Спектрофотоколориметрия 6. Рефрактометрия Вещества в препарате должно быть 2,7-3,3%. Хранение: в склянках темного стекла с притертой пробкой, в прохладном месте без доступа света. Применение: антисептическое, дезодорирующее, депигментирующее и кровоостанавливающее средство Другие препараты перекиси водородаPerhydrolum – 30% H2O2. Hydroperitum – 33-35% H2O2, (NH2)2CO, лимонная кислота. Magnesii peroxydum–25%MgO2+75%MgO. |
