68г5ег8. Коллоквиум по разделу Физиология кровообращения
 Скачать 2.48 Mb. Скачать 2.48 Mb.
|
|
СОКРАТИМОСТЬ сердечной мышцы существенно отличается от сократимости скелетной мышцы. 1) Сердечная мышца в отличие от скелетной подчиняется закону «все или ничего»: сердечная мышца либо не отвечает на раздражение, если оно ниже порогового, либо отвечает максимальным сокращением, если раздражитель достигает пороговой или сверхпороговой силы. Увеличение силы раздражения выше пороговой не ведет к увеличению силы сокращения, как при действии на скелетную мышцу. Это объясняется тем, что скелетная мышца проводит возбуждение изолированно по отдельным мышечным волокнам, на соседние волокна возбуждение не переходит. У сердечной мышцы возбуждение, возникнув в одном месте, распространяется диффузно по всем кардиомиоцитам, и все они вовлекаются в сокращение. 2) У сердечной мышцы более длительный период одиночного сокращения: он примерно соответствует длительности ПД (у предсердий — около 100 мс, у желудочков — 300—400 мс). При увеличении частоты сердечных сокращений продолжительность одного сокращения укорачивается. Если частота сердечных сокращений становится меньше, систола желудочков и предсердий удлиняется. 3) Сердечная мышца в отличие от скелетной не может сокращаться тетанически. Это объясняется тем, что у нее длительный рефрактерный период: он равен продолжительности ПД и одиночного сокращения мышцы. Это означает, что весь период сокращения мышца сердца невозбудима. Возникновение тетанического сокращения могло бы нарушить нагнетательную функцию сердца. 4) Существенно отличается роль внеклеточного Са2+ в электромех. сопряжении мышцы сердца. Система продольных трубочек, служащих внутриклеточным резервуаром Са2+, выражена в меньшей степени, чем в скелетных мышцах. Поэтому Са2+, входящий в клетку при возбуждении, не только играет важную роль в электромех. сопряжении, но участвует в деполяризации клетки и увеличивает длительность ПД кардиомиоцитов. Входящий Са2+ запускает процесс освобождения внутриклеточного Са2+ из саркоплазматического ретикулума, далее он обеспечивает до 30 % общего внутриклеточного количества Са2+, необходимого для взаимодействия нитей актина и миозина. Остальные 70 % Са2+ выбрасываются саркоплазматическим ретикулумом. РАСТЯЖИМОСТЬ И ЭЛАСТИЧНОСТЬ сердечной мышцы также играют важную роль в выполнении нагнетательной функции сердца. 1) Оба этих свойства смягчают гидравлический удар, возникающий в результате несжимаемости жидкости и быстро сокращающихся стенок сердца. 2) Эластические силы, возникающие вследствие растяжения стенок сердца при его наполнении кровью, в том числе и при сокращении предсердий, увеличивают силу сокращений миокарда в начале систолы. 3) Эластичность структурных элементов сердца обеспечивает возникновение в конце систолы упругих сил, способствующих расслаблению сократившегося (сжавшегося) миокарда после прекращения его возбуждения. Стенки (особенно желудочков) расслабляются — расправляются, как предварительно сдавленная резиновая груша, так как различное направление отдельных мышечных слоев друг относительно друга увеличивает упругость стенок сердца, которая превышает упругость скелетной мышцы. ПРОВОДИМОСТЬ сердечной мышцы принципиально отличается от проводимости скелетной мышцы. В миокарде возбуждение распространяется из любой точки во всех направлениях — диффузно (генерализованный характер распространения возбуждения). Это объясняется особенностью строения сердечной мышцы. Клетки миокарда соединены между собой вставочными дисками: одни из них выполняют механическую функцию; другие обеспечивают транспорт; третьи, нексусы (тесные контакты) с низким электрическим сопротивлением, обеспечивают распространение возбуждения от одного миоцита к другому. Таков же механизм передачи возбуждения по клеткам проводящей системы, а также от клеток проводящей системы к клеткам рабочего миокарда. Благодаря нексусам миокард, хотя и состоит из отдельных клеток, как и скелетная мышца, но функционирует как единое целое — синцитий. Мышечное волокно сердца представляет собой цепочку из клеток миокарда, соединенных конец в конец и заключенных в общую саркоплазматическую оболочку (основную мембрану). Скорость проведения возбуждения по миокарду — около 1 м/с, что в 3,5 раза меньше, чем у скелетной мышцы. 4. Особенности возбудимости, возникновение, распространение возбуждения в сердце. Особенности возбудимости и возбуждения сердечной мышцы. Величина ПП составляет -80 мВ. Он формируется в основном градиентом, ионов К+. Амплитуда ПД равна 120 мВ. Длительность ПД кардиомиоцитов желудочков (300 — 350 мс) почти соответствует длительности сокращения мышцы сердца. Продолжительность ПД кардиомиоцитов предсердия до 120 мс, почти столько же длится систола предсердий. Длительность ПД кардиомиоцита значительно уменьшается, если очередной импульс приходит непосредственно после окончания рефрактерной фазы. Ионный механизм возникновения ПД кардиомиоцитов. 1) Фаза деполяризации и восходящая часть фазы инверсии осущ. в основном за счет входа Na+ в клетку, как у скелетных миоцитов. В данный период увеличена проницаемость мембраны для Na+ в связи с открытием быстрых Na-каналов: когда деполяризация достигает КП (примерно -40 мВ), Na+ лавиной входит в клетку. В фазу деполяризации Na+ идет в клетку, согласно концентр. и эл.градиентам (клетка в эту фазу внутри еще имеет «-» заряд). В 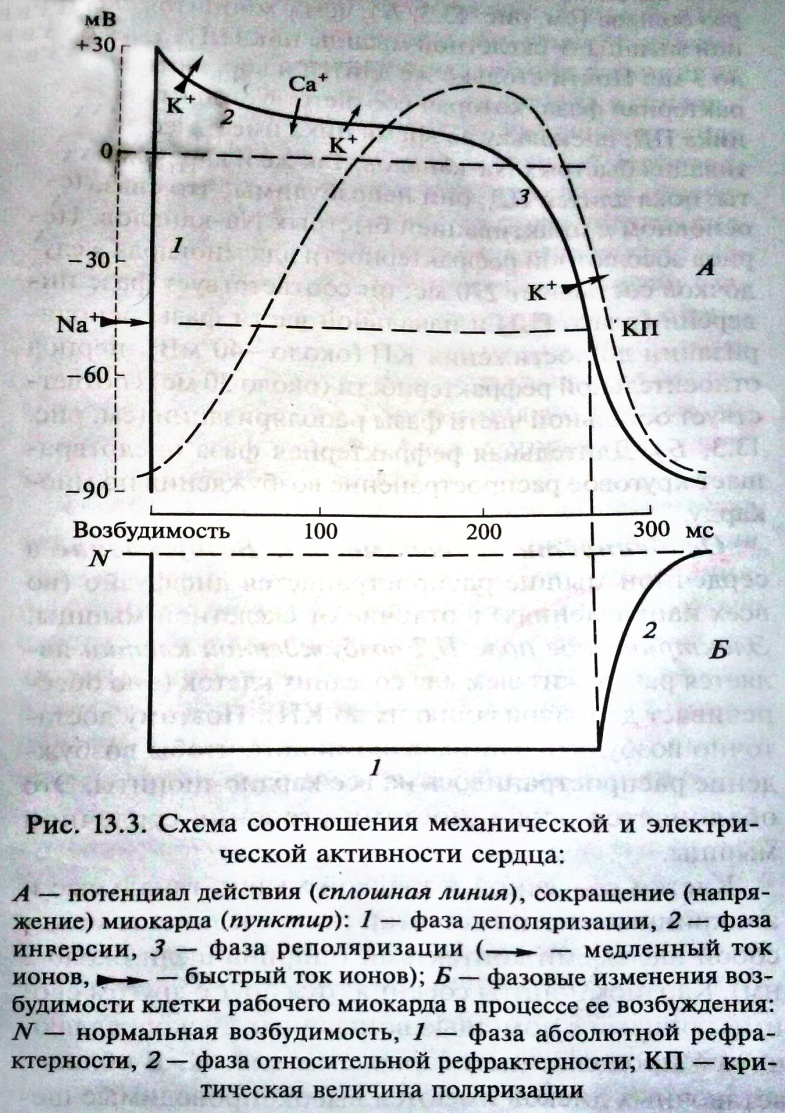 восходящую часть фазы инверсии Na+входит в клетку согласно концентрационному градиенту, но вопреки эл. — в этот период клетка перезаряжается: внутри нее формируется «+» заряд, снаружи «-». Нарастание ПД прекращается вследствие инактивации быстрых Na-каналов. Если в эксперименте уменьшить конц-ю Na+ вне клетки с 140 мМ до 20 мМ, клетка становится невозбудимой. восходящую часть фазы инверсии Na+входит в клетку согласно концентрационному градиенту, но вопреки эл. — в этот период клетка перезаряжается: внутри нее формируется «+» заряд, снаружи «-». Нарастание ПД прекращается вследствие инактивации быстрых Na-каналов. Если в эксперименте уменьшить конц-ю Na+ вне клетки с 140 мМ до 20 мМ, клетка становится невозбудимой.2) Нисходящая часть фазы инверсии начинается в результате активации К-каналов и выхода К+ из клетки. Вначале снижение ПД происходит быстро, вследствие быстрого выхода К+ из клетки согласно концентрационному и электрическому градиентам, поскольку вначале эл. градиент К+ максимальный, затем этот градиент снижается и выход К+ замедляется. Далее медленный суммарный вход Са2+ в клетку становится примерно равным медленному выходу К+ из клетки, что обеспечивает возникновение плато ПД в нисходящую фазу инверсии. Медленный спад плато свидетельствует о том, что выход К+ из клетки несколько превышает вход Са2+ в клетку вследствие начинающейся инактивации медленных Са-каналов (L-типа, от лат. long — долгий). 3) Фаза реполяризации начинается вследствие инактивации медленных Са-каналов и активации быстрых К-каналов, в результате чего К+ начинает лавиной выходить из клетки, что обеспечивает развитие фазы реполяризации кардиомиоцитов. МП возвращается к исходной величине -80 мВ. В фазу инверсии (нисходящая часть) К+ выходит из клетки согласно конц. и эл. градиентам, в фазу реполяризации — согласно концентрационному, но вопреки эл.: в эту фазу клетка снаружи уже снова заряжена «+», изнутри «-». Са2+ из кардиомиоцита после ПД выносится Ca/Na-обменником, частично — Са-АТФазой. Длительность абсолютной рефрактерной фазы кардиомиоцитов желудочков примерно в 100 раз больше, чем у миоцитов скелетной мышцы. У скелетной мышцы пик ПД длится около 3 мс. Почти столько же длится и абсолютная рефрактерная фаза, которая соответствует длительности пика ПД, поскольку во время пика имеет место инактивация быстрых Na-каналов. Так же и кардиомиоциты: пока длится ПД, они невозбудимы, что связано в основном с инактивацией быстрых Na-каналов. Период абсолютной рефрактерности для миокарда желудочков составляет 270 мс; он соответствует фазе инверсии (плато ПД) и начальной части фазы реполяризации до достижения КП (около -40 мВ), период относительной рефрактерности (около 30 мс) соответствует остальной части фазы реполяризации. Длительная рефрактерная фаза предотвращает круговое распространение возбуждения по миокарду. 5. Изменение возбудимости при возбуждении типичных кардиомиоцитов. Электромеханическое сопряжение. Экстрасистола. Компенсаторная пауза. ПД клеток миокарда желудочков у человека при частоте сердцебиений 75 раз в 1 мин длится около 0,3 с. С момента возникновения ПД и до конца его плато мембрана клетки становится невосприимчивой к действию других раздражителей, т.е. находится в абсолютной рефрактерности. Различают период абсолютной рефрактерности (полная невозбудимость), который в миокарде человека продолжается 0,27 с; период относительной рефрактерности, во время которого сердечная мышца может ответить сокращением лишь на очень сильные раздражения (продолжается 0,03 с и соответствует фазе быстрой реполяризации ПД), и период супернормальной возбудимости, когда сердечная мышца может отвечать сокращением на подпороговые раздражения. Сокращение (систола) миокарда продолжается около 0,3 с, что по времени примерно совпадает с общей рефрактерностью, представляющей собой сумму абсолютной и.относительной рефрактерности. Сдедовательно, в периоде сокращения сердце неспособно реагировать на другие раздражители. Наличие длительной рефрактерной фазы препятствует развитию непрерывного укорочения (тетанус) сердечной мышцы, что привело бы к невозможности осуществления сердцем нагнетательной функции. Раздражение, нанесенное на миокард в период расслабления (диастола), когда его возбудимость частично или полностью восстановлена, вызывает внеочередное сокращение сердца — экстрасистолу. Если внеочередное возбуждение возникает в синусно-предсердном узле в тот момент, когда рефрактерный период закончился, но очередной автоматический импульс еще не появился, наступает раннее сокращение сердца — синусовая экстрасистола. Пауза, следующая за такой экстрасистолой, длится такое же время, как и обычная. Внеочередное возбуждение, возникшее в миокарде желудочков, не отражается на автоматизме синусно-предсердного узла. Этот узел своевременно посылает очередной импульс, который достигает желудочков в тот момент, когда они еще находятся в рефрактерном состоянии после экстрасистолы, поэтому миокард желудочков не отвечает на очередной импульс, поступающий из предсердия. Затем рефрактерный период желудочков кончается и они опять могут ответить на раздражение, но проходит некоторое время, пока из СА-узла придет следующий импульс. Таким образом, экстрасистола, вызванная возбуждением, возникшим в одном из желудочков (желудочковая экстрасистола), приводит к продолжительной, так называемой компенсаторной паузе желудочков при неизменном ритме работы предсердий. У человека экстрасистолы могут появиться при наличии очагов раздражения в самом миокарде, в области предсердного или желудочковых водителей ритма. Экстрасистолы могут возникать в результате влияний, поступающих к сердцу из ЦНС. Наличие или отсутствие экстрасистол, а также их характер определяются при регистрации электрокардиограммы. *ЭЛЕКТРОМЕХАНИЧЕСКОЕ СОПРЯЖЕНИЕ– связь между возбуждением и сокращением. Важнейшую роль в запуске сокращения кардиомиоцитов играет саркоплазматический ретикулум - сложная система канальцев и цистерн, оплетающих миофибриллы. В миокарде он выражен слабее, чем в скелетных мышцах. С внеклеточным пространством СПР не сообщается, однако к нему тесно примыкают Т-трубочки (поперечные трубочки) - инвагинации сарколеммы , идущие вдоль линий Z. Потенциал покоя рабочих кардиомиоцитов составляет от -80 до -100 мВ. Он обусловлен двумя причинами: - сарколемма в покое почти непроницаема для Na+ , но хорошо пропускает К+ ; - за счет работы Na+,К+-АТФазы образуется значительный концентрационный градиент для К+ , направленный наружу (внутриклеточная концентрация К+ значительно выше внеклеточной). В результате К+ выходит из клетки, создавая трансмембранную разность потенциалов. Напротив, внутриклеточные концентрации Na+ и Са2+ существенно ниже внеклеточных. Во время плато потенциала действия (фаза 2) Са2+ входит в клетку по так называемым медленным кальциевым каналам. Этого входа Са2+ недостаточно для сокращения, и поэтому главную роль играет выброс гораздо большего количества Са2+ из саркоплазматического ретикулума . Этот выброс обусловлен следующим механизмом: при возбуждении деполяризация распространяется не только вдоль кардиомиоцита , но и в Т-трубочки , через их кальциевые каналы в кардиомиоцит входит Са2+ и соединяется с особыми рецепторами саркоплазматического ретикулума . Это приводит к открыванию кальциевых каналов ретикулума и выходу из него Са2+ . Таким образом, выброс Са2+ из саркоплазматического ретикулума - это самоусиливающийся процесс. Далее Са2+ диффундирует к миофибриллам и связывается с тропонином С , создавая возможность для образования поперечных мостиков. При реполяризации Са2+ снова закачивается в СПР путем активного транспорта. Концентрация Са2+ в области миофибрилл снижается до уровня, когда взаимодействие актина и миозина становится невозможным, и мышца расслабляется. 6. Проводящая система сердца. Автоматия, её природа, центры и градиент. Механизм возникновения медленной диастолической деполяризации. Автоматия сердца — это способность сердца сокращаться под действием импульсов, возникающих в нем самом. Автоматией обладают только атипические мышечные волокна. В состав проводящей системы входят узлы (СА и АВ), образованные скоплением атипических мышечных клеток, пучки и волокна. Водителем ритма сердца — пейсмекером — в котором возникают ритмические импульсы, является синоатриальный узел, расположенный в стенке правого предсердия между впадением в него верхней полой вены и ушком правого предсердия. П-клетки расположены в центральной части узлов, именно они обладают автоматией, сократимость отсутствует. Промежуточные Т-клеткирасположены в периф. части узлов, они проводят ПД от П-клеток к рабочим кардиомиоцитам и клеткам проводящих путей, автоматия у последних выражена слабо. Клетки проводящих путей (пучков Гиса, волокон Пуркинье, межузловых путей) также передают возбуждение на рабочие кардиомиоциты, они имеют хорошую проводимость, слабую автоматию и очень слабую сократимость. МЕХАНИЗМ АВТОМАТИИ. Активация и инактивация электроупавляемых Na-, К- и Са-ионных каналов П –клеток осущ. изменением величины и знака заряда МБ. Главное же заключается в том, что у П-клеток повышена проницаемость для Na+ и Са2+, что делает неустойчивым МП, создаваемый К+. Из-за преобладания входа в клетку Na+ и Са2+ над выходом К+ из клетки во время диастолы развивается медленная диастолическая деполяризация (МДД) П-клеток. Когда МДД достигает КП, возникает ПД П-клеток. Весь цикл ПД проходит следующим образом. К 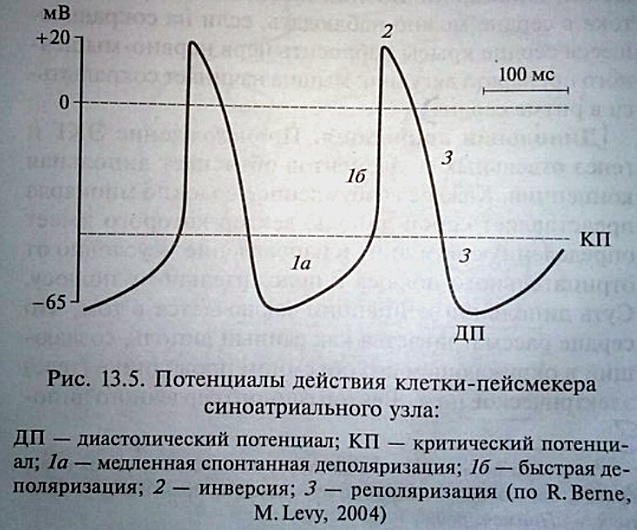 онечная реполяризация П-клеток (гиперполяризация) активирует специф. электроуправляемые Na-каналы («странные»). Ионы Na+ начинают входить в П-клетки, при этом продолжает уменьшаться выход К+ из клетки (как обычно в конце реполяризации инактивируются электроуправляемые К-каналы), поэтому в начале диастолы вход Na+ в клетку преобладает над выходом К+ из клетки, вследствие чего начинается МДД, которая в свою очередь активирует электроуправляемые Са-каналы. Вход в клетку Са2+ вместе с Na+ ускоряет МДД, и когда деполяризация достигает КП (-40 В), активируется большое число Са-каналов и Са2+ быстро поступает в клетку, а выход К+ быстро уменьшается вследствие инактивации К-каналов, развивающейся деполяризацией П-клеток. Быстрая деполяризация П-клеток осуществляется благодаря входу Са2+ в клетки (вход Na+ в клетки прекращается, так как странные электроуправляемые Na-каналы в начале быстрой деполяризации инактивируются). Нарастание ПД прекращается вследствие инактивации электроуправляемых Са-каналов и активации электроуправляемых К-каналов. Выход К+ обеспечивает реполяризацию, в конце которой гиперполяризация вновь активирует странные Na-каналы, и начинается новый цикл и т. д. Денервированный синоатриальный узел возбуждается до 120/мин. онечная реполяризация П-клеток (гиперполяризация) активирует специф. электроуправляемые Na-каналы («странные»). Ионы Na+ начинают входить в П-клетки, при этом продолжает уменьшаться выход К+ из клетки (как обычно в конце реполяризации инактивируются электроуправляемые К-каналы), поэтому в начале диастолы вход Na+ в клетку преобладает над выходом К+ из клетки, вследствие чего начинается МДД, которая в свою очередь активирует электроуправляемые Са-каналы. Вход в клетку Са2+ вместе с Na+ ускоряет МДД, и когда деполяризация достигает КП (-40 В), активируется большое число Са-каналов и Са2+ быстро поступает в клетку, а выход К+ быстро уменьшается вследствие инактивации К-каналов, развивающейся деполяризацией П-клеток. Быстрая деполяризация П-клеток осуществляется благодаря входу Са2+ в клетки (вход Na+ в клетки прекращается, так как странные электроуправляемые Na-каналы в начале быстрой деполяризации инактивируются). Нарастание ПД прекращается вследствие инактивации электроуправляемых Са-каналов и активации электроуправляемых К-каналов. Выход К+ обеспечивает реполяризацию, в конце которой гиперполяризация вновь активирует странные Na-каналы, и начинается новый цикл и т. д. Денервированный синоатриальный узел возбуждается до 120/мин.Характерными особенностями ПД П-клеток синоатриального узла являются меньшая крутизна подъема по сравнению с ПД клеток рабочего миокарда (электроуправляемые ионные каналы более медленные), отсутствие плато, небольшое значение ПД (70 мВ), что объясняется незначительной его инверсией и более низким потенциалом покоя -60...-70 мВ), чем у клеток рабочего миокарда (-80 мВ — рис. 13.5). Это связано с низкой проницаемостью мембраны П-клеток для К+ и повышенной проницаемостью для Na+ и Са2+, поступающих в клетку Градиент автоматии. Водителем ритма сердца явл. СА узел. Взаимодействуя с экстракардиальными нервами, они определяют частоту сокращений сердца — 60—80 в 1 мин. В случае повреждения главного узла автоматии функции водителя ритма выполняет АВ узел (40—50), далее — пучок Гиса (30 — 40 в 1 мин) и волокна Пуркинье (20 в 1 мин), т. е. имеет место градиент автоматии. Его наличие можно доказать, например, в опыте Станниуса с накладыванием лигатур между различными отделами сердца лягушки и последующим подсчетом сокращений различных отделов сердца. Активность всех нижележащих отделов проводящей системы сердца проявляется только в пат. случаях, в норме они функционируют в ритме, навязанном им СА узлом, поэтому собственный их ритм проявиться не успевает. Скорость распространения возбуждения в сердце от СА узла по рабочему миокарду и проводящей системе предсердий одинаковая — около 1 м/с. Далее возбуждение переходит на АВ узел, где имеет место задержка возбуждения на 0,05 с. Задержка объясняется тем, что проводящая синоатриальная ткань контактирует с атриовентрикулярным узлом посредством волокон рабочего миокарда, причем толщина их слоя здесь небольшая, типичные нексусы отсутствуют. Эта задержка обеспечивает последовательное сокращение предсердий и желудочков. Затем возбуждение по пучку Гиса, его ножкам и волокнам Пуркинье переходит на клетки рабочего миокарда. Скорость распространения возбуждения по проводящей системе желудочков равна 3 м/с, по субэндокардиальным окончаниям волокон Пуркинье и клеткам рабочего миокарда желудочков, как и по миокарду предсердий, 1 м/с. Большая скорость распр-я возбуждения по проводящей системе обеспечивает быстрый, практически синхронный охват возбуждением всех отделов желудочков, что увеличивает мощность их сокращений. При меньшей скорости проведения возбуждения различные отделы сердца сокращались бы не одновременно, что значительно снизило бы мощность желудочков. От проводящей системы сердца к рабочему миокарду желудочков возбуждение передается с помощью волокон Пуркинье, причем сначала на сосочковые мышцы, а затем на верхушку сердца и далее на все отделы желудочков. Но различие во времени мало, практически весь миокард сокращается одновременно. Незначительное опережение сокращений сосочковых мышц обеспечивает натяжение их нитей еще до повышения давления в желудочках и более плотное закрывание атриовентрикулярных клапанов. Таким образом, проводящая система сердца обеспечивает: 1) автоматию сердца; 2) последовательность сокращений предсердий и желудочков за счет атриовентрикулярной задержки; 3) синхронное сокращение всех отделов желудочков, что увеличивает их мощность; 4) надежность в работе сердца — при повреждении основного водителя ритма его в какой-то степени могут заменить другие отделы проводящей системы сердца, тоже обладающие автоматией. |
