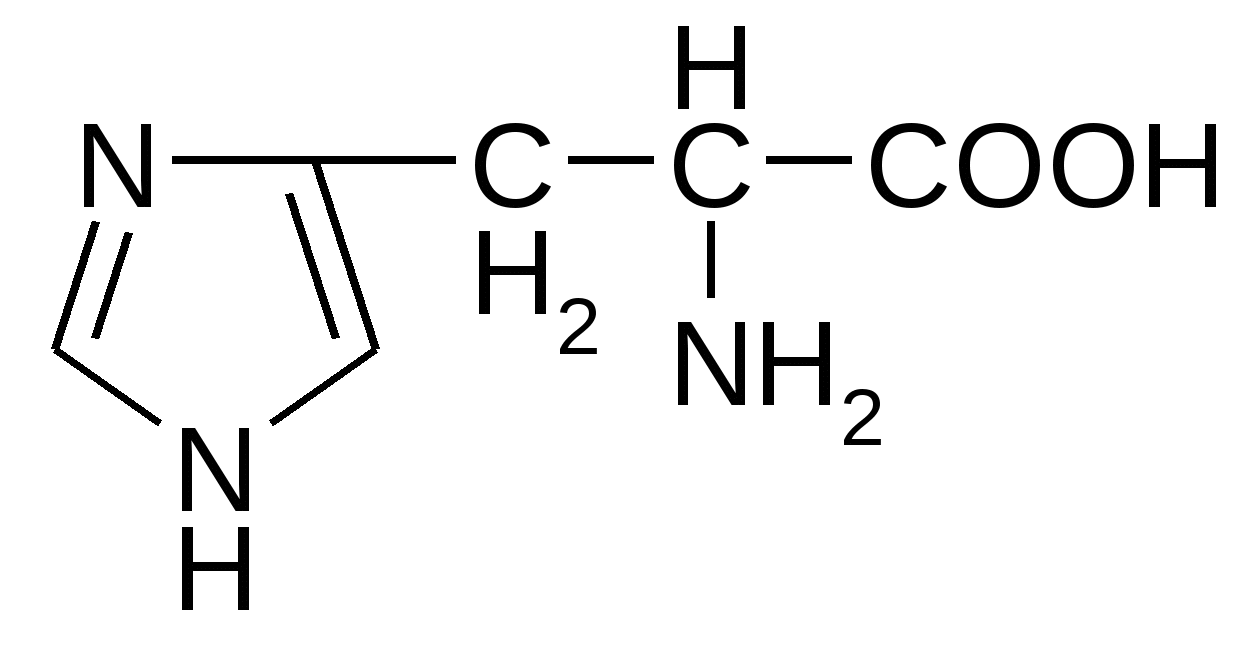
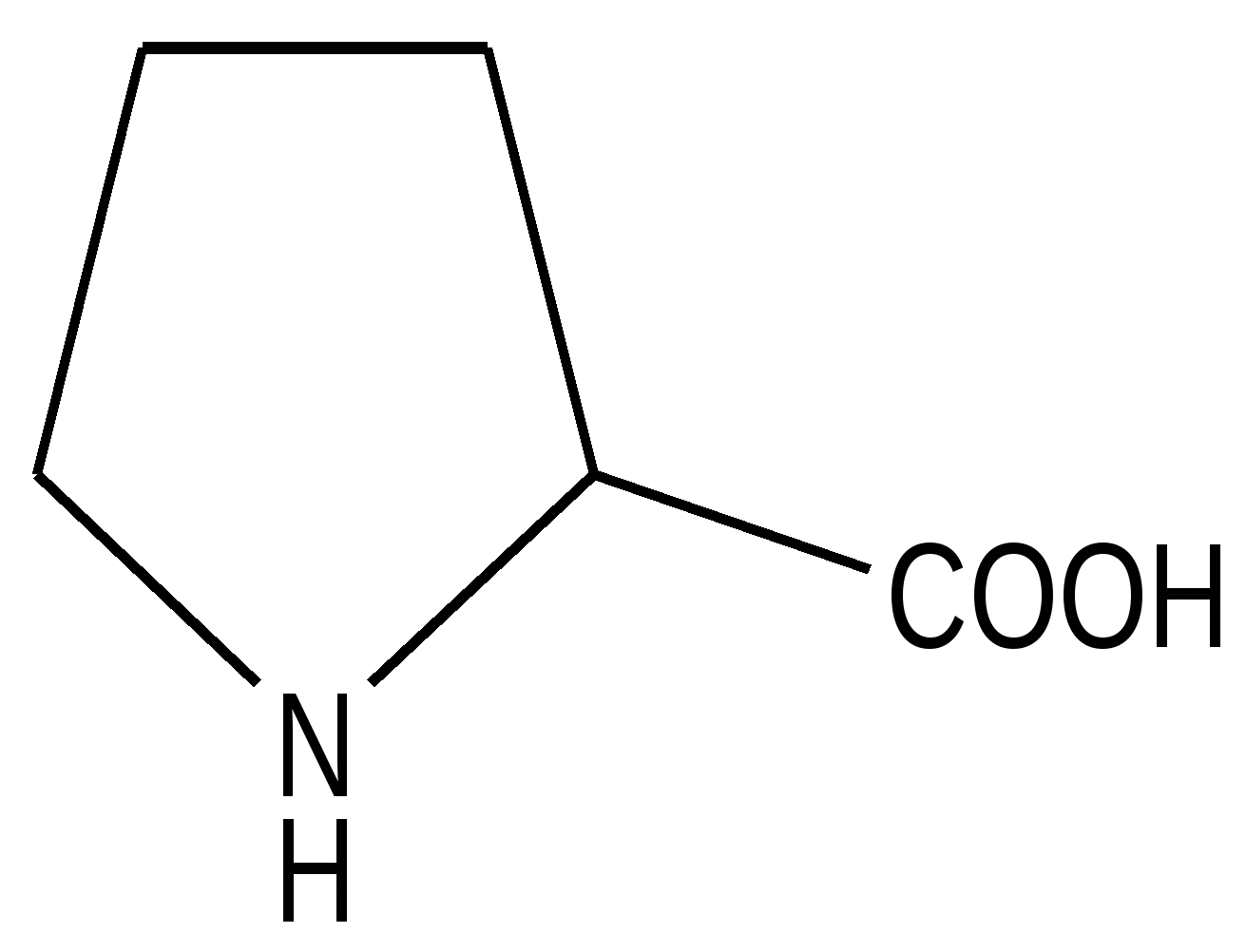
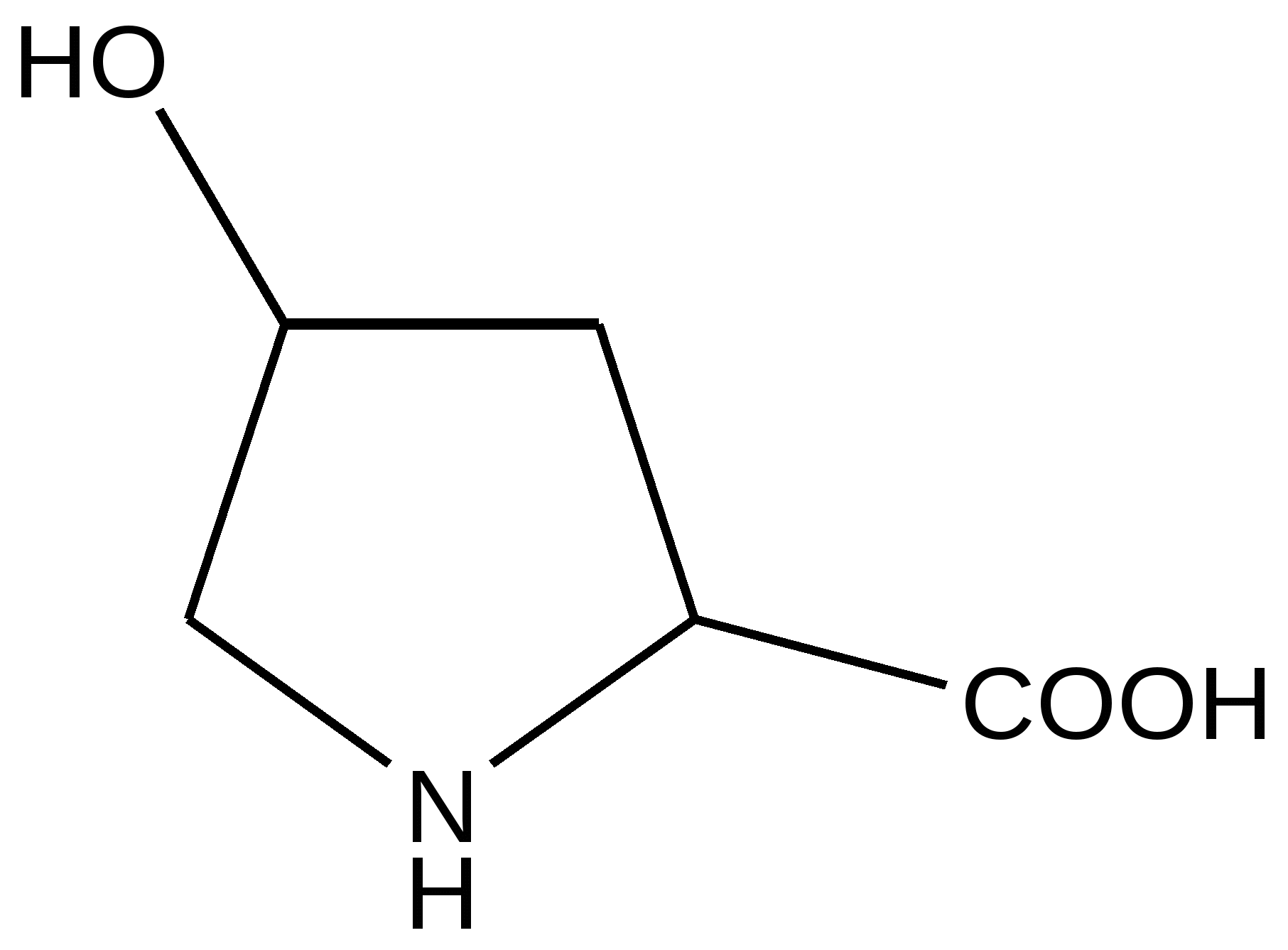
Курс лекций по биоорганической химии. Курс лекций по биоорганической химии учебное пособие для студентов 1 курса очного обучения
 Скачать 4.37 Mb. Скачать 4.37 Mb.
|
|
Элиминирование аминогруппы Реакция характерна для бактерий и грибов. Для примера можно привести превращение аспарагиновой кислоты в фумаровую Н СООН НООС- СН2-СН-СООН ———> > С = С < + NH3 | НООС Н NH2 фумаровая кислота( транс-бутендиовая) Окислительное дезаминирование Рассмотрите внимательно еще раз схему трех наиболее важных реакций трансаминирования. В двух из них участвует а-кетоглутаровая кислота, а образуется глутаминовая. Для непрерывности процесса необходимо превратить обратно глутаминовую кислоту в а -кетоглутаровую. В клетках организма человека это происходит путем реакции окислительного дезаминирования. В организме человека только глутаминовая кислота участвует в обратимой реакции окислительного дезаминирования, схема которой приведена ниже. НООС-СН2-СН2 -СН-СООН + НАД + —> НООС-СН2-СН2-С-СООН + НАДН + Н+ | | | NH2 NH глутаминовая кислота иминоглутаровая Далее иминоглутаровая кислота подвергается гидролизу , образуется кетоглутаровая кислота и аммиак НООС-СН2-СН2-С-СООН + НОН —> НООС-СН2-СН2-С-СООН + NH3 | | | | NH О а-кетоглутаровая кислота 7.7. Строение витамина В6 и механизм реакции с его участием Каталитическая роль витамина В6 в реакциях декарбоксилирования и транстаминирования аминокислот сводится к образованию промежуточного соединения - азометина ( основания Шиффа)( реакция нуклеофильного присоединения- элиминирования воды). Витамин В6 существует в трех активных формах. В реакции декарбоксилирования участвует пиридоксамин, а в переаминировании - амино- и альдегидная. 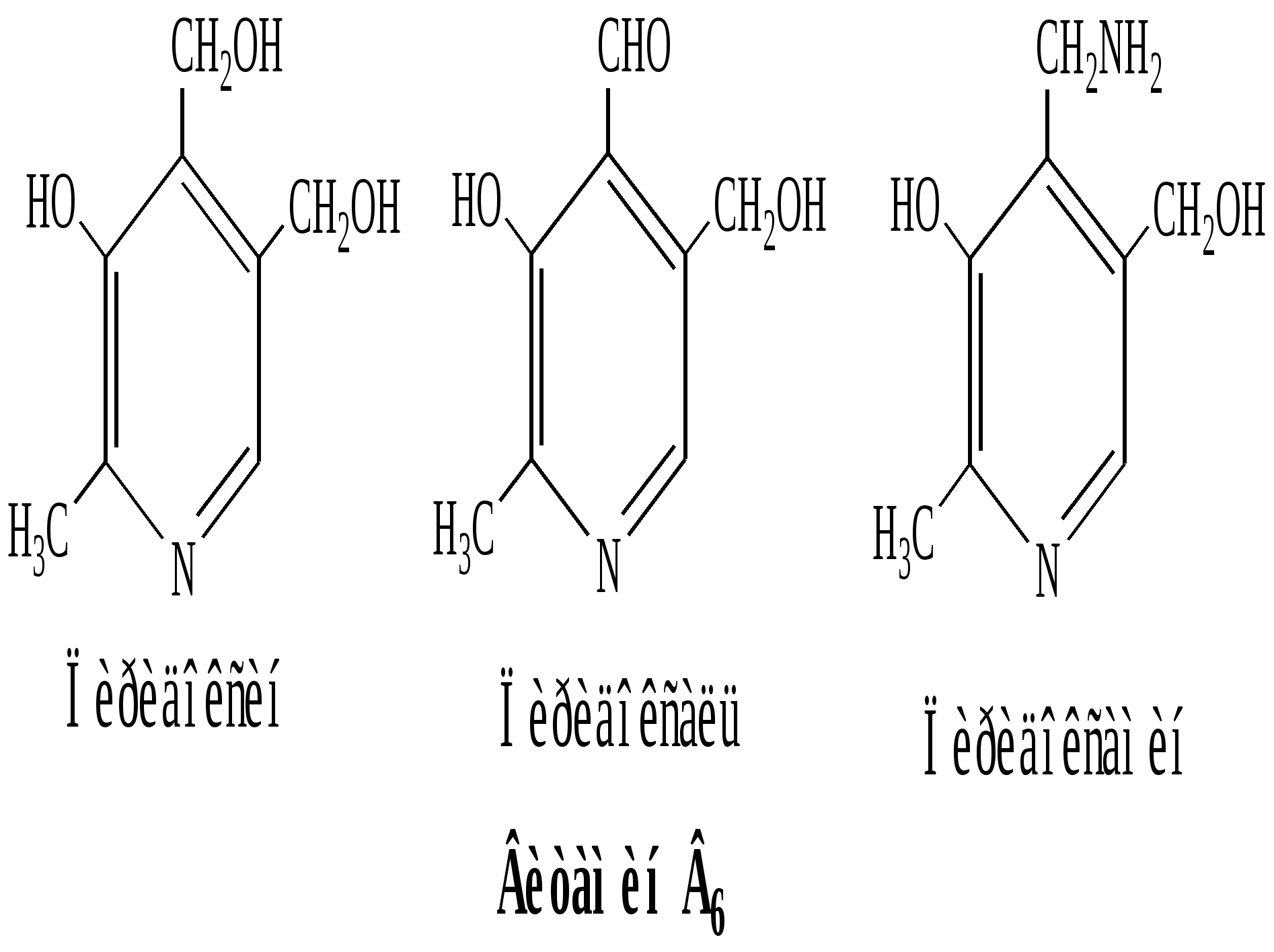 Все 3 формы витамина — бесцветные кристаллы, хорошо растворимые в воде. Активны в виде фосфорных эфиров – пиридоксальфосфата , пиридоксаминофосфата R - OH + АТФ ———> R – OРО3 Н2 + АДФ активный витамин В6 Схема реакции переаминирования - НОН изомеризация R1 - CH –COOH + В6 – СН = О < =======> R1 - CH –COOH < =======> | | NH2 N=СН - В6 аминокислота пиридоксальфосфат азометин ( 1) + НОН R1 - C –COOH < =======> R1 - C –COOH + В6 – СН2 - NH2 | | гидролиз | | N — СН2 - В6 О азометин( 2) кетокислота пиридоксаминфосфат Аминокислота реагирует с пиридоксальфосфатом - альдегидной формой витамина В6 . Образуется азометин(1), который изомеризуется в азометин (2). После гидролиза образуется кетокислота и аминоформа витамина В6- пиридоксаминфосфат. Пиридоксаминфосфат реагирует с новой кетокислотой, реакция проходит в обратном направлении в соответствии со схемой через образование азометина (2), затем азометина(1) . Кетокислота в итоге превращается в аминокислоту, а витамин В6 вновь возвращается в альдегидную форму. 7.8. Реакция поликонденсации, образование полипептидов Аминокислоты способны к поликонденсации, в результате которой образуется полимер- полиамид. Полимеры, состоящие из а – аминокислот , называются полипептидами, или пептидами. Амидная связь ( СО- NH ) в таких соединениях называется пептидной связь ( пептидной группой). Механизм реакции поликонденсации SN аналогичен реакции образования амидов кислот( см. лекцию «Карбоновые кислоты») В биологических системах синтез полипептидов происходит на рибосомах, каждая аминокислота связана с транспортной РНК , различные ацил -тРНК последовательно удлиняют полипептидную цепь в соответствии с триплетным кодом иРНК, локализованной на рибосоме. Началом полипептидной цепи является аминогруппа. содержащая свободную а-аминогруппу, а концом – содержащая свободную а- карбоксильную группу. В последовательное соединение аминокислот принято называть первичной структурой белка. NH2 - СН- СООН + NH2 - СН- СООН + NH2 - СН- СООН + … ——> | | | R1 R 2 R3 пептидная группа nН2О + NH2 - СН- СО- NH - СН- СО- [ NH - СН- СО]х - NH - СН- СООН….  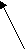 | | | | | | | | R1 R 2 R3 Rn начало цепи конец цепи N- концевая С- концевая аминокислота аминокислота N -конец С-конец Номенклатура пептидов Полипептиды называют как производные С-концевой аминокислоты, название начинают с N- концевой аминокислоты, перечисляют все по порядку( изменяя окончание на ил ), заканчивают С-концевой аминокислоой . Можно записывать полные названия, сокращенные( в латинской транскрипции или на русском языке ) Пример: глицилаланилглутамилвалин ( gly- ala – gly- val или гли-ала-глу-вал) 7. 9. Медико - биологическое значение аминокислот Кроме участия в биосинтезе белков, аминокислоты выполняют множество других самостоятельных функций.
- из аминокислоты серина образуется медиатор парасимпатической нервной системы ацетилхолин - из фенилаланина или тирозина образуется медиатор симпатической нервной системы норадреналин и гормоны адреналин, тироксин. - из глутаминовой кислоты синтезируется ГАМК 2. аминокислоты глицин, глутаминовая обладают нейромедиаторными функциями 3. аспарагиновая кислота необходима в синтезе азотистых оснований нуклеиновых кислот( аденина, гуанина, урацила, тимина, цитозина) 4. глутаминовая и аспарагиновая кислоты участвуют в обезвреживании аммиака 5. аминокислота метионин передает свою активную метильную группу для образования тимина., холина, адреналина. 6. в условиях углеводного голодания из аминокислот в организме человека синтезируется глюкоза. Поэтому аминокислоты используются в качестве лекарственных препаратов: глутаминовая, метионин, глицин, цистеин, триптофан. 7. 10. Применение аминокислот и их производных в качестве лекарственных препаратов ( Для проверки усвоения темы рекомендуем ответить на вопросы, которые содержатся в этом разделе ) Аминалон (Aminalonum) – 4- аминобутановая кислота( ГАМК)- белый кристаллической порошок с горьким вкусом. Легко растворим в воде, очень мало в спирте. Среда 5% водного раствора близкая к нейтральной( рН= 6, 5 -7 , 5) Применение связано с высокой биологической активностью в качестве тормозного нейромедиатора и участием в метаболических процессах в мозге . Применяют при сосудистых заболеваниях мозга, головными болями, сопровождающихся нарушением памяти, речи , после травм мозга и инсульта., при алкогольной болезни. У детей при нарушении нейро-психического развития, при детских церебральных параличах. Форма выпуска – таблетки. Вопросы 1. Почему это соединение плохо растворимо в спирте, хотя 1-аминобутан и бутановая кислота, содержащие одинаковое с аминалоном число атомов углерода, хорошо растворимы в спирте ? Цистеин ( Cysteinum) – 2-амино - 3- меркаптопропановая кислота Белый кристаллический порошок, легко растворим в воде. Цистеин участвует во многих метаболических процессах в организме, НS – группы участвуют в стабилизации третичной структуры белка, образовании сульфогруппы - OSO3H , которая присутствует в полисахаридах ( например, антикоагулянте крови гепарине). Цистеин необходим для обмена веществ в хрусталике глаза, недостаток цистеина способствует развитию катаракты. Цистеин применяют в виде 2% водного раствора для электрофореза, глазных ванночек, приготовления глазных капель. Выпускают порошок во флаконах из темного стекла, плотно закрытых, пробки заливают парафином. Растворы готовят непосредственно перед применением . Хранят в темном, защищенном от света месте. Вопросы
Постарайтесь записать уравнения реакций. Меркамин ( Mercaminum)-2- аминоэтантиол- 1 Оказывает профилактическое радиозащитное действие при остром лучевом поражении, в профилактических целях перед возможным облучении( космический полет), повышает устойчивость организма к действию радиации. Уменьшает возникновение свободных радикалов в тканях , защищает тиольные группы ферментов от окисления. Применяют в виде солей: хлороводородной и с аскорбиновой кислотой. Вводят внутривенно 1-2 мл в виде 10% раствора. Вопросы.
Постарайтесь написать уравнения реакций.
Цистамин – дисульфид меркамина Имеет аналогичные показания. Назначают реr оs( внутрь) Вопрос. 1. Запишите структурную формулу цистамина 2. Может ли оказывать радиопротекторное действие сам цистамин или необходимо его превращение в иное химическое соединение? Гистамин ( Histaminum ) Выпускается в виде дигидрохлорида. Белый кристаллический порошок, легко растворим в воде, рН водного раствора 4,0 – 5,0. В организме человека вырабатывается тучными клетками и выделяется в ответ на появление в организме чужеродных веществ- аллергенов. Свободный гистамин вызывает спазм гладкой мускулатуры( в том числе и бронхов), расширение капилляров, снижение артериального давления. Усиливает секрецию соляной кислоты в составе желудочного сока.Применениекак лекарственного средства ограничено . Используется в фармакологии, физиологии, биохимии для экспериментальных исследований. Вопросы.
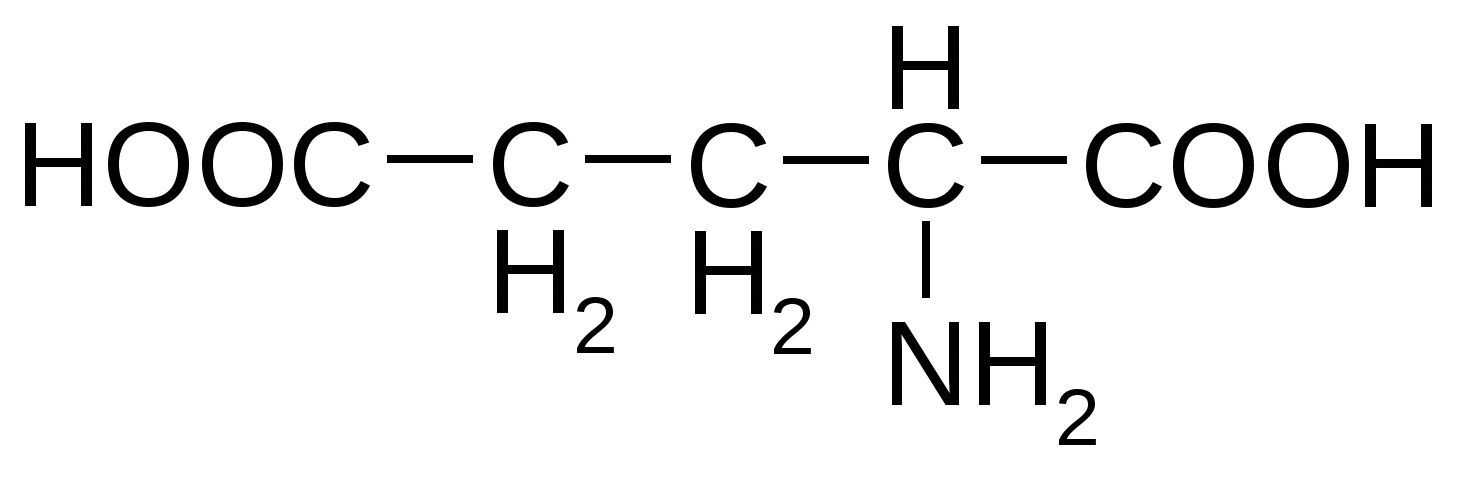
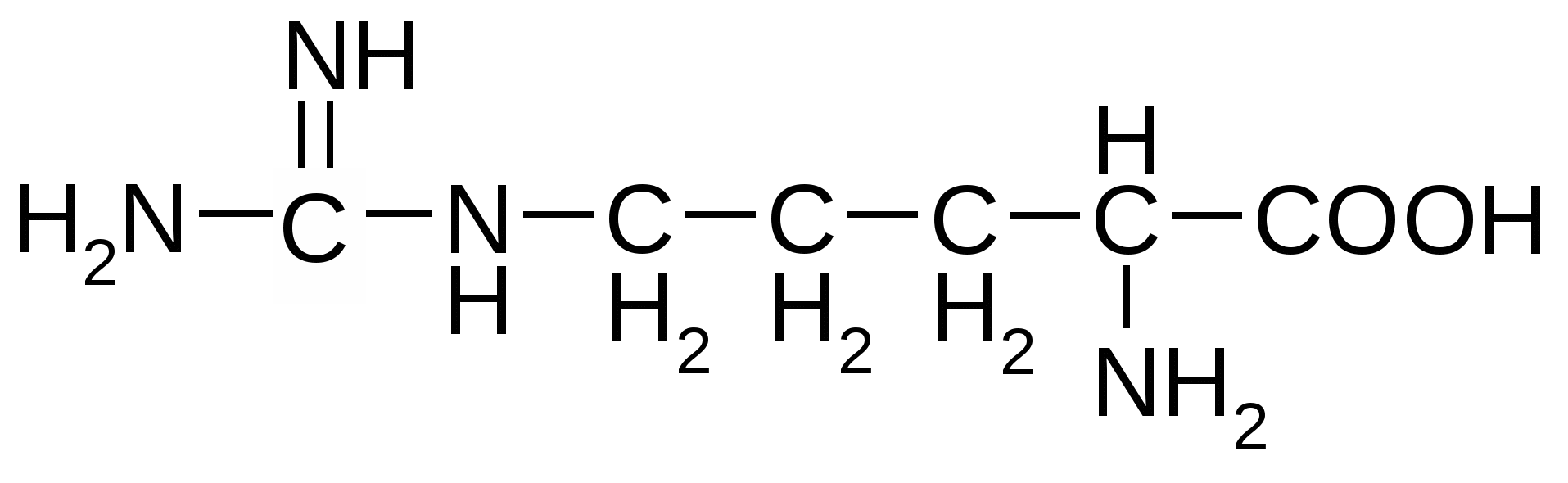
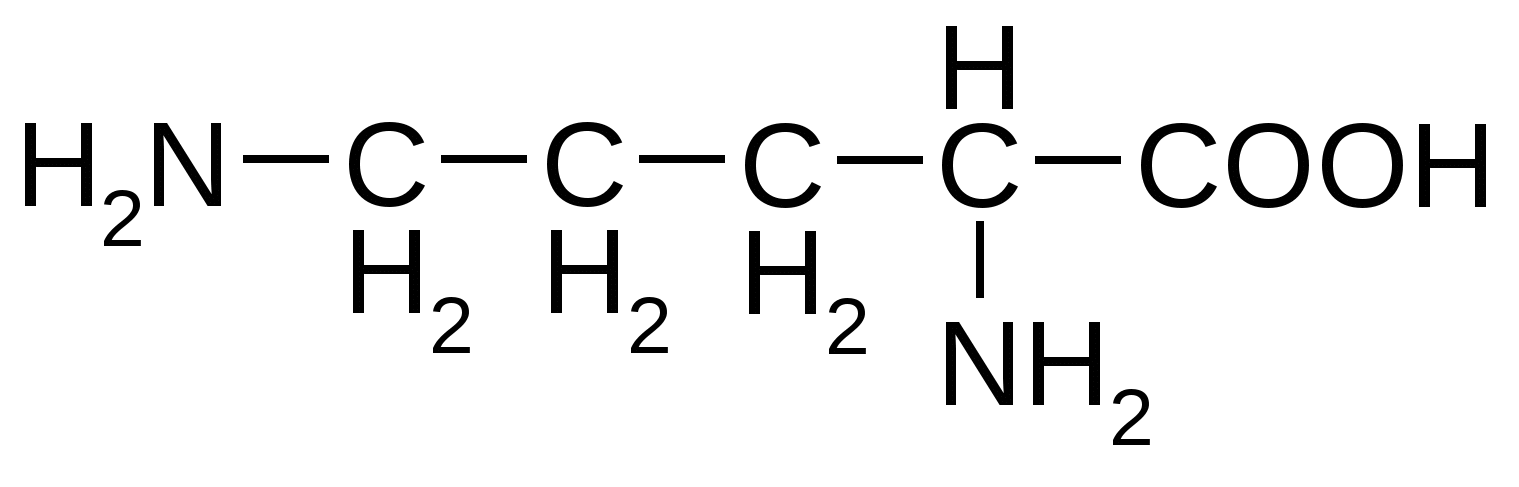
Приложение Общий список аминокислот и сокращенные обозначения ( лат) Алифатические аминокислоты моноаминомонокарбоновые Аланин( Ala ) Валин ( Val) Глицин ( Gly) Изолейцин( Ile ) Лейцин ( Leu ) Ароматические аминокислоты моноаминокарбоновые Тирозин ( Tyr ) Фенилаланин ( Phe) Гетероциклические ароматические аминокислоты моноаминомонокарбоновые Гистидин ( His ) Триптофан ( Trp ) Циклическая аминокислота Пролин( Pro ) Моноаминодикарбоновые аминокислоты и их амиды Аспарагиновая ( Asp ) Аспарагин ( Asn ) Глутаминовая ( Glu ) Глутамин( Gln ) Диаминомонокарбоновые кислоты Аргинин ( Arg ) Лизин ( Lys) Оргинитин( не входит в состав белков) Гидроксисодержащие алифатические аминокислоты Серин ( Ser ) Треонин( Thr ) Серусодержащие алифатические аминокислоты Метионин ( Met ) Цистеин ( Cys ) Гидрофобные аминокислоты : Аланин, валин, лейцин, изолейцин, метионин, пролин, триптофан, фенилаланин. Гидрофильные аминокислоты: Аргинин, аспарагиновая кислота, аспарагин, гистидин, глутаминовая кислота, глутамин, лизин. серин, тирозин, треонин, фенилаланин. L-Аминокислоты ОРГАНИЗМА Незаменимые аминокислоты обозначены звездочкой*
Алифатические аминокислоты
Кислые аминокислоты
Основные аминокислоты
Аминокислоты, содержащие амидную группу
Серусодержащие аминокислоты
Гидроксиаминокислоты
Карбоциклические ароматические аминокислоты
Гетероциклические ароматические аминокислоты
Циклические аминокислоты
Для полного усвоения темы надо знать формулы биогенных аминов( ГАМК, ß- аланин, аминоэтанол, 2-аминоэтантиол, гистамин) и амидов- глутамина и аспарагина. Кислотно-основные свойства аминокислот
данные схему образования цвиттер- иона? |

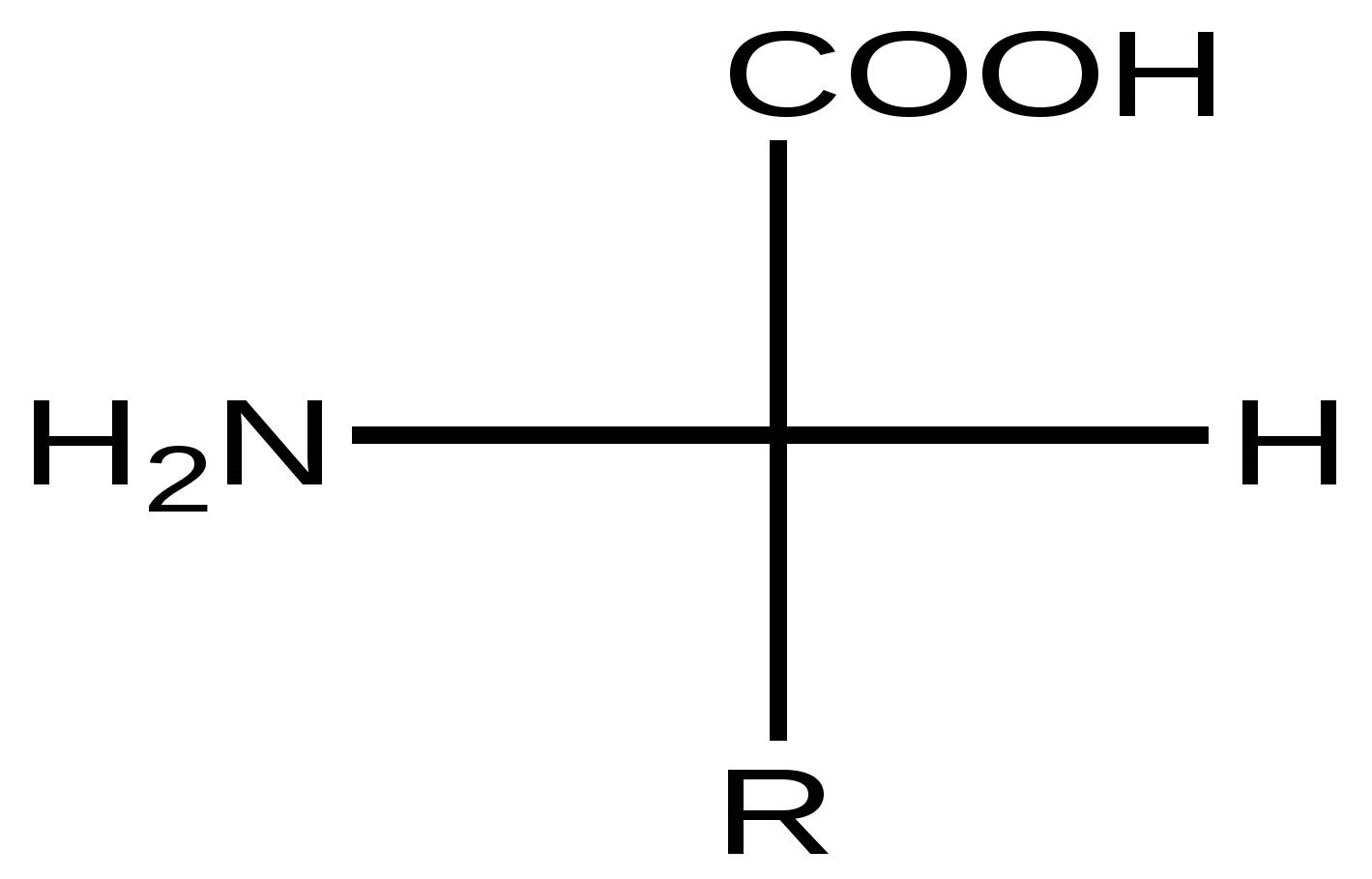
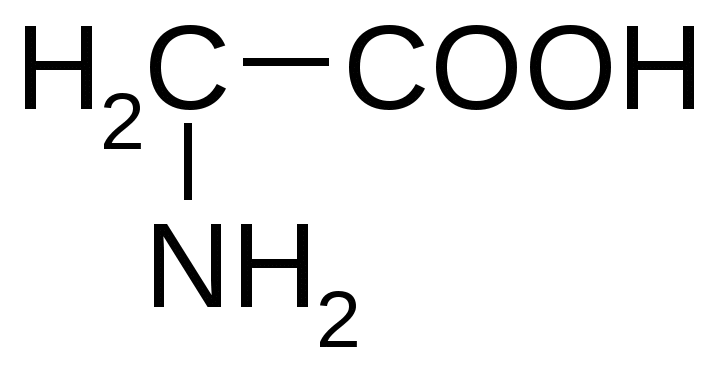
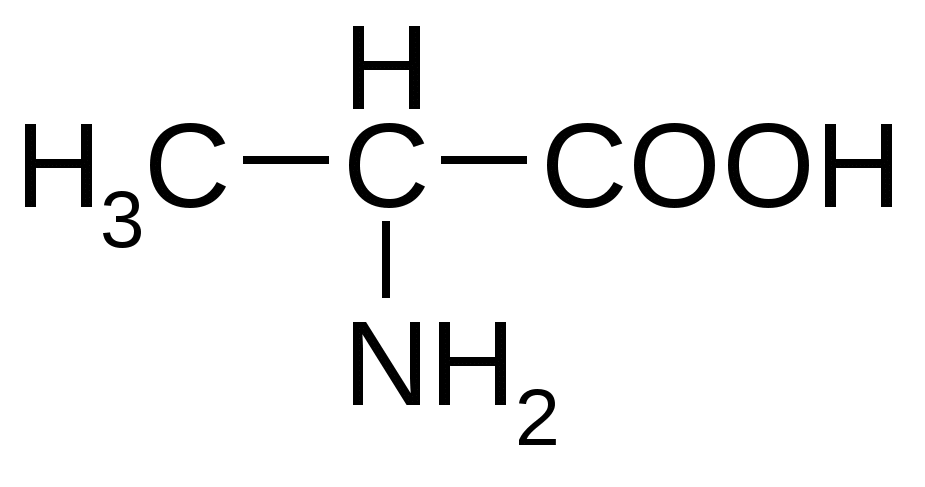
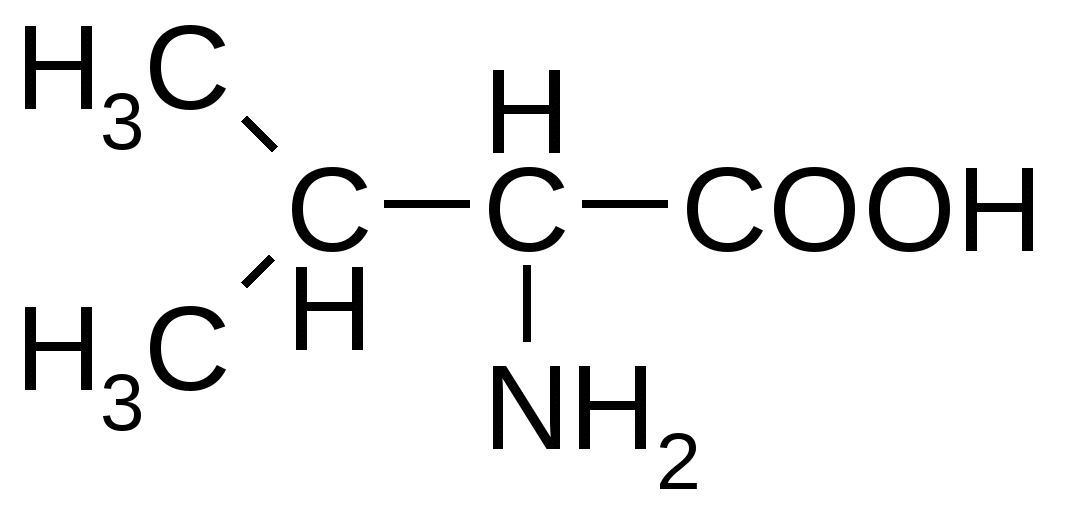
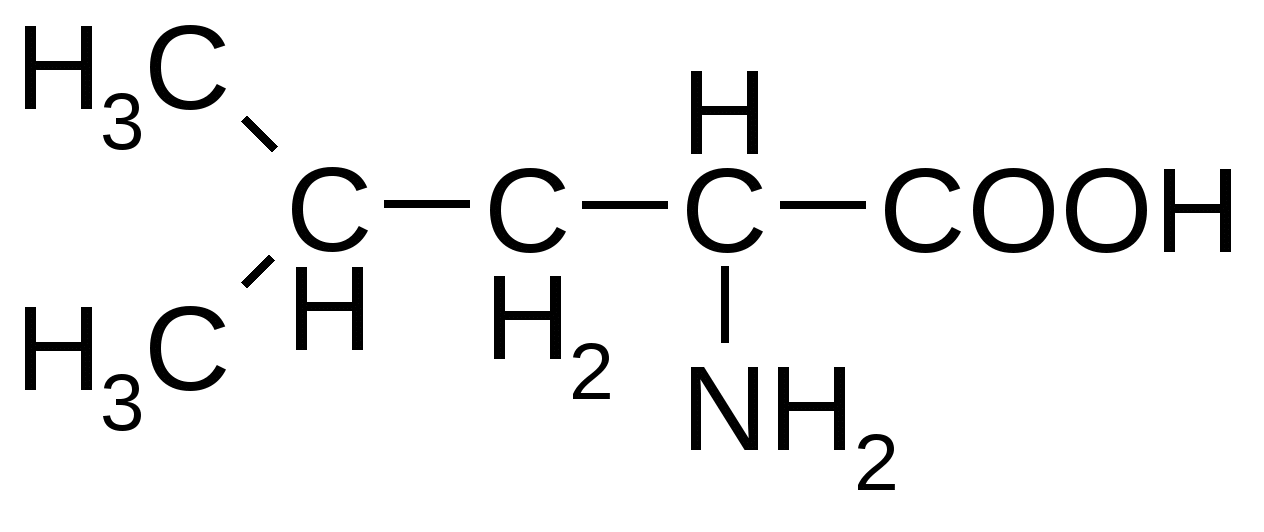
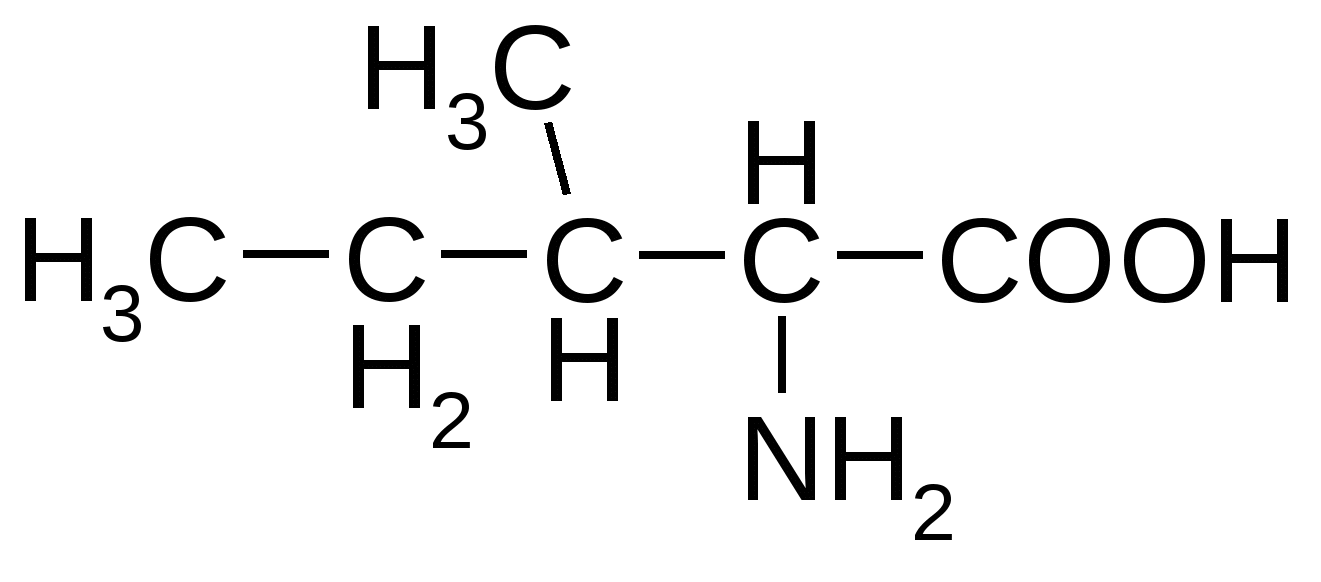
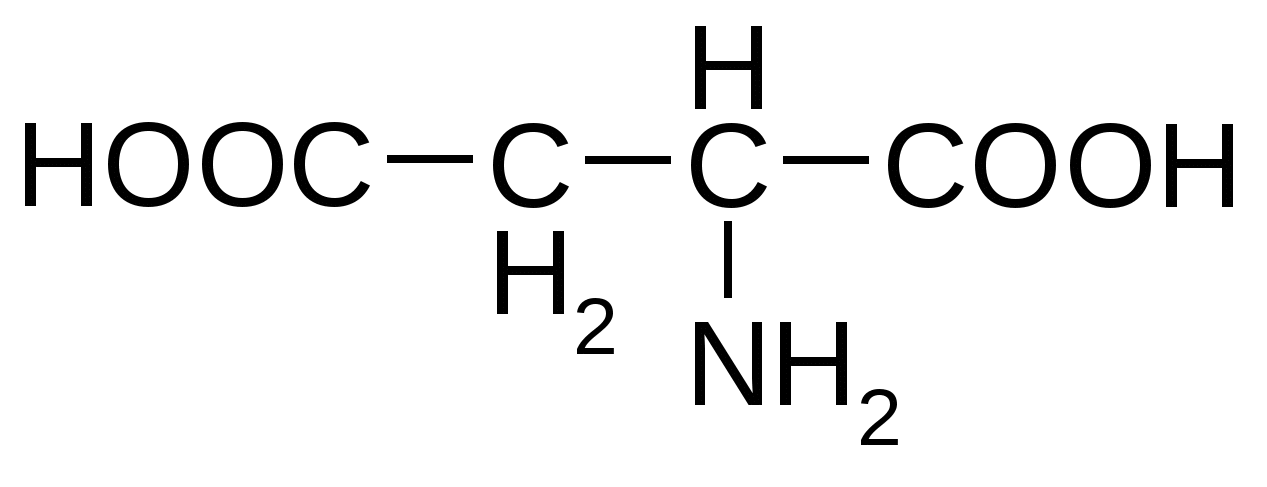
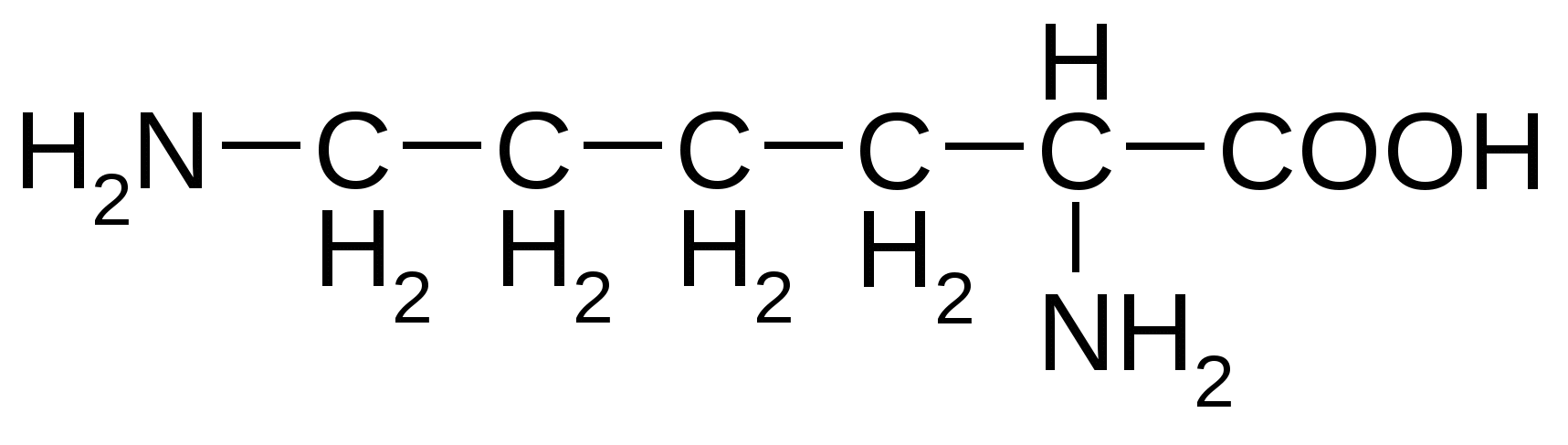
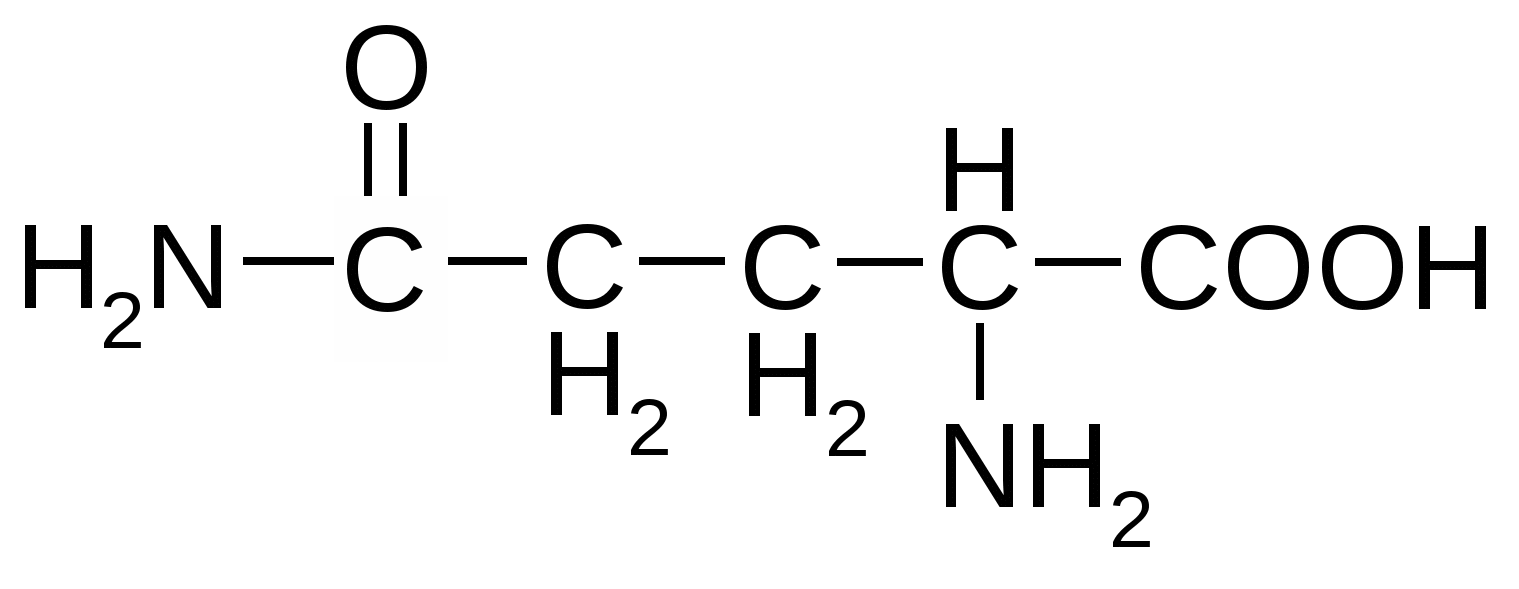
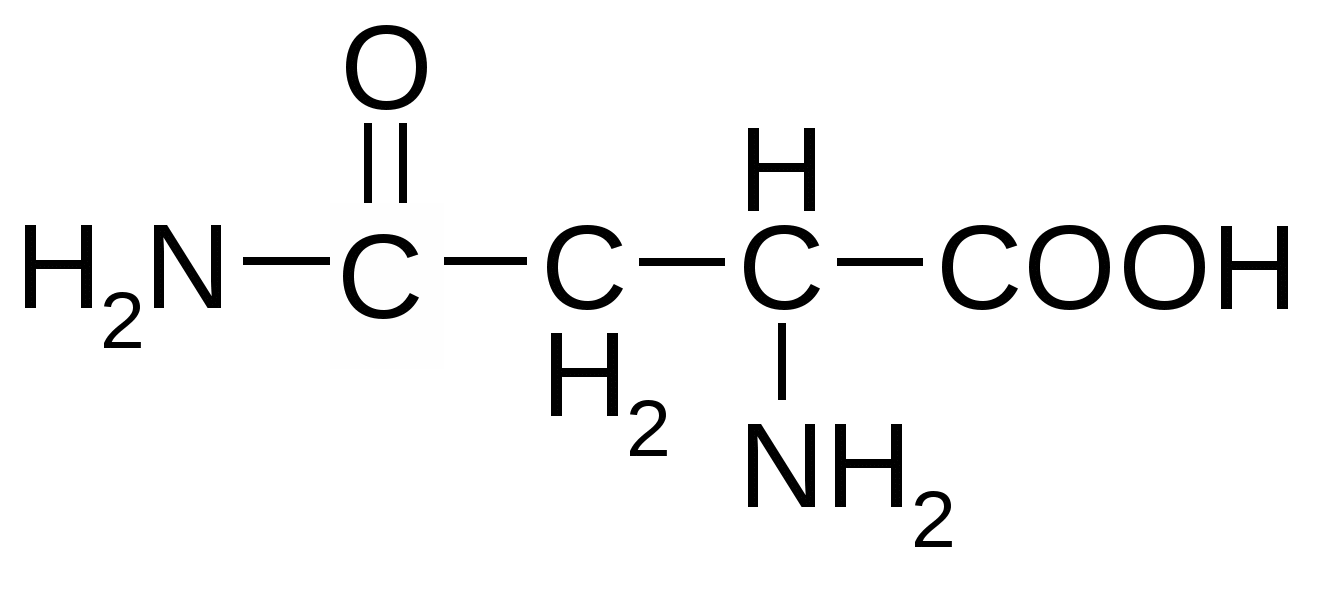
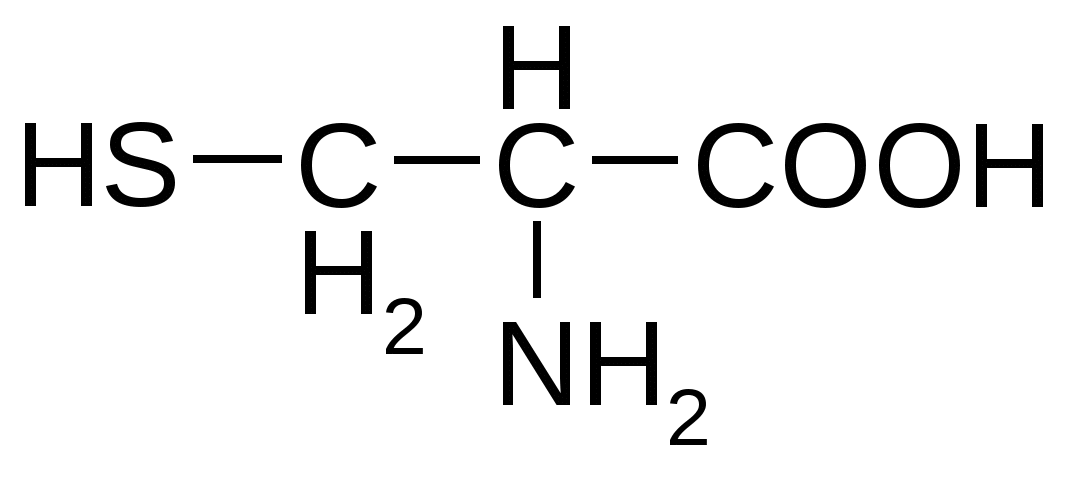
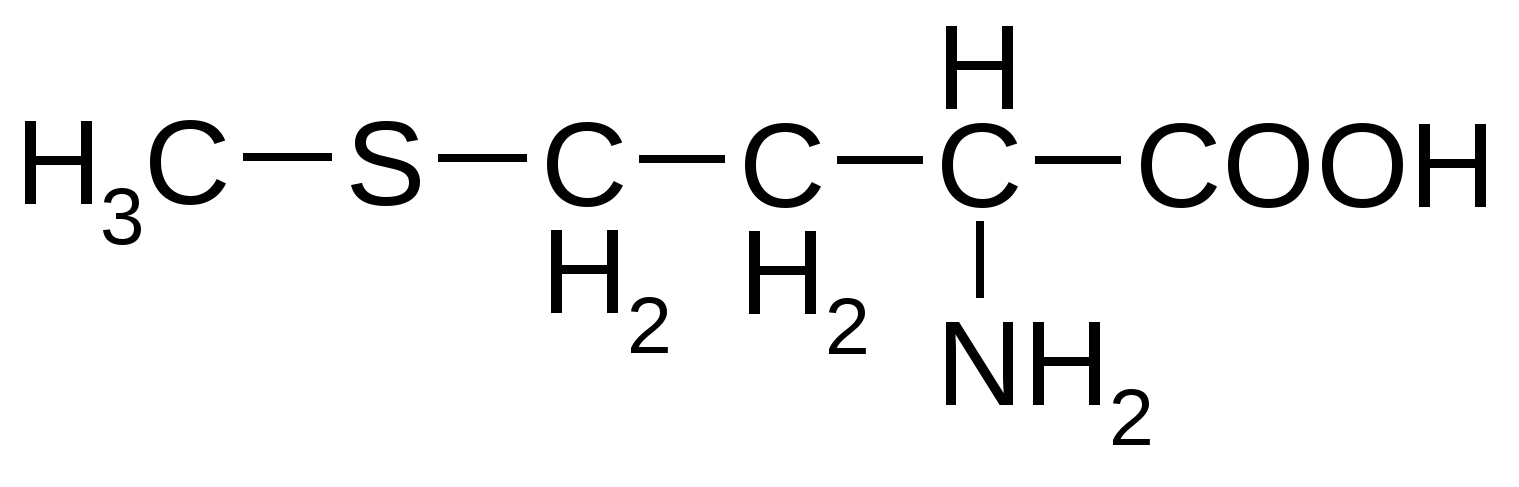
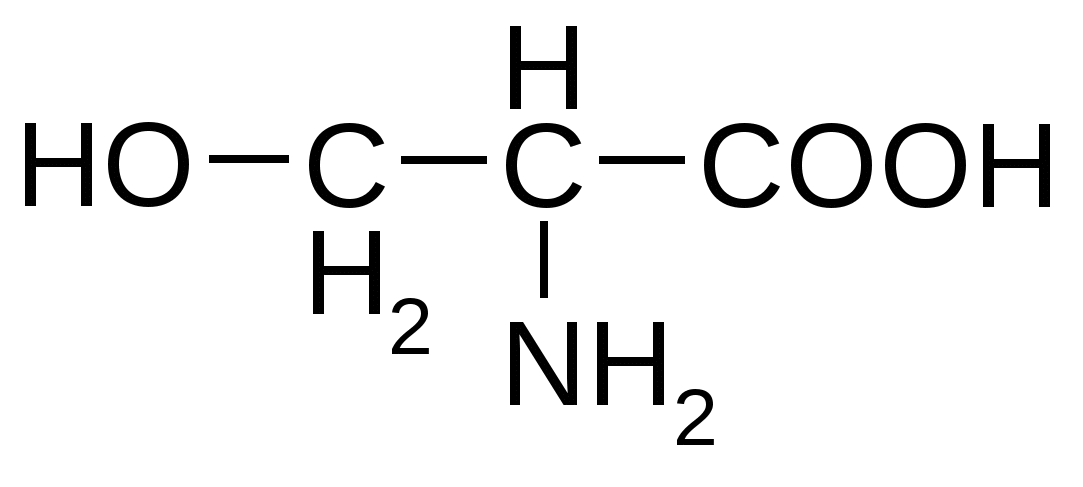
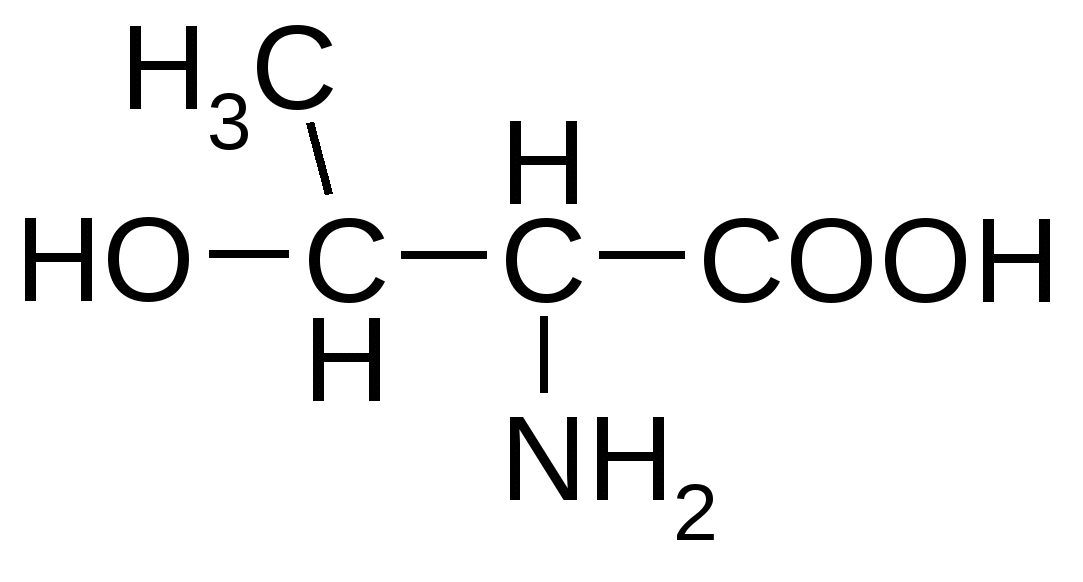
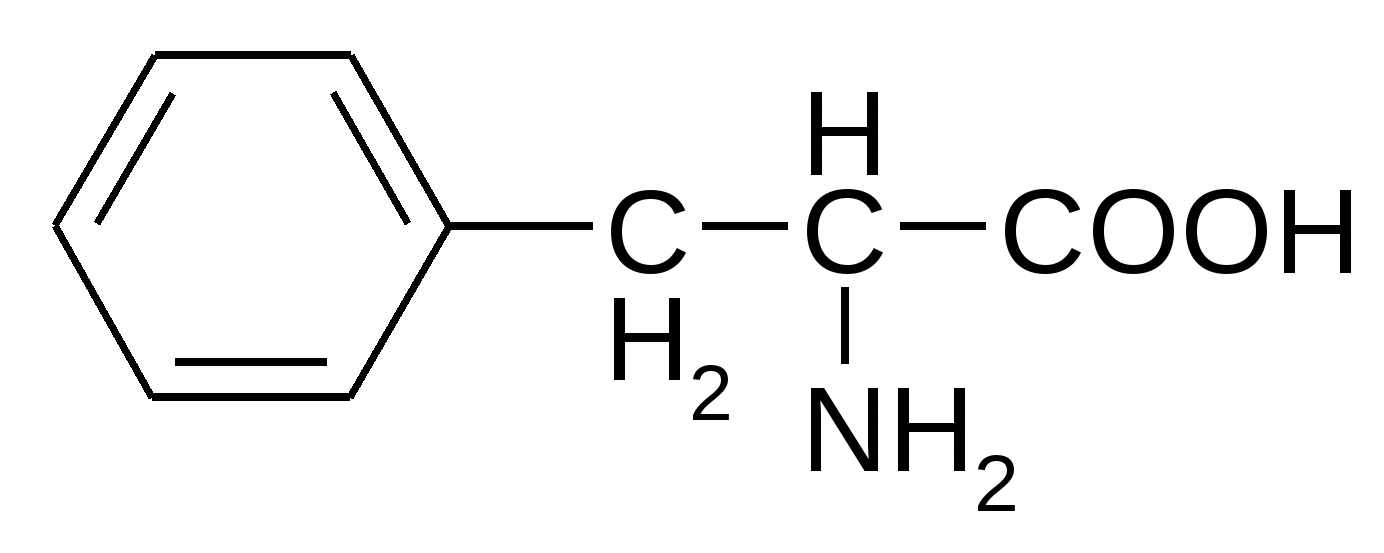
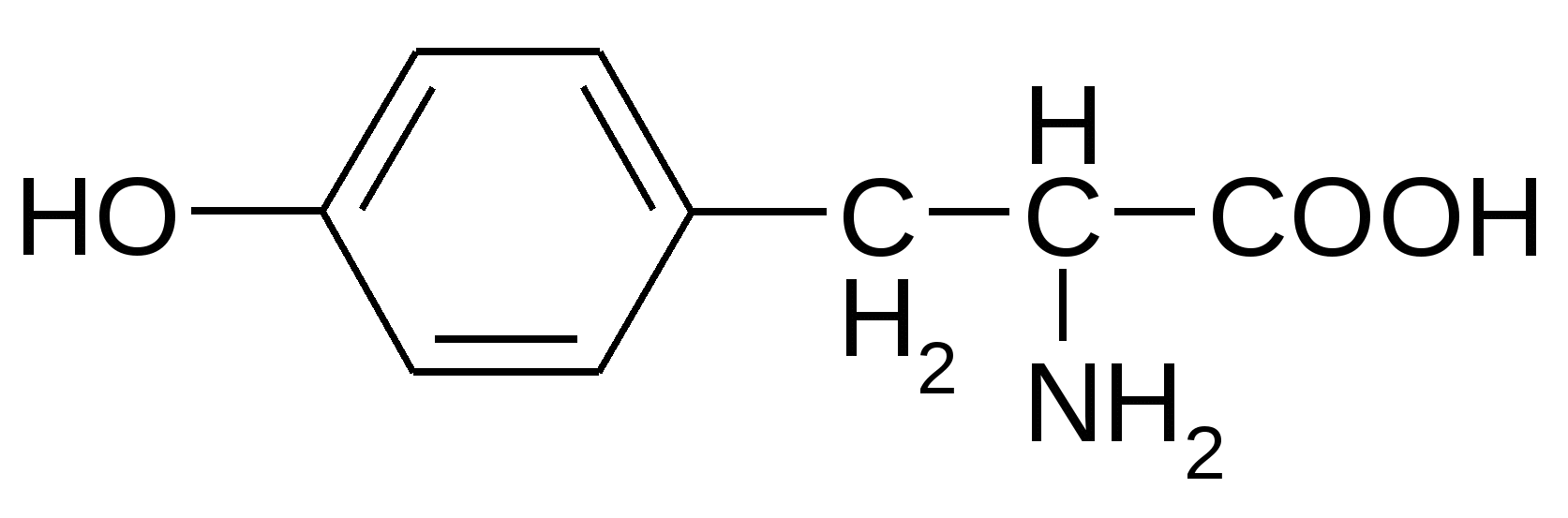
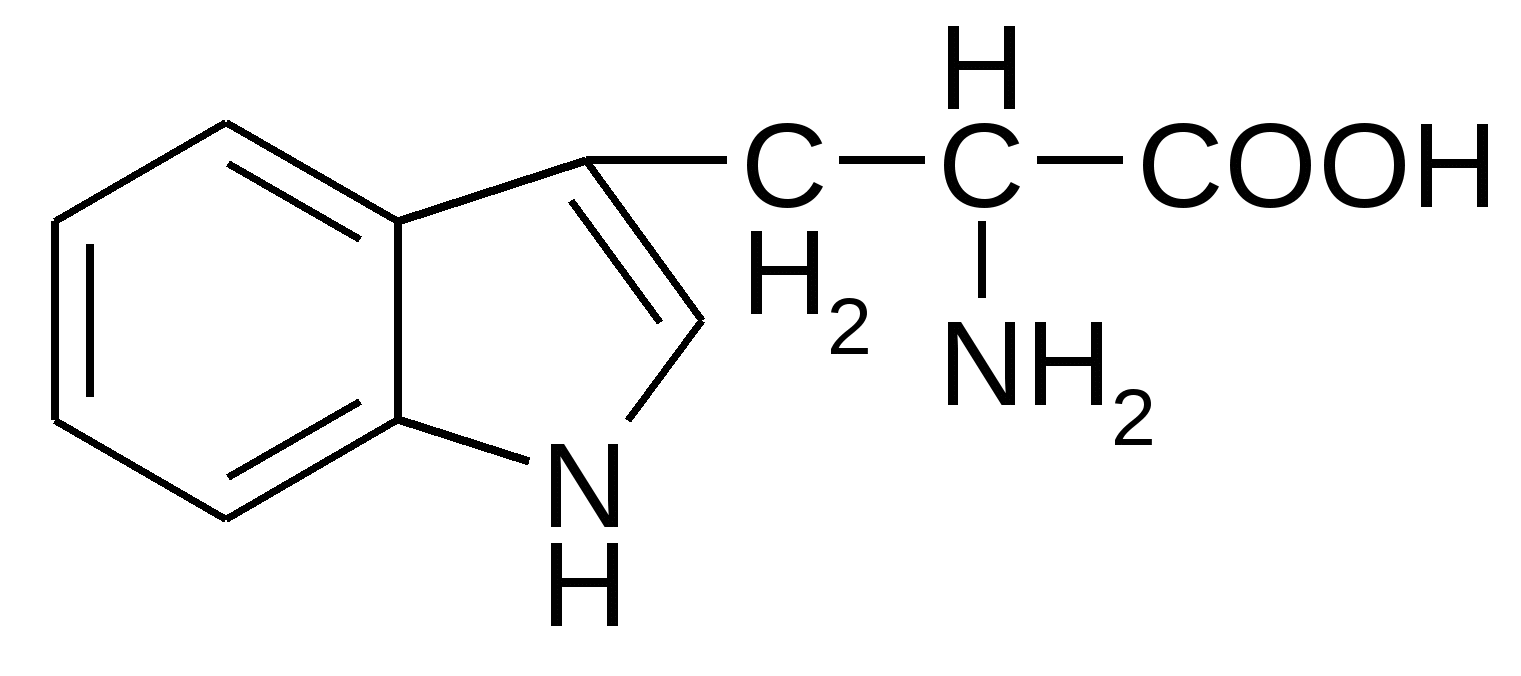 Триптофан*
Триптофан*