Лекция патология почек мочевыделительная система включает почки, мочеточники, мочевой пузырь и мочеиспускательный канал. Основные функции почек
 Скачать 185 Kb. Скачать 185 Kb.
|
Внепочечные проявления заболеваний почек1. Одним из внепочечных проявлений при остром или хроническом поражении клубочков нефрона, связанным с нарушением почечного кровотока, является артериальная гипертония. В настоящее время не вызывает сомнений, что почка способствует как повышению, так и понижению артериального давления. В эпителиоидных клетках юкстагломерулярного (околоклубочкового) аппарата почек образуется ренин-протеолитический фермент. Он соединяется с ангиотензиногеном плазмы крови, превращает его в ангиотензин I, который под действием конвертирующего фермента крови превращается в ангиотензин II, обладающий сосудосуживающим эффектом. Сосудосуживающий эффект ангиотензина II усиливается симпатическим отделом вегетативной нервной системы, альдостероном. В норме ангиотензин быстро исчезает из системы кровообращения, так как разрушается в почках под действием фермента ангиотензиназы. При нарушении гемодинамики в обеих почках их ангиотензиназная активность резко снижается, что способствует повышению артериального давления. Ренин-ангиотензиновый механизм является пусковым механизмом развития гипертонии. Тот факт, что после удаления обеих почек развивается стойкая хроническая гипертензия дали повод для предположения, что почки обладают депрессорной функцией. Нормальные почки обладают способностью контролировать действие почечных и внепочечных прессорных веществ (вазопрессин, катехоламины, альдостерон), т.е. обладают антипрессорной (противогипертензивной) функцией. Эта функция осуществляется фосфолипидным ингибитором ренина и простагландинами типа А и Е. Выключение этой функции при нарушении кровообращения в почке ведет к развитию гипертонии. Простагландины образуются в мозговом веществе почек. Контроль за секрецией простагландинов осуществляется ангиотензинном II. Повышенное его количество в плазме крови стимулирует образование простагландинов. Простагландины не только расширяют артериолы, но и вызывают усиленное выведение натрия с мочой, что также предотвращает развитие гипертонии. 2. Вторым внепочечным проявлением, связанным с поражением клубочков нефронов, является анемия. В основе развития анемии лежит нарушение функции юкстамедуллярного аппарата, выражающееся: уменьшением продукции эритропоэтина; увеличением выработки ингибитора эритропоэза. Следствием выпадения эритропоэтической функции почек является развитие анемии. Развивающаяся анемия является нормоцитарной; гипорегенераторной. В механизмах развития анемии при заболевании почек имеют значение: угнетение функций костного мозга азотистыми веществами; развивающаяся гематурия; потеря трансферрина при значительной протеинурии; дефицит цианкобаламина. 3. Третьим внепочечным синдромом является нарушение гемокоагуляции. В физиологических условиях почки участвуют в синтезе урокиназы, гепарина, факторов свертывания (V, VII, VIII, IX и X), депонировании и выделении гепарина и веществ, обладающих коагулирующим и антикоагулирующим действием. В поддержании коагуляционно-фибринолитического равновесия важную роль играет урокиназа (белок синтезируемый эндотелиальными клетками юкстамедуллярного аппарата почки). Ее роль состоит в: активации фибринолитической системы крови и мочи, направленной на растворение фибрина в сосудах клубочков; предотвращении нарушений клубочковой фильтрации и образования кровяных сгустков по ходу мочевых путей; растворении уромукополисахаридов, которые являются основой для образования мочевых камней. При очаговом и диффузном гломерулонефрите наблюдается гиперкоагуляция крови и понижение активности фибринолиза. В терминальной стадии заболевания развивается гипокоагуляция крови с клиническими проявлениями гемморрагического синдрома. УремияУремия – сложный клинический симптомокомплекс, заключающийся в аутоинтоксикации организма продуктами обмена веществ и экзогенными соединениями в норме выводимыми почками. Непосредственной причиной развития уремии является почечная недостаточность (острая или хроническая). Основными факторами повреждения тканей и органов при уремии и почечной коме являются: интоксикация организма избытком аммонийных соединений (аммиаком, производными аммония), образующихся в процессе трансформации мочевины в кишечнике; токсическое действие продуктов метаболизма ароматических аминокислот (фенол, индол, скатол); повреждение мембран и ферментов клеток; нарушение энергетического обеспечения клеток органов и тканей; нарастание ацидоза. В патогенезе уремии лежат следующие механизмы: нарушение объема фильтрации и экскреции азотистых соединений; нарушение контроля выведения воды и электролитов; расстройство метаболизма витамина Д3; снижение выработки эритропоэтина, простагландинов, кининов и др. веществ. Накопление азотистых шлаков оказывает ряд токсических эффектов: ингибирует потребление кислорода мозгом; повышает проницаемость клеточных мембран и чувствительность миокарда к гиперкалиемии; повышает агрегацию тромбоцитов; вызывает адинамию и депрессию; вызывает расстройства желудочно-кишечного тракта. Перечисленные эффекты приводят к нарушению функции и структуры большинства органов. Развивается дистрофия миокарда из-за гипоксии, дефицита макроэргов и артериальной гипертензии. В результате гиперкалиемии и гипермагниемии возникает экстрасистолия, может развиться блокада и даже остановка сердца. Развивается отек легких, нарушается функция внешнего дыхания, что проявляется дыханием Куссмауля, которое сменяется дыханием Чейн-Стокса. Анемия развивается из-за нехватки эритропоэтина. Тромбоцитопения лежит в основе кровоточивости. Азотистые метаболиты начинают выделяться через потовые железы, дыхательные пути, пищеварительный тракт, серозные оболочки и полости суставов. Следствием этого являются кожный зуд, характерный уремический запах изо рта (запах мочи и аммиака), налет мочевины на коже, слизистой рта, желудка и кишечника, рвота, понос, перикардит, плеврит. Перикардит проявляется шумом трения перикарда у основания сердца. Этот шум называют «похоронным звоном». Нарушения со стороны нервной системы выражаются психической депрессией, потерей сознания, коматозным состоянием, судорагами, параличами жизненно важных центров. Эти нарушения связаны с интоксикацией, гипоксией, расстройством кислотно-основного равновесия. Терминальным признаком уремического отравления является гипотермия. Температура тела падает до 32 и даже 30°С. Смерть наступает при низкой температуре тела. Для нормализации нарушений гомеостаза и очищения крови больных от «уремических токсинов» применяют гемодиализ – искусственную почку, что позволяет продлить жизнь таких больных на несколько лет. Более радикальным методом является пересадка почки. Нефротический синдромНефротический синдром это клинико-биохимический симптомокомплекс, характеризующийся высокой протеинурией (до 10-20 г/сутки), гипопротеинемией, гиперхолестеринемией и развитием распространенных отеков. По происхождению нефротический синдром бывает первичным и вторичным. В основе возникновения первичного нефротического синдрома чаще всего лежит генетически обусловленный дефицит обмена веществ (липоидный нефроз) или трансплацентарный перенос специфических противопочечных антител от матери к плоду (врожденный семейный нефроз). Вторичный нефротический синдром развивается при: хронических инфекционный процессах; нефропатии беременных; сахарном диабете; системной красной волчанке; амилоидозе; стафилококковом сепсисе; сывороточной болезни; отравлении солями тяжелых металлов; обширных ожогах; радиационном поражении; применении некоторых лекарственных средств (сульфаниламиды, кортикостероиды, пенициллины); при болезнях системы крови. Основой развития нефротического синдрома является увеличение проницаемости стенки капиллярных сосудов для плазменных белков, обусловленной иммунологическими механизмами. Источниками антигенов могут быть экзогенные факторы: бактериальные, вирусные, паразитарные, лекарственные, пищевые и др. Эндогенными антигенами могут быть ДНК, денатурированные нуклеопротеины, белки опухолевого происхождения и др. Антитела, продуцируемые в ответ на антигены, принадлежат к классу IgM. Механизм развития отеков при нефротическом синдромеВыраженная протеинурия, обусловливает гипоальбуминемию, это приводит к понижению онкотического давления в плазме и усиленному выходу жидкости из сосудов в межклеточное пространство. Возникает гиповолемия, это активирует ренин-ангиотензин-альдостероновую систем, в результате повышается секреция альдостерона и антидиуретического гормона. Это приводит к задержке в организме воды и натрия. Объем крови увеличивается, но происходит ее разжижение, нарастает гипопротеинемия и гипоонкия, в связи с чем вода не задерживается в кровяном русле и перемещается в ткани, способствуя развитию отеков. 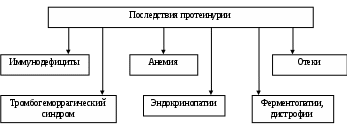 Последствия потери белков при нефротическом синдроме. При нефротическом синдроме развивается гиперлипидемия, в крови повышается содержание холестерина, триглицеридов, фосфолипидов. Гиперлипидемия патогенетически связана с нарушением белкового обмена и угнетением липолитической активности плазмы крови.  Патогенез отеков при нефротическом синдроме. В результате повышения проницаемости сосудистой стенки при нефротическом синдроме происходит усиленное выведение с мочой белковых субстанций, в том числе иммуноглобулинов, факторов свертывания, витаминсвязывающих белков, трансферрина и других металлосвязывающих белков. 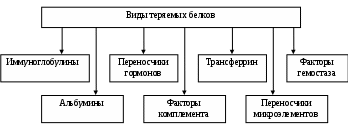 Белки, теряемые организмом при нефротическом синдроме. В связи с этими потерями наблюдается склонность к тромбоэмболии, понижению устойчивости к инфекциям, развитию железодефицитной анемии, развитию гиповитаминозов Д и С, гипокальциемии. Скачано с www.znanio.ru |
