МЯДЕЛЕЦ ОБЩ.ГИСТ.. Литература для медицинских вузов все факультеты о. Д. Мяделец основы цитологии, эмбриологии и общей гистологии
 Скачать 4.75 Mb. Скачать 4.75 Mb.
|
|
СВЯЗЬ ЗАРОДЫША С ОРГАНИЗМОМ МАТЕРИ. ПЛАЦЕНТА Тесная связь зародыша с организмом матери начинает формироваться с момента имплантации, т.е. на седьмой день эмбрионального развития Мы можем предположить наличие этой связи и раньше, т.е. в момент продвижения зиготы по яйцеводам: именно в это время происходит переход зародыша от аутотрофного типа питания (за счет собственных питательных веществ) к гистотрофному питанию — питанию за счет секрета половых путей. Однако наиболее тесная связь двух организмов устанавливается с момента образования плаценты (плацентация) и перехода к ге-мотрофному (из крови матери) типу питания. ПЛАЦЕНТА. Плацента выполняет такие функции: 1. Трофическая. Через плаценту поступают все необходимые для развития зародыша вещества. 2. Депонирующая. В плаценте депонируются многие необходимые для организма соединения: макро- и микроэлементы, витамины С, A, D, Е и др. 3. Плацента — орган дыхания плода. Через нее из крови матери к плоду поступает кислород, в противоположном направлении выделяется углекислый газ. 4. Экскреторная функция — выделение из организма плода в кровь матери конечных продуктов обмена. 5. Эндокринная функция: начиная с четвертого месяца эмбриогенеза желтое тело ослабляет свои функции, и плацента берет на себя выработку многих гормонов, регулирующих развитие плода и протекание беременности. Эти гормоны такие: — прогестерон и релаксин; — эстрогены; — хориогонический гонадотропин. Он способствует сохранению беременности за счет стимуляции желтого тела. Вторая важная роль этого Гормона — подавление функции лимфоцитов матери. В результате не Происходит иммунологическая реакция на ткани плода со стороны материнского организма; — соматомаммотропин, или плацентарный лактоген, стимулирующий рост ацинусов молочной железы; — фактор роста фибробластов; — трансферрин, связывающий необходимое для нормального эмбриогенеза железо, а также участвующий в предотвращении иммунологического конфликта (см. ниже); — кортиколиберин. Предполагают, что этот гормон может предопределять срок наступления родов; — плацента синтезирует (а возможно, просто депонирует) ряд гормонов типа гипофизарных: тиротропин, адренокортикотропин, мелантотро-пин. Очевидно, эти гормоны участвуют в регуляции развития собственного гипофиза плода; — плацента синтезирует андрогены и кортикоиды. Местом синтеза плацентарных гормонов является симпластотрофоб- ласт. 6. Плацента регулирует процессы свертывания и фибринолиза крови, которая омывает ее ворсины. 7. Барьерно-защитная, детоксикационная и иммунологическая функции плаценты. Ряд веществ не проходит через плаценту из крови матери к плоду. Однако барьерная роль плаценты не абсолютна, зависит от свойства повреждающего вещества, срока беременности и состояния организма матери. В последнее время установлено, что в течение всей беременности мать и плод отличаются друг от друга по антигенам. При этом между ними возникают иммунные взаимоотношения, которые не переходят в иммунный конфликт. Таким образом, плацента формирует иммунный барьер между организмом матери и организмом плода. Механизмы этого барьера будут рассмотрены позднее. РАЗВИТИЕ ПЛАЦЕНТЫ. Источником развития плаценты является хорион. Из него образуется плодная часть плаценты. Кроме того, в образовании плаценты участвует часть эндометрия, которая является источником развития материнской части плаценты. Хорион, или ворсинчатая оболочка, развивается из трофобласта и внезародышевой мезенхимы. Его развитие подробно описано выше. Материнская часть плаценты формируется из децидуальной оболочки. При наступлении беременности эндометрий резко утолщается. Особенносильно утолщается его функциональный слой, формирующий децидуаль ную (отпадающую) оболочку. По мере.увеличения размеров зародыша де цидуальная оболочка разделяется на три неравномерные части. Располо женная под эмбрионом часть формирует материнскую часть плаценты и называется базальной частью (deciduabasalis). В базальной части содер жится много маточных желез, исчезающих после 6-го месяца беременное ти. Расположенная над эмбрионом часть децидуальной оболочки является капсулярной частью (deciduacapsularis). По мере развития плода она вы пячивается в полость матки и срастается с пристеночной, или париетальной, частью децидуальной оболочки (deciduaparietalis). Эта часть покры вает всю незанятую плодом часть полости матки. В пристеночной и кап сулярной частях децидуальной оболочки постепенно исчезают железы и децидуальные клетки, напротив, в базальной части эти клетки увеличива ются в количестве и размерах. Базальная часть децидуальной оболочки дифференцируется на два слоя: наружный губчатый и внутренний компактный (см. рис. 5.9). Третичные ворсины хориона, сильно ветвясь, образуют в большом количестве протеолитические ферменты, которые разрушают вначале ком пактный, затем губчатый слои базальной отпадающей оболочки и спиралевидные артерии, из которых изливается кровь, омывающая ворсины хориона и формирующая гемохориальное пространство, или лакуны. Это происходит на 6-й неделе беременности. Базальная децидуальная оболочка подвергается разрушению на различную глубину: та ее часть, которая находится между ворсинами, разрушается незначительно и формирует соединительнотканные септы. Неразрушенный глубокий слой базальной децидуальной оболочки эндометрия и септы формируют материнскую часть плаценты. Котиледоны как структурно-функциональные единицы плаценты начинают формироваться после 50-го дня беременности, их образование заканчивается к 4-му месяцу, когда в плаценте имеется 10—12 больших, 40—50 мелких и до 150 рудиментарных катиледонов. СТРОЕНИЕ ПЛАЦЕНТЫ. В зависимости от строения у млекопитающих различают четыре типа плацент (рис. 6.4): — эпителиохориальные; — десмохориальные; — эндотелиохориальные; — гемохориальные. В плацентах первого типа слизистая оболочка матки не разрушается. Трофобласт тесно прилегает к эпителию эндометрия. Питательные вещества поступают к плоду через стенку капилляров, перикапиллярное пространство из РВНСТ и неповрежденный эпителий эндометрия. Такие плаценты имеют место у лошадей, свиней, верблюдов. В плаценте десмохориального типа ворсины хориона полностью разрушают эпителий слизистой оболочки матки и частично — ее соединительную ткань. Такой тип плацент у коров, овец. В плацентах эпителиохориального и десмохориального типа хорион осуществляет расщепление белков, поступающих из крови матери, до аминокислот и биосинтез белков, специфических для эмбриона. В эндотелиохориальных плацентах происходит разрушение всех оболочек сосудов эндометрия, за исключением эндотелиального слоя. Эти плаценты встречаются у кроликов. В гемохориальных плацентах разрушается и эндотелиальный слой, при этом ворсины непосредственно контактируют с кровью матери. Такие плаценты характерны для приматов, в том числе и для человека. Поскольку в эндотелиохориальных и особенно в гемохориальных плацентах возможно непосредственное усвоение аминокислот из материнской крови, в этих плацентах хорион не выполняет протеолитическую функцию. 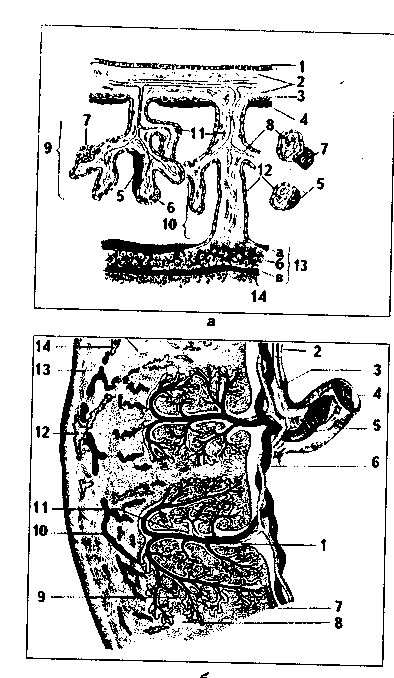 Таким образом, при эволюции плацентная связь организма матери и плода становилась все более тесной. ПЛОДНАЯ ЧАСТЬ ПЛАЦЕНТЫ (рис. 6.5, 6.6). Представлена хориаль-ной пластинкой, от которой отходят ворсины. Хориальная пластинка образована РВНСТ, в которой находятся кровеносные сосуды и многочисленные макрофаги (клетки Гофбауэра—Кащенко). Снаружи хориальная пластинка покрыта трофобластом, разделенным на цито- и симпластотрофобласт. Цитотрофобласт представлен однослойным эпителием. Со второго месяца эмбриогенеза он начинает исчезать. Во второй половине беременности истончается и в отдельных участках может исчезать также симпластотрофобласт. В этих участках из фибрина и компонентов распада трофобласта образуется фибриноид (фибриноид Нитабух), слой которого в некоторых случаях очень выражен, причем фибриноид может пропитывать на большую толщину соединительную ткань хориальной пластинки. Достаточно часто в хориальной пластинке встречаются децидуальные клетки, мигрировавшие из базальной пластинки.  Отходящие от хориальной пластинки ворсины имеют древовидную форму. Часть ворсин доходит до базальной пластинки материнской части плаценты и прикрепляется к пей. Это якорные ворсины, фиксирующие хорион к матке. Ворсины, как и хориальная пластинка, покрыты снаружи трофобластом, а внутри содержат соединительную ткань с макрофагами Гофбауэра—Кащенко. Со второго месяца эмбриогенеза цитотрофобласт ворсин начинает исчезать, а во второй половине беременности истончается, и в отдельных участках может исчезать также симпластотрофобласт. Такие участки ворсин, лишенные трофобласта, также покрываются фибриноидом. Этот фибриноид называется фибриноидом Лангханса. Ворсина хориона вместе с ее многочисленными ветвлениями, ограниченная септами, формирует структурно-функциональную единицу плаценты, которая называется КОТИЛЕДОНОМ. Лакуны (гемохориальное пространство) содержат в целом до 150 мл по стоянно обновляющейся материнской крови, омывающей ворсины и по ставляющей к плаценте питательные и регуляторные вещества, а также кислород. Из гемохориального пространства кровь оттекает в краевой си нус, а затем в маточные вены. Общая поверхность ворсин, на которой про исходит контакт с кровью, составляет около 14 кв. м. МАТЕРИНСКАЯ ЧАСТЬ ПЛАЦЕНТЫ. Представлена базальной пластинкой и соединительнотканными септами, отделяющими котиледоны друг от друга. Базальная пластинка представляет собой глубокий (губ чатый) слой отпадающей оболочки эндометрия. В местах контакта базальной пластинки с якорными ворсинами трофобласт с ворсин мигрирует на базальную пластинку и септы, покрывая их. Этот трофобласт называется периферическим трофобластом. Во второй половине беременности он постепенно атрофируется и заменяется фибриноидом (фибриноид Рора). (Полагают, что фибриноид Рора имеет некоторые гистохимические и биохимические отличия от фибриноидов Лангханса и Нитабух наряду с отличиями топографическими.) В базальной пластинке в большом количестве содержатся децидуаль-ные клетки. Это крупные, богатые гликогеном клетки с оксифильной цитоплазмой и крупными ядрами. Они могут мигрировать по септам в хори-альную пластинку. Считают, что часть этих клеток имеют костномозговое происхождение и являются макрофагами, участвующими в иммунных реакциях. По мере дифференцировки плаценты децидуальные клетки претерпевают изменения: вначале резко увеличены и сходны с фибробласта-ми. Затем их размеры еще более увеличиваются, клетки приобретают округлую форму, ядра становятся более светлыми, клетки располагаются очень плотно. К 4—6-й неделям эмбриогенеза количество клеток несколько уменьшается. Все децидуальные клетки по морфологическому принципу разделяют на большие и малые, а по функциональному — на макрофаги, эндокриноциты (апудоциты) и натуральные киллеры (NK-клетки). Функции децидуальных клеток следующие: 1) органичивают разрастание трофобласта; 2) принимают участие в образовании фибриноида; 3) появились данные, что часть этих клеток являются эндокринными, вырабатывающими ряд гормонов: простагландины, гормон, подобный прогестерону, биогенные амины; 4) вырабатывают вещества типа тромбопласти-на. 5) оказывают иммуносупрессивное действие на материнские иммуно-компетентные клетки. ПЛАЦЕНТАРНЫЙ БАРЬЕР. Это барьер между кровью матери в лакунах и кровью плода в сосудах ворсин. В состав этого барьера на разных этапах эмбриогенеза входят разные структуры (рис. 6.7). В первую половину беременности его образуют следующие компоненты: 1. Эндотелий капилляров ворсин непрерывного типа. 2. Непрерывная базальная мембрана капилляра. 3. Гемохориальное пространство из РВНСТ с макрофагами Гофбауэра—Кащенко. 4. Базальная мембрана трофобласта. 5. Цитотрофобласт. 6. Симпластотрофобласт. Во вторую половину беременности цитотрофобласт и симпластотрофобласт начинают исчезать, и тогда вместо них в состав барьера входит фибриноид Лангханса. Плацентарный барьер препятствует проникновению в кровь плода ряда токсических веществ, бактерий. Однако он не является идеальным барьером, так как пропускает вирусы (в том числе и вирус коревой краснухи, играющий большую роль в возникновении аномалий развития), алкоголь, никотин и ряд других веществ, которые могут вызвать нарушение эмбрионального развития и уродства. Через барьер могут проходить даже некоторые клетки, в частности, лимфоциты как материнской, так и плодной крови. 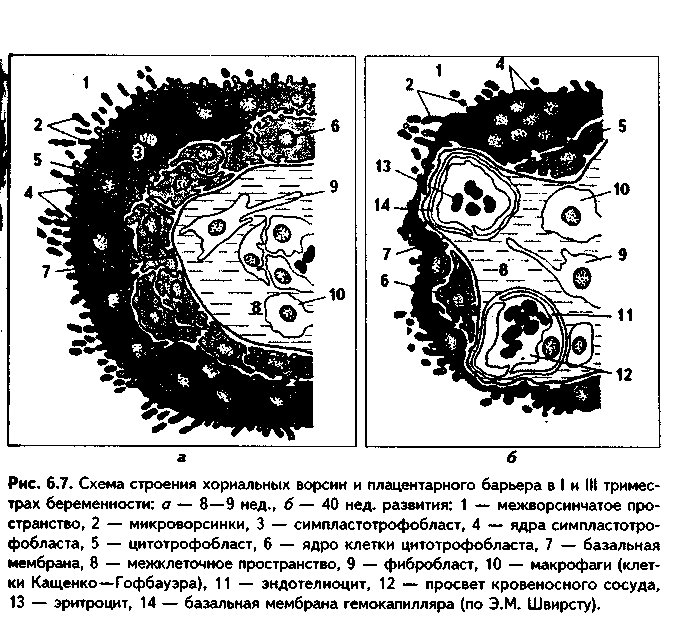 ПЛОДНЫЕ ОБОЛОЧКИ. Развивающиеся зародыш и плод окружаются плодными оболочками (рис. 6.8). Наиболее внутреннее положение занимает амниотическая оболом ка. По мере роста плода она m > более приближается к безвор синчатому хориону, а затем е< соединительнотканный слой не плотно срастается с соедините;! >. ной тканью хориальной плат тинки. Снаружи от хориона рас полагается decidua capsularis которая при доношенной беременности хорошо различим;! только в нижнем полюсе. В кап сулярной децидуальной оболочке отсутствует поверхности ый эпителий. К капсулярной децидуальной оболочке тесно прилежит и даже срастается с ней безворсинчатый хорион. Та ким образом, амниотическая, хо-риальная и капсулярная дециду-альная оболочки тесно соприкасаются друг с другом. ФУНКЦИЯ плодных оболочек заключается в ограничении амниоти-ческого пространства и поддержании гомеостаза амниотической жидкости. Накануне родов плодные оболочки естественно или искусственно разрываются. Это ведет к отхождению околоплодных вод, что является одним из пусковых моментов родов. 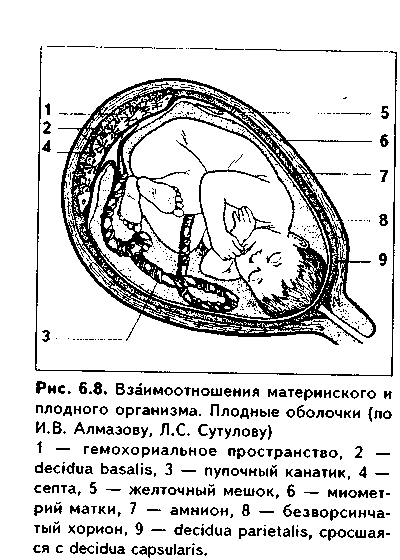 ПОНЯТИЕ О ФУНКЦИОНАЛЬНОЙ СИСТЕМЕ «МАТЬ-ПЛОД» Основным результатом нормально протекающей беременности является рождение здорового жизнеспособного ребенка. Следовательно, вся деятельность женского организма во время беременности направлена на обеспечение нормального развития плода. Эта деятельность определяется постоянной координацией функций двух организмов: матери и плода. Главным связующим звеном между ними является плацента. Так формируется функциональная система "мать—плацента—плод" или просто "функциональная система "мать—плод", ФСМП. Разработка представлений о ФСМП полностью является заслугой советских ученых: А.А. Логинова, Н.А. Гармашевой и их учеников. ФСМП состоит из двух подсистем: функциональной подсистемы "мать"(ФСМ) и функциональной подсистемы "плод"(ФСП). Каждая из подсистем включает рецепторные, регуляторные и исполнительные звенья, i между которыми происходят постоянные взаимодействия, в том числе и щ по принципу обратной связи (рис. 6.9). Основными физиологическими параметрами, регулируемыми ФСМП, являются: частота сердцебиений плода, величина артериального давления, концентрация в крови кислорода и углекислого газа, величина осмотического давления плазмы, показатели рН, концентрация питательных и биологически активных веществ, интенсивность двигательной активности плода и др. Рецепторы в материнском организме располагаются в матке, кровеносных сосудах, а в организме плода — в пупочных сосудах, коже и кишечнике. Регуляторные механизмы включают нервную, эндокринную и иммунную системы как организма матери, так и организма плода. Исполнительные механизмы обеспечиваются различными специфическими органами материнского и плодного организма. При этом между одноименными системами органов и органами матери и плода устанавливаются тесные связи. 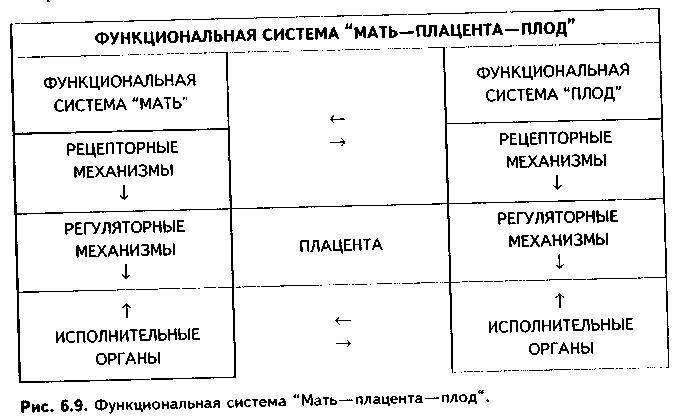 При нарушениях в ФСМП происходят отклонения от нормального развития плода. Так, если мать страдает сахарным диабетом, то повышается продукция инсулина островковым аппаратом поджелудочной железы плода, что приводит к увеличению массы плода (рождение ребенка с массой 4 кг и более является одним из признаков скрытого сахарного диабета у матери и является показанием к детальному се обследованию). При поражении ш"■■ ни у матери патологические изменения в этом органе наблюдаются и у пл* да, а при резекциях части материнской-печени в печени плода в легких сд\ чаях отмечается полная потеря гликогена, в тяжелых случаях — некроз уч;к тков паренхимы. Взаимоотношения в ФСПМ можно проиллюстрировать также на приме ре иммунологических взаимоотношений. ИММУНОЛОГИЧЕСКИЕ ВЗАИМООТНОШЕНИЯ ОРГАНИЗ МА МАТЕРИ И ОРГАНИЗМА ПЛОДА. Плод является своего рода се миаллотрансплантантом в организме матери, потому что на 50% состой: из чужеродных для организма матери антигенов. Однако в норме иммунная реакция отторжения не происходит, напротив, возникает иммун нологическая терпимость, толерантность. Механизмы ареактивности организма матери по отношению к организму плода достаточно сложны м обеспечиваются рядом факторов. Они могут: А. Продуцироваться плацентой; Б. Продуцироваться в организме матери; В. Синтезироваться в организме зародыша и плода. А. Факторы, связанные с плацентой. Симпластотрофобласт содержит несколько факторов, блокирующих иммунную систему матери: а) блокирующее действие фибриноида. В нем много сиаломуцинов, которые формируют отрицательный заряд, препятствующий взаимодействию симпластотрофобласта с лимфоцитами крови матери; б) симпластотрофобласт синтезирует белки, блокирующие иммунную систему матери. В первую очередь к ним относится трансферрин; в) в симпластотрофобласте вырабатывается и поддерживается высокая концентрация гормонов с выраженным иммуносупрессивным действием: хориогонический гонадотропин, прогестерон, эстрогены, а также кортизолс-вязывающий глобулин; г) полная изоляция друг от друга кровеносных систем плода и матери за счет плацентарного барьера; д) утрата симпластотрофобластом способности синтезировать антигены в иммуногенной форме. Установлено, что в симпластотрофобласте отсутствуют HLA-антигены, тогда как другие клетки ворсинок несут эти антигены. Кроме того, имеющиеся антигены трофобласта маскируются блокирующими антителами, а также упоминавшимися трансферрином и фибриноидом; е) в трофобласте вырабатываются лизины — факторы, разрушающие Т-лимфоциты и NK-клетки материнского организма; ж) в материнской плаценте часть децидуальных клеток, а также NK-клетки вырабатывают белки с иммуносупрессивным действием. Б. Факторы, продуцируемые в организме матери: а) повышенный синтез надпочечниками глюкокортикоидов, обладающих иммуносупрессивным действием; б) синтез фактора ранней беременности (ФРБ). Этот фактор впервые обнаруживается в крови матери чс]ю:{ G—72 ч после оплодотворения. Место синтез ФРБ в организме матери не установлено. Данный фактор является одним из наиболее ранних иммуносупрессивных факторов. Механизм его действия включается в супрессии Т-лимфоцитов и натуральных киллеров организма матери. При нарушении продукции ФРБ наступает самопроизвольный выкидыш. Определение ФРБ в сыворотке крови женщины может быть использовано для ранней диагностики беременности. Предполагается, что кроме материнского организма источником ФРБ может явиться зигота; в) синтез блокирующих антител, в том числе и антител, подавляющих созревание цитотоксических Т-лимфоцитов против антигенов плода; г) образование в большом количестве Т-супрессоров. Они формируются в регионарных маточных лимфоузлах. В. Факторы, синтезируемые в организме зародыша и плода: а) Т-супрессоры; б) лимфокины; в) альфафетопротеин; г) фактор ранней беременности (?); д) в амниотической жидкости накапливаются иммуносупрессивные факторы. Кроме указанных факторов, определенную роль играет блестящая зона (ZP), существующая до стадии бластоцисты. Она, во-первых, аналогична по антигенному составу материнскому организму, во-вторых, препятствует проникновению к зародышу Т-лимфоцитов матери. Вместе с тем показано, что сама блестящая зона содержит антигены, воспринимаемые иммунной системой матери как чужеродные. У страдающих бесплодием женщин в крови часто обнаруживают антитела к ZP. ИММУНОЛОГИЧЕСКИЕ ОСЛОЖНЕНИЯ БЕРЕМЕННОСТИ. В ряде случаев указанных механизмов защиты плода недостаточно, и антигенная несовместимость матери и плода может привести к иммунноло-гическому конфликту. К наиболее частым его вариантам относятся: гемолитическая болезнь новорожденных (при несовместимости по резус-фактору); аутоиммунная нейтрофилоцитопения, при которой в тяжелых случаях возникают воспалительные процессы, бактериемия, заканчивающиеся летально; тромбоцитопеническая пурпура; привычное невынашивание беременности и самопроизвольный аборт. В последнем случае иногда применяют трансплантацию женщине кусочков кожи супруга для выработки толерантности. Изменения и нарушения нормальных иммунологических взаимоотношений в системе "мать—плод" могут также привести к аномалиям, уродствам, различным болезням потомства, смерти зародыша или плода. Могут быть проявления конфликта и со стороны женского организма. К ним относятся бесплодие, поздние токсикозы беременных. ИММУНОЛОГИЧЕСКИЕ ПОДХОДЫ К РЕГУЛЯЦИИ ФЕРТИЛЬ НОСТИ. Существует два аспекта регуляции фертилыюсти: 1) борьба с бесплодием, обусловленным иммунологическим конфликтом: 2) использование иммунологических методов для контрацепции. Примером решения вопросов, связанных с первым аспектом, являете! предупреждение резус-конфликта, иммунотерапия спонтанных абортов, блокада антиспермальных антител и. т.д. Иммунологические методы контрацепции могут быть различными: 1. Иммунизация антигенами спермы; 2. Иммунизация антигенами блестящей оболочки; 3. Иммунизация стадиоспецифическими антигенами (т.е. антигенами, появляющимися у зародыша на определенных стадиях развития); 4. Иммунизация гормонами, отвечающими за нормальное протекание беременности; 5. Иммунизация ФРБ. В настоящее время уже получены вакцины против хориогонического гонадотропииа, люлиберина, белков спермы, антигенов ZP. Для их клинического применения необходимо решить проблемы, связанные с безопасностью использования и побочными эффектами. ОСНОВНЫЕ КОМПОНЕНТЫ ЭМБРИОНАЛЬНОГО РАЗВИТИЯ Нормальный эмбриогенез обеспечивается целым рядом механизмов, которые называются компонентами эмбриогенеза. Эти компоненты уже рассматривались при освещении гистогенеза: 1. Размножение клеток. 2. Рост клеток. Эти два явления приводят к увеличению количества клеток и их размеров, а в целом — к увеличению размеров зародыша. 3. Детерминация, или выбор пути дифференцировки клетки. Этот путь закрепляется в геноме клеток путем активации одних и репрессии других генов. Детерминированные клетки похожи друг на друга по морфологии, но различаются набором активных генов. Детерминация инициируется многими внутриядерными, внутриклеточными и внеклеточными веществами. В самих генах имеются участки, включающие ген (эн-хансеры), и участки, выключающие его (сплансеры). Различные химические вещества (лиганды) способны отделять от генов-операторов либо бс-лок-репрессор, либо белок-активатор. Единственным морфологическим признаком детерминации является появление деконденсации хроматина, увеличение содержания эухроматина. 4. Дифференциронка, или появление специфических черт строения у клеток. Эти черты строения определяются выполняемыми функциями. Бла- тдаря дифференцировке одинаковые клетки, например, бластомеры, приобретают специфические различия. Различают несколько этапов дифференцировки. 1. Геномно-молекулярный заключается в транскрипции экспрес-еированных генов, сплайсинге и процессинге и-РНК. 2. Молекулярно-цитоплазматический — синтез специфических белков под контролем активированных генов. 3. Клеточный, или микроскопический, уровень - образование из специфических белков соответствующих функции орга-нелл и цитореценторои. Дифференциронка имеет четыре уровня: — оотипический — возникновение различий в строении разных зон яйцеклетки; — бластомерный — появление различий у бластомеров; — зачатковый — появление зародышевых листков и эмбриональных зачатков, различных по строению; — гистогенетический — появление в одном зародышевом листке зачатков разных тканей. 5. Избирательная сортировка, или сегрегация клеток. Установлено, что если смешать клетки различных зародышевых листков, то вначале они смешиваются в беспорядке, но затем клетки, принадлежащие к разным листкам, сами сортируются и вступают в контакт только с клетками из этого же листка. В результате клеточный беспорядочный агрегат вновь разделяется на зародышевые листки. Таким образом, клеточная сегрегация имеет важное значение в эмбриогенезе, прежде всего для образования зародышевых листков, хотя ее роль следует рассматривать значительно шире. 6. Адгезия клеток, или их склеивание. Благодаря адгезии зародыш не распадается на отдельные клетки, а существует как отдельный организм. Адгезия осуществляется при помощи молекул клеточной адгезии. 7. Закономерное перемещение клеток — миграция. Без миграции были бы невозможны такие процессы, как гаструляция, нейруляция и образование органов, а также множество других процессов. 8. Эмбриональная индукция. Это явление основано на регуляции развития одних зачатков другими зачатками при помощи растворимых веществ — индукторов. Например, хордомезодерма индуцирует превращение нервной пластинки в нервную трубку и т.д. 9. Гибель клеток путем апоптоза. В эмбриогенезе происходит не только деление, но и гибель клеток. Это ведет к исчезновению ненужных органов, частей органов. Например, в эмбриогенезе формируется хвост, который затем редуцируется. ПОНЯТИЕ О КРИТИЧЕСКИХ ПЕРИОДАХ ЭМБРИОГЕНЕЗА И ПОСТНАТАЛЬНОГО ОНТОГЕНЕЗА Начало развития учения о критических периодах положил в 1907 г. У.Р. Стоккард. Он представлял онтогенез как ряд последовательных этапов, различающихся скоростью развития. Критические периоды по Стоккарду >,, растеризуются наибольшей скоростью развития организма, поэтому о становится чувствительным к различным вредным воздействиям. Внешни! факторы, к которым особенно велика чувствительность в эти периоды, могу; ускорять, замедлять или приостанавливать развитие организма. В развита представлений о критических периодах внесли вклад также Г. Грегг (1944 i В.М. Коровина (1953). Оригинальную гипотезу критических периодов предложил в 1960 i советский эмбриолог П.Г. Светлов. Он различал три группы воздействии внешней среды: 1) повреждающие воздействия, приводящие к смерти или патологии; 2) модифицирующие воздействия, вызывающие отклонения не патологического характера, которые назвал морфозами, или мутациями; 3) закономерное действие среды, обеспечивающее нормальное развитие. Эти воздействия (наличие или недостаток кислорода, питание, температур,! и т.д.) не бросаются в глаза, но представляют большой интерес, т.к. влияют на последующую устойчивость организма и нормальное развитие. Критические периоды онтогенеза связаны со следующими событиями: 1. В эти периоды происходит включение в действие определенной новой части наследственной информации, которая обеспечивает развитие организма на следующем этапе. 2. В результате детерминации организм вступает в новый этап развития. 3. Происходит смена типа питания, и в связи с этим интенсифицируется обмен веществ. 4. Временно снижается регуляторная деятельность развивающегося организма. 5. Временно замедляется рост структур организма, возрастает его энтропия. Все критические периоды можно разделить на несколько видов. 1. Периоды, критические для всего организма, когда вредные воздействия могут привести к гибели зародыша. Наиболее частая гибель зародышей происходит в первый лунный месяц эмбриогенеза. 2. Частные критические периоды (различные для каждого органа и ткани). 3. Критические периоды для клетки. 4. Появляются сообщения о критических периодах для отдельных органелл. Критическими периодами для организма в целом являются: 1. Развитие половых клеток —- ирогенез. Половые клетки во время развития могут быть подвержены самым разнообразным мутациям. 2. Оплодотворение. В этот период происходит сегрегация цитоплазмы и активируются обменные процессы, происходят ранние детерминация и диф-ференцировка, которые чувствительны к различным воздействиям. 3. Гаструляция. В эту стадию происходит образование стадиоспецифи-ческих и тканеспецифических антигенов. 4. Имплантация, при которой происходит смена типов питания зародыша. 5. Плацентация. Также характеризуется сменой типа питания и, кроме того, образованием органоспецифических антигенов. 6. Развитие осевых зачатков (нотогенез), гистогенез и органогенез. Вредные факторы среды в это время могут вызвать различные аномалии развития. В дальнейшем для каждого органа определяются свои критические периоды. 6. Рождение. Оно связано с резким изменением окружающей среды, что является сильной стресс-реакцией. Одновременно начинается функционирование дыхательной системы и малого круга кровообращения, идет перестройка в связи с этим сердечно-сосудистой системы, возрастает нагрузка на сердце. В постнаталыюм развитии критическими периодами являются период новорожденное™ и период полового созревания. В период новорожденнос-ти происходит адаптация ребенка к новым условиям существования, резко возросшему объему информации и антигенов внешней среды и др. В период полового созревания включаются новые регуляторные механизмы, идет становление репродуктивной системы, активируется рост, происходит перестройка многих органов, изменяется психика и др. ВЛИЯНИЕ ЭКЗО- И ЭНДОГЕННЫХ ФАКТОРОВ НА ЭМБРИОГЕНЕЗ Каждый эмбриональный зачаток и развивающийся из него орган имеют период повышенной чувствительности к повреждающим факторам (свой критический период), и их действие нарушает нормальный ход эмбриогенеза. Причины, которые вызывают нарушение нормального хода эмбриогенеза, могут быть эндогенными (наследственные факторы) и экзогенными (действие алкоголя, никотина, токсических веществ, вирусов и т.д.). В 10% случаев аномалии вызываются наследственными факторами, в 10% — влиянием экзогенных факторов, а в 80% наблюдается сочетание эндо- и экзогенных факторов. Непосредственной причиной аномалий в критические периоды может быть или остановка развития органа, или нарушение скорости его развития. Различают эмбриопатии, или фетопатии — нарушение развития всего плода, пороки развития и уродства — нарушение развития одного органа или системы органов. Весьма тяжелые изменения плода может вызвать алкоголь, который легко пропитает через плацентарный барьер. Недавно описан алкогольный синдром плода у женщин-алкоголиков. Он проявляется задержкой развития плода, уменьшением размеров мозга, аномалиями костей, развитием пороков сердца и другими аномалиями Очень чувствителен плод и к действию никотина, радиации. Тяжелые пора жения вызывают многие вирусы и бактерии. Так, вирус краснушной инфекции вызывает иногда несовместимые с жизнью изменения в организме плода или тяжелые пороки развития. РЕГУЛЯТОРНЫЕ ФАКТОРЫ ЭМБРИОГЕНЕЗА Эмбриогенез человека находится под жестким контролем, осуществляю щимся на разных уровнях. 1. Генетический уровень регуляции. В первую очередь, эмбриогенез на ходится под контролем генетических факторов. Они определяют все последовательности процессов развития, а также определяют регуляторные механизмы, служат их основой. Зигота, бластомеры и все клетки зародыша содержат гены-регуляторы, которые принимают участие в управлении процессами развития. Эти гены именуют гомеозисными. Они обладают способностью регулировать активность других генов. Выявлены также гены, определяющие сегментацию тела зародыша. Эти гены называются генами-гомеобоксами. Есть хроногены, т.е. гены, от действия которых зависит время наступления дифференцировки тех или иных клеток зародыша. Деятельность этих генов включается при достижении клеткой определенной пространственно-временной позиции. В то же время, в самих генах имеются особые участки, включающие их (энхансеры), и участки, подавляющие экспрессию данного гена (сплансеры). Все указанные молекулярно-генети-ческие факторы и процессы определяют такие компоненты эмбриогенеза, как размножение, рост и запрограммированную гибель клеток, детерминацию, дифференцировку, адгезию и миграцию клеток, эмбриональную индукцию. 2. Внутриклеточный уровень регуляции. Он состоит в том, что в клетках синтезируются регуляторные вещества, которые способны регулировать активность генома этих же клеток. Примером таких факторов являются триггерные белки. 3. Эпигенетический уровень регуляции. Включает все регуляторные факторы, являющиеся внешними по отношению к любой клетке развивающегося организма. Эпигенетические регуляторные факторы включают: межклеточные (гомотипические) и межтканевые (гетеротипические) взаимодействия. Межклеточйые взаимодействия могут заключаться в механических контактах, восприятии лучевых, химических и других сигналов, которые в конечном итоге изменяют направление дифференцировки клеток. К межклеточным механизмам регуляции относится также кей-лонная регуляция. Межтканевые взаимодействия могут сводиться к: 1 . Индукционным взаимодействиям; 2. Появлению градиентов (организационных центров) в тканях и органах — участков с наибольшей активностью физиологических процессов. 4. Организменный уровень регуляции. На этом уровне регуляция обеспечивается нервной, эндокринной и иммунной системами материнского организма, а в последующем — и организма плода. Нервная регуляция. Поскольку между организмами матери и плода отсутствуют анатомические нервные связи, то влияние нервной системы матери на эмбрион опосредуется нейромедиаторами, которые после синтеза их нервными образованиями материнского организма проникают через плацентарный барьер и влияют на развитие эмбриона (прямое влияние). Кроме того, они могут изменять кровоток в плаценте и тем самым — и эмбриогенез (непрямое влияние). После достижения собственной нервной системой необходимого уровня развития она включается в регуляцию эмбриогенеза. Ее роль заключается в инициации дифференцировки формирующихся морфофункциональных единиц органа, в нервно-трофическом влиянии на них. Эндокринная регуляция. На развитие зародыша оказывает выраженное влияние эндокринная система матери. Это влияние имеет место во все периоды эмбриогенеза. Нарушение гормонального статуса материнского организма, равно как и прием гормональных лекарственных веществ может приводить к нарушению развития плода вплоть до развития уродств. После становления плаценты она также включается в регуляцию развития плода. Наконец, с момента становления эндокринной системы плода она начинает влиять на эмбриогенез: рост организма плода, отдельных его органов, развитие функций этих органов. При этом устанавливаются строгое согласование между функцией тождественных эндокринных органов матери и плода. Иммунная регуляция. В настоящее время установлено, что для нормального эмбриогенеза необходимы нормальные иммунологические взаимоотношения между материнским организмом и организмом зародыша или плода. Иммунная система матери, обладая толерантностью к антигенам зародыша (плода), способна оказывать регулирующее воздействие на клетки эмбриона. Собственная иммунная система плода после ее развития определяет регуляцию качественной и количественной сторон происходящих в эмбриогенезе процессов. Включение вышеназванных механизмов регуляции происходит в строго определенном порядке. Новый механизм регуляции начинает действовать тогда, когда организм эмбриона подготовлен к его восприятию, при этом действие предыдущего регулирующего фактора либо заканчивается, либо происходит наложение одного фактора на другой. Момент смены регулирующих факторов относится к критическим периодам. КЛИНИЧЕСКИЕ АСПЕКТЫ. Клинические аспекты медицинской эмбриологии заключаются в следующем. 1. Регуляция фертильности (рождаемости, численности человеческом популяции). Знание эмбриологии позволяет успешно применять как кон трацепцию для предотвращения беременности, так и бороться с бесплодием. 2. Большое клиническое значение имеет знание врачом-акушером критических периодов эмбриогенеза и последствий действия на организм зародыша тератогенных факторов. Это лежит в основе профилактики врож денных аномалий и уродств. 3. Знание закономерностей эмбриогенеза позволяет акушерам-гинекологам правильно оценивать течение беременности, определять режим жизнедеятельности беременной женщины. 4. Клонирование человека. В последние годы благодаря достижениям клеточной инженерии ученые вплотную подошли к получению клонов человека, т.е. совершенно идентичных его копий. Для этого после получения зародышей путем экстракорпорального оплодотворения вскрывают блестящую оболочку и разделяют зародыш на части, которые подсаживают на новые z. pellucida. Эти части после имплантации в полость матки дают развитие совершенно идентичных индивидуумов (клонов). Вначале эмбриологи, проводя такие исследования, манипулировали на эмбрионах, находящихся на стадии 2—8 бластомеров, а в последующем положительные результаты были получены также с морулами и бластоцистами. В настоящее время уже получены клоны домашних животных путем пересадки соматических ядер в яйцеклетку. Возможности клонирования человека обусловлены достижениями в трансплантации ядер клеток, в частности ядер соматических клеток в половые клетки. Дальнейшее развитие исследований в этом направлении может сделать реальностью и клонирование человека. Это наряду с положительными моментами может создать целый ряд проблем морально-этического, криминального плана (появление людей-двойников и др). и т.д. Глава 7 ОСНОВЫ УЧЕНИЯ О ТКАНЯХ (ВВЕДЕНИЕ В ОБЩУЮ ГИСТОЛОГИЮ) |
