М.И.Кузин. Хирургические болезни. Литература для студентов медицинских вузов Хирургические болезни Под редакцией
 Скачать 10.27 Mb. Скачать 10.27 Mb.
|
|
Р 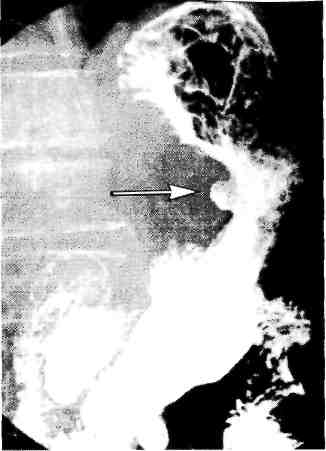 ис. 11.6. Язва желудка. "Ниша" на контуре кривизны в верхней трети тела желудка. Рентгенограмма желудка. ис. 11.6. Язва желудка. "Ниша" на контуре кривизны в верхней трети тела желудка. Рентгенограмма желудка.Прямым рентгенологическим признаком язвы является симптом "ниши" — стойкое депо контрастного вещества на рельефе слизистой оболочки или на контуре стенки органа. При язве желудка часто выявляют "нишу" на стенке желудка в виде кратера, заполненного барием (рис. 11.6), или "нишу" рельефа в виде стойкого бариевого пятна с конвергенцией складок слизистой оболочки к его центру (рис. 11.7). При язвенной болезни желудка эвакуация его содержимого, как правило, замедлена. Язва двенадцатиперстной кишки выявляется в виде ниши рельефа или ниши, выводящейся на контур. Имеются конвергенция складок слизистой оболочки к язве, рубцовая деформация луковицы двенадцатиперстной кишки в виде трилистника, трубкообразного сужения и др. (рис. 11.8). В процессе сморщивания рубцов формируется стеноз в области луковицы (рис. 11.9). На фоне зажившей или открытой язвы двенадцатиперстной кишки в ряде случаев появляется язва желудка. П 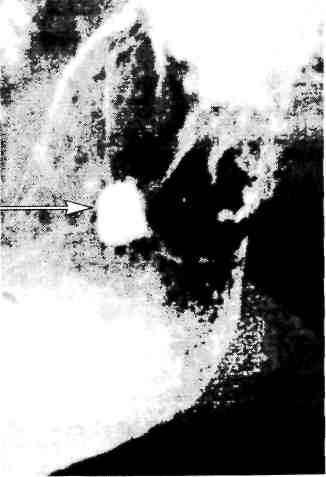 ри язвенной болезни двенадцатиперстной кишки наблюдается усиление моторики желудка и двенадцатиперстной кишки. Эвакуация из желудка ускорена. Для точной количественной оценки скорости и характера эвакуации пищи из желудка используют динамическую радионуклидную гастросцинтигра-фию. Для этого перед исследованием больным дают стандартный пробный завтрак, меченный короткоживущим изотопом ("Тс), а затем через опреде ленные промежутки времени измеряют активность над желудком, что позволяет судить о скорости эвакуации принятого "завтрака". ри язвенной болезни двенадцатиперстной кишки наблюдается усиление моторики желудка и двенадцатиперстной кишки. Эвакуация из желудка ускорена. Для точной количественной оценки скорости и характера эвакуации пищи из желудка используют динамическую радионуклидную гастросцинтигра-фию. Для этого перед исследованием больным дают стандартный пробный завтрак, меченный короткоживущим изотопом ("Тс), а затем через опреде ленные промежутки времени измеряют активность над желудком, что позволяет судить о скорости эвакуации принятого "завтрака".Рис. 11.7. Язва желудка. Депо бария с конвергенцией складок слизистой оболочки желудка. Прицельная рентгенограмма желудка. Дифференциальная диагностика. Нет сомнений в том, что для дифференциальной диагностики важно учитывать жалобы и анамнез заболевания. Характер болей, время их появления, связь с приемом пищи, сезонность обострений, возраст пациента — все эти данные позволяют поставить предварительный диагноз, но не избавляют от возможных ошибок. Решающее значение в диагностике язвенной болезни желудка имеет эндоскопическое исследование с прицельной биопсией и гистологическим исследованием биоптатов. Гистологическое исследование биоптатов дает точный диагноз в 95%, цитологическое — в 70% случаев. Однако возможны ложноотрицательные результаты (5—10%), когда злокачественное поражение не подтверждается данными гистологического исследования. Это может быть обусловлено неадекватной биопсией вследствие подслизистого роста опухоли. Р 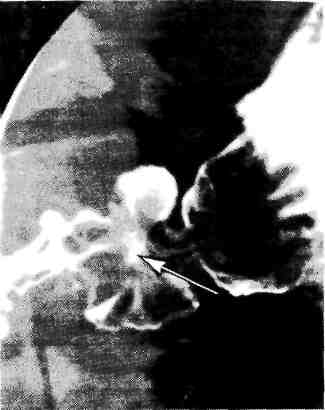 ис. 11.8. Язва луковицы двенадцатиперстной кишки. Депо бария на рельефе с конвергенцией складок слизистой оболочки в деформированной луковице. Прицельная рентгенограмма луковицы двенадцатиперстной кишки. ис. 11.8. Язва луковицы двенадцатиперстной кишки. Депо бария на рельефе с конвергенцией складок слизистой оболочки в деформированной луковице. Прицельная рентгенограмма луковицы двенадцатиперстной кишки.Диагноз язвенной болезни двенадцатиперстной кишки в типичных клинических наблюдениях не представляет трудностей. Однако надо иметь в виду, что болевой синдром, свойственный язве двенадцатиперстной кишки, может наблюдаться при локализации язвы в препилорической части желудка, а боли при первично-язвенной форме рака желудка, часто локализующейся в антральном отделе, нельзя отличить от болей, характерных для желудочной язвы. Только сочетание рентгенологического исследования с эндоскопическим и прицельной гастробиопсией может гарантировать правильный диагноз. Б 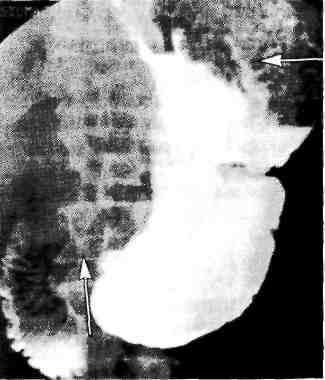 олевой синдром при язвенной болезни двенадцатиперстной кишки может иметь сходство с болями, возникающими при хроническом холецистите и хроническом панкреатите, которые могут ей сопутствовать. Для дифференциального диагноза важны результаты ультразвукового сканирования печени, желчного пузыря, поджелудочной железы. Следует также учитывать возмож ность частого сочетания различных заболеваний органов пищеварительной системы. олевой синдром при язвенной болезни двенадцатиперстной кишки может иметь сходство с болями, возникающими при хроническом холецистите и хроническом панкреатите, которые могут ей сопутствовать. Для дифференциального диагноза важны результаты ультразвукового сканирования печени, желчного пузыря, поджелудочной железы. Следует также учитывать возмож ность частого сочетания различных заболеваний органов пищеварительной системы.Рис. 11.9. Пилоробульбарный стеноз. Желудок расширен. Над бариевой взвесью жидкость. Пилорический канал сужен. В двенадцатиперстной кишке небольшое количество контраста. Рентгенограмма желудка. Течение язвенной болезни без лечения практически не изучено, терапевтические вмешательства изменяют естественное развитие процесса. Для язвенной болезни характерно циклическое течение, при котором период обострения сменяется периодом ремиссии. Выделяют три фазы заболевания: острую (активную) фазу, или обострение, неполную ремиссию (затухающее обострение), полную ремиссию. В острой фазе и при обострении у больного имеются типичные симптомы язвенной болезни, при обследовании выявляется язвенный дефект слизистой оболочки с выраженным воспалением вокруг. Затухающее обострение (неполная ремиссия) характеризуется свежими рубцами на месте язвы, сохраняющимся воспалением (наличием буль-бита или антрального гастрита), отсутствием клинических симптомов обострения. Это состояние поддерживается лечением, при отмене которого наблюдается быстрый возврат объективных и субъективных клинических признаков обострения. Фаза ремиссии характеризуется отсутствием клинических симптомов, стойким заживлением язвы с образованием зрелого рубца, исчезновением активного геликобактерного воспаления и колонизации слизистой ободочки Н. pylori. По клиническим проявлениям болезни принято различать легкую, сред-нетяжелую и тяжелую формы. При легкой форме болезни обострения возникают не чаще одного раза в год, они легко купируются под влиянием лечения, проявляются немногочисленными легкими симптомами. Среднетяжелая болезнь характеризуется обострениями, возникающими 2—3 раза в год, которые купируются только при полноценном курсе противоязвенной терапии. Тяжелая (агрессивная) форма проявляется типичными частыми обострениями, отсутствием стойкой ремиссии, выраженной клинической симптоматикой, сочетанием с другими заболеваниями органов брюшной полости (панкреатит, желчнокаменная болезнь и др.). Часто рецидивирующее тяжелое течение болезни может быть связано с неадекватной медикаментозной терапией. Различают также неосложненную и осложненную (стеноз, кровотечение, перфорация) формы язвенной болезни. Лечение. Общие принципы консервативного и хирургического лечения язвенной болезни желудка и двенадцатиперстной кишки основаны прежде всего на устранении этиологических факторов (рис. 11.10; 11.11). Консервативное лечение должно быть спланировано так, чтобы воздействовать на основные механизмы язвообразования. Для этого необходимо:
В настоящее время при лечении язвенной болезни не придерживаются столь строгого режима питания, как раньше. Диета не оказывает существенного влияния на течение язвенной болезни. Однако настоятельно рекомендуется 5-разовое питание пищей, приготовленной на пару, исключение из рациона острых блюд, маринадов и копченостей, кофе, алкоголя; прекратить курение, прием нестероидных противовоспалительных препаратов (аспирин, бутадион, индометацин, волтарен и др.). Эффективная эрадикация геликобактерной инфекции, подавление продукции соляной кислоты и заживление язвы достигается при триплекснои терапии, т. е. сочетании антисекреторных препаратов (омепразол, ранити-дин, фамотидин) с двумя антибиотиками (наиболее часто кларитромицин + амоксициллин) или сочетании де-нола, обладающего цитопротективным действием, с амоксициллином и метронидазолом. Хороший эффект достигается при поддержании рН желудочного сока на уровне 4,0—6,0. Эрадика-ция геликобактерной инфекции приводит к тому, что частота рецидива язвенной болезни после адекватного медикаментозного курса лечения снижается до 4—6% в течение первого года после лечения. При неосложненной язвенной болезни двенадцатиперстной кишки рано начатое адекватное медикаментозное лечение у большинства больных обеспечивает стойкую ремиссию при впервые выявленной язве, рецидивах до 2 раз в год, а также у пациентов с неизлеченной инфекцией Н. pylori. Но даже при этих условиях остается группа больных, которым непрерывная поддерживающая терапия противоязвенными препаратами показана: 1) при безуспешности прерывистого курса лечения с рецидивами язвы 3 раза и более в год; 2) при осложненном течении болезни (кровотечение или перфорация в анамнезе); при эрозивном рефлюкс-эзофагите, а также грубых Рубцовых изменениях в стенках двенадцатиперстной кишки и желудка в анамнезе. 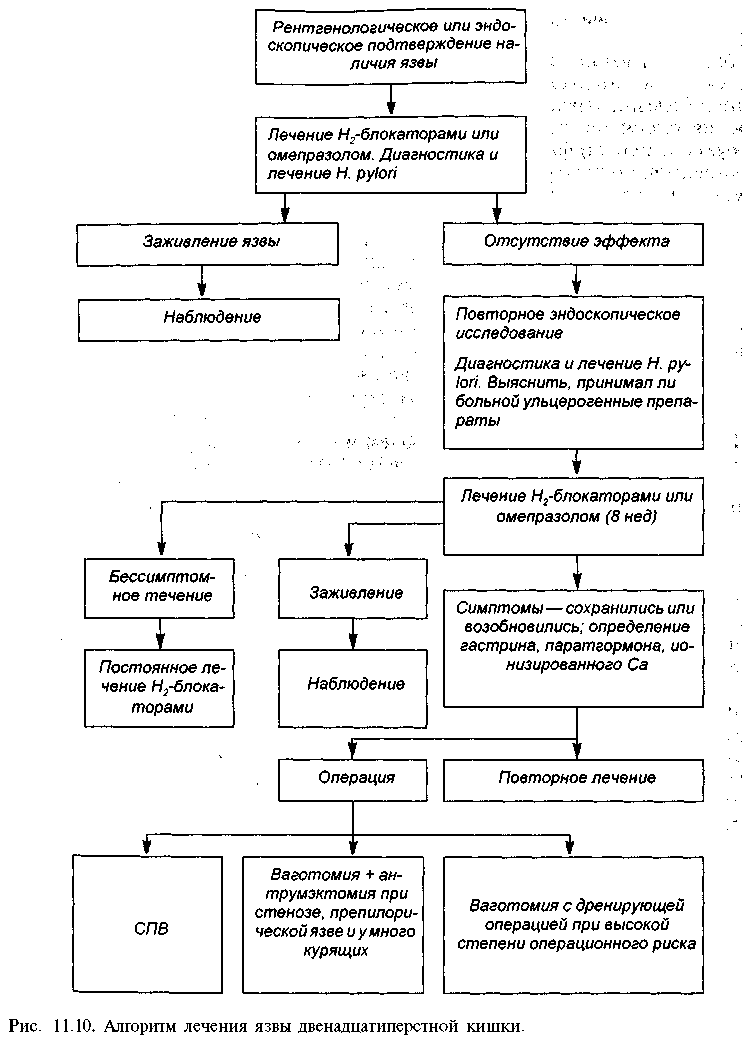 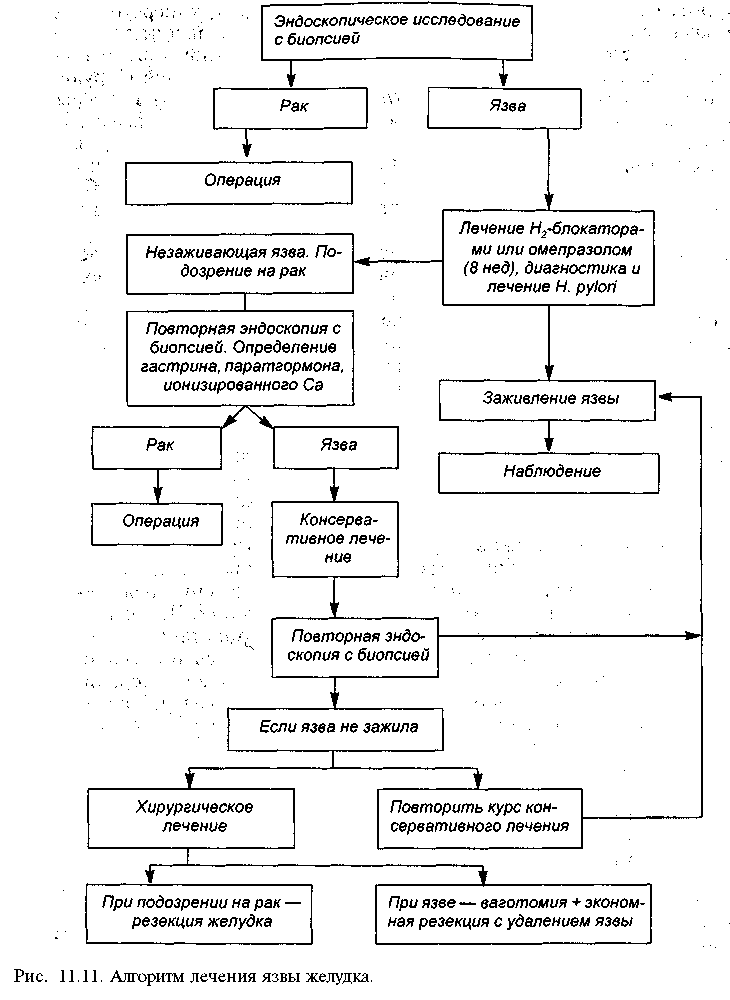 Резистентные к медикаментозной терапии язвы требуют более настойчивого длительного лечения с заменой применявшихся препаратов более эффективными или увеличением дозы и длительности лечения. Столь настойчивое медикаментозное лечение привело к тому, что число плановых операций по поводу язвенной болезни резко сократилось, а число больных, поступающих в хирургические стационары с кровотечением, перфорацией и стенозом, значительно возросло, операции приходится проводить по неотложным показаниям, на фоне опасных для жизни осложнений. Этот факт отмечается повсеместно как в России, так и за ее пределами. Общеизвестно, что летальность при оперативных вмешательствах по поводу кровотечения, перфорации или стеноза в 10—15 раз выше, чем при плановых операциях. С учетом этих обстоятельств возникает вопрос о целесообразности оперативного лечения больных, нуждающихся в дорогостоящем непрерывном или поддерживающем повторном противоязвенном лечении, для того чтобы предупредить развитие опасных для жизни осложнений (кровотечение, перфорация, стеноз). Оперативное лечение целесообразно проводить в плановом порядке, до развития осложнений. Чем чаще возникают обострения заболевания, тем более выраженными становятся сопутствующие нарушения функций поджелудочной железы, печени, желчного пузыря, уменьшаются шансы на хороший результат плановой операции. Своевременная плановая операция предупреждает развитие опасных для жизни больного осложнений. Одновременно с этим она резко уменьшает риск хирургического вмешательства. Показания к хирургическому лечению разделяют на абсолютные и относительные. Абсолютными показаниями считают перфорацию язвы, профуз-ное или рецидивирующее гастродуоденальное кровотечение, пилородуоде-нальный стеноз и грубые рубцовые деформации желудка, сопровождающиеся нарушениями его эвакуаторной функции. Относительным показанием к операции является безуспешность полноценного консервативного лечения:
Е 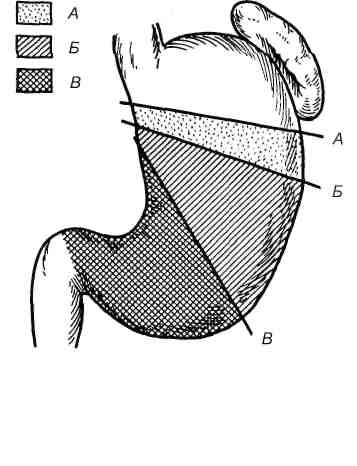 сли 3—4-кратное лечение в стационаре в течение 4—8 нед при адекватном подборе лекарственных препаратов не приводит к излечению или длительным ремиссиям (5—8 лет), то следует настоятельно ставить вопрос о хирургическом лечении, чтобы не подвергать пациентов риску появления опасных для жизни осложнений. сли 3—4-кратное лечение в стационаре в течение 4—8 нед при адекватном подборе лекарственных препаратов не приводит к излечению или длительным ремиссиям (5—8 лет), то следует настоятельно ставить вопрос о хирургическом лечении, чтобы не подвергать пациентов риску появления опасных для жизни осложнений.Современные плановые операции типа ваготомии не калечат больных, как ранее широко применявшиеся резекции желудка, летальность менее 0,3%. Рис. 11.12. Размеры удаляемой части желудка. А — субтотальная резекция желудка; Б — резекция 1/3 желудка. В – антрумэктомия. Вовремя сделанная ваготомия, помимо обеспечения безопасности больного, экономит его личные и государственные средства, улучшает качество жизни. Врач должен помнить, что он не имеет права подвергать пациента риску возникновения опасных для жизни осложнений. Хирургическое лечение язвенной болезни двенадцатиперстной кишки преследует те же цели, что и консервативное. Оно направлено на устранение агрессивного кислотно-пептического фактора и создание условий для свободного прохождения пищи в нижележащие отделы желудочно-кишечного тракта. Эта цель может быть достигнута различными способами.
Наиболее часто применяют следующие виды оперативных вмешательств: а) стволовую в аготомию с пилоропластикой (по Гейнеке—Микуличу, Финнею, Жабуле) (рис. 11.13; 11.14; 11.15) или, что наиболее выгодно, с дуоденопластикой ; б) ваготомию с ант румэктомией и анастомозом по Бильрот-I, Бильрот-П или по Ру; в) селективную проксимальную ваготомию; г) резекцию желудка; д) гастрэктомию. При резекции желудка удаляют обычно дистальную часть его (дистальная резекция) (рис. 11.16). Непрерывность желудочно-кишечного тракта восстанавливают по различным модификациям Бильрот-I, Бильрот-П или по Ру. Удаление значительной части тела желудка производят для снижения ки-слотопродукции за счет уменьшения зоны расположения обкладочных клеток, продуцирующих соляную кислоту. Естественно, при этом удаляют язву и весь антральный отдел, продуцирующий гастрин. При резекции желудка во время его мобилизации неизбежно пересекают желудочные ветви блуждающих нервов вместе с сосудами малой и большой кривизны. Резекция желудка практически всегда сопровождается селективной ваготомией, выполняемой вслепую, без выделения пересекаемых желудочных ветвей вагуса. После удаления 2/3 желудка раньше, как правило, накладывали гастроеюнальный анастомоз позади поперечной ободочной кишки на короткой петле (по Бильрот-Н в модификации Гофмейстера—Финстерера). Это в большинстве случаев приводит к рефлюксу содержимого двенадцатиперстной кишки в желудок, к развитию рефлюкс-гастрита и рефлюкс-эзофагита. Некоторые хирурги предпочитают накладывать анастомоз впереди ободочной кишки, используя длинную петлю тонкой кишки. Между приводящей и отводящей петлями (по Бальфуру) накладывают энтероэнтероанастомоз для устранения рефлюкса содержимого приводящей петли кишки (желчь, панкреатический сок) в культю желудка. Однако и в этом случае наблюдается, хотя и менее выраженный, рефлюкс. В последние годы предпочтение отдают гастроеюнальному Y-анастомозу на выключенной по Ру петле. Этот способ более надежно предотвращает рефлюкс желчи и панкреатического сока в культю желудка, возникновение рефлюкс-гастрита и последующую метаплазию эпителия, уменьшает вероятность развития рака культи желудка в последующем. Позадиободочный гастроеюнальный анастомоз (по Гофмейстеру—Фин-стереру) на короткой петле многие хирурги считают порочным, устаревшим, так как он способствует рефлюксу желчи и панкреатического сока в культю желудка, развитию рефлюкс-гастрита, метаплазии эпителия желудка и в ряде случаев возникновению рака культи. У больных, оперированных по этому способу, чаще всего появляются тяжелые пострезекционные синдромы. 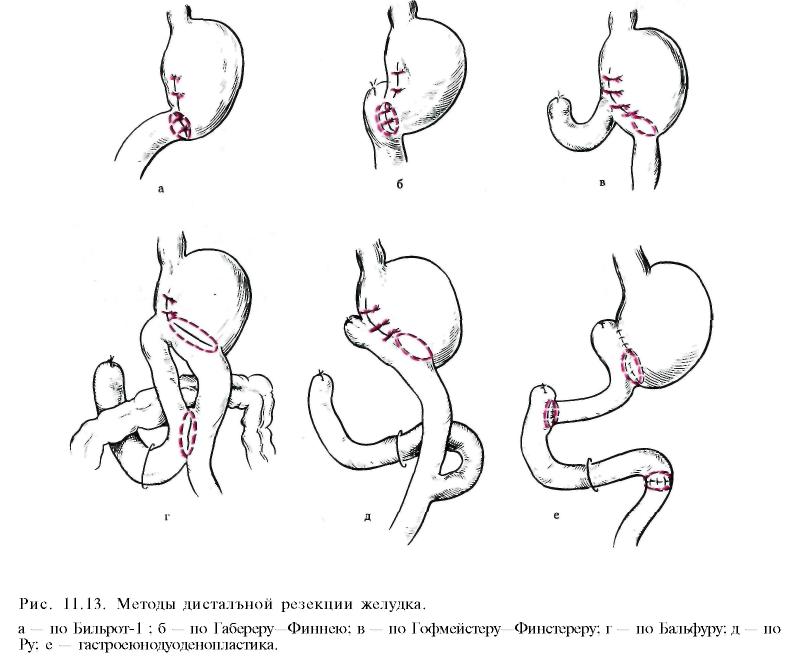 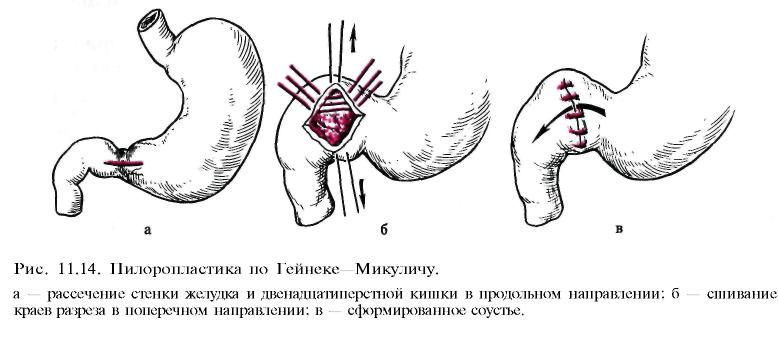 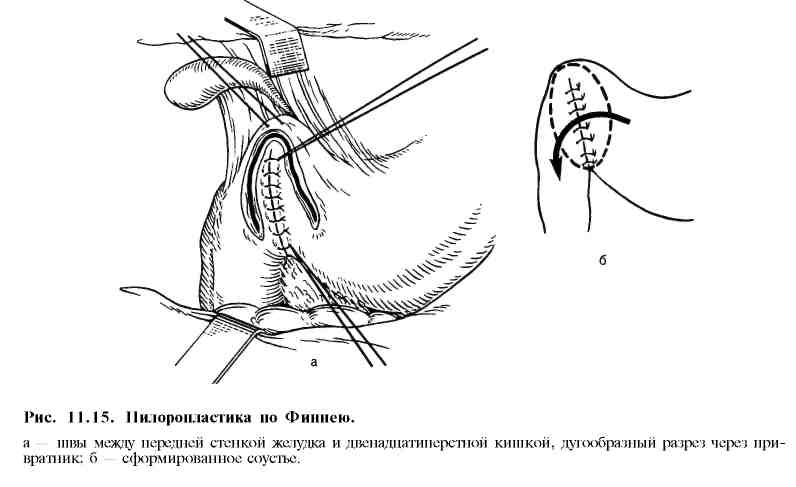 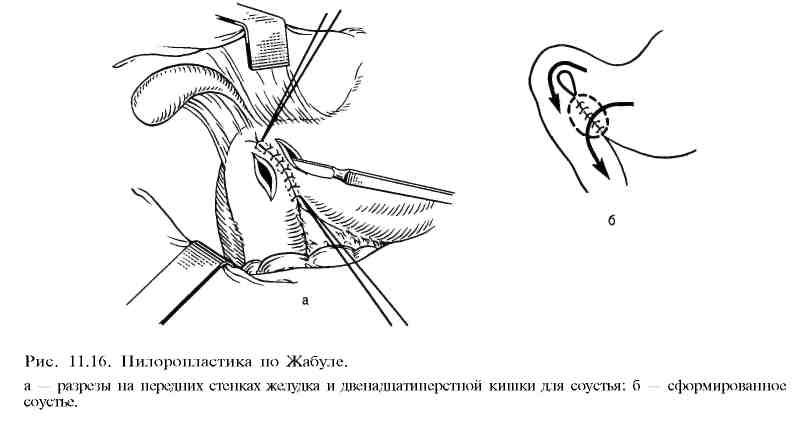 Преимуществом резекции желудка по Бильрот-I является сохранение физиологического прохождения пищи через двенадцатиперстную кишку. Однако этот метод также не предотвращает возможность рефлюкса дуоденального содержимого в культю желудка и не всегда выполним (инфильтрат, рубцовая деформация двенадцатиперстной кишки, возможность натяжения тканей соединяемых органов и опасности расхождения швов анастомоза). Для обеспечения пассажа пищи по двенадцатиперстной кишке при реконструктивных операциях по поводу демпинг-синдрома используют интерпозицию петли тощей кишки длиной 15—20 см между маленькой культей желудка и культей двенадцатиперстной кишки (гастроеюнодуоденопла-стика). Это увеличивает резервуарную функцию культи желудка, предупреждает рефлюкс-гастрит и устраняет некоторые пострезекционные синдромы. Комбинированные операции, при которых сочетают стволовую ваготомию с антрумэктомией и анастомозом на выключенной по Ру петле или га-строеюнальным анастомозом по Бильрот-I, Бильрот-П, позволяют даже при очень высокой секреции соляной кислоты сохранить резервуарную функцию желудка и подавить условнорефлекторную и желудочную фазы секреции желудочного сока. Антрумэктомию в сочетании со стволовой ваготомией часто используют при лечении больных язвенной болезнью двенадцатиперстной кишки. В ряде стран этот тип операции применяется наиболее часто, его называют "золотым стандартом". П 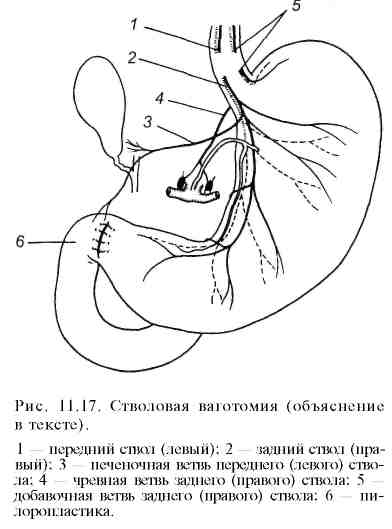 ри хронической дуоденальной непроходимости целесообразно завершить стволовую ваготомию с антрумэктомией гастроеюнальным анастомозом на выключенной по Ру петле тощей кишки. Многие хирурги предпочитают накладывать этот тип анастомоза при всякой резекции желудка. Послеоперационная летальность при этом методе составляет около 1 , 5%, что значительно ниже, чем после обширной дистальной резекции. Рецидивы пептических язв после этой операции очень редки. Частота и выраженность постгастрорезекционных синдромов после антрумэктомии или гемигастр-эктомии в сочетании со стволовой ваготомией значительно меньше, чем после обширной (2/3—3Д желудка) дистальной резекции желудка с гастроею-нальным анастомозом по Гофмейстеру—Финстереру. ри хронической дуоденальной непроходимости целесообразно завершить стволовую ваготомию с антрумэктомией гастроеюнальным анастомозом на выключенной по Ру петле тощей кишки. Многие хирурги предпочитают накладывать этот тип анастомоза при всякой резекции желудка. Послеоперационная летальность при этом методе составляет около 1 , 5%, что значительно ниже, чем после обширной дистальной резекции. Рецидивы пептических язв после этой операции очень редки. Частота и выраженность постгастрорезекционных синдромов после антрумэктомии или гемигастр-эктомии в сочетании со стволовой ваготомией значительно меньше, чем после обширной (2/3—3Д желудка) дистальной резекции желудка с гастроею-нальным анастомозом по Гофмейстеру—Финстереру.После обширной дистальной резекции желудка летальность составляет 3—5%. У большинства больных наступает ахлоргидрия. Тем не менее рецидивы язв возникают у 1—7% больных. В первый год после резекции желудка около половины больных находятся на инвалидности, а 15—30% становятся инвалидами пожизненно и вынуждены менять профессию. У 10—15% перенесших резекцию желудка развиваются постгастро-резекционные синдромы, резко ухудшающие качество жизни. Тяжесть течения некоторых пострезекционных синдромов значительно превосходит тяжесть симптомов язвенной болезни, больные нуждаются в повторных реконструктивных операциях. Высокая послеоперационная летальность, большой процент неудовлетворительных результатов после обширной дистальной резекции желудка, особенно по методу Бильрот-П с позадиободочным анастомозом по Гофмейстеру—Финстереру, явились причиной поиска менее травматичных и более физиологичных операций. Из нерезекционных (органосо-храняющих) методов в настоящее время широко применяют различные варианты ваготомии. В клинической практике распространены стволовая ваготомия с пилоропла-стикой по Гейнеке—Микуличу или Финнею или гастродуоденоанастомоз по Жабуле. Стволовая ваготомия заключается в пересечении стволов блуждающих нервов и пересечением мелких ветвей по всей окружности пищевода на протяжении не менее 6 см выше отхождения от них печеночной и чревной ветвей (рис. 11.17). Стволовая ваготомия в сочетании с пилоропластикой в плановой хирургии язвенной болезни сопровождается низкой послеоперационной летальностью (менее 1%). Частота рецидивов язв при ней составляет в среднем 8—10%. Обычно рецидивы язв легко поддаются медикаментозному лечению и редко служат поводом для повторных операций. С 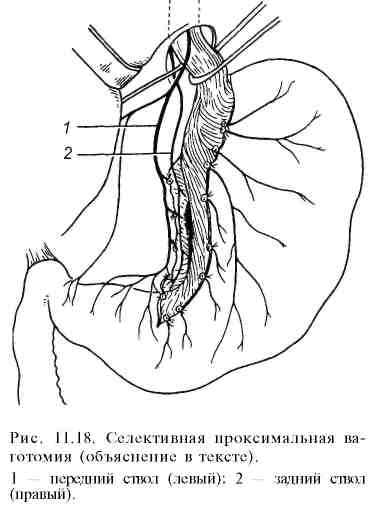 елективная проксимальная ваготомия (рис. 11.18) заключается в пересечении мелких ветвей желудочного нерва Латарже, иннервирующих тело и свод желудка, где расположены кислотопродуцирующие обкладочные клетки. Дистальные ветви нерва Латарже, иннервирующие антральный отдел и привратник, при этой операции сохраняют, что обеспечивает нормальную моторику антрального отдела и нормальную эвакуацию содержимого. При отсутствии стеноза в пилоропластике нет необходимости. Чтобы селективная проксимальная ваготомия была полноценной, необходимо соблюдать следующие условия: 1) пересечь все мелкие ветви вокруг пищевода на протяжении 6—7 см, не повреждая стволы вагуса (при скелетизации рецидивов на протяжении 2—3 см резко возрастает частота рецидивов вследствие неполной денервации фундального отдела); 2) пересечь ветви нерва Латарже, идущие к кислотопродуцирующей зоне желудка по малой кривизне, до уровня, отстоящего от привратника на 6—7 см; 3) пересечь правую желудочно-сальниковую артерию на расстоянии 6 см от привратника. елективная проксимальная ваготомия (рис. 11.18) заключается в пересечении мелких ветвей желудочного нерва Латарже, иннервирующих тело и свод желудка, где расположены кислотопродуцирующие обкладочные клетки. Дистальные ветви нерва Латарже, иннервирующие антральный отдел и привратник, при этой операции сохраняют, что обеспечивает нормальную моторику антрального отдела и нормальную эвакуацию содержимого. При отсутствии стеноза в пилоропластике нет необходимости. Чтобы селективная проксимальная ваготомия была полноценной, необходимо соблюдать следующие условия: 1) пересечь все мелкие ветви вокруг пищевода на протяжении 6—7 см, не повреждая стволы вагуса (при скелетизации рецидивов на протяжении 2—3 см резко возрастает частота рецидивов вследствие неполной денервации фундального отдела); 2) пересечь ветви нерва Латарже, идущие к кислотопродуцирующей зоне желудка по малой кривизне, до уровня, отстоящего от привратника на 6—7 см; 3) пересечь правую желудочно-сальниковую артерию на расстоянии 6 см от привратника. В настоящее время селективная проксимальная ваготомия без пилоро-пластики является стандартной операцией при лечении не поддающейся стойкому излечению язвы двенадцатиперстной кишки, в том числе язв с осложнениями в анамнезе. Дренирующие желудок операции (пилоропластику по Гейнеке—Мику-личу, гастродуоденостомию по Жабуле или дуоденопластику) применяют при селективной проксимальной ваготомии, если имеется стеноз привратника. Пилоропластику всегда производят при стволовой ваготомии. Дополнение ваготомии операцией, дренирующей желудок, связано с разрушением привратника. В ряде случаев (6—7%) это приводит к развитию легкого демпинг-синдрома вследствие неконтролируемого сброса желудочного содержимого в тонкую кишку. Разрушение привратника (пилоропла-стика) или его шунтирование (гастродуоденоанастомоз) создает условия для развития дуоденогастрального рефлюкса и "щелочного" рефлюкс-гастрита. Поэтому "идеальной" операцией при язвенной болезни двенадцатиперстной кишки (операцией выбора) считают стандартную селективную проксимальную ваготомию (СПВ). Если нет стеноза, то СПВ выполняют без дренирующей желудок операции. При стенозе в луковице двенадцатиперстной кишки рекомендуется производить дуоденопластику, так как она позволяет значительно лучше сохранить функцию привратника. После СПВ развитие дуо-деногастрального рефлюкса маловероятно, редко наблюдается диарея или демпинг-синдром легкой степени. Дренирующая операция снижает положительные качества СПВ, поэтому при дуоденальном стенозе, по возможности, необходимо выполнять дуоденопластику (аналог пилоропластики по Гейнеке—Микуличу или Финнею, но только в пределах деформированной и стенозированной луковицы двенадцатиперстной кишки). Послеоперационная летальность после СПВ составляет 0,3% и менее. Рецидив пептической язвы наблюдается у 10—12% больных, что бывает связано с неадекватной или неполной ваготомией. Хирургическое лечение язвенной болезни желудка производят по тем же показаниям, что и при лечении язвенной болезни двенадцатиперстной кишки. Однако сроки консервативного лечения при желудочных язвах нужно сокращать тем увереннее, чем больше язва, чем глубже ниша, чем старше больной и ниже кислотность (С. С. Юдин). Основным методом хирургического лечения язв желудка является стволовая ваготомия с антрумэктомией и га-строеюнальным анастомозом на выключенной по Ру петле или анастомозом по Бильрот-I. В связи с трудностями дифференциальной диагностики между пептической язвой и первично-язвенным раком отношение к ваготомии как методу лечения язв желудка сдержанное. При крупных язвах верхней части желудка выполняют дистальную лестничную резекцию с анастомозом по Ру. При сочетанных язвах желудка и двенадцатиперстной кишки применяют стволовую ваготомию с антрумэктомией и удалением язв обеих локализаций. Операцию завершают гастроеюнальным анастомозом по Ру. Препилорические язвы и язвы пилорического канала по патогенезу и клиническим симптомам аналогичны язвам двенадцатиперстной кишки. Показания к операции и методы хирургического вмешательства при них такие же, как при дуоденальной язве. Если хирург не уверен в доброкачественной природе язвы, то показана резекция (3/4) желудка с удалением сальника и лимфаденэктомией (региональные лимфатические узлы) в пределах D2 (см. "Рак желудка"). Операцию заканчивают гастроеюнальным анастомозом по Ру или одному из вариантов Бильрот-I или Бильрот-П. Органосберегающую стволовую ваготомию с пилоропластикой для лечения язвенной болезни желудка можно применять только в специализированных стационарах, при полной уверенности в доброкачественном характере язвы. Для этого до операции проводят курс интенсивной противоязвенной терапии, который в большинстве случаев заканчивается заживлением язвы. Во время лечения производят 2—3-кратную прицельную биопсию с гистологическим исследованием биоптатов. Заживление язвы и уменьшение воспалительных изменений в тканях вокруг язвы облегчают выполнение операции, во время которой иссекают послеязвенный рубец или незажившую язву, проводят их срочное гистологическое исследование (для исключения признаков язвенной формы рака). После этого выполняют стволовую ваготомию с пилоропластикой. Опыт ряда клиник показал надежность такого типа оперативного вмешательства. При выборе метода хирургического лечения у конкретного больного необходимо учитывать локализацию и особенности течения язвенной болезни, осложнения, общее состояние больного, степень технической подготовленности хирурга к выполнению различных типов ваготомий. Перед операцией хирург должен ответить себе на ряд вопросов: 1) хорошо ли он знает анатомию ветвей вагуса и их роль в секреции желудочного сока и моторной функции желудка; 2) владеет ли он современной техникой различных видов ваготомий; 3) осведомлен ли он о возможных технических ошибках, которые могут привести к неполной ваготомий и частым рецидивам; 4) правильно ли он определил показания и противопоказания к различным видам ваготомий и их комбинации с экономной резекцией желудка; 5) сумел ли он критически осмыслить достоинства и недостатки методов оперативного лечения язв желудка и двенадцатиперстной кишки для того, чтобы выбрать наиболее приемлемый для данного больного вариант оперативного вмешательства. |
