тест по химии высокой сложности. тест. Методическая разработка по химии Композиция тестовых заданий на уроках химии
 Скачать 0.6 Mb. Скачать 0.6 Mb.
|
|
3. 6 Азот и его соединения По данной теме мы разработали несколько тестов. Тест «Азот – элемент и простое вещество», «Аммиак и соли аммиака», «Азотная кислота» рекомендованы для текущего контроля, а тест «Азот и его соединения» для тематического контроля. Первые три теста содержат задания с выбором нескольких правильных ответов, что уменьшает вероятность случайного угадывания. При использовании таких заданий можно пользоваться политомической оценкой при анализе результатов тестирования. В данных тестах значительное внимание отводится проверке и закреплению таких опорных понятий, как степень окисления, окислительно- восстановительные возможности азота и его соединений, ионные реакции и их направленность, донорно - акцепторный механизм взаимодействия аммиака с кислотами. План теста: «Азот- элемент простое вещество».
План теста: «Аммиак и соли аммония».
План теста: «Азотная кислота».
План теста: «Азот и его соединения».
Тест: «Азот- элемент и простое вещество». Обвести кружком номера всех правильных ответов. 1. ВЫСШУЮ СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТ ПРОЯВЛЯЕТ В СОЕДИНЕНИЯХ: (1) NH3 (4) HNO3 (2) N2O5 (5) HNO2 (3) Mg3N2 (6) Cu(NO3)2 2. ОТРИЦАТЕЛЬНУЮ СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТ ПРОЯВЛЯЕТ В СОЕДИНЕНИЯХ: (1) Li3N (4) NH3 (2) Ba3N2 (5) HNO2 (3) NO (6) N2O5 3. КАКИЕ СОЕДИНЕНИЯ АЗОТА МОГУТ ПРОЯВЛЯТЬ КАК ОКИСЛИТЕЛЬНЫЕ, ТАК И ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА ? (1) NH3 (4) N2O5 (2) HNO2 (5) NaNO2 HNO3 4. ФОРМУЛЫ СОЕДИНЕНИЙ АЗОТА, КОТОРЫЕ НАЗЫВАЮТ НИТРИДАМИ: (1) Na3N (4) AlN (2) Ba3N2 (5) NH4NO3 (3) Ba(NO3)2 (6) NaNO2 5. АЗОТ ВЫПОЛНЯЕТ РОЛЬ ОКИСЛИТЕЛЯ ПРИ ВЗАИМОДЕЙСТВИИ С:  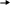 (1) N2+H2 (3) N2+Li (1) N2+H2 (3) N2+Li 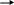 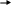 (2) N2+O2 (4) N2+Mg (2) N2+O2 (4) N2+MgОтветы:
Тест: «Аммиак и соли аммония». Обвести кружком номера всех правильных ответов: 1. МОЛЕКУЛА АММИАКА ИМЕЕТ ФОРМУ: (1) изогнутую (3) плоскостную (2) линейную (4) пирамидальную * 2. КАКИМ ИЗ ПРЕДЛОЖЕННЫХ СПОСОБОВ МОЖНО СОБРАТЬ АММИАК ? (1) * (2) (3) 3. В РЕЗУЛЬТАТЕ КАКИХ УРАВНЕНИЙ ОБРАЗУЕТСЯ ИОН АММОНИЯ? N 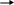 H3+HCl * H3+HCl * N 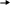 O2+H2O O2+H2ON 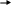 H3+O2 H3+O2( 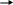 4) NH3+H2SO4 * 4) NH3+H2SO4 * ( 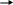 5) NH3+H2O * 5) NH3+H2O *4. ДОБАВЛЕНИЕ КАКИХ ВЕЩЕСТВ, ФОРМУЛЫ КОТОРЫХ ПЕРЕЧИСЛЕНЫ НИЖЕ, ПОДАВЛЯЕТ ДИССОЦИАЦИЮ ВОДНОГО РАСТВОРА АММИАКА ? NH4Cl * H2O H2SO4 (4) NaOH * (5)NH4NO3* 5. РЕАКЦИИ, ОТРАЖАЮЩИЕ КАЧЕСТВЕННУЮ РЕАКЦИЮ НА ИОН АММОНИЯ: N 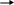 H4Cl+NaOH * H4Cl+NaOH *N 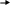 H4Cl+AgNO3 H4Cl+AgNO3 N 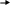 H4NO3+ KOH * H4NO3+ KOH *( 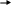 4) (NH4)2SO4+Ba(NO3)2 4) (NH4)2SO4+Ba(NO3)2( 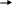 5) NH4NO3+H2SO4 5) NH4NO3+H2SO4Тест: «Азотная кислота» Отметьте номера всех правильных ответов. 1. ФОРМУЛА ОКСИДА, КОТОРОМУ СООТВЕТСТВУЕТ АЗОТНАЯ КИСЛОТА: (1) N2O (4) N2O3 (2) NO2 (5) NO (3) N2O5 * 2. КАКИЕ РЕАКЦИИ, СХЕМЫ КОТОРЫХ ПРИВЕДЕНЫ НИЖЕ, МОЖНО ЗАПИСАТЬ В ВИДЕ КРАТКОГО ИОННОГО УРАВНЕНИЯ: H++OH- =H2O 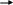 (1) HNO3+NaOH * (1) HNO3+NaOH *  (2) HNO3+NH4OH (2) HNO3+NH4OH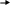 (3) HNO3+Ba(OH)2 * (3) HNO3+Ba(OH)2 * (4) HNO3+Ba(NO3)2 (4) HNO3+Ba(NO3)2( 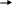 5) HNO3+Fe(OH)3 5) HNO3+Fe(OH)33. В КАКИХ ИЗ РЕАКЦИЙ ВЫДЕЛЯЕТСЯ ВОДОРОД : H 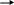 NO3+Zn NO3+ZnH  2SO4 (разб) +Zn * 2SO4 (разб) +Zn * H 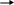 Cl+Cu Cl+CuH 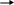 NO3(конц)+Cu NO3(конц)+CuH  Cl(разб)+Fe * Cl(разб)+Fe *4. КАКИЕ ИЗ РЕАКЦИЙ МОЖНО ИСПОЛЬЗОВАТЬ ДЛЯ ПОЛУЧЕНИЯ АЗОТНОЙ КИСЛОТЫ: K 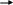 NO3+H2SO4 (в растворе) NO3+H2SO4 (в растворе) N  aNO3(T)+H2SO4 (конц) * aNO3(T)+H2SO4 (конц) *N  aNO3+HCl (в растворе) aNO3+HCl (в растворе) N  2O5+H2O * 2O5+H2O *B 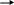 a(NO3)2+H2SO4 (в растворе) * a(NO3)2+H2SO4 (в растворе) *5. МЕХАНИЗМ ВЗАИМОДЕЙСТВИЯ АММИАКА С КИСЛОТАМИ И ВОДОЙ. АТОМ АЗОТА В МОЛЕКУЛЕ АММИАКА: отдает протон окисляется восстанавливается, принимает протон * является донором электронной пары* Тест: «Азот и его соединения». Вариант I Обведите номер правильного ответа. 1. ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ ВНЕШНЕГО ЭНЕРГЕТИЧЕСКОГО УРОВНЯ АТОМОВ ЭЛЕМЕНТОВ VА ГРУППЫ МОЖЕТ БЫТЬ ПРЕДСТАВЛЕНА В ВИДЕ ОБЩЕЙ ФОРМУЛЫ: ns2(n-1)d3 (2) ns2np3 (3) ns1(n-1)d4 2. УСТОЙЧИВОСТЬ ВОДОРОДНЫХ СОЕДИНЕНИЙ В РЯДУ NH3- PH3- AsH3- SbH3- BiH3 (1) возрастает (3) не изменяется (2) уменьшается (4) уменьшается, а затем возрастает 3 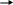 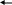 . ПРИ ПОВЫШЕНИИ ДАВЛЕНИЯ РАВНОВЕСИЕ СИСТЕМЫ, ОПИСЫВАЕМОЕ УРАВНЕНИЕМ N2(Г)+3H2(Г) 2NH3(Г), СДВИГАЕТСЯ ТАКИМ ОБРАЗОМ, ЧТО: . ПРИ ПОВЫШЕНИИ ДАВЛЕНИЯ РАВНОВЕСИЕ СИСТЕМЫ, ОПИСЫВАЕМОЕ УРАВНЕНИЕМ N2(Г)+3H2(Г) 2NH3(Г), СДВИГАЕТСЯ ТАКИМ ОБРАЗОМ, ЧТО:образуется больше NH3 образуется больше N2 образуется больше N2 и H2 ни каких изменений не наблюдается 4. ОТРИЦАТЕЛЬНАЯ СТЕПЕНЬ ОКИСЛЕНИЯ ПРОЯВЛЯЕТСЯ АЗОТОМ В СОЕДИНЕНИИ: (1) N2O (3) NO2 (2) NO (4) Na3N 5. АЗОТ ВЫПОЛНЯЕТ ФУНКЦИИ ОКИСЛИТЕЛЯ ПРИ ВЗАИМОДЕЙСТВИИ С: кислородом (2) водородом (3) магнием 6. ПОЛУЧЕНИЕ АММИАКА В ЛАБОРАТОРИИ ОСУЩЕСТВЛЯЕТСЯ ПО СХЕМЕ:  (1) H2+N2 t, кат (1) H2+N2 t, кат  (2) Zn+HNO3 (разб) (2) Zn+HNO3 (разб)N  aOH (тв)+ NH4Cl aOH (тв)+ NH4Cl7. МЕХАНИЗМ ОБРАЗОВАНИЯ ИОНА АММОНИЯ ПРИ РЕАКЦИИ АММИАКА С КИСЛОТАМИ: донорно-акцепторный радикальный ионный 8. ИЗ ОКСИДОВ АЗОТА NO2, NO, N2O3, N2O5 КИСЛОТЫЕ СВОЙСТВА ПРОЯВЛЯЮТ: все оксиды N2O3, NO, N2O5 N2O3, N2O5 9. ПРИ ТЕРМИЧЕСКОМ РАЗЛОЖЕНИИ НИТРАТА СЕРЕБРА ОБРАЗУЮТСЯ: нитрид серебра и кислород оксид серебра и кислород оксид серебра, бурый газ и кислород серебро, бурый газ и кислород 10. АЗОТНАЯ КИСЛОТА НЕ ВЗАИМОДЕЙСТВУЕТ С: (1) Cu (3) Pt (2) Zn (4) Fe 11. ВЗАИМОДЕЙСТВИЕ МЕДНОЙ СТРУЖКИ С КОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТОЙ ПРИВОДИТ К ОБРАЗОВАНИЮ ГАЗА: (1) NO2 (3) N2O (2) NO (4) NH3 12. СУММА КОЭФФИЦИЕТОВ РЕАКЦИИ, ПРИВЕДЁННОЙ В ВОПРОСЕ 11, РАВНА: 10 (2) 20 (3)24 Вариант II Обведите номер правильного ответа. 1. ЭЛЕКТРОННАЯ КОНФИГУРАЦИЯ АТОМА АЗОТА МОЖЕТ БЫТЬ ПРЕДСТАВЛЕНА СЛЕДУЮЩИМ ОБРАЗОМ: (1) N (3) N (2) N (4) N 2. С РОСТОМ ПОРЯДКОВОГО НОМЕРА ЭЛЕМЕНТА КИСЛОТНЫЕ СВОЙСТВА ОКСИДОВ N2O3- P2O3- As2O3- Sb2O3- Bi2O3 усиливаются ослабевают остаются неизменными усиливаются, а затем ослабевают 3. СВОБОДНЫЙ АЗОТ МОЖЕТ ВЫДЕЛИТЬСЯ ПРИ РЕАКЦИИ, ИДУЩЕЙ ПО СХЕМЕ: а 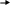 ) NH3+O2 Pt ) NH3+O2 Ptб  ) NH3+O2 горение ) NH3+O2 горениев  ) Zn+HNO3 (конц) ) Zn+HNO3 (конц)г  ) KNO3 t ) KNO3 tд 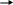 ) NH4NO2 t ) NH4NO2 t(1) а,в (3) в,г (2) б, д (4) г,д 4.ОТРИЦАТЕЛЬНАЯ СТЕПЕНЬ ОКИСЛЕНИЯ ПРОЯВЛЯЕТСЯ АЗОТОМ В СОЕДИНЕНИИ: NH4Cl (2) NO2 (3) NaNO3 5. АЗОТ ВЫПОЛНЯЕТ ФУНКЦИИ ВОССТАНОВИТЕЛЯ ПРИ ВЗАИМОДЕЙСТВИИ С: (1) кислородом (2) водородом (3) литием 6. В ПРОМЫШЛЕННОМ СИНТЕЗЕ АММИАКА КАТАЛИЗАТОРОМ СЛУЖИТ: оксид железа с добавкой оксида алюминия оксид ванадия (V) сплав родия и палладия никель 7. РАСТВОРЫ АММИАКА В ВОДЕ ИМЕЮТ ЩЕЛОЧНУЮ РЕАКЦИЮ, ТАК КАК: (1) молекулы NH3 вступают во взаимодействие с водой по донорно-акцепторному механизму, освобождая ионы OH- (2) молекулы NH3 диссоциируют в воде с отщеплением иона водорода (3) растворяясь в воде, молекулы NH3 усиливают диссоциацию молекул воды, повышая тем самым концентрацию ионов OH- 8. ОКСИД АЗОТА (IV) ПРОЯВЛЯЕТ СВОЙСТВА: кислотного оксида основного оксида несолеобразующего оксида 9. ПРИ ТЕРМИЧЕСКОМ РАЗЛОЖЕНИИ НИТРАТА МЕДИ (II) ОБРАЗУЕТСЯ: нитрит меди (II) и кислород оксид азота (IV) и кислород оксид меди (II), бурый газ и кислород гидроксид меди (II), кислород и азот 10. С КАКИМ ИЗ ПЕРЕЧИСЛЕННЫХ НИЖЕ ВЕЩЕСТВ РЕАГИРУЕТ КОНЦЕНТРИРОВАННАЯ АЗОТНАЯ КИСЛОТА? CO2 C Na2SO4 11. СУММА КОЭФФИЦИЕНТОВ В ХИМИЧЕСКОЙ РЕАКЦИИ, ПРИВЕДЁННОЙ В ВОПРОСЕ 10, РАВНА: 6 12 16 12. ПРИ ВЗАИМОДЕЙСТВИИ АКТИВНОГО МЕТАЛЛА МАГНИЯ С ОЧЕНЬ РАЗБАВЛЕННЫМ РАСТВОРОМ АЗОТНОЙ КИСЛОТЫ ПРОИСХОДИТ ВОССТАНОВЛЕНИЕ ПОСЛЕДНЕЙ ПРЕИМУЩЕСТВЕННО ДО: (1) NO2 (3) N2O (2) NO (4) NH3 Ответы:
3. 7 Амины. Цели тестирования: проверить знания учащихся о строении и свойствах аминов; умения составлять структурные формулы аминов, давать им названия, составлять уравнения реакции, характеризующие химические свойства аминов, сравнивать свойства аминов со свойствами аммиака. План теста:
Вариант I Обведите кружком букву правильного ответа. 1. КАКОЕ ВЕЩЕСТВО СОДЕРЖИТ ФУНКЦИОНАЛЬНУЮ ГРУППУ NH2: а) нитроглицерин б) анилин в) формальдегид 2.ОБЩЕЕ ЧИСЛО ИЗОМЕРОВ ВСЕХ АМИНОВ СОСТАВА C3H9N РАВНО: а) 1 б) 2 в) 3 3. БОЛЕЕ СИЛЬНОЕ ОСНОВАНИЕ-… а) анилин б) этиламин 4. СВОЙСТВА АМИНОВ, КАК ОСНОВАНИЙ, ОПРЕДЕЛЯЮТСЯ: а) способностью к диссоциации в водных растворах б) наличием пары электронов у атома азота в) взаимным влиянием атомов в молекуле 5. ПРОДУКТАМИ ВЗАИМОДЕЙСТВИЯ АМИНОВ С ХЛОРОВОДОРОДОМ ЯВЛЯЮТСЯ: а) соли б) хлорпроизводные углеводородов в) нитросоединения 6. КАКОЕ ВЕЩЕСТВО НАДО ВЗЯТЬ, ЧТОБЫ ПОЛУЧИТЬ ПРИ ВОССТАНОВЛЕНИИ ОРТО- ФЕНИЛЕНДИАМИН ? а) орто - ксилол б) 1,2 - динитробензол в) орто - нитротолуол 7. КАКИЕ ИЗ ПРИВЕДЁННЫХ НИЖЕ АМИНОВ РАСПОЛОЖЕНЫ В ПОРЯДКЕ ВОЗРАСТАНИЯ ИХ ОСНОВНОСТИ ? а) (CH3)3N; (CH3)2NH; CH3NH2 б) C6H5NH2; (C6H5)2NH; (C6H5)3N в) C6H5NH2; NH3; CH3NH2 8. АНИЛИН ПОЛУЧАЮТ РЕАКЦИЕЙ: а) гидрирования фенола б) гидратации хлорбензола в) гидрирования нитробензола г) гидролиза белка 9. ДЛЯ ПОЛУЧЕНИЯ 1 МОЛЯ АНИЛИНА НЕОБХОДИМО ____ ГРАММ АЦЕТИЛЕНА а) 5,2 в) 52 б) 26 г) 78 10. УКАЖИТЕ, КАКИЕ НАЗВАНИЯ СООТВЕТСТВУЮТ СОЕДИНЕНИЯМ А, В И С В СЛЕДУЮЩЕЙ СХЕМЕ ПРЕВРАЩЕНИЙ: HNO3 6[H] 3Br2 Б    ЕНЗОЛ A B C ЕНЗОЛ A B C H2SO4 а) бензолсульфокислота; бензол;1,3,5- трибромбензол б) нитробензол; анилин; 1,3,5- триброманилин в) нитробензол; анилин; 2,4,6- триброманилин Вариант II Обведите кружком букву правильного ответа. 1. СКОЛЬКО ВЕЩЕСТВ ИЗ ПЕРЕЧИСЛЕННЫХ ОТНОСЯТСЯ К АМИНАМ ? 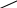 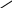 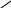 CH3 O CH3 O  - N ; CH3- O- NH2 ; CH3- C ; NH2- CH- COOH - N ; CH3- O- NH2 ; CH3- C ; NH2- CH- COOHCH3 NH2 CH3 а) одно в) три б) два г) четыре 2. СРЕДИ ИЗОМЕРОВ ВСЕХ АМИНОВ СОСТАВА C3H9N ВСТРЕЧАЮТСЯ: а) только первичные амины б) первичные и вторичные амины в) первичные, вторичные и третичные амины 3. АМИНЫ ПРОЯВЛЯЮТ СВОЙСТВА: а) основные б) кислотные в) амфотерные 4. СКОЛЬКО - СВЯЗЕЙ ИМЕЕТСЯ В МОЛЕКУЛЕ АНИЛИНА : а) шесть в) двенадцать б) девять г) четырнадцать 5. КАКОЕ ВЕЩЕСТВО НЕ ВЗАИМОДЕЙСТВУЕТ С МЕТИЛАМИНОМ: а) серная кислота в) хлороводород б) кислород г) гидроксид натрия 6. ПРИ ВЗАИМОДЕЙСТВИИ АНИЛИНА С БРОМНОЙ ВОДОЙ ОБРАЗУЕТСЯ: а) бромид фениламмония б) 2,4,6 - триброманилин в) орто - броманилин 7. ДЛЯ ВЫДЕЛЕНИЯ БЕНЗОЛА ИЗ ЕГО СМЕСИ С АНИЛИНОМ СЛЕДУЕТ ПРОПУСТИТЬ ЧЕРЕЗ РАСТВОР: а) HCl б) CO2 в) H2 8. СХОДСТВО МЕЖДУ АНИЛИНОМ И АММИАКОМ ПРОЯВЛЯЕТСЯ ВО ВЗАИМОДЕЙСТВИИ С: а) кислотами в) водой б) щелочами г) гидроксидом меди (II) 9. ХЛООРОВОДОРОДНАЯ СОЛЬ ПЕРВИЧНОГО АМИНА СОДЕРЖИТ 43,55 % ХЛОРА. ФОРМУЛА АМИНА: а) CH3NH2 б) C2H5NH2 в) C3H7NH2 10. УКАЖИТЕ, КАКИЕ НАЗВАНИЯ СООТВЕТСТВУЮТ СОЕДИНЕНИЯМ А, В И С В СЛЕДУЮЩЕЙ СХЕМЕ ПРЕВРАЩЕНИЙ: HNO3 Fe+HCl(изб) NaOH Б    ЕНЗОЛ А В С ЕНЗОЛ А В С H2SO4 а) бензолсульфокислота; железная соль бензолсульфокислоты; гидроксид железа (III) б) нитробензол; хлорид фениламмония; анилин в) нитробензол; анилин; анилин (реакция не идёт) Ответы теста:
3. 8 Аминокислоты. Белки. Цели тестирования: проверить и закрепить знания учащихся о составе, строении и свойствах аминокислот и белков. План теста: (см. стр. 17) Вариант I Обведите кружком номер правильного ответа. 1. ВОЗМОЖНОЕ ЧИСЛО ИЗОМЕРОВ АМИНОБУТАНОВОЙ КИСЛОТЫ РАВНО: 3 5 7 2. ДЛЯ ВОДНЫХ РАСТВОРОВ ЭТИЛОВОГО ЭФИРА АМИНОУКСУСНОЙ КИСЛОТЫ ХАРАКТЕРНА СЛЕДУЮЩАЯ РЕАКЦИЯ СРЕДЫ: основная кислая нейтральная 3  . РАСТВОР ЛИЗИНА H2N- CH2- CH2- CH2- CH2- CH- COOH ИМЕЕТ . РАСТВОР ЛИЗИНА H2N- CH2- CH2- CH2- CH2- CH- COOH ИМЕЕТ NH2 СЛЕДУЕЩЕЕ ЗНАЧЕНИЕ pH: >7 <7 =7 4. АМИНОКИСЛОТЫ МОГУТ ВЗАИМОДЕЙСТВОВАТЬ С: кислотами щелочами кислотами и щелочами 5. СКОЛЬКО РАЗЛИЧНЫХ ДИПЕПТИДОВ МОЖЕТ БЫТЬ ПОЛУЧЕНО ИЗ ГЛИЦИНА И АЛАНИНА: (1) один (3) три (2) два (4) четыре 6. В СОСТАВ БЕЛКОВ ВХОДЯТ: - аминокислоты алифатические аминокислоты аминокислоты неразветвлённого строения 7. СКОЛЬКО ВЕЩЕСТВ МОЖЕТ ОБРАЗОВАТЬСЯ В РЕЗУЛЬТАТЕ ПОЛНОГО ГИДРОЛИЗА СОЕДИНЕНИЯ: О NH2 - CH2 – C – NH – CH – C – NH – CH – C – O - C2H5 O CH3 O CH2OH (1) три (3) пять (2) четыре (4) шесть 8. ПРОЦЕСС ДЕНАТУРАЦИИ БЕЛКА СОПРОВОЖДАЕТСЯ: разрушением вторичной, третичной и четвертичной структуры распадом молекулы белка на исходные аминокислоты окислением аминокислот, входящих в состав белка. 9. УКАЖИТЕ, КАКИЕ НАЗВАНИЯ СООТВЕТСТВУЮТ СОЕДИНЕНИЯМ A, B, C, D И F В СЛЕДУЮЩЕЙ СХЕМЕ ПРЕВРАЩЕНИЙ: H2O Ag2O Cl2 NH3 фермент а      цетилен A B C D F цетилен A B C D F Hg2+ NH3 свет (1) этанол; этилат серебра; хлорэтан;этиламин; аминоуксусная кислота (2) уксусный альдегид; уксусная кислота; хлоруксусная кислота; глицин; дипептид глицина (3) ацетальдегид; уксусная кислота; хлорэтан; этиламин; аминоуксусная кислота Вариант II Обведите кружком номер правильного ответа. 1. У ______ НЕ МОЖЕТ БЫТЬ ОПТИЧЕСКИХ ИЗОМЕРОВ: H (1) аланин NH2 - C - COOH CH3 (2) глицина NH2 – CH2 – COOH (3) пролина CH2 – CH2 CH2 - CH – COOH N H 2. ДЛЯ ВОДНЫХ РАСТВОРОВ ХЛОРИДА АМИНОУКСУСНОЙ КИСЛОТЫ ХАРАКТЕРНА СЛЕДУЮЩАЯ РЕАКЦИЯ СРЕДЫ: основная кислая нейтральная 3. РАСТВОР ГЛУТАМИНОВОЙ КИСЛОТЫ: HOOC-CH2-CH2-CH-COOH ИМЕЕТ СЛЕДУЮЩЕЕ ЗНАЧЕНИЕ pH : NH2 (1) >7 (2) <7 (3) =7 4. -АМИНОПРОПИОНОВАЯ КОСЛОТА НЕ РЕАГИРУЕТ С: NaOH (2)HCl (3) NaCl 5. В РЕЗУЛЬТАТЕ РЕАКЦИИ ____ ОБРАЗУЕТСЯ ДИПЕПТИД:  а) NH2-CH-COOH-NH2-CH-COOH а) NH2-CH-COOH-NH2-CH-COOHR1 R2  б) NH2-CH-COOH+R2-CH2-COOH б) NH2-CH-COOH+R2-CH2-COOHR1 а (2) б (3) а и б 6. БЕЛКОВЫЕ МОЛЕКУЛЫ ИЗ АМИНОКИСЛОТ ОБРАЗУЮТСЯ ПО РЕАКЦИИ: полимеризации поликонденсации дегидрогенизации 7. СКОЛЬКО ВЕЩЕСТВ МОЖЕТ ОБРАЗОВАТЬСЯ В РЕЗУЛЬТАТЕ ПОЛНОГО ГИДРОЛИЗА СОЕДИНЕНИЯ: О O О O H2N – CH – C – NH -CH-C-NH-CH – C – NH -CH-C-NH-CH2-COOH CH-OH CH3 (CH2)2 CH2 CH3 S SH CH3 (1) три (3) пять (2) четыре (4) шесть 8. КАЧЕСТВЕННОЙ РЕАКЦИЕЙ НА БЕЛОК ЯВЛЯЕТСЯ РЕАКЦИЯ: со свежеосажденным гидроксидом меди (II) с аммиачным раствором оксида серебра с азотной кислотой 9. ПРИ ПОЛУЧЕНИИ КАПРОНА ИЗ - АМИНОКАПРОНОВОЙ КИСЛОТЫ ВЫДЕЛИЛОСЬ 72 КГ. ВОДЫ. МАССА ПОЛУЧЕННОГО КАПРОНА РАВНА: 588 кг. 452 кг. 72 кг. Ответы теста:
3. 9 Виды изомерии. Гомологи. Цели тестирования: проверить и закрепить знания учащихся об основных видах изомерии; умения записывать структурные формулы разных видов изомеров из различных классов органических соединений, называть их и по названию записывать формулы, отличать изомеры от гомологов. План теста:
Инструкция для учащихся: На выполнение теста отводится 25 минут. Задания рекомендуется выполнять по порядку не пропуская ни одного, даже самого лёгкого. Если задание не удаётся выполнить сразу, перейдите к следующему. Если останется время, вернитесь к пропущенным заданиям. К каждому заданию дано несколько ответов, среди которых только один верный. Выберите верный, по вашему мнению, ответ и занесите его в лист ответов. 1  . ИЗОМЕРЫ . ИЗОМЕРЫГОМОЛОГИ – ЭТО: ИЗОМЕРЫ вещества, одинаковые по химическому составу, но различные по химическому строению и свойствам вещества, сходные по строению и свойствам, но различные по составу на одну или несколько групп CH2 макромолекулы, состоящие из большого количества повторяющихся звеньев.  C5H10O2 2  . СОЕДИНЕНИЕ С ОБЩЕЙ ФОРМУЛОЙ C4H10O ОТНОСИТСЯ К . СОЕДИНЕНИЕ С ОБЩЕЙ ФОРМУЛОЙ C4H10O ОТНОСИТСЯ К КАРБОНОВЫХ КИСЛОТ C5H10O КЛАССУ ОДНОАТОМНЫХ СПИРТОВ . ЕМУ СООТВЕТСТВУЕТ АЛЬДЕГИДОВ СЛЕДУЮЩЕЕ ЧИСЛО ИЗОМЕРОВ: (1) 4 (3) 7 (2) 5 (4) 9  ЦИС- БУТЕН-2 И ТРАНС- БУТЕН- 2 ЦИС- БУТЕН-2 И ТРАНС- БУТЕН- 23. СОЕДИНЕНИЯ БУТЕН- 1 И БУТЕН- 2 ЯВЛЯЮТСЯ: 2,2- ДИМЕТИЛ-БУТАН И 2,2-ДИМЕТИЛ ПРОПАН (1) гомологами (3) геометрическими изомерами  (2) структурными изомерами (4) одним и тем же веществом (2) структурными изомерами (4) одним и тем же веществом 4. АМИНОКИСЛОТЫ КАРБОНОВЫЕ КИСЛОТЫ ИМЕЮТ ОДНОАТОМНЫЕ ПРЕДЕЛЬНЫЕ СПИРТЫ СЛЕДУЮЩИЕ ТИПЫ ИЗОМЕРИИ : углеводородной цепи углеводородной цепи, положения функциональной группы углеводородной цепи, положения функциональной группы, цис- транс изомерии углеводородной цепи, положения функциональной группы, цис- транс, положения двойной связи.  C4H8 C4H8 5. СОЕДИНЕНИЕ С ОБЩЕЙ ФОРМУЛОЙ C4H10 ОТНОСИТСЯ К  АЛКЕНОВ C4H6 АЛКЕНОВ C4H6 КЛАССУ АЛКАНОВ ЕМУ СООТВЕТСТВУЕТ СЛЕДУЮЩЕЕ ЧИСЛО АЛКИНОВ ИЗОМЕРОВ: (1) 7 (4) 3 (2) 5 (5) 2 (3) 4  ИЗОМЕРАМИ УГЛЕВОДОРОДНОЙ ЦЕПИ ИЗОМЕРАМИ УГЛЕВОДОРОДНОЙ ЦЕПИ6. ГОМОЛОГАМИ ЯВЛЯЮТСЯ: ИЗОМЕРАМИ ПОЛОЖЕНИЯ ФУНКЦИОНАЛЬНОЙ ГРУППЫ (1) 1- бутанол и 2- метил 1- пропанол (2) цис- олеиновая кислота и транс- олеиновая кислота (3) бутановая и пропионовая кислоты (4) 4- аминобутановая кислота и 2- аминобутановая кислота 7. ЧИСЛО ИЗОМЕРОВ СРЕДИ ВЕЩЕСТВ, ФОРМУЛЫ КОТОРЫХ а) CH3-(CH2)2-O-CH2CH3 в) HOOC-(CH2)3-CH3 б) CH3-(CH2)3-CHO г) C2H5- COO-C2H5 РАВНО: (1) 1 (3) 3 (2) 2 (4) 4 8  . C15H31COOH . C15H31COOHC17H33COOH ХАРАКТЕРНА ИЗОМЕРИЯ: C17H35COOH углеводородной цепи углеводородной цепи, положения функциональной группы положения функциональной группы, цис- транс углеводородной цепи, цис- транс 9. ИЗОМЕРОМ АМИНОМАСЛЯННОЙ КИСЛОТЫ НЕ ЯВЛЯЕТСЯ: NH2- CH2-CH2-CH2-COOH CH3-CH2-CH(NH2)-CООH CH3-CH(NH2)-COOH NH2-CH2-CH2-CH(NH2)-COOH 10. ИЗОМЕРАМИ ЯВЛЯЮТСЯ: пропионовая кислота и 2- метил пропионовая кислота метиловый эфир уксусной кислоты и пропионовая кислота этанол и этаналь пропан и бутан Варианты ответов:
Оценка: Данный тест был апробирован. При анализе результатов тестирования мы пользовались дихотомической оценкой. За правильное выполнение задания учащийся получает один балл, а за неправильное - ноль. Ученик, набравший 10- 9 индивидуальных баллов получает оценку «отлично»; 8 баллов- «хорошо»; 7 баллов- «удовлетворительно»; 6 и менее баллов – «неудовлетворительно». О  бработка результатов тестирования бработка результатов тестирования
Интерпретация результатов тестирования: Из полученной матрицы видно, что для учащихся данного 11 класса задание № 6 оказалось более трудным, так как с ним справилось чуть больше половины класса (17 человек), в то время, как задания № 3,7,9 у подавляющего большинства группы не вызвало затруднений (данные задания не выполнили только четверо учащихся). По итогам тестирования 7 учащихся получили оценку «отлично», из них три человека не допустили ни одной ошибки в тесте;10 учеников выполнили тест на оценку «хорошо»; 8- на «удовлетворительно» и 3 учащихся не справились с заданиями теста. Общая оценка класса за тест- «удовлетворительно». Основные ошибки, допускаемые испытуемыми при выполнении теста: путают изомеры и гомологи; затрудняются в составлении структурных формул изомеров и в названии различных видов изомерии у конкретных классов органических соединений. |

 № задания
№ задания № тестового задания
№ тестового задания № тестового задания
№ тестового задания Тестовые задания
Тестовые задания