модуль 5. Модуль 5 опухоли пищеварительного тракта
 Скачать 0.53 Mb. Скачать 0.53 Mb.
|
|
Анатомическая классификация первичного рака печени Макроскопически первичный рак печени представлен тремя разными формами: массивной, узловой и диффузной. • Массивная форма представлена одним крупным узлом (простая массивная форма) или крупным узлом с метастазами по периферии (массивная форма с сателлитами). • При узловой форме рака в печени обычно находят несколько сравнительно одинаковых по размеру опухолевых узлов. • Диффузная форма встречается реже и представлена опухолью в виде неравномерной инфильтрации паренхимы печени. Гистологическая классификация первичного рака печени Первичный рак печени по гистологическому строению подразделяют на гепатоцеллюлярный рак, холангиоцеллюлярный рак и смешанный гепатохолангиоцеллюлярный рак.
• Гепатоцеллюлярный рак по строению различают: - трабекулярный, состоящий из более крупных клеток, чем нормальные гепатоциты, с обильной эозинофильной цито- плазмой, при этом клетки формируют двух-, трёх- или многорядные трабекулы и тяжи; - железистый; - псевдожелезистый (ацинарный); - компактный (солидный, при этом иногда светлоклеточный); - скиррозный; - низкодифференцированный с признаками анаплазии и гигантскими многоядерными клетками. • Холангиоцеллюлярный рак - злокачественная опухоль печени, представленная клетками, напоминающими эпителий желчных протоков. Железистоплоскоклеточный и плоскоклеточный рак - редко встречающиеся формы холангиоцеллюлярного рака печени, источником их развития считают метаплазированный эпителий желчных протоков. • Смешанный гепатохолангиоцеллюлярный рак содержит явные элементы как гепатоцеллюлярного рака, так и холангиоцеллюлярного рака. Для строения опухоли характерна продукция желчи и признаки секреции слизи. Такие опухоли встречаются редко. Классификация первичного рака печени по системе TNM • Классификация по системе TNM применима только для первичного гепатоцеллюлярного и холангиоцеллюлярного рака. Т - первичная опухоль. - Тх - недостаточно данных для оценки первичной опухоли. - T0 - первичная опухоль не определяется. - T1 - солитарная опухоль до 5 см в наибольшем измерении без инвазии сосудов. - T2 - солитарная опухоль до 5 см в наибольшем измерении с инвазией сосудов или множественные опухоли до 5 см в наибольшем измерении без инвазии сосудов, ограниченные одной долей, или солитарная опухоль более 5 см в наибольшем измерении без инвазии сосудов. - T3 - солитарная опухоль более 5 см в наибольшем измерении с инвазией сосудов или множественные опухоли не более 5 см в наибольшем измерении с инвазией сосудов, ограниченные одной долей, или ограниченные одной долей множественные опухоли, любая из которых более 5 см с или без инвазии сосудов.
- T4 - множественные опухоли в обеих долях или опухоль, поражающая основную ветвь портальной или печёночной вены, или опухоль с распространением на соседние органы, кроме желчного пузыря, или опухоль, прорастающая висцеральную брюшину. • N - регионарные лимфатические узлы (регионарными лимфатическими узлами печени считают узлы ворот печени, расположенные в гепатодуоденальной связке). - Nx - недостаточно данных для оценки регионарных лимфатических узлов. - N0 - лимфоузлы ворот печени и гепатодуоденальной связки не поражены. - N1 - имеется поражение лимфатических узлов ворот печени или гепатодуоденальной связки метастазами. • М - отдалённые метастазы. - Мх - недостаточно данных для определения отдалённых метастазов. - M0 - нет данных за наличие отдалённых метастазов. - M1 - наличие отдалённых метастазов. Первичный рак печени можно сгруппировать по стадиям согласно Международной классификации по системе TNM (табл. 5-3). Таблица 5-3. Стадии первичного рака печени согласно Международной классификации по системе TNM 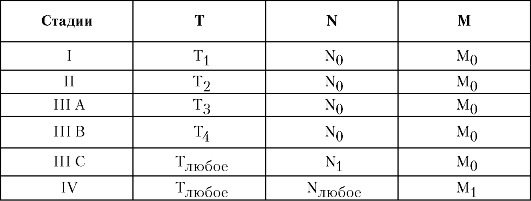 Диагностика • Для диагностики первичного рака печени применяют УЗИ, КТ, ангиографию, иммуногистохимические и другие методы исследования. УЗИ позволяет диагностировать большинство случаев очагового поражения печени. Под его контролем возможно выполнить чрескожную пункционную аспирационную цитобиопсию опухоли печени с последующим цитологическим исследованием полученного материала, что позволяет в 76,5% решить вопрос о наличии опухолевого процесса в печени. • КТ обладает большей чувствительностью и специфичностью, чем УЗИ, особенно при диагностике опухолей диаметром менее 1 см. На большинство вопросов, связанных с распространённос- тью опухолевого поражения печени, может ответить аксиальная рентгеновская КТ. Кроме того, КТ сканирование имеет особую ценность для определения степени распространённости, чётких анатомических границ опухоли и возможности её резекции. Методом КТ достаточно достоверно дифференцируют кистозные и солидные образования в печени. Для дифференциальной диагностики сосудистых новообразований (гемангиом) и несосудистых опухолей печени используют эмиссионную КТ печени с мечеными эритроцитами. Методика основана на использовании in vivo меченых эритроцитов (посредством внутривенного введения специальных радиопрепаратов). Последующая сцинтиграфия позволяет визуализировать анатомические органы и структуры, содержащие значительное количество крови (сердце, кровеносные сосуды, селезёнку и гемангиомы).
• Ангиография выявляет патологические изменения печени в 95,2%. Проводя такое исследование при подозрении на неопластический процесс в печени, возможно чётко локализовать анатомическую область поражения (доля, сегмент), выяснить характер поражения (доброкачественное, злокачественное) и предположить гистологический вариант строения опухоли. • Иммуногистохимические и молекулярно-биологические методы диагностики у больных с гепатоцеллюлярным раком печени в последнее время приобрели большое значение. Применяют реакцию на выявление эмбриоспецифического α-фетопротеина (АФП), получившую название реакции Абелева-Татаринова. Суть заключается в том, что у здоровых людей и лиц, больных различными неонкологическими заболеваниями печени, АФП в сыворотке крови отсутствуют, а при гепатоцеллюлярном раке печени его удаётся обнаружить у 75-80% обследованных. Лечение Для лечения первичного рака печени используют локальные методы опухолевой деструкции, химиотерапию и хирургические методы. • Локальные методы опухолевой деструкции: алкоголизация, радиочастотная термоаблация и интраартериальная химиоэмболизация. - Алкоголизация (абляция этанолом). К числу региональных методов лекарственного лечения относят чрескожную абляцию этанолом или 50% уксусной кислотой, выполняемую под контролем УЗИ или КТ. Локальная деструкция опухоли может быть использована в лечении опухолей, не превышающих в диаметре 2 см. Опухоли большего размера (3-5 см) или многоузлового строения характеризуются 50% частотой достижения полного эффекта. При увеличении размеров узлов частота эффективности процедуры снижается. Методы деструкции, большинство из которых предусматривает её проведение чрескожно под визуальным контролем, разработаны в качестве минимально инвазивной тактики лечения у пациентов с малым гепатоцеллюлярным раком. Рецидивирование опухоли после эффективного чрескожного лечения возникает так же часто, как и после резекции печени: 50% через 3 года и свыше 70% - через 5 лет.
- Радиочастотная термоабляция. Высокочастотная деструкция, разработанная в Италии в 1993 г., представляет новое направление среди методов деструкции, суть которого заключается в индукции коагуляционного некроза опухоли посредством термического воздействия. Рандомизированные исследования показывают преимущество высокочастотной деструкции над чрескожным введением этанола в техническом и раннем прогностическом аспектах. - Внутриартериальная химиоэмболизация - региональная лекарственная терапия, которая применима при опухолях более крупного размера, чем подлежащие абляции, но связана с большим риском осложнений. Сам по себе факт эмболизации лишает или по меньшей мере ограничивает кровоснабжение опухолевых клеток. Дополнение эмболизации воздействием цитостатика в виде суспензии в жировом рентгенконтрастном веществе, создаёт условия для длительного цитостатического действия на опухоль, теоретически без системных токсических эффектов. Для химиоэмболизации при первичном раке печени применяют доксорубицин, иногда в комбинации с митомицином или цисплатином. Наиболее серьёзные ослож- нения - печёночная недостаточность, инфаркты, абсцессы печени и билиарный некроз наблюдают в 3-4% случаев. • Системная химиотерапия. Очевидно, что при всех возможностях хирургического и регионального лекарственного лечения остаётся большая группа больных гепатоцеллюлярным раком, для которых по степени распространения опухоли и другим показателям «методом выбора» остаются попытки системной химиотерапии. В качестве монохимиотерапевтических агентов наибольшую противоопухолевую активность проявляют эпирубицин (17% ответа), цисплатин (17%), доксорубицин (11-32%), митоксантрон (27%) и гемцитабин (36%). • Хирургическое лечение первичного рака печени проводят методом резекции и трансплантации.
- В настоящее время резекция печени остаётся методом выбора в лечении первичного рака печени. Абсолютные противопоказания к резекции печени: генерализация опухолевого процесса на обе половины печени, множественные метастазы в лимфатических узлах и органах (лёгкие, поджелудочная железа, сердце), выраженный цирроз печени, поражение опухолевыми узлами кавальных и портальных ворот печени, нижней полой вены, тяжёлое общее состояние больного. Относительные противопоказания к резекции печени: одиночные метастазы в регионарных лимфатических узлах, лёгком. Хирург может удалить до 70% поражённой печени при условии отсутствия цирроза, и в течении 2-6 нед после операции печень регенерирует. Резекция обеспечивает получение отличных результатов в случае одиночных узлов при хорошо сохранённой функции печени. Пятилетняя выживаемость после резекции печени различна в разных странах и колеблется от 27% до 49%. Послеоперационные осложнения после резекции печени при раке варьируют в пределах от 6% до 52%, по данным отечественных и зарубежных клиник. Специфическими осложнениями принято считать кровотечение из культи печени, желчные перитониты, желчные свищи, поддиафрагмальные абсцессы, секвестрацию участков печени и печёночную недостаточность. Процент летальности колеблется в различных пределах - 3,45-21,8%. - Трансплантация печени показана пациентам с декомпенсированным циррозом печени или на ранних стадиях развития опухоли с многоузловым ростом (3 узла диаметром не более 3 см). Биологическая несовместимость чужеродных тканей весьма затрудняет трансплантацию. Ортотопическая пересадка печени относится к разряду самых сложных оперативных вмешательств, находящих своё применение при обширных поражениях паренхимы печени гепатоцеллюлярным раком. К настоящему времени в мире насчитывается более 200 трансплантационных центров по пересадке печени, имеющих опыт проведения более 100 тыс. операций. Пятилетняя выживаемость пациентов после трансплантации печени по поводу ранних стадий первичного рака печени сравнима с выживаемостью после пересадки печени у лиц без злокачественных опухолей (70%), а частота рецидивов не превышает 25%.
МЕТАСТАТИЧЕСКИЙ РАК ПЕЧЕНИ Метастатическое поражение печени встречают в клинической практике значительно чаще, чем первичное. Установлено, что у каж- дого третьего онкологического больного независимо от локализации первичной опухоли встречают метастазы в печени. При локализации опухоли в зонах, дренируемых воротной веной, печень становится первым и часто единственным, органом-мишенью для возможного метастазирования. В первую очередь печень поражают метастазы рака органов желудочно-кишечного тракта (ЖКТ). У 60% онкологических больных с опухолями желудка и толстой кишки на аутопсиях обнаруживают метастатическое поражение печени. Лечение больных с метастатическим поражением печени - трудная задача. Оно включает хирургический подход, химиотерапию, иммунотерапию и выбирается в зависимости от общего состояния больного, возраста, гистологической характеристики первичной опухоли, размеров, анатомической локализации и соотношения с соседними органами, количества опухолевых узлов в паренхиме, от состояния паренхимы в целом, наличия цирроза, вирусного гепати- та B, C и др. Основным методом лечения, дающим шанс на существенное продление жизни при метастатическом поражении печени у больных колоректальным раком, является хирургическое удаление новообразований. Пятилетняя выживаемость при хирургическом лечении изолированных метастазов колоректального рака в печени, по данным Российского Онкологического Научного Центра им. Н.Н. Блохина, составляет 37,5%. Пятилетней выживаемости среди больных, получавших химиотерапию или симптоматическое лечение, у больных с солитарными и единичными метастазами в печени, не было. Целесообразность хирургической тактики при метастатических опухолях печени других первичных локализаций выступает объектом изучения. В результате проведённого в Российском Онкологическом Научном Центре им. Н.Н. Блохина сравнительного анализа отдалённых результатов хирургического и лекарственного лечения в зависимости от локализации первичной опухоли, определена тактика лечения больных с метастазами не колоректальных опухолей в печень. Показано выполнение резекции печени по поводу метастазов сразу же при их выявления больным с локализацией первичной опухоли в почке, надпочечнике, желудке, желчном пузыре, при нейроэндокринных опухолях. Больным с лока- лизацией первичной опухоли в яичниках, яичке, молочной железе, показано выполнение резекции печени по поводу метастазов в плане комбинированной терапии после проведения лекарственного лечения. Больным с локализацией первичной опухоли в поджелудочной железе, фатеровом сосочке, лёгком, а также с меланомой кожи выполнение резекции печени по поводу метастазов не показано.
ТЕСТОВЫЕ ЗАДАНИЯ Выберите один или несколько правильных ответов 1. Какие факторы способствуют развитию первичного рака печени? A. Гепатиты. Б. Цирроз. B. Паразитарные заболевания. Г. Длительный приём гормональных контрацептивов. Д. Курение. Е. Пожилой возраст. Ж. Всё перечисленное. 2. Микроскопические формы первичного рака печени (1 ответ). A. Гепатоцеллюлярный рак. Б. Холангиоцеллюлярный рак. B. Лимфосаркома. Г. Липосаркома. Д. Ангиосаркома; Е. Злокачественная фиброзная гистиоцитома. Ж. Всё перечисленное. 3. Пути метастазирования при первичном раке печени (1 ответ). A. Гематогенный путь. Б. Лимфогенный путь. B. Имплантационный путь. Г. Всё перечисленное. 4. Куда наиболее часто метастазирует первичный рак печени (3 о т вета)? A. Печень. Б. Кости. B. Лимфоузлы ворот печени. Г. Головной мозг. Д. Лёгкие. Е. Почки. Ж. Всё перечисленное. 5. Какие методы наиболее часто применяют для диагностики и оценки распространённости опухолевого поражения печени (5 ответов)? A. УЗИ брюшной полости. Б. КТ брюшной полости. B. Сканирование костей скелета. Г. Пункционная биопсия опухоли. Д. Определение опухолевых маркёров. Е. Рентгенологическое исследование лёгких. Ж. КТ головного мозга. 6. Уровень каких опухолевых маркёров наиболее часто повышен при первичном раке печени (1 ответ)? A. РЭА. Б. СА 19-9. B. СА 125. Г. АФП. Д. ПСА. Е. ХГЧ. Ж. Всё перечисленное. 7. Уровень каких опухолевых маркёров наиболее часто повышен при колоректальном метастатическом раке печени (1 ответ)? А. РЭА. Б. СА 19-9. В. СА 125. Г. АФП. Д. ПСА. Е. ХГЧ. Ж. Всё перечисленное. 8. Какой метод морфологической верификации опухоли печени наиболее доступен (1 ответ)? A. Лапароскопическая биопсия. Б. Биопсия под контролем УЗИ. B. Интраоперационная биопсия.
9. Клинические признаки первичного рака печени (1 ответ). A. Гепатомегалия. Б. Боль. B. Похудание. Г. Понижение аппетита. Д. Общая слабость. Е. Повышение температуры. Ж. Асцит. З. Желтуха. И. Всё перечисленное. |
