Конспект по електронике. Навчальний посібник за загальною редакцією С.І. Проценка Рекомендовано вченою радою Сумського державного університету Суми
 Скачать 2.49 Mb. Скачать 2.49 Mb.
|
|
Контрольні запитання 1. Хід виконання роботи. 2. У чому полягає явище епітаксії? Який фізичний зміст температур То і Те? 3. Які параметри конденсації визначають ступінь монокристалічності плівок (проілюструвати на прикладі плівок Ві/(001)NаСl)? 4. Розказати порядок проведення експерименту. 5. Як препарують зразки для дифракційних досліджень? 6. Чим за зовнішнім виглядом відрізняються електронограми від полікристалічної та епітаксіальної плівок? 7. Як відрізняються питомі опори полікристалічної і епітаксіальної плівок? 8. Які методи використовуються для вивчення орієнтованого росту плівки? Список літератури 1. Палатник Л. С. Ориентированная кристаллизация / Л. С. Палатник, И. И. Папиров. – Москва : Металургия, 1964. – 408 с. 2. Проценко І. Ю. Прилади і методи дослідження плівкових матеріалів: навч. посіб. / І. Ю. Проценко, А. М. Чорноус, С. І. Проценко. – Суми : Вид-во СумДУ, 2007. – 264 с. Лабораторна робота 3 Вивчення законів електролізу та електролітів для одержання металевих плівок Мета роботи – ознайомитися з основними електролітами, що використовуються під час виробництва мікросхем; визначити хімічний, електрохімічний еквівалент міді, число Фарадея та заряд електрона. Елементи теорії. На різних етапах технічного процесу виготовлення багатьох типів напівпровідникових приладів та інтегральних мікросхем на пластини, кристали або деталі корпусів наносять металеві покриття. При цьому використовують різні методи осадження. Одним із таких методів є електрохімічний, тобто одержання плівки із електроліту. Матеріали для електролітів та технологія повинні задовольняти деякі вимоги. По-перше, в електроліті не повинно бути домішок, які можуть змінити склад плівок та їх електрофізичні властивості. Посуд для електроліту повинен бути з кераміки, скла, кварцу або пластмас, оскільки з металевого посуду в електроліт можуть потрапити домішки. Крім цього, домішки можуть потрапити в електроліт з матеріалом анода. Вимоги, поставлені до матеріалу електроліту, пов'язані з технологічним процесом одержання плівок; це: - нагрівостійкість; - розчинність у кислотах, лугах, воді; - електропровідність, теплопровідність; - стійкість до денного світла; - незмінність складу з часом, небезпечність. Матеріали, з яких виготовляють електроліт, не повинні утворювати бульбашок, виділяти газ. Розглянемо деякі поняття та фізичні процеси, ЩО відбуваються в електролітах. При розчиненні у воді деяких речовин внаслідок взаємодії молекул води з молекулами речовини дуже послаблюються сили зв'язку між окремими атомами. Послаблення приводить до того, що енергії теплового руху молекул води стає достатньо для того, щоб розірвати цей зв'язок. В результаті утворюються заряджені частинки, які мають назву іонів. Такий процес одержав назву електролітичної дисоціації (обернений процес має назву асоціації). Наприклад, NaClNa+Cl-. Розчин, у якому відбулася дисоціація, називається електролітом. Іони в електроліті є носіями електричного заряду. Розглянемо процес перебігу електричного струму Iчерез електроліт. Внаслідок дії електричного поля зовнішнього джерела іони прийдуть в упорядкований рух. Позитивні іони (катіони) почнуть рухатися до негативного електрода (катода), а негативні (аніони) – до анода. Нехай за деякий час tна катод осіло N іонів, це приведе до збільшення його маси на m: 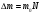 , (1) , (1)де m0 – маса одного катіона. При цьому буде переноситися заряд 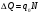 , (2) , (2)де q0– заряд катіона. Знаючи те, що 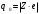 , дe Z – валентність іона; e – заряд електрона, матимемо: , дe Z – валентність іона; e – заряд електрона, матимемо: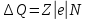 . (3) . (3)Поділивши (1) на (2), маємо 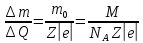 , (4) , (4)де 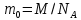 , М– молярна маса; NA– число Авогадро. , М– молярна маса; NA– число Авогадро.Звідси 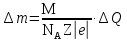 або або 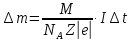 . (5) . (5)Останній вираз носить назву першого закону Фарадея для електролізу: маса речовини, що виділяється на електроді, пропорційна заряду, який пройшов через електроліт. Величина 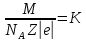 має назву електрохімічного еквівалента, має назву електрохімічного еквівалента, 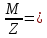 – хімічний еквівалент. – хімічний еквівалент.Із першого закону Фарадея випливає другий – електрохімічний еквівалент, пропорційний хімічному: 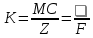 , (6) , (6)де 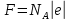 – число Фарадея. Воно показує, який заряд потрібно пропускати через електроліт для виділення на електроді одного моля речовини (F=9,64845104 Кл/моль). – число Фарадея. Воно показує, який заряд потрібно пропускати через електроліт для виділення на електроді одного моля речовини (F=9,64845104 Кл/моль).Далі розглянемо склад основних електролітів, які використовуються під час виробництва мікроелектронних приладів. Електроліти для покриття міддю. Мідь використовують як підшар для покриття нікелем, хромом, сріблом та золотом, при цьому покриття наносять із ціанистих та кислих електролітів. Ціанисті електроліти виготовляють на основі ціанистої міді, а інколи вводять сірчанокислий натрій, який зменшує витрату ціаніду на відтворення іонів двовалентної міді. Під час виготовлення мідних ціаністих електролітів концентрований розчин ціанистого натрію, змішуючи, додають до ціанистої міді, а потім вводять решту компонентів. Найчастіше використовують вісім електролітів. Наприклад, склад електроліту № 1 такий: 15 г/л ціанистої міді, 10 г/л ціанистого натрію, 15 г/л вуглекислого натрію, 30 г/л сірчанокислого натрію. Процес проходить при Т = 18 – 20 C та густині струму 0,3-0,5 А/дм2. Вихід щодо струму 70 %. Електроліт № 4 складається із 120 г/л ціанистої міді, 20 г/л вуглекислого натрію, 20 г/л роданистого калію та 35 г/л їдкого натру. Процес проводять при 75 С і густині струму 10 А/дм2. Вихід щодо струму 98 %. Кислотні електроліти в основному складаються із мідного купоросу та кислоти. Для покращання структури шару міді в електроліт додають фенол, етиловий спирт, сірчанокислий натрій та інші компоненти. Наприклад, електроліт № 1 складається з 200 г/л мідного купоросу, 5 г/л сірчаної кислоти та 1–2 г/л етилового спирту або фенолу. Процес проводять при 20–25 °С та густині струму 2–3 А/дм2. Вихід щодо струму 95 %. Електроліти для покриття сріблом. Срібні покриття використовують у виробництві напівпровідникових приладів та інтегральних мікросхем для підвищення електропровідності струмопровідних елементів, покриттів внутрішніх поверхонь хвилеводів. Для цього широко використовують ціанисті електроліти, головним чином розчини ціанистих солей срібла, оскільки вони утворюють дрібнокристалічні, непористі плівки срібла. Із неціанистих електролітів використовують залізосинеродисті, іодні або роданисті, проте вони відрізняються гіршою якістю покриттів. У електролітах для сріблення як аноди використовують пластини зі срібла марки Ср99,9. Наприклад, електроліт № 1 складається з 2–5 г/л хлористого срібла та 80–100 г/л ціанистого калію. Процес проводять при 18 – 25 С та густині струму 1,5–2 А/дм2. Електроліт використовують для попереднього покриття сріблом. Електроліт № 2 складається з 27 г/л хлористого срібла та 48 г/л вуглекислого калію. Процес проводять при 18–20°С, при густині струму 0,3 А/дм2. Електроліт використовують для кінцевого покриття сріблом. Електроліти для позолочення. Позолочення – один із найбільш поширених в електронній техніці вид покриттів. Для цього використовують чотири типи електролітів: лужні, слаболужні, нейтральні та кислі на основі комплексних ціанистих солей, у яких золото знаходиться у вигляді іона диціаноурату. Найбільш часто використовують лужні електроліти. Крім основних компонентів – комплексної золотої солі та вільного ціаніду, до електроліту можуть входити різні домішки, що покращують колір покриття та його механічні властивості. Як анод використовують пластини із золота, нержавіючої сталі та графіту. Наприклад, електроліт № 1 складається з 1 г/л диціаноурату калію (К[Au(CN2)]), 1,5 г/л хлористого калію, 1,3 г/л біфталату калію, 2,5 г/л лимонної кислоти, 3 г/л вольфрамовокислого натрію та 0,2 г/л трилону. Процес проводять при 90 °С та густині струму 0,5 А/дм2. Електроліт № 6 складається з 2,6 г/л золотохлористої водневої кислоти (Н(АuС14)+4Н20), 15–20 г/л залізноціанистого калію та 20–25 г/л соди. Процес проводять при 50–55 °С та густині струму 0,1–0,2 А/дм2. Електроліти для покриття хромом. Дзеркальні хромові покриття за відновною здатністю поступаються лише срібним. Крім цього, вони стійкі до впливу зовнішніх умов, основ, кислот. Деталі та елементи корпусів інтегральних мікросхем та напівпровідникових приладів хромуються для захисту їх від корозії та з метою надання їм гарного зовнішнього вигляду. Основною складовою частиною хромових електролітів є хромовий ангідрид, від концентрації якого залежить якість покриття, з домішками сірчаної кислоти (близько 1 %). Наприклад, електроліт № 2 складається з 150 г/л хромового ангідриду та 1–1,5 г/л сірчаної кислоти. Процес проходить при 50 – 55 °С та густині струму 30–40 А/дм2. Вихід щодо струму 12–13%. Порядок виконання роботи 1. Підготувати 10–15 % розчин CuSО4. 2. Очистити від корозії пластини. 3. Зважити катод. Визначити площу опущеної в електроліт пластини. За схемою (рис. 1) ввімкнути послідовно джерело постійного струму та електролітичну ванну. 5. Підібрати силу струму не більше 0,02 А на кожний квадратний сантиметр катода. В протилежному разі осяде крихкий, забруднений шар міді. 6. Пропускати струм 20 - 30 хвилин, стежачи за показниками амперметра та підтримуючи їх постійними. 7. Вимкнути струм та просушити катод. Зважити його, знайти m. 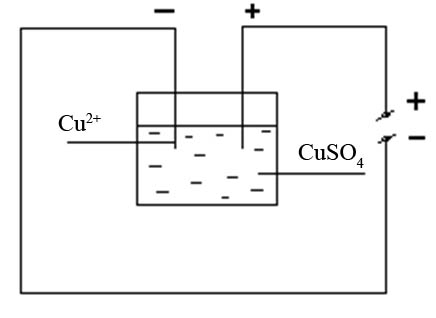 Рисунок 1 – Схема електричної комутації для електролітичного осадження міді. Константи, необхідні для розрахунків: NA = 6,022·1023 моль-1, |e| = 1,6·10-19 Кл, МCu = 63,546·10-3 кг/моль, F = 9,64845·104 кг/моль, Z = 2 8. Розрахувати: К, , F, |e|. Визначити відносну похибку розрахунку заряду електрона за формулою 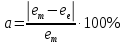 , (7) , (7)де ет – теоретичний заряд електрона; ее – заряд електрона, що визначений експериментально. Зміст звіту Номер, назва, мета роботи. Конспект методичних вказівок. Таблиця з експериментальними результатами. Висновки. Контрольні запитання Які вимоги поставлені до матеріалу електроліту? Що таке асоціація та дисоціація? Одержати закони Фарадея для електролізу. 4. Який фізичний зміст числа Фарадея? 5. Розповісти про електроліти для покриття міддю, сріблом, золотом та хромом. 6. Зобразити схему електричної комутації для електролітичного осадження міді. 7. Як підібрати силу струму для одержання якісного покриття з міді? Список літератури Загальна фізика. Лабораторний практикум: навч. посібник / В. М. Барановський, Н. В. Бережний, І. І. Горбачук та ін. – Київ: Вища школа, 1992. – 509 с. Курносов А. И. Материалы для полупроводниковых приборов и интегральных микросхем / А. И. Курносов – Москва : Высшая школа, 1980.– 327с. Лабораторна робота 4 Корпуси для інтегральних мікросхем Мета роботи – ознайомлення з конструкцією, типами та технологією виготовлення корпусів для інтегральних мікросхем. Елементи теорії. Корпуси для інтегральних мікросхем (ІМС) повинні задовольняти ряд вимог, що забезпечують їх надійну експлуатацію. Корпус повинен мати достатню механічну міцність, щоб витримувати навантаження, які виникають під час складання ІМС та у процесі експлуатації. Потрібно, щоб він мав якомога менші розміри та форму, яка б дозволяла виконувати компактне збирання. Конструкція корпусу повинна дозволяти легко та надійно виконувати електричні з’єднання між кристалом або платою мікросхеми та зовнішніми виводами. Паразитні індуктивності та ємності, незважаючи на високу густину провідників у корпусі, повинні бути мінімальними, електропровідні елементи у корпусі надійно ізольованими один від одного. Тепловий опір між мікросхемою та навколишнім середовищем повинен мати мінімально можливе значення. Корпус інтегральної мікросхеми має бути герметичним. Внутрішнє середовище у корпусі не повинне позначитися на її робочих характеристиках та надійності. Корпус повинен захищати пристрій чи мікросхему від зовнішнього впливу, в тому числі світла та іншого зовнішнього випромінювання, хімічної дії (наприклад, кисню або вологи). Корпуси повинні бути уніфікованими. Для напівпровідникових мікросхем розроблено велику кількість різних типів корпусів, серед них найбільш поширені плоский металоскляний або керамічний модифікований варіант транзисторного корпусу типу ТО та пластмасовий корпус. Для гібридних мікросхем застосовують частіше металоскляний квадратний або прямокутний та пенальний корпуси. Плоский керамічний корпус може бути прямокутним або квадратним. Деталі конструкції плоского керамічного корпусу зображені на рис. 1. Цей корпус складається з трьох основних частин: керамічної основи у вигляді плоскої пластини 1; виводів 5, виконаних з металу у вигляді фігурних тонких стрічок, що відповідають за формою пазам у рамці, в яких вони розташовуються під час збирання; керамічної кришки 7. 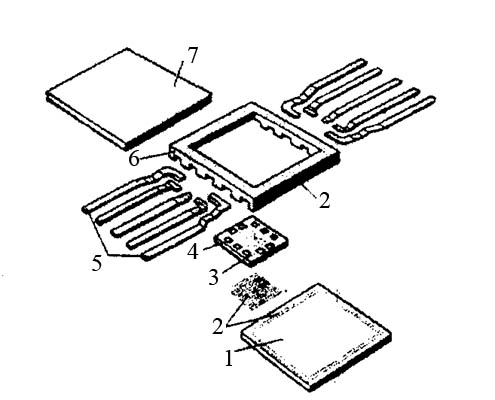 Рисунок 1 – Деталі плоского керамічного корпусу: 1 – керамічна основа; 2 – скляний припій; 3 – кристал мікросхеми; 4 – контактні площадки; 5 – металеві виводи; 6 – рамка; 7 – керамічна кришка Корпус типу ТО має круглу форму (діаметр становить 9,6 мм, висота – 4,6 мм), вісім, десять або дванадцять виводів. Корпуси характеризуються високою надійністю, забезпечують гарне екранування мікросхеми від зовнішніх електромагнітних полів. Окремі деталі корпусу наведені на рис. 2. Фланець має ключ у вигляді виступу. Виводи в основі корпусу герметизують металоскляним спаєм. Герметизацію корпусу виконують за допомогою зварювання металевих фланців балона та кришки. Корпус може мати у деяких випадках вивід, який приварюється до фланця і служить для заземлення. З розмірами корпусу можна ознайомитися, скориставшись рис. 3 та табл. 1. 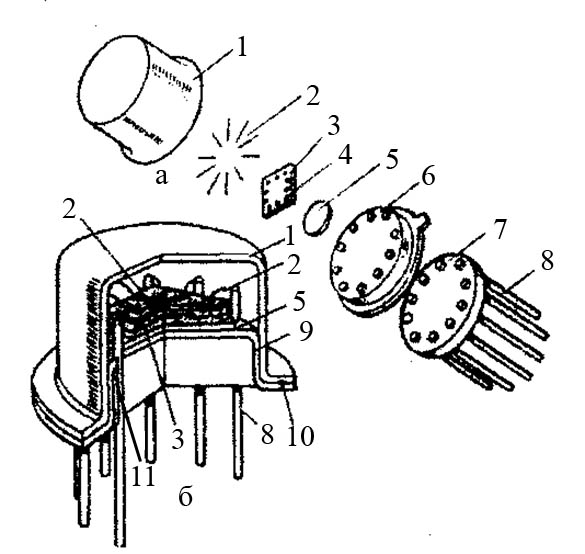 Рисунок 2 – Деталі корпусу типу ТО (а) та корпус у зібраному вигляді (б): 1 – балон; 2 – з'єднувальні провідники із золотого дроту; 3 – кристал мікросхеми; 4 – контактні площадки; 5 – припій; 6 – ковпачок; 7 – скло; 8 – виводи; 9 – місце з'єднання скла з металевим ковпачком; 10 – з'єднувальні фланці; 11 – місце з'єднання виводів зі склом 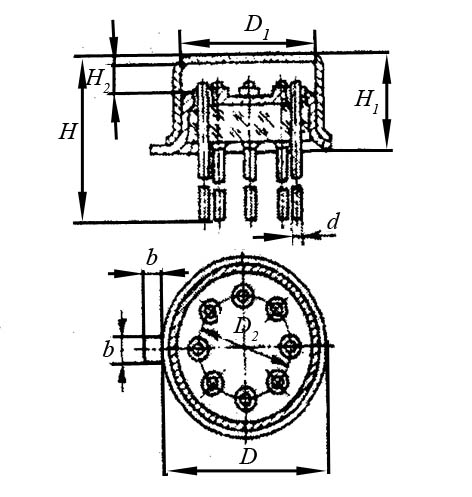 Рисунок 3 – До вимірювання розмірів металоскляного круглого корпусу Таблиця 1 – Параметри металоскляного круглого корпусу
Пластмасовий корпус все більше використовується для напівпровідникових мікросхем завдяки порівняно невисокій вартості. На відміну від корпусів інших типів він не має здатності відводити теплоту і не може працювати у великих температурних межах, які потрібні в деяких пристроях. Але у багатьох випадках використання пластмасового корпусу цілком можливе. Загальний вигляд пластмасового корпусу показаний на рис. 4. Розміри корпусу можна визначити, скориставшись рис. 5, а результати вимірювання потрібно занести до табл. 2. 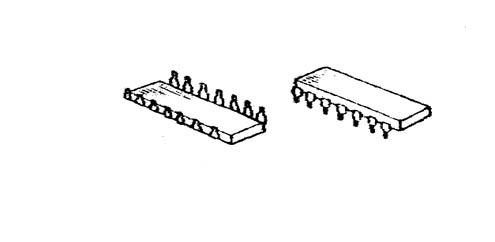 Рисунок 4 – Зовнішній вигляд пластмасового корпусу для напівпровідникових мікросхем 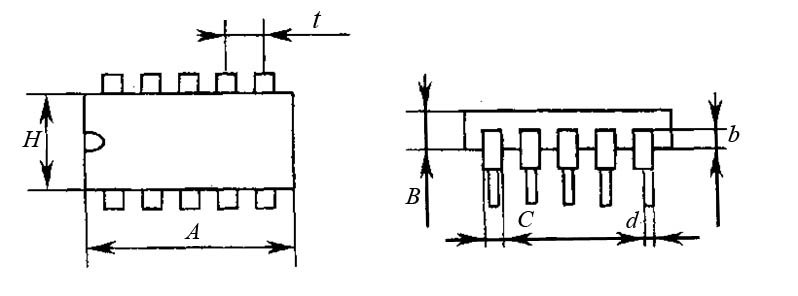 Рисунок 5 – До вимірювання розмірів пластмасового корпусу Металоскляний квадратний корпус (рис. 6) складається з металевої основи 1 зі впаяними ізольованими виводами 4, ізолятора 3 і металевої кришки 2. Виводи в основі корпусу герметизують металоскляним спаєм. Після остаточного монтажу мікросхеми герметизацію корпусу виконують електронно-променевим зварюванням фланців основи та кришки. Розміри корпусу наведені у табл. 3. 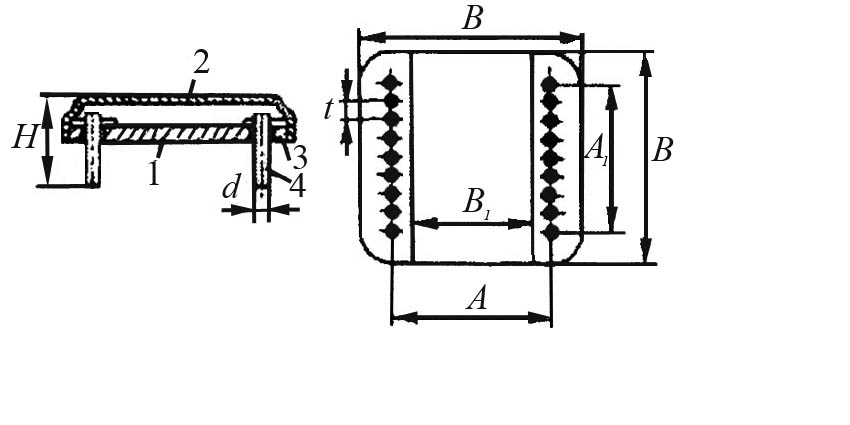 Рисунок 6 – Металоскляний корпус для гібридної ІМС Крім розглянутих видів, застосовують пенальні корпуси. Пенальний корпус (рис. 7) складається з алюмінієвого кожуха 1, в який вставляють плату з плівковою мікросхемою 2. До контактних площадок 3 приварюють контактну гребінку з виводами 4. Транзистори розташовують у касеті 5, яку закріплюють на платі клеєм. Розміри корпусу L= 16 мм; l= 1,2 мм; В= 1,7 мм; В1 = 1,3 мм; В= 0,08 мм; Н= 9 мм; Н1 =5 мм; а= 0,4 мм; t=1 мм; число виводів 14. Герметизацію корпусу виконують шляхом заливу компаундом з боку виводів. 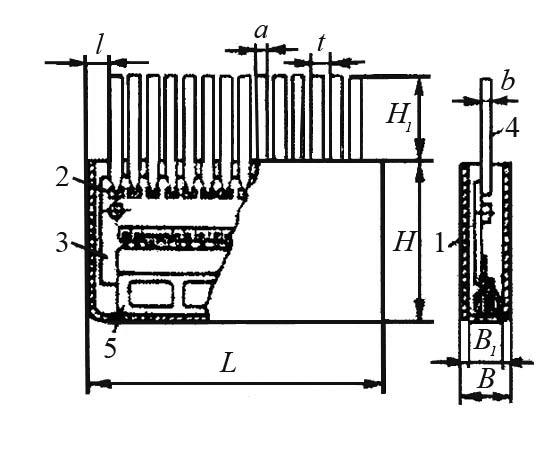 Рисунок 7 – Пенальний квадратний корпус Розглянуті корпуси забезпечують довгострокову експлуатацію мікросхеми в умовах підвищеної відносної вологості (до 98 %) і в температурному діапазоні від -60 °С до +125 °С. Для великих інтегральних мікросхем використовують корпуси, що мають більшу кількість виводів. Наприклад, для великих гібридних схем серії 230 застосовують металокерамічний прямокутний корпус із 50 виводами. Гібридні ВІС серії 231 розміщують у металокерамічному прямокутному корпусі з 48 виводами. Гібридні мікросхеми НВЧ-діапазону розміщують у корпусах спеціальної конструкції, що забезпечують мінімальний взаємний вплив високочастотних ланцюгів. Наприклад, мікросхеми серії 272 (НВЧ-підсилювачі потужності) розміщують у металоскляному корпусі з трьома виводами. Умовне позначення конструкції корпусу складається із шифру типорозміру корпусу, числа, що зазначає кількість виводів, та номера модифікації. Шифр типорозміру корпусу складається із позначення типу корпусу (1, 2, 3 або 4) і двоцифрового числа (від 01 до 99), що визначає номер типорозміру. Наприклад, корпус 201.14-2 – прямокутний корпус типу 2, типорозміру 01, число виводів 14, модифікація друга. | ||||||||||||||||||||||||||||||||||||||||||||||||||||
