Местное обезболивание. все темы местн обезбол. Обезболивание в хирургической стоматологии
 Скачать 1.17 Mb. Скачать 1.17 Mb.
|
|
Секобарбитал и фенобарбитал широко используются при премедикации, поскольку они обладают достаточно выраженным седативным действием без серьезного угнетения сердечно сосудистой системы и дыхания. Однако, после появления бензодиазепинов барбитураты стали менее популярными Сравнительные исследования показали, что бензодиазепины более эффективны для проведения премедикации и легче воспринимаются больными, чем барбитураты. В течение многих лет хлоралгидрат, триклофос и барбитураты были наиболее популярными снотворными. Недавние исследования показали, что бензодиазепины (флуразепам, лоразепам, триазолам, темазепам) гораздо предпочтительнее, нежели барбитураты, в качестве снотворного, назначаемого в ночь перед операцией. Бензодиазепины имеют эффекты, которые делают их наиболее предпочтительными для проведения премедикации (успокоительный эффект, противосудорожная активность, амнезия, седативный эффект и даже миорелаксация). К тому же, имеется специфический антагонист бензодиазепинов - флумазенил, пригодный в том случае, если необходимо быстро снять явления передозировки бензодиазепинов. Для перорального применения также имеется большое количество препаратов данной группы. Диазепам, типичный представитель группы бензодиазепинов, вызывает уменьшение тревожности больного в зависимости от дозы, обладает седативным действием и способностью вызывать амнезию. А как же диазепам по сравнению с лоразепамом? Хотя оба препарата обладают примерно одинаковой способностью вызывать седатацию, обладают одинаковым анксиолитическим эффектом, при использовании диазепама больные чаще отмечают боль в месте инъекции и чаще развиваются тромбофлебиты, тогда как при применении лоразепама больные дольше просыпаются после наркоза. Однако, самыми важными различиями между этими двумя препаратами являются отношение время - эффект для каждого из них. По сравнению с лоразепамом, эффект диазепама на ЦНС развивается практически сразу же после внутривенного введения и продолжается 30-60 минут после него. В эксперименте было выявлено также, что бензодиазепиновые рецепторы имеют более высокое сродство к диазепаму, нежели к лоразепаму. Итак, хотя у диазепама примерно вдвое большее время полувыведения, чем у лоразепама (20-40 часов по сравнению с 10-15 часами), продолжительность его клинического действия меньше, поскольку он очень быстро присоединяется к бензодиазепиновым рецепторам. Главный метаболит диазепама - дисметилдиазепам обладает некоторой фармакологической активностью, тогда как лоразепам сразу превращается в неактивные метаболиты. Наконец, на распределение и метаболизм лоразепама печень оказывает минимальное влияние, тогда как диазепам метаболизируется в основном в печени. Несмотря на это, у пожилых людей дозы бензодиазепинов при проведении премедикации следует снижать, поскольку даже относительно небольшое превышение дозы может вызвать у них депрессию ЦНС. В качестве альтернативы данным широко используемым препаратам может применяться как триазолам (0.125 - 0.5 мг перорально) так и темазепам (15-30 мг перорально), причем во многих ситуациях они обладают несомненными преимуществами. Эти бензодиазепины быстро адсорбируются при пероральном введении и быстро метаболизируются до неактивных метаболитов. Мидазолам представляет собой новый препарат с коротким временем полужизни (2-4 часа) и примерно в два раза сильнее диазепама по силе действия. Как седативный препарат, он примерно в три-пять раз мощнее остальных. Поскольку мидазолам плохо растворяется в воде, то для его введения необходим растворитель (пропиленгликол), который может вызвать раздражение стенки вены и влиять на абсорбцию препарата при его внутримышечном введении. в связи с быстрым развитием седативного и анксиолитического эффекта мидазолам представляется хорошим препаратом для премедикации как при пероральном, так и при внутримышечном и ректальном введении у больных в педиатрической практике. К тому же, краткое время его полувыведения снижает риск накопления препарата при его множественном применении. Мидазолам быстро метаболизируется в печени до неактивных метаболитов. Поэтому при пероральном применении применение препарата несколько ограничено его высоким метаболизмом в печени. Аналогично диазепаму, клиренс мидазолама несколько снижен у пожилых и старых больных, поэтому его дозу у таких пациентов необходимо уменьшать. Клинические исследования показали, что мидазолам по сравнению с другими седативными препаратами представляет определенное преимущество при внутримышечном введении, причем его действие при этом развивается несколько быстрее, чем у других препаратов, а пробуждение больных после наркоза также происходит быстрее. По сравнению с бензодиазепинами, большие транквилизаторы (фентиазины и буторфеноны) и антигистаминные препараты (гидроксазин и дифенилгидрамин) обеспечивают только седативный эффект. Хотя седативное действие данных антипсихотических препаратов очень сильное, это может иметь и отрицательные стороны (слишком сильный седативный эффект и невозможность для больного объяснить свои мысли). Интересно, что многие врачи ошибаются в плане наличия анксиолитического действия у данных препаратов. Дроперидол - это нейролептик класса буторфененов, который очень популярен среди анестезиологов и применяется для премедикации в том числе и из-за своего сильного антиэметического эффекта. Тучные пациенты, больные, которым предстоят офтальмологические и гинекологические вмешательства, пациенты, получающие наркотические аналгетики или этомидат, а также те больные, в анамнезе у которых имеются указания на тошноту и рвоту после предыдущей анестезии, часто отмечают, что введение дроперидола значительно улучшило их состояние. Низкие (0.25-1.25 мг) дозы дроперидола позволяют избавить больных от послеоперационной тошноты и рвоты. Однако, даже очень низкие дозы дроперидола могут вызвать появление экстрапирамидных симптомов в связи с его способностью блокировать гистаминовые рецепторы. Гидроксазин является уникальным транквилизатор нефенотиазинового ряда, который обладает антигистаминным действием, угнетает ЦНС, обладает седативным, анксиолитическим действием, оказывает антиэметический, бронхолитический и антихолинергический эффект. По сравнению с бензодиазепинами он оказывает более выраженное анксиолитическое действие, а также вызывает амнезию. Хотя его аналгетические возможности ограничены, при использовании препарата вместе с наркотическими аналгетиками можно получить довольно эффективное обезболивание. Интересно, что по сравнению с дроперидолом в качестве профилактического антиэметика, гидроксазин более эффективен в дозах, которые оказывают примерно одинаковый седативный эффект и время пробуждения больных после операций одинаково. Дифенилгидрамин (0.5-1.0 мг на кг перорально) - это еще один препарат антигистаминного ряда, который рекомендуется для премедикации в целях профилактики интраоперационных аллергических реакций у больных с хроническими аллергическими реакциями в анамнезе, а также для тех больных, которым проводят манипуляции, заведомо могущие привести к аллергическим реакциям (сцинтиграфические исследования, химиотерапия). У больных с повышенным риском аллергических реакций вместе с дифенилгидрамином назначается локатор Н-2 рецепторов. Опиоиды - наркотические аналгетики В прошлом наркотические аналгетики в качестве премедикации применялись для облегчения индукции и для уменьшения потребности в ингаляционном анестетике. Однако, способность наркотических аналгетиков снижать потребность в ингаляционном анестетике весьма незначительна в клиническом плане. Действительно, традиционное использование наркотических аналгетиков в качестве средства для премедикации подвергалось сомнению многими исследователями. Coheen и Beecher много лет назад отметили, что " пока нет боли, нет необходимости применять наркотики для премедикации". Интересно, что при назначении только морфина у больных наблюдается некоторое чувство дисфории примерно у 80 % больных, которые не испытывают боли, и только у 10% возникает чувство эйфории. Для больных с болевым синдромом или зависимостью от наркотических аналгетиков ситуация может разительно отличаться. Главной проблемой, связанной с использованием наркотических аналгетиков, является огромное количество их побочных эффектов: тошнота, рвота, зуд, депрессия дыхания, возбуждение и другие. В недавно опубликованных исследованиях было сообщено, что тошнота после введения наркотических аналгетиков наблюдается в 40-57 процентах случаев. Когда наркотические аналгетики назначают либо поодиночке, либо в комбинации с седативными препаратами, риск предоперационного угнетения дыхания еще более увеличивается. Премедикация комбинацией морфина и скополамина может значительно снизит сатурацию во время перевозки больного в операционную и во время подготовки к проведению инвазивного мониторинга. Добавление лоразепама для уменьшения беспокойства не увеличивает депрессии дыхания, как это происходит при использовании комбинации морфина и скополамина. Однако, использование лоразепама у кардиохирургических больных (по сравнению с комбинацией морфина со скополамином) значительно более угнетает кровообращение у больного во время индукции. В попытке уменьшить побочные эффекты наркотических аналгетиков и увеличить их эффективность применяются многие препараты. Скополамин, обладающий центральной антихолинергической активностью, увеличивает анксиолитический, и седативный эффект наркотических аналгетиков, однако, он не снижает побочных эффектов морфина. Хотя дроперидол снижает частоту развития тошноты и рвоты, связанной с применением наркотических аналгетиков, при применении данной комбинации частота дисфорических реакций непредсказуема. Некоторые странные сообщения утверждают, что между наркотическими аналгетиками и седативными препаратами существует потенцирование их аналгетических свойств. Эти наблюдения действительно имеет место, поскольку спокойный человек менее чувствителен к боли, однако это не означает, что существует какое-то фармакодинамическое взаимодействие. Прометацин - это популярный препарат фенотиазинового ряда, улучшает анксиолитическое и седативное действие морфина при премедикации. В то же самое время, аналгезия, полученная с помощью комбинации морфина с гидроксазином гораздо эффективнее аналгезии, полученной при использовании только морфина. Чаще всего эти комбинации безопасны, однако известно, что комбинация бензодиазепинов и наркотических аналгетиков может вызвать гипоксемию и апноэ. Антихолинергические средства Использование антихолинергических препаратов в качестве стандартной части премедикации связано с их способностью резко уменьшать продукцию слюны и ваголитическим эффектом. Хотя большинство исследователей не считают это решающим, применение данных препаратов в качестве компонента премедикации давно стало традицией. Во время индукции ингаляционными анестетиками они действительно уменьшают секрецию слюнных желез, вдобавок к этому, атропин предупреждает рефлекторную брадикардию и угнетение кровообращения у маленьких детей. Для премедикации применяется также гликопироллат, препарат с периферическим антихолинергическим эффектом. У взрослых одинаковый эффект оказывает доза гликопироллата в 0.2 мг в/м и доза атропина в 1.5 мг в/м, однако гликопироллат не оказывает существенного влияния на ЧСС больного. К тому же, ни один из этих препаратов не влияет на объем и кислотность желудочного содержимого. Предоперационное введение гликопироллата не снижает риска развития аспирационного пневмонита у больных из группы риска. Пробуждение после анестезии быстрее при и применении гликопирролата, поскольку он не проникает через гематоэнцефалический барьер. Другой антихолинергический препарат центрального действия, скополамин, примерно в восемь-десять раз активнее атропина, но значительно слабее его по периферическому эффекту. Недавние исследования показали, что скополамин в дозе 0.5-1.5 мг за 72 часа трансдермально обладает седативным и антиэметическим действием, а также угнетает секрецию слюнных желез. Однако это действие мало предсказуемо у больных с мышечной слабостью и эпизодами тошноты и рвоты после предыдущих анестезий К сожалению, даже не слишком большие дозы скополамина могут вызвать синдром делирия, слабость, нарушения речи, галлюцинации и кому, что носит общее название "центральный холинергический синдром". Средства, влияющие на моторику желудка Метоклопрамид увеличивает тонус нижнего пищеводного сфинктера, снижает интрагастральное давление и улучшает моторику желудка, пищевода и начальных отделов тонкой кишки. Он оказывает периферический холинергический и центральный антидопаминэргический эффект. Наиболее частыми побочными эффектами метоклопрамида следует считать дистонические реакции (то есть экстрапирамидную симптоматику). Некоторые исследователи утверждают, что у метоклопрамида есть антиэметический эффект, другие же оспаривают его наличие. Однако использование метоклопрамида в комбинации с дроперидолом внутривенно предупреждают развитие послеоперационной тошноты и рвоты даже лучше, чем сам по себе дроперидол в малых дозах. К тому же, метоклопрамид может быть использован в качестве адъюванта к Н-2 гистаминоблокаторам для предупреждения аспирации. Новый препарат этого класса, клебоприд, обладает влиянием на моторику желудка и антиэметическим эффектом, однако, его роль в клинической анестезии пока еще не велика. Н-2 гистаминоблокаторы Антихолинергические средства, препараты, влияющие на моторику желудка и, с недавнего времени, Н-2 гистаминоблокаторы, часто назначаются больным, у которых имеется повышенный риск развития послеоперационного пневмонита. Пациенты с нарушениями сознания, аномалиями глотания или нарушениями моторики желудочно-кишечного тракта, а также больные с "полным желудком" только выигрывают от использования данных препаратов. Беременные, больные с ожирением и диабетом также нуждаются в предоперационном назначении этих препаратов. Использование Н-2 гистаминоблокаторов повышает рН желудочного содержимого в предоперационном периоде в зависимости от дозы, а также снижают базальную желудочную секрецию. В общем, при назначении нескольких доз (вечером перед днем операции и утром в день операции) более эффективно, нежели назначение одной дозы в целях уменьшения кислотности и объема желудочного содержимого. Оба широко используемых Н-2 гистаминоблокатора (циметидин и ранитидин) значительно повышают рН желудочного содержимого в течение часа после их парентерального введения. Хотя данные препараты способны снижать риск возникновения аспирации, однако ни один из них не может устранить этот риск полностью. Таким образом, использование этих препаратов ни в коей мере не снижает важности тщательного интраоперационного мониторинга и защиты дыхательных путей больного во время интубации. К тому же, циметидин обладает потенциальной способностью угнетать активность фермента оксидазы в печени, таким образом, удлиняя время элиминации некоторых препаратов, используемых во время анестезии (диазепама, хлордиазепоксида, теофиллина, пропранолола и лидокаина). Ранитидин, более современный Н-2 гистаминоблокатор, более мощный, специфичный, и дольше действует, нежели циметидин. Ранитидин в дозе 100-200 перорально также эффективен, как и циметидин в дозе 200-400 мг перорально, причем при его использовании значительно снижается риск послеоперационного пневмонита и практически не наблюдается побочных эффектов и отрицательных взаимодействий между ним и другими лекарственными препаратами. Данные исследований говорят о том, что от 40 до 80 процентов больных при плановом хирургическом вмешательстве имеют рН < 2.5 и или объем желудочного содержимого более 25 мл во время интубации трахеи. Эти данные могут рассматриваться как факторы риска развития синдрома Мендельсона. Итак, необходимо проводить профилактику аспирации, так как после нее развивается тяжелейшее осложнение - аспирационная пневмония. Что же использовать в качестве профилактического средства? Большинство исследователей утверждают, что помочь в данной ситуации могут антациды. К сожалению, коллоидные суспензии антацидов при их аспирации вызывают серьезные повреждения легких и только широко распространенные твердые лекарственные формы антацидов (цитрат натрия) могут помочь, однако они менее эффективны. Предоперационное назначение цитрата натрия поднимает рН желудочного содержимого выше 2.5 у 64-84 процентов больных, однако, этот препарат увеличивает объем желудочного содержимого. По сравнению с циметидином цитрат гораздо менее эффективен в плане предупреждения аспирационного пневмонита. Предоперационное назначение 300 мг циметидина или 150 мг ранитидина перорально в комбинации с метоклопрамидом значительно снижают риск развития послеоперационного аспирационного пневмонита. O Sullivan et al продемонстрировали, что комбинированное применения метоклопрамида и ранитидина является наиболее эффективными в плане предупреждения тяжелого аспирационного пневмонита. Вазоконстрикторы Местные анестетики, за исключением мепивакаина, не вызывают сужения сосудов или даже расширяют их. В результате снижается глубина и продолжительность обезболивания так как: – увеличивается поглощение анестетика сердечно-сосудистой системой и, следовательно, снижается его концентрация в месте инъекции; – повышается уровень анестетика в плазме крови, следовательно, возрастает риск побочных эффектов; – препарат интенсивно уходит в сосудистое русло и в результате быстро снижается его концентрация в месте инъекции, что ведет к сокращению времени действия и эффективности анестетика; – усиливается кровоточивость в месте инъекции. С целью предотвращения подобных явлений в большинство местных анестетиков добавляют вазоконстрикторы. Исключение составляют препараты на основе мепивакаина, поскольку это вещество само проявляет легкое сосудосуживающее действие. Мепивакаин, поэтому, без применения вазоконстрикторов обезболивает пульпу на 20–40 мин, а мягкие ткани— на 2–3 ч. В качестве сосудосуживающих препаратов в большинство местных анестетиков добавляют адреналин, реже норадреналин. Адреналин (Аdrenalinum). Синонимы: Adnephrine, Adrenamine, Adrenine, Epinephrinum, Epinephrine, Epirenan, Epirinamine, Eppy, Glaucon, Glauconin, Glaukosan, Hypernephrin, Levorenine, Nephridine, Paranephrine, Renostypticin, Styptirenal, Suprarenalin, Suprarenin, Tonogen и др. Белый или белый с сероватым оттенком кристаллический порошок. Легко изменяется под действием света и кислорода воздуха. Легко растворим в воде, мало в спирте. Адреналин содержится в разных органах и тканях, в значительных количествах образуется в хромаффинной ткани, особенно в мозговом веществе надпочечников. Выпускается в виде адреналина гидрохлорида и адреналина гидротартрата. Действие адреналина при введении в организм связано с влиянием на aльфа- и бета-адренорецепторы и во многом совпадает с эффектами возбуждения симпатических нервных волокон. 0н вызывает сужение сосудов органов брюшной полости, кожи и слизистых оболочек; в меньшей степени суживает сосуды скелетной мускулатуры. Артериальное давление повышается. Однако прессорный эффект адреналина в связи с возбуждением бета-адренорецепторов менее постоянен, чем эффект норадреналина. Изменения сердечной деятельности носят сложный характер: стимулируя адренорецепторы сердца, адреналин способствует значительному усилению и учащению сердечных сокращений; одновременно, однако, в связи с рефлекторными изменениями из-за повышения артериального давления происходит возбуждение центра блуждающих нервов, оказывающих на сердце тормозящее влияние; в результате этого сердечная деятельность может замедляться. Могут возникать аритмии сердца, особенно в условиях гипоксии. Адреналин вызывает расслабление мускулатуры бронхов и кишечника, расширение зрачков (вследствие сокращения радиальных мышц радужной оболочки, имеющих адренергическую иннервацию). Под влиянием адреналина происходит повышение содержания глюкозы в крови и усиление тканевого обмена. Адреналин улучшает функциональную способность скелетных мышц (особенно при утомлении); его действие сходно в этом отношении с эффектом возбуждения симпатических нервных волокон (явление, открытое Л. А. Орбели и А. Г. Гинецинским). На ЦНС адреналин в терапевтических дозах выраженного влияния обычно не оказывает. Могут, однако, наблюдаться беспокойство, головные боли, тремор. У больных паркинсонизмом под влиянием адреналина усиливаются ригидность мышц и тремор. Применяют адреналин при анафилактическом шоке, аллергическом отеке гортани, при бронхиальной астме (купирование острых приступов), аллергических реакциях, развивающихся при применении лекарств (пенициллин, сыворотки и др.) и при действии других аллергенов, при гипогликемической коме (при передозировке инсулина). Адреналин является эффективным средством для снятия бронхиолоспазма при бронхиальной астме. Однако он действует не только на адренорецепторы бронхов, но и на адренорецепторы миокарда, вызывая тахикардию и усиление сердечного выброса; возможно ухудшение снабжения миокарда кислородом. Кроме того, в связи с возбуждением aльфа-адренорецепторов наступает повышение артериального давления. На бронхи более избирательное действие, чем адреналин, оказывают изадрин, орципреналин и др. Адреналин имеет применение и как местное сосудосуживающее средство. Раствор прибавляют к местноанестезирующим веществам для удлинения их действия и уменьшения кровотечений. Норадреналина Гидротартрат (Nоrаdrenalini hydrotartras). Синонимы: Аrterenol, Noradrenalinum hydrotartaricum, Levarterenol, Levarterenoli bitаrtras, Levarterenol bitartratе, Levophed, Nоrartrinal, Norepinephrinе, Norexadrinе и др. Белый или почти белый кристаллический порошок без запаха. Легко растворим в воде, мало — в спирте. Легко изменяется под действием света и кислорода воздуха. Водные растворы (рН 3,0–4,5) стерилизуют при +100 °С в течение 15 мин. По химическому строению норадреналин отличается от адреналина отсутствием метильной группы у атома азота, аминогруппы боковой цепи. Действие норадреналина связано с преимущественным влиянием на aльфа-адренорецепторы. Отличается от адреналина более сильным сосудосуживающим и прессорным действием, меньшим стимулирующим влиянием на сокращения сердца, слабым бронхолитическим эффектом, слабым влиянием на обмен веществ (отсутствие выраженного гипергликемического эффекта). Кардиотропное действие норадреналина связано со стимулирующим его влиянием на бета-адренорецепторы сердца, однако бета-адреностимулирующее действие маскируется рефлекторной брадикардией и повышением тонуса блуждающего нерва, вызванными повышением артериального давления. Введение норадреналина вызывает увеличение сердечного выброса, вследствие повышения артериального давления возрастает перфузионное давление в коронарных артериях. Вместе с тем значительно возрастает периферическое сосудистое сопротивление и центральное венозное давление. Применяют для повышения артериального давления при остром его понижении вследствие хирургических вмешательств, травм, отравлений, сопровождающихся угнетением сосудодвигательных центров и т. п., а также для стабилизации артериального давления при оперативных вмешательствах на симпатической нервной системе после удаления феохромоцитомы и др. Норадреналин является весьма эффективным средством для повышения артериального давления и усиления сердечных сокращений. Однако повышение артериального давления связано главным образом с увеличением периферического сосудистого сопротивления и частоты сердечных сокращений. Под влиянием норадреналина уменьшается также кровоток в почечных и мезентериальных сосудах. Возможно возникновение желудочковых аритмий. Поэтому при кардиогенном шоке, особенно в тяжелых случаях, применение норадреналина считают нецелесообразным (Е.И. Чазов). Обычно тяжелые случаи кардиогенного (и геморрагического) шока сопровождаются вазоконстрикторной реакцией периферических сосудов. Введение в этих случаях норадреналина и других веществ, повышающих сопротивление периферических сосудов, может оказать отрицательный эффект. Следует также учитывать, что под влиянием норадреналина (и других симпатомиметических аминов) возрастает потребность, миокарда в кислороде. Следует остерегаться введения раствора норадреналина под кожу и в мышцы из-за опасности развития некрозов. Введение норадреналина противопоказано при фторотановом и циклопропановом наркозе. Не следует применять норадреналин также при полной атриовентрикулярной блокаде, при сердечной слабости, резко выраженном атеросклерозе. Форма выпуска: 0,2% раствор в ампулах по 1 мл. Хранение: список Б. В защищенном от света месте. Как видно из характеристики адреналина и норадреналина в организме человека оба эти вещества оказывают влияние на диаметр сосудов и регуляцию кровообращения. Адреналин и норадреналин действуют через альфа- и бета-адренорецепторы. Большинство альфа-адренорецепторов расположено в сосудах и отвечают за их сокращение. Бета-адренорецепторы в основном встречаются в сердце и легких и ответственны за работу этих органов. В стоматологической практике применяется минимальное количество адреналина и норадреналина, которое не оказывает существенного влияния на нормальное функционирование организма. Адреналин действует почти в 4 раза сильнее, чем норадреналин. Сродство адреналина к альфа- и бета-адренорецепторам примерно одинаковое в отличие от норадреналина, у которого сродство к альфа-адренорецепторам приблизительно в 9 раз выше, чем к бета-адренорецепторам. Даже незначительная концентрация норадреналина резко нарушает циркуляцию крови и ведет к некрозу ткани в месте инъекции. Повреждение ткани при этом носит необратимый характер. Для предотвращения подобного побочного действия целесообразно в качестве вазоконстриктора для местных анестетиков в стоматологической практике использовать исключительно адреналин. Как уже было отмечено выше, адреналин и норадреналин подвергаются быстрому распаду при контакте с кислородом воздуха. Кислород может проникнуть в карпулу в процессе ее заполнения местн Взаимодействие местноанестезирующих препаратов с другими лекарствам 1.6.1. Взаимодействие местных анестетиков с другими лекарствами. При выборе местноанестезирующих препаратов следует учитывать возможность их взаимодействия с препаратами, которые принимает пациент, имеющий соматические или психоневрологические заболевания. Вазоконстрикторы (эпинефрин, норэпинефрин), суживая сосуды, усиливают и пролонгируют действие местных анестетиков и уменьшают их токсичность. Добавление натрия бикарбоната к растворам местных анестетиков повышает рН раствора, увеличивает концентрацию анестетика-основания и ускоряет развитие анестезии. Препараты калия повышают эффект местных анестетиков. Антагонисты кальция усиливают угнетающее действие местных анестетиков на проводимость и сократимость миокарда. ß-адреноблокаторы (пропранолол, пиндалол), симпатолитики (резерпин) и противоаритмические препараты (амиодарон, верапамил, мексилетин, новокаинамид, хинидин) усиливают кардиодепрессивное действие местных анестетиков. ß-адреноблокаторы (пиндалол, пропранолол, соталол), уменьшая печеночный кровоток, замедляют биотрансформацию и снижают клиренс местных анестетиков группы амидов, повышая риск системных токсических эффектов. Местные анестетики ослабляют кардиотонический эффект сердечных гликозидов. При сочетании сердечных гликозидов с местноанестезирующими растворами, содержащими эпинефрин (адреналин), повышается риск возникновения сердечных аритмий. Антихолинэстеразные препараты (прозерин, галантамин) замедляют метаболизм и повышают токсичность местных анестетиков группы сложных эфиров. Ингибиторы печеночных ферментов (индометацин, циметидин, левомицетин, эритромицин, флувоксамин и другие препараты, угнетающие микросомальное окисление в печени), замедляя процесс биотрансформации в печени местных анестетиков группы амидов, увеличивают их концентрацию в крови, повышая риск развития системных токсических эффектов. Препараты, ускоряющие процессы биотрансформации в печени (фенобарбитал, гидантоины и др.), могут снижать концентрацию в крови местных анестетиков группы амидов. Местные анестетики потенцируют действие недеполяризующих миорелаксантов (тубокурарин, панкурония бромид) и угнетающее влияние аминогликозидов и полимиксина на нервно-мышечную передачу. Сукцинилхолин и прокаин (новокаин), гидролизующиеся псевдохолинэстеразой, при сочетании дают взаимное усиление эффекта. Местные анестетики усиливают депрессорный эффект на дыхание общих анестетиков и наркотических анальгетиков. При сочетании средств, угнетающих ЦНС, с местными анестетиками действие препаратов взаимно усиливается. При сочетании местных анестетиков с галотаном (фторотаном), энфлураном, изофлураном повышается чувствительность миокарда к катехоламинам и 30 увеличивается риск развития аритмий. При сочетании местных анестетиков с ингибиторами ЦНС увеличивается риск появления сонливости, с алкоголем – усиление седативного действия. Ропивакаин усиливает токсическое действие других местных анестетиков и препаратов, которые по структуре схожи с местными анестетиками амидного типа. Опиоидные анальгетики и α2 – адреномиметики усиливают обезболивающий эффект местных анестетиков. При сочетании местных анестетиков с нейролептиками (дроперидол, галоперидол, производные фенотиазина), симпатолитиками, ß-адреноблокаторами, ингибиторами АПФ и нитратами наблюдается усиление гипотензивного эффекта. Циметидин уменьшает клиренс внутривенно введенного лидокаина. Применение средств, угнетающих ЦНС (седативные, снотворные), усиливает угнетающее действие лидокаина на дыхательный центр. Атропина сульфат, ингибиторы МАО (моноаминооксидаза), транквилизаторы и снотворные усиливают анестезирующее действие прокаина (новокаина). Прокаин ослабляет диуретическое действие мочегонных средств, усиливает эффект препаратов для общей анестезии. Антибактериальное действие сульфаниламидов могут снижать местные анестетики группы сложных эфиров (тетракаин, прокаин), в процессе метаболизма которых образуется пара-аминобензойная кислота, имеющая сходство по структуре с сульфаниламидами. Взаимодействие эпинефрина (адреналина) с другими лекарствами. При сочетании местноанестезирующих препаратов, содержащих эпинефрин, с трициклическими антидепрессантами (имизин, амитриптилин, азафен) могут наблюдаться побочные явления, в том числе повышение артериального давления и аритмии. Действие оральных гипогликемических препаратов (хлорпропамид, глибенкламид) эпинефрин (адреналин) снижает. Эпинефрин (адреналин) увеличивает эффект эуфиллина и препаратов, повышающих функцию щитовидной железы. Прометазин (пипольфен) может извращать сосудосуживающий эффект эпинефрина (адреналина). Спиронолактон (верошпирон), нитроглицерин могут снижать сосудосуживающий эффект эпинефрина (адреналина). Алкоголь увеличивает почечную экскрецию эпинефрина (адреналина). Антидепрессанты (трициклические и ингибиторы МАО) повышают адренергический эффект эпинефрина (адреналина), что увеличивает риск развития сердечных аритмий и повышения кровяного давления. ß-адреноблокаторы уменьшают действие эпинефрина (адреналина) на сердце, бронхи и сосуды, содержащие ß2 - адренорецепторы, увеличивают риск брадикардии. Сегодня местные анестетики – это одни из самых применяемых в стоматологической практике лекарств, что стимулирует появление на фармацевтическом рынке новых препаратов данной группы. За последние годы в России зарегистрировано большое количество отечественных и зарубежных местноанестезирующих препаратов, но не каждый из них является инновационным, т.е. впервые синтезированным, оригинальным, показавшим при проведении полного цикла доклинических и клинических исследований значительное отличие от имеющихся препаратов данной группы, т.е. отражает прорыв в фармакологической науке. Инновационные лекарственные средства должны повышать эффективность и гарантировать безопасность лечения, улучшать качество жизни пациента, снижать затраты на лечение. При создании инновационного препарата активные его ингредиенты фирма-изобретатель патентует на определенный срок, в течение которого она выступает в качестве единственного поставщика оригинального препарата на фармацевтическом рынке. По истечении срока действия патента, любая фармацевтическая фирма имеет право на воспроизводство данного препарата, т.е. на создание дженериков (генериков), которые поступают на фармацевтический рынок под торговым названием, присвоенным производящей его фирмой. Высокой потребностью в препаратах для местного обезболивания объясняется наличие в торговой сети большого количества дженериков, т.е. лекарств созданных на основе одного и того же местного анестетика и, соответственно, однотипно действующих, но имеющих разные торговые названия (табл.4). 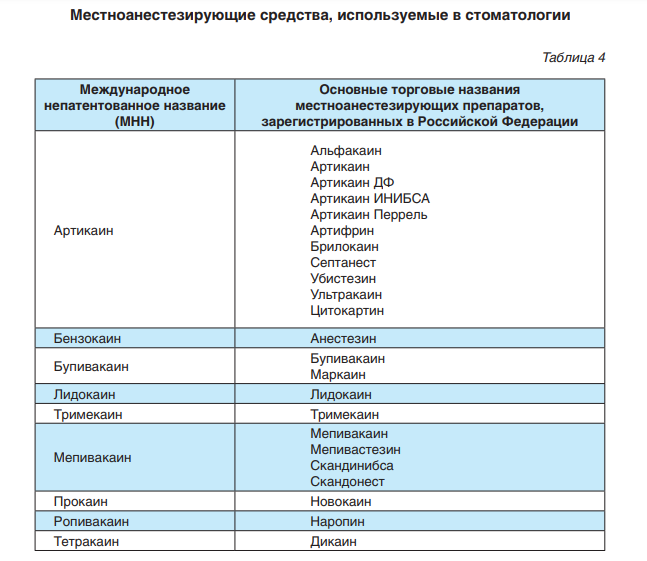 Это создает определенные сложности для врача, которому становится все сложнее ориентироваться в этом множестве лекарств. Чтобы врачам было легче разобраться во всем многообразии однотипно действующих лекарств, на любом препарате, в том числе и на местноанестезирующем, под торговым названием стоит его международное непатентованное название (МНН), т.е. унифицированное международное название основных действующих веществ, входящих в состав данного лекарства. Например, под торговыми названиями местноанестезирующих препаратов альфакаин, артикаин, артикаин ДФ, артикаин ИНИБСА, артикаин Перрель, артифрин, брилокаин, септанест, убистезин и ультракаин обязательно будет указано международное непатентованное название основных действующих веществ: артикаин (местный анестетик) и при наличии в растворе вазоконстриктора – эпинефрин (адреналин). Препараты артикаина, создаваемые на разных фирмах, могут иметь определенные отличия, связанные с технологией приготовления, количественным и качественным составом вспомогательных веществ, различием в рН раствора, но основная направленность действия этих препаратов будет обусловлена одним и тем же местным анестетиком – артикаином и наличием или отсутствием в растворе вазоконстриктора. Увеличение ассортимента местноанестезирующих препаратов расширяет возможности местного обезболивания, но нередко врачи испытывают трудности при выборе критериев для оценки их эффективности и безопасности. Форма выпуска местноанестезирующих препаратов Местноанестезирующие растворы, применяемые в стоматологии для инъекционных методов обезболивания, выпускаются в ампулах и карпулах (картриджах). Использование ампульных растворов местных анестетиков и многоразовых инструментов позволяло проводить местную анестезию только в специальных условиях хирургических отделений, а современная карпульная технология создает условия выполнения ее врачами-стоматологами общей практики или других стоматологических специальностей (терапевтами, ортопедами, ортодонтами) непосредственно на своих рабочих местах, что сокращает затраты времени и улучшает качество лечения. Весь процесс приготовления карпул, содержащих местноанестезирующие растворы, в том числе и добавление вазоконстриктора, выполняется в заводских условиях с соблюдением всех требований стерильности и высокой надежности. Процесс автоматизирован, контролируется на всех этапах – от очистки воды, до введения вазоконстриктора с высокой точностью разведения и соблюдением всех технологий их изготовления. Применение карпульной технологии при проведении местной анестезии позволило повысить безопасность и эффективность работы врача-стоматолога. Карпула состоит из стеклянного или пластмассового цилиндра с резиновым поршнем с одного конца и резиновой пробкой с металлическим колпачком с другого (рис. 2,3).   Внутренний объем карпулы обычно составляет 2 мл, но за счет наличия пробки он сокращается до 1,7-1,8 мл. Пластмассовые карпулы более устойчивы и реже разбиваются при транспортировке и проведении анестезии под давлением (например, интралигаментарной), но они менее прозрачны, чем стеклянные карпулы. На каждой карпуле имеется информация о содержащемся в ней растворе (с укзанием активных и вспомогательных веществ), его стерилизации, номере партии и сроке хранения (рис. 4).  Карпулы обычно укладываются в металлический контейнер или пластиковую упаковку (блистер). На упаковке с анестетиком представлено торговое и международное непатентованное название препарата. Указывается название и содержание всех входящих в состав раствора компонентов (местного анестетика, вазоконстриктора, стабилизаторов, консервантов и др.), название фирмы и адрес производителя, номер партии анестезирующего раствора и срок хранения . Карпулированные анестетики должны храниться при комнатной температуре (не выше 25°С), в темном, защищенном от солнечных лучей месте, т. к. на свету может разрушаться вазоконстриктор. Анестетики следует хранить в местах, недоступных для детей. Перед употреблением резиновую пробку и металлическую крышку дезинфицируют 700 спиртом. Другие способы обеззараживания не допускаются. Условия для работы с местноанестезирующими препаратами.Состав местноанестезирующего раствора. При работе с местноанестезирующими препаратами врач должен следить за выполнением некоторых обязательных условий: - иметь разрешение на применение данного препарата от Фармакологического комитета Минздрава РФ; - наличие сертификата соответствия партии препарата, который подтверждает его качественные характеристики (номер партии указан на упаковке и карпуле); -учитывать срок хранения препарата (просроченные карпулы не используются); - проверить целостность карпулы и ее герметичность, что обеспечивает полную стерильность препарата. Не допускается к использованию карпулы со следующими изменениями: - пожелтение, помутнение раствора; - наличие осадка; ржавчина на карпуле; - вмятины, трещины и другие повреждения; - большой пузырек воздуха и сдвинутое положение шприца (возможно после замораживания и оттаивания содержимого карпулы). В состав карпулы местноанестезирующего раствора могут входить: =Активные вещества - Местный анестетик. - Вазоконстриктор. =Вспомогательные вещества - Натрия хлорид, натрия бисульфит, иногда парабены, ЭДТА,вода для инъекций. Хлорид натрия вводится в состав местноанестезирующих растворов, изготавливаемых с использованием апирогенной воды для сохранения осмотического равновесия. Бисульфит натрия вводится в состав местноанестезирующего раствора в качестве антиоксиданта для предотвращения окисления вазоконстриктора эпинефрина (адреналина). ЭДТА в состав местноанестезирующего раствора вводится для предотвращения реакции сосудосуживающих средств (эпинефрина/адреналина) с ионами металлов, выделяемых стеклом карпулы. Метилпарабен иногда включается в состав местноанестезирующего раствора в качестве консерванта для сохранения стерильности раствора. Технологии изготовления карпульных анестетиков постоянно развиваются. В музее кафедры стоматологии общей практики и анестезиологии представлена экспозиция развития обезболивающих средств от конца XIX века к современным препаратам . Целью современного развития карпульных технологий является максимальное снижение возможных побочных эффектов от присутствия в составе местноанестезирующих препаратов вспомогательных веществ. Так, нанесение силиконового покрытия на внутреннюю стенку стеклянных карпул, предотвращает контакт стекла с сосудосуживающими средствами, присутствующими в анестетике, что позволяет не включать в состав местноанестезирующего раствора ЭДТА. Это, в свою очередь, уменьшает вероятность развития побочных эффектов, вызываемых ЭДТА - плохое самочувствие после инъекции анестетика, головная боль, тошнота, рвота. Современные технологии изготовления карпульных анестетиков обеспечивают стерильность раствора, что позволяет избежать включения в их состав консерванта метилпарабена, ответственного за развитие аллергических реакций у пациентов с повышенной чувствительностью к парабенам. Таким образом, применение карпульных технологий позволяет значительно повысить эффективность и безопасность обезболивания, сократить время и улучшить качество стоматологического лечения. Литература :С.А. Рабинович, Е.Н. Анисимова, Л.А. Аксамит, Е.В. Зорян, Т.Д. Бабич, А.А. Цветкова, Н.Т. Бутаева. Средства и способы местного обезболивания в стоматологии. - М.2013.- 136 с.: ил. Обоснование выбора препарата в зависимости от возраста, соматического и эмоционального состояния пациента, объема оперативного вмешательства. Особенности обезболивания у пациентов с факторами риска. |
