Клиническая химия в диагностике и лечении. Обмен натрия и воды обмен калия лечение диуретиками гомеостаз ионов водорода
 Скачать 3.99 Mb. Скачать 3.99 Mb.
|
ГИПОТАЛАМУС И ГИПОФИЗОБЩИЕ ПРИНЦИПЫ ДИАГНОСТИКИ ЭНДОКРИННЫХ ЗАБОЛЕВАНИЙ В этой и последующих трех главах кратко описаны принципы лабораторной диагностики эндокринных расстройств. В этом разделе упомянуты некоторые общие положения. Железы внутренней секреции могут продуцировать избыточные или недостаточные количества гормонов. Это может быть вызвано либо первичными аномалиями самих желез внутренней секреции, либо эти нарушения могут быть вторичными по отношению к расстройствам механизмов регуляции, связанных обычно с функционированием гипоталамуса пли гипофиза. В последнем случае в самих железах внутренней секреции может первоначально не быть отклонений от нормы. На секрецию большинства гормонов прямо или косвенно воздействуют конечные продукты секреторной деятельности эндокринных желез или образующиеся под влиянием соответствующих гормонов продукты метаболизма. Это обычно отрицательная обратная связь. В результате этого явления нарастание конечных продуктов (гормонов или негормонов) тормозит секреторную функцию эндокринных желез. На основе этих представлений проводят многие исследования функций желез внутренней секреции. Если результаты предварительных исследований близки к границам нормы, необходимо уточнить наличие или отсутствие дисфункций эндокринных желез. При обнаружении бесспорных аномалий следует помнить, что они могут быть первичными или вторичными, обусловленными дисфункциями одного из регуляторных механизмов. Если при сопоставлении получаемых данных с результатами клинических наблюдений эти вопросы выяснить не удается, следует провести так называемые динамические тесты. В таких тестах ответная реакция желез или механизмов обратной связи стимулируется или подавляется применением экзогенных гормонов. Для дифференциальной диагностики избыточной секреции гормонов обычно применяют тесты на угнетение. Учитывают эффекты вводимых в организм соединений (или их аналогов), которые в норме угнетают секрецию гормонов по принципу обратной связи. Отсутствие такого угнетения указывает на возможность осуществления процесса секреции, нерегулируемого при участии нормального механизма обратной связи (автономная секреция). Для дифференциальной диагностики недостаточности секреции гормонов обычно применяют тесты на стимуляцию. При проведении этих тестов учитывают эффекты вводимых в организм тропных гормонов, которые в норме стимулируют секреторную функцию эндокринных желез. Отсутствие стимуляции подтверждает предположение о недостаточности секреции гормонов соответствующими эндокринными железами, тогда как обнаружение нормальной стимуляции позволяет исключить указанное предположение. В данной главе мы обсуждаем дисфункции гипофиза и гипоталамуса. В гл. VI, VII и VIII будут рассмотрены заболевания соответствующих эндокринных железмишеней, а именно коры надпочечников, половых желез и щитовидной железы. Гипоталамус и гипофиз Существует тесная взаимосвязь между нервной и эндокринной системами; она становится особенно очевидной на примере функций гипоталамуса и двух долей гипофиза. В норме гормоны, синтезируемые в гипоталамусе, определяют функционирование обеих долей гипофиза, хотя по генезу и функциональным особенностям передняя и задняя доли гипофиза совершенно различны. Гипоталамус имеет обширные анатомические связи с другими структурами головного мозга. Поэтому нет ничего удивительного в том, что при состоянии стресса и расстройствах психики изменяется секреция гормонов гипофиза и, следовательно, гормонов многих других эндокринных желез. Гормоны гипоталамуса В гипоталамусе происходит биосинтез двух основных групп гормонов, которые соответственно связаны с функционированием задней и передней долей гипофиза. Гипоталамус и задняя доля гипофиза В гипоталамусе синтезируется 3 пептида, которые мигрируют вдоль нервных проводящих путей ножки гипофиза, а затем поступают в тканевые резервы задней доли гипофиза. Гипоталамус осуществляет регуляцию высвобождения этих пептидов в кровоток. Пептидными гормонами задней доли гипофиза являются: 1) антидиуретический гормон (АДГ, аргининвазопрессин), который мы рассматривали в гл. II; 2) окситоцин—гормон (сходный по структуре с АДГ), который регулирует выделение молока из лактирующей молочной железы, а также может участвовать в инициации сокращений матки при родовом акте, хотя в норме роды возможны и в отсутствие окситоцина. В акушерской практике этот гормон можно использовать для стимуляции родовой деятельности; 3) нейрофизин, функция которого не выяснена, но который может способствовать транспорту и переходу в резервные формы в задней доле гипофиза двух других указанных выше пептидных гормонов. Гипоталамус и передняя доля гипофиза Гипоталамус не имеет прямой иннервационной связи с передней долей гипофиза. Однако в гипоталамусе осуществляется биосинтез низкомолекулярных соединений (регулирующих гормонов или факторов), которые транспортируются к клеткам передней доли гипофиза через гипоталамическую портальную систему. Сеть кровеносных капилляров, относящихся к системе гипоталамического воротного кровообращения, в срединном возвышении головного мозга образует вены, которые проходят по ножке гипофиза, а затем разделяются на вторичную капиллярную сеть в передней доле гипофиза. Высокая местная концентрация гормонов гипоталамуса стимулирует или подавляет секрецию в общий кровоток гормонов из клеток передней доли гипофиза. Среди клеток передней доли гипофиза различают ацидофилы, базофилы и хромофобы. Эта простая классификация основана на различии свойств данных клеток при их взаимодействии с красителями. При помощи более совершенных методов можно идентифицировать клетки, секретирующие определенные гормоны. К числу яцидофилов относятся клетки двух типов. Одни из них секретируют гормон роста (ГР), другие—пролактин. Эти простые полипептиды, в молекулах которых последовательность аминокислотных остатков частично одинакова, могут непосредственно воздействовать на периферические ткани. Нервные импульсы оказывают ясно выраженное влияние на стимуляцию или ингибирование функций гипоталамуса. Базофилы секретируют гормоны, воздействующие на другие эпдокриппыс железы. Процесс стимуляции их функционирования обеспечивает главным образом гипоталамус. Различают три типа клеток. Одни из них секретируют тиротропин (ТТР, тиреотропный гормон), который действует на щитовидную железу. Другие секретируют гонадотропины, фолликулостимулирующий гормон (ФСГ, фоллитропин) и лютепнизирующий гормон (ЛГ, лютропин), которые действуют на половые железы. Эти гормоны по структуре сходны с гликопротеинами. В секреции данных гормонов нервная регуляция играет менее важную роль, чем регуляторные механизмы, функционирующие по принципу обратной связи. В клетках третьего типа происходит биосинтеза высокомолекулярного полипептида (проопиокортина), являющегося прогормоном и для адренокортикотропного гормона (АКТГ; кортикотропин), и для рлипотропина (ЛПТ), которые секретируются параллельно. В коре надпочечников АКТГ стимулирует секрецию, но не альдостерона, а других стероидных гормонов. В молекуле АКТГ имеется фрагмент, обладающий меланопитостимулирующей активностью. Поэтому при высоком содержании АКТГ в циркулирующей крови часто отмечают усиление пигментации. ЛПТ, возможно является предшественником эндорфинов, напоминающих по свойствам опиаты. Более подробно рассматривать эндорфины мы не будем. Хромофобы, которых ранее считали лишенными гормональной активности, содержат в действительности секреторные гранулы. Аденомы, состоящие из хромофобов, часто секретируют гормоны, особенно пролактин. Регуляция секреции гормонов передней доли гипофиза Двумя наиболее важными физиологическими факторами, воздействующими на секрецию гормонов передней доли гипофиза, являются механизмы нейрональной регуляции, а также регуляции, осуществляемой по принципу обратной связи (рис. 15). Внегипоталамические нервные импульсы модифицируют (и иногда превосходят) эффекты других механизмов регуляции. Физический или эмоциональный стресс, психические заболевания могут приводить к таким же результатам и даже дать толчок развитию эндокринного заболевания. Для тестирования функций передней доли гипофиза используют стресс гипогликемией, вызываемой введением инсулина. Стресс может также стимулировать секрецию гормона задней доли гипофиза АДГ. Функционирование механизма обратной связи опосредуется содержанием гормонов железымишени в циркулирующей крови. Секрецию тройного гормона обычно угнетает повышение содержания гормона железымишени в кровотоке. Эта отрицательная обратная связь может либо непосредственно угнетать секрецию гормона гипоталамуса, либо изменять его воздействие на клетки гипофиза (большая система обратной связи). Нарастание содержания гормона гипофиза может также угнетать секрецию гормона гипоталамуса (малая система обратной связи). Врожденные ритмы. Высвобождение гормонов гипоталамуса (и, следовательно, гипофиза) происходит периодически. Существуют определенные закономерные ритмы секреции некоторых гормонов. Данные о нарушении этих ритмов могут иметь диагностическое значение. В соответствующих разделах мы вернемся к рассмотрению этого вопроса. 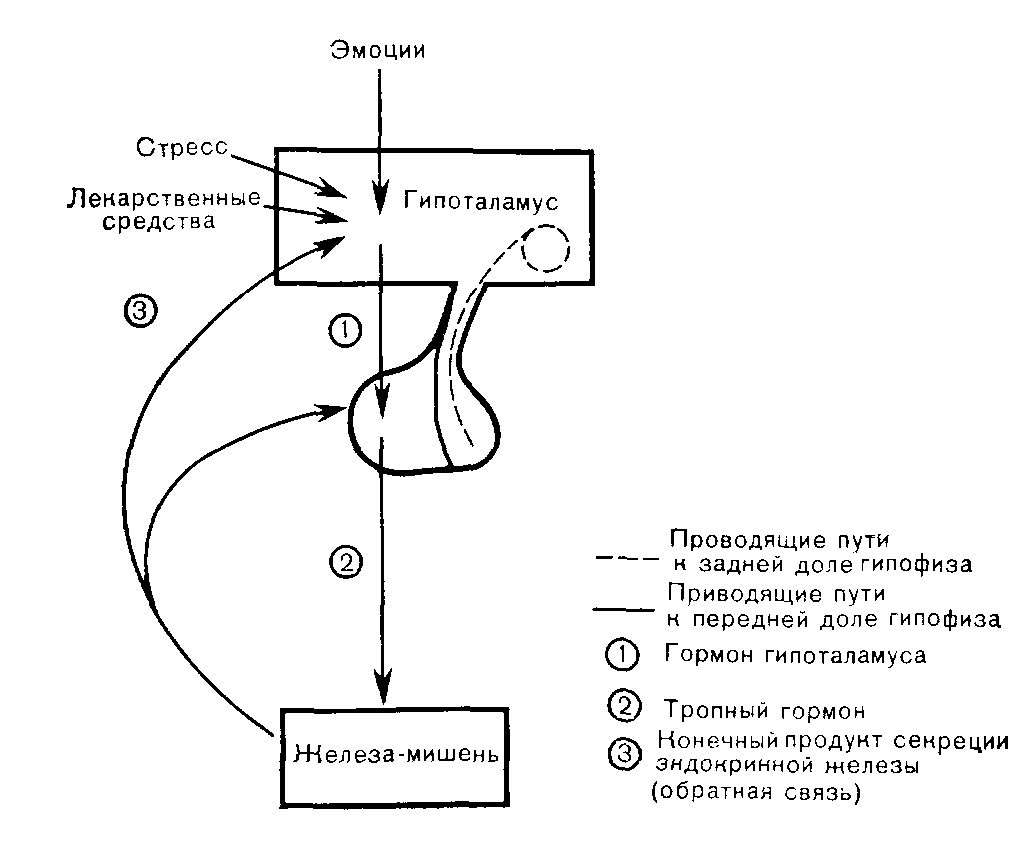 Рис. 15. Регуляция секреции гормонов гипофиза. Таблица 12. Последствия первичного нарушения секреции гормона передней доли гипофиза
Воздействия лекарственных средств. Гипоталамус опосредует передачу нервных импульсов к химическим механизмам секреции гормонов. Не удивительно поэтому, что лекарственные средства, стимулирующие или блокирующие действие химических медиаторов нервных импульсов (таких как катехоламины, ацетилхолин и серотопин), воздействуют на секрецию гормонов гипоталамуса и, следовательно, гипофиза. Например, такие лекарственные средства, как аминазин, препятствуют эффекту дофамина, что приводит к уменьшению секреции ГР (ослабленный эффект рилизингфактора) и повышению секреции пролатина (ослабленный эффект ингибирующего фактора). Противоположное действие в организме здорового человека оказывают бромокриптин (2бромаэргокриптин), стимулирующий присоединение дофамина к рецепторам гипофиза, и LДОФА (Ь3,4диоксифенилаланин), который превращается в дофамин. У больных акромегалией бромокриптин вызывает парадоксальное угнетение избыточной секреции ГР. В последующих разделах мы обсуждаем эти эффекты, используемые в диагностике и терапии гипоталамогипофизарных расстройств. Определение гормонов гипофиза. Все гормоны гипофиза представляют собой пептиды. Для определения их содержания обычно применяют радиоиммунологические методы. Клиницисту следует помнить, что специфичность и точность методов определения пептидных гормонов несопоставимы с таковыми, например, определения натрия. Получаемые результаты следует поэтому интерпретировать с должной осторожностью. Нарушения секреции гормонов гипофиза. В табл. 12 представлены основные клинические симптомы, указывающие на избыточ ность или недостаточность секреции гормонов гипофиза. Недостаточность секреции гормонов часто бывает множественной, но при избыточной секреции речь обычно идет об одном гормоне. ГОРМОН РОСТА (ГР) Секрецию гормона роста ацидофильными клетками передней доли гипофиза регулирует соотношение между гипоталамическим ГРрилизинг гормоном (высвобождающим ГР) и соматостатином (ингибирующим высвобождение ГР). Относительно редкие периоды повышения секреции ГР обычно связаны с физической нагрузкой, погружением в глубокий сон, снижением содержания глюкозы в крови приблизительно через 1 ч после приема пищи. В другие периоды уровень ГР может быть очень низким или не поддающимся определению, особенно у детей. Соматостатин может также ингибировать секрецию ТТР. Он обнаружен не только в гипоталамусе и других отделах головного мозга, но также в клетках желудочнокишечного тракта и островков Лангерганса поджелудочной железы. Он ингибирует секрецию многих гормонов желудочнокишечного тракта. Главной функцией ГР является стимуляция роста. Об этом свидетельствует тот факт, что недостаточность ГР в детском возрасте приводит к низкорослости, а избыток — к чрезмерному росту. Установлено, что ГР благоприятствует биосинтезу белка и, взаимодействуя с инсулином, стимулирует поступление аминокислот в клетки. Воздействие ГР на рост, по-видимому, опосредовано соматомединами, которые представляют собой полипептидные факторы роста, синтезируемые в печени. Для нормального роста требуются и другие факторы, такие как адекватное питание и тироксин. Ускорение роста при половом созревании, вероятно, обусловлено андрогенами. ГР также оказывает влияние на метаболизм углеводов и жиров. Он препятствует поступлению в клетки глюкозы, тогда как инсулин способствует этому процессу. Непереносимость к углеводам может быть обусловлена избытком ГР, которому обычно противостоит повышенная секреция инсулина. ГР стимулирует липолиз, и поскольку нарастающие концентрации свободных жирных кислот (СЖК) также противодействуют освобождению и действию инсулина, трудно провести грань между прямыми и косвенными антиинсулиновыми эффектами. Гипогликемия (в противоположность гипергликемии) стимулирует секрецию ГР. Недостаточность ГР у взрослых очень редко приводит к развитию какихлибо симптомов. Регуляция. Помимо упомянутых выше факторов, секрецию ГР могут стимулировать стресс, голодание, быстрое снижение содержания глюкозы в крови, введение некоторых аминокислот или лекарственых средств (таких как LДОФА). Секрецию ГР, на которую воздействует также содержание других гормонов, угнетает гипергликемия. Нарушения ответной реакции на перечисленные выше стимулирующие воздействия могут быть при ожирении, гипотиреоизе и понижении внутренней секреции половых желез, в некоторых случаях синдрома Кушинга и у пациентов, которым вводят большие дозы стероидов. Эстрогены потенциируют эффекты факторов, регулирующих секрецию ГР. Избыток ГР: акромегалия и чрезмерный рост У большинства пациентов с избытком ГР имеется ацидофильная аденома гипофиза, что, по-видимому, является следствием чрезмерной стимуляции гипоталамуса. Поэтому после удаления аденомы гипофиза такое патологическое состояние может развиться вновь. Клинические симптомы зависят от того, развивается ли данное патологическое состояние до или после окостенения эпифизов костей. В детском возрасте избыток ГР приводит к чрезмерному росту. Сопутствующее недоразвитие половых желез может задерживать окостенение эпифизов, и в отдельных случаях рост пациентов может превышать 2,4 м. После завершения процессов окостенения могут развиться признаки акромегалии. Такие гиганты часто умирают в юности от инфекционных заболеваний или в связи с прогрессирующим ростом опухолей. У взрослых после окостенения эпифизов избыток ГР вызывает акромегалию. При этом нарастает общая масса костей и мягких тканей, что приводит к увеличению размеров рук и других частей тела в результате утолщения мягких тканей. Возможны усиленный рост волос и стимуляция секреторной деятельности кожных желез. Часто заметны изменения черт лица в результате увеличения челюстей и пазух лицевых костей. Однако то обстоятельство, что черты лица пациента постепенно становятся более грубыми, может оставаться незамеченным в течение многих лет. Первоначально больные могут жаловаться на то, что становятся теснылш обувь, обручальные кольца. Размеры внутренних органов также нарастают; часто наблюдается кардиомегалия. Несмотря на увеличение щитовидной железы, ее функция у больных акромегалией, как правило, не нарушается. Обычно имеют место расстройства менструального цикла. В результате прорастания опухоли гипофиза в окружающие структуры могут появляться другие симптомы. Так, например, сдавливание перекреста зрительных нервов вызывает искажение полей зрения. Если процесс разрушения железы внутренней секреции продолжается, может возникать недостаточность других гормонов передней доли гипофиза. Однако содержание пролактина может быть повышено. Приблизительно в 25% случаев можно обнаружить нарушение толерантности к глюкозе. Но лишь примерно в половине из етих случаев развивается симптоматический диабет. Как правило, поджелудочная железа способна секретировать достаточно инсулина для того, чтобы превысить антагонистический эффект ГР. По-видимому, в этих условиях диабет развивается только у предрасположенных к нему пациентов. Иногда акромегалия — одно из проявлений множественного аденоматоза желез внутренней секреции. Диагностика Диагноз акромегалии ставят на основании результатов клинических наблюдений и рентгенологических исследований. Содержание ГР в сыворотке крови при акромегалии обычно выше, чем в норме, и может достигать нескольких сот мЕд/п. Однако поскольку диапазон пределов в норме очень велик, результаты обследования амбулаторных пациентов не позволяют отличить больных акромегалией с умеренно повышенным содержанием ГР в сыворотке крови от здоровых людей. Диагноз подтверждается обнаружением повышенного содержания ГР, не устраняемого при повышении концентрации глюкозы в плазме крови. Во время проведения теста на толерантность к глюкозе (ТТГ) у здорового человека содержание ГР в плазме крови значительно снижается. При акромегалии секреция ГР автономна, и содержание ГР в плазме крови может оставаться неизменным, даже нарастать или лишь незначительно снижаться. Данные о содержании ГР в плазме крови могут быть также использованы для контроля эффективности проводимого лечения. Недостаточность гормона роста Недостаточность ГР относительно редко бывает у нормально сложенных, но низкорослых детей. Приблизительно у половины из них имеется также недостаточность других гормонов. У некоторых пациентов возможны органические поражения передней доли гипофиза или гипоталамуса, описана редкая, наследуемая по аутосомнорецессивному типу, форма заболевания, но во многих случаях причину карликового роста установить не удается. Прогресирующая задержка роста может быть замечена уже на протяжении первых двух лет жизни. Единственный способ лечения основан на применении ГР, запасы которого ограничены. Поэтому так важно доказать, что у больного действительно дефицит ГР. Расстройства эмоциональной сферы могут сопровождаться явлениями недостаточности ГР, которые не удается отличить с помощью лабораторных проб от недостаточности ГР, обусловленной органическими причинами. Диагностика У здоровых детей содержание ГР в плазме крови обычно низкое, и на основании определений концентрации ГР в крови редко удается поставить диагноз. Если брать кровь для анализов в те моменты, когда предполагаются физиологически высокие уровни ГР, можно избежать проведения неприятных для пациента тестов стимуляции секреции ГР. В качестве таких моментов выбирают время между 60 и 90 мин после погружения в сон и приблизительно через 20 мин после усиленной физической нагрузки. Если упомянутые выше исследования не позволяют исключить предположение о недостаточности ГР, приходится применять тест (один или более), связанный со стимуляцией секреции ГР. Однозначное доказательство получения нормального ответа на стимуляцию опровергает диагноз, тогда как явное нарушение такого ответа подтверждает диагноз. После того, как доказана недостаточность ГР, следует установить ее причину с помощью соответствующих клинических и рентгенологических методов. Недостаточность гипофиза Причины недостаточности гипофиза К числу обычных причин этого патологического состояния относятся: 1) разрушение или повреждение гипофиза или гипоталамуса первичными или вторичными опухолями. Наиболее распространенными источниками вторичных опухолей являются молочные железы или бронхи; 2) инфаркты, как правило, послеродовые (синдром Шихена) или в редких случаях другие тяжелые заболевания сердечнососудистой системы; 3) хирургические операции на гипофизе или воздействия на гипофиз ионизирующей радиации. К редко встречающимся причинам недостаточности гипофиза относятся: 1) травмы головы; 2) инфекции или гранулемы. Явления недостаточности отдельных гормонов могут носить идиопатический характер. Для недостаточности гипофиза характерна описываемая ниже клиническая картина. Это заболевание, однако, встречается редко. Предположение о гипофункции передней доли гипофиза обычно возникает в следующих случаях: 1) при существовании клинических и рентгенологических доказательств наличия опухоли гипофиза или соответствующим образом локализованной опухоли головного мозга; 2) прп понижении внутренней секреции половых желез, гипотиреозе или недостаточности коры надпочечников, которые, по данным предварительного тестирования, имеют вторичное происхождение; 3) при низкорослости, обусловленной (согласно данным тестов) недостаточностью ГР. Хотя иногда и может быть недостаточность того или иного отдельно взятого гормона (в частности, гормона роста или гонадотропинов), как правило, развивается дефицит нескольких гормонов. Поэтому, если доказана недостаточность одного гормона, важно установить, нарушена или соответствует норме секреция Других гормонов. Выяснение этого вопроса необходимо не только в связи с проблемами заместительной терапии, но также для оценки способности гипофиза реагировать на стресс, например, на такой как хирургические операции. Передняя доля гипофиза обладает значительными функциональными резервами. Клинические симптомы недостаточности функций передней доли гипофиза обычно отсутствуют до тех пор, пока патологическими процессами не разрушены приблизительно 70% ткани железы. Исключение составляют случаи, сопровождающиеся гиперпролактинемией, когда аменорея и бесплодие могут быть ранними симптомами. Последствия недостаточности гормонов Нарастающее поражение гипофиза патологическими процессами, как правило, прежде всего вызывает недостаточность гонадотропинов и ГР. Содержание в плазме крови АКТГ и/или ТТР может оставаться в пределах нормы и понизиться спустя месяцы или даже годы. Ниже мы перечисляем клинические и биохимические последствия недостаточности железмишеней. Симптомами вторичной гипофункции половых желез, обусловленной недостаточностью гонадотропинов, являются аменорея, бесплодие, атрофия вторичных половых признаков, импотенция или утрата полового влечения. Характерна утрата волосяного покрова подмышечных областей и на лобке. У детей отмечается задержка полового созревания. Задержка роста у детей может быть обусловлена недостаточностью гормона роста и ТТР. Вторичный гипотиреоз (недостаточность ТТР) клинически бывает невозможно отличить от первичного гипотиреоза. Вторичная гипофункция коры надпочечников (недостаточность АКТГ) в нескольких отношениях отличается от ее первичной формы (болезни Аддисона). У пациентов не отмечается гиперпигментации, поскольку имеется недостаточность (но не избыток) секреции АКТГ. Столь типичной для болезни Аддисона недостаточности натрия при вторичной гипофункции коры надпочечников не отмечается, поскольку секреция альдостерона (регулируемая не АКТГ, а апгиотензином) в пределах нормы. Однако может быть существенная гппонатриемия, обусловленная разбавлением крови в результате недостаточности кортизола, необходимого для нормальной экскреции воды. Кортизол необходим также для поддержания нормального давления крови; недостаточность АКТГ сопровождается гипотонией. Гиперкалиемия не является обычной. В связи с недостаточностью кортизола и/или гормона роста такие пациенты очень чувствительны к воздействию инсулина, и гипогликемия при голодании может быть характерным признаком. Нарушения лактации, обусловленные недостаточностью пролактина, могут развиться в условиях послеродовых инфарктов гипофиза (синдром Шихена). Однако при недостаточности функций гипофиза, обусловленной ростом новообразований, содержание пролактина часто повышено, что может вызывать галакторею (секрецию молочных желез). При недостаточности функций гипофиза, как и при болезни Аддисона, пациенты могут погибнуть в связи с дефицитом секреции АКТГ и, следовательно, кортизола в условиях стресса, вызванного, например, инфекционным заболеванием или хирургической операцией. Другие опасные для жизни осложнения — гипогликемия, чрезмерное обводнение тканей и гипотермия. Оценка функции передней доли гипофиза Интерпретация результатов исследований гормонов гипофиза часто бывает затруднена, поскольку низкое содержание этих гормонов не всегда указывает на заболевание, а нормальный уровень гормонов не позволяет исключить поражение гипофиза, обладающего большими функциональными резервами. Наиболее четкое подтверждение или опровержение предполагаемого диагноза недостаточности функций гипофиза получают путем прямого измерения содержания гормонов гипофиза после стимуляции. Если прямые определения содержания гормонов гипофиза невозможны, косвенные доказательства недостаточности функций гипофиза могут быть получены путем обнаружения сниженной секреции железымишени в условиях введения соответствующего тропного гормона (см. гл. VI, VII и VIII), но результаты исследований часто бывает трудно интерпретировать. Следует помнить, что длительная недостаточность гипофиза может привести к вторичной атрофии железымишени, в результате чего развивается снижение ответа на стимуляцию железы. Отметим, что лабораторные исследования доказывают только наличие или отсутствие недостаточности гипофиза. Для выяснения ее причины необходимы клинические и рентгенологические методы. Гипоталамус или гипофиз! В предшествующем изложении мы не проводили различий между гипоталамическими и гипофизарными факторами, приводящими к недостаточности гормонов гипофиза, или, иными словами, между дефицитом рилизингфакторов и недостаточностью секреции гормонов гипофиза. Недостаточность отдельных гормопов чаще бывает гипоталампческого, но не гипофизарпого происхождения. Одновременное наличие несахарного диабета указывает на возможность поражения гипоталамуса, но соответствующие симптомы первоначально могут не выявляться в связи с недостаточностью АКТГ и, следовательно, кортизола. Существуют тесты как для суммарной оценки функций гипоталамуса и гипофиза, так и для характеристики функций только гипофиза. В некоторых случаях удается идентифицировать локализацию патологического процесса. Так, например, ответ ТТР на воздействие ТРФ различен в случаях вторичного гипотиреоза гипоталамического или гипофизарного происхождения. При недостаточности функций половых желез можно постулировать гипоталамический генез патологического состояния, если базальный уровень гонадотропинов низок и если ответ на ЛГ/ФСГрилизингфактор (РФ), хотя количественно и не выходящий за пределы нормы, запаздывает. Когда станут доступными и другие синтетические рилизинггормоны, может появиться возможность дифференцировать гипоталамический и гипофизарный компоненты недостаточности ГР и АКТГ путем сопоставления ответов на стресс (оба компонента) и на воздействие рилизингфактора (только гппофизарный компонент). Опухоли гипофиза Клинические симптомы опухолей гипофиза зависят от гистологического строения и размера опухоли. В тех случаях, когда опухоль состоит из секреторных клеток, отмечают клинические проявления избыточной секреции гормонов: 1) ГР—акромегалия или чрезмерный рост; 2) АКТГ— синдром Кушинга; 3) пролактина — бесплодие, аменорея, в некоторых случаях галакторея. Большие опухоли гипофиза могут сопровождаться такими симптомами, как: 1) нарушение зрения и головные боли, что обусловлено сдавливанием перекреста зрительных нервов или повышением внутричерепного давления; 2) недостаточность некоторых (или всех) гормонов передней доли гипофиза. Несекретирующие опухоли трудно диагностировать при помощи биохимических тестов, хотя комбинированная проба на стимуляцию гипофизарных гормонов может выявить функциональные нарушения, которые еще не проявляются клинически. Однако во многих случаях такие опухоли сопровождаются бессимптомными гиперпролактинемиями либо потому, что опухоль секретирует пролактин, либо потому, что нарушается естественное гипоталамическое ингибирование. Краткое описание исследований, рекомендуемых при подозрениях на дисфункцию гипофиза, представлено в гл. VII. ЗАКЛЮЧЕНИЕ 1. Передняя доля гипофиза секретирует гормон роста (ГР), пролактин, адренокортикотропный гормон (АКТГ, кортикотропин), рлипотропин (ТТР, тиреоидстимулирующий гормон) и два гипофизарных гонадотропина: фолликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ). Задняя доля гипофиза секретирует антидиуретический гормон (АДГ) и окситоцин. 2. Секрецию гормонов передней доли гипофиза контролируют регуляторные факторы гипоталамуса. Последние в свою очередь находятся под регулирующим воздействием концентрации гормо нов в циркулирующей крови (по принципу обратной связи) или реагируют на импульсы, поступающие из высших центров голов ного мозга. 3. ГР регулирует рост и оказывает ряд воздействий на промежуточные реакции обмена веществ. Избыточная секреция ГР вызывает чрезмерный рост или акромегалию. Доказательством автономности секреции ГР является отсутствие снижения его концентрации в плазме крови во время проведения теста на толерантность к глюкозе. Недостаточность ГР в детском возрасте приводит к низкорослостп (карликовость). Диагностика такой недостаточности основана на обнаружении сниженного ответа ГР на адекватные стимулы. 4. При дисфункциях передней доли гипофпза обычно имеет место недостаточность нескольких гормонов. Более редко встречается недостаточность одного гормона. Клиническими признаками недостаточности: гипофиза являются дефицит гонадотропинов и половых гормонов, а также вторичная гипофункция коры надпочечников и щитовидной железы. Диагноз ставится при обнаружении снижения функциональных резервов передней доли гипофиза после стимуляции. 5. Опухоли гипофиза могут секретировать избыток ГР, АКТГ, пролактина или приводить к недостаточности функций гипофиза. Возможна гиперпролактинемия в отсутствие явных симптомов расстройств функций эндокринных желез. ГЛАВА VI |
