Начальные лекции по фармакологии общие вопросы, рецептура, фармакокинетика и фармакодинамика.. Начальные лекции по фармакологии общие вопросы, рецептура, фарма. Общая фармакология и рецептура
 Скачать 0.63 Mb. Скачать 0.63 Mb.
|
|
30. Клиническое значение биотрансформации лекарств. Влияние пола, возраста, массы тела, экологических факторов, курения, алкоголя на биотрансформацию лекарств. Клиническое значение биотрансформации ЛС: т.к. доза и частота приема, необходимые для достижения эффективной концентрации в крови и тканях, могут варьировать у больных из-за индивидуальных различий в распределении, скорости метаболизма и элиминации ЛС, важен их учет в клинической практике. Влияние на биотрансформацию ЛС различных факторов: а) функциональное состояние печени: при ее заболеваниях клиренс ЛС обычно уменьшается, а период полуэлиминации возрастает. б) влияние факторов среды: курение способствует индукции цитохрома P450, в результате чего ускоряется метаболизм ЛС в ходе микросомального окисления в) у вегетарианцев биотрансформация ЛС замедлена г) у пожилых и молодых пациентов характерна повышенная чувствительность к фармакологическому или токсическому действию ЛС (у лиц пожилого возраста и у детей до 6 мес активность микросомального окисления снижена) д) у мужчин метаболизм некоторых ЛС происходит быстрее, чем у женщин, т.к. андрогены стимулируют синтез микросомальных ферментов печени {этанол} е) высокое содержание в пище белков и интенсивная физическая нагрузка: ускорение метаболизма ЛС. ж) алкоголь и ожирение замедляют метаболизм ЛС 31. Метаболическое взаимодействие лекарств. Болезни, влияющие на их биотрансформацию. Метаболическое взаимодействие ЛС: 1) индукция ферментов метаболизма ЛС – абсолютное увеличение их количества и активности вследствие воздействия на них определенных ЛС. Индукция ведет к ускорению метаболизма ЛС и (как правило, но не всегда) к снижению их фармакологической активности (рифампицин, барбитураты – индукторы цитохрома P450) 2) ингибирование ферментов метаболизма ЛС – угнетение активности ферментов метаболизма под действием некоторых ксенобиотиков: а) конкурентное метаболическое взаимодействие – ЛС с высоким аффинитетом к определенным ферментам снижают метаболизм ЛС с более низким аффинитетом к этим ферментам (верапамил) б) связывание с геном, индуцирующим синтез определенных изоферментов цитохрома P450 (цимедин) в) прямая инактивация изоферментов цитохрома P450 (флавоноиды) Болезни, влияющие на метаболизм ЛС: а) болезни почек (нарушение почечного кровотока, острые и хронические заболевания почек, исходы длительных почечных заболеваний) б) болезни печени (первичный и алкогольный циррозы, гепатиты, гепатомы) в) болезни ЖКТ и эндокринных органов в) индивидуальная непереносимость некоторых ЛС (отсутствие ферментов ацетилирования – непереносимость аспирина) 32. Пути и механизмы выведения лекарств из организма. Возможности управления выведением лекарств. Пути и механизмы выведения ЛС: элиминация ЛС печенью и почками и некоторыми другими органами: а) почками путем фильтрации, секреции, реабсорбции б) печенью путем биотрансформации, экскреции с желчью в) через легкие, слюну, пот, молоко и т.д. путем секреции, испарения Возможности управления процессами выведения ЛС: 1. управление pH: в щелочной моче повышается выведение кислых соединений, в кислой – выведение основных соединений 2. применение желчегонных препаратов (холензим, аллохол) 3. гемодиализ, перитонеальный диализ, гемосорбция, лимфосорбция 4. форсированный диурез (в/в NaCl или глюкоза для водной нагрузки + фуросемид или маннитол) 5. промывание желудка, применение клизм 33. Концепция рецепторов в фармакологии, молекулярная природа рецепторов, сигнальные механизмы действия лекарств (типы трансмембранной сигнализации и вторичные посредники). Рецепторы – молекулярные компоненты клетки или организма, которые взаимодействуют с ЛС и индуцируют ряд биохимических событий, ведущих к развитию фармакологического эффекта. Концепция рецепторов в фармакологии: 1. Рецепторы детерминируют количественные закономерности действия ЛС 2. Рецепторы ответственны за селективность действия ЛС 3. Рецепторы посредники действия фармакологических антагонистов Концепция рецепторов - основа целенаправленного применения лекарственных средств, влияющих на регуляторные, биохимические процессы и коммуникации. Молекулярная природа рецепторов: 1. регуляторные белки, посредники действия различных химических сигналов: нейромедиаторов, гормонов, аутокоидов 2. ферменты и трансмембранные белки переносчики (Na+, K+ АТФаза) 3. структурные белки (тубулин, белки цитоскелета, клеточная поверхность) 4. ядерные белки и нуклеиновые кислоты Сигнальные механизмы действия лекарств: 1) проникновение растворимых в липидах лигандов через мембрану и их действие на внутриклеточные рецепторы. 2) сигнальная молекула связывается с внеклеточным доменом трансмембранного белка и активирует ферментативную активность его цитоплазматического домена. 3) сигнальная молекула связывается с ионным каналом и регулирует его открытие. 4) сигнальная молекула связывается с рецептором на поверхности клетки, который сопряжен с эффекторным ферментом посредством G-белка. G-белок активирует вторичный посредник. Типы трансмембранной сигнализации: а) через 1-TMS-рецепторы, обладающие и не обладающие тирозинкиназной активностью б) через 7-ТMS-рецепторы, связанные с G-белком в) через ионные каналы (лиганд-зависимые, потенциал-зависимые, щелевые контакты) Вторичные посредники: цАМФ, ионы Ca2+, ДАГ, ИФ3. 34. Физико-химические и химические механизмы действия лекарственных веществ. а) Физико-химическое взаимодействие с биосубстратом – неэлектролитное действие. Основные фармакологические эффекты: 1) наркотическое 2) обще депрессивное 3) парализующее 4) местно раздражающее 5) мембранолитическое действия. Химическая природа веществ: химически инертные углеводороды, эфиры, спирты, альдегиды, барбитураты, газовые наркотические средства Механизм действия – обратимое деструирование мембран. б) Химический (молекулярно-биохимический) механизм действия лекарственных средств. Основные типы химического взаимодействия с биосубстратом:
Значение нековалентных взаимодействий ЛС: действие неспецифично, не зависит от химического строения вещества. Значение ковалентных взаимодействий ЛС: действие специфично, критически зависит от химических строения, реализиуется посредством влияния на рецепторы. 35. Термины и понятия количественной фармакологии: эффект, эффективность, активность, агонист (полный, частичный), антагонист. Клиническое различие понятий активность и эффективность лекарств. Э 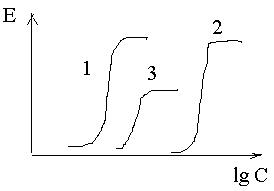 ффект (ответ) – количественный выход реакции взаимодействия клетки, органа, системы или организма с фармакологическим агентом. ффект (ответ) – количественный выход реакции взаимодействия клетки, органа, системы или организма с фармакологическим агентом. Эффективность – мера реакции по оси эффекта – величина отклика биологической системы на фармакологическое воздействие; это способность ЛС оказывать максимально возможное для него действие. Т.е. фактически это максимальная величина эффекта, которую можно достигнуть при введении данного лекарства. Численно характеризуется величиной Еmax. Чем выше Еmax, тем выше эффективность лекарства Активность – мера чувствительности к ЛС по оси концентраций, характеризует аффинность (сродство лиганда к рецептору), показывает, какая доза (концентрация) ЛС способна вызвать развитие стандартного эффекта, равного 50% от максимально возможного для этого лекарства. Численно характеризуется величиной ЕС50 или ED50. Чем выше активность ЛС, тем меньшая его доза требуется для воспроизведения терапевтического эффекта. Эффективность: 1=2>3 Активность: 1>3>2 В клинической деятельности важнее знать эффективность, а не активность, т.к. нас больше интересует способность ЛС вызывать определенное действие в организме. Агонист – лиганд, который связывается с рецептором и вызывает биологическую реакция, срабатывание физиологической системы. Полный агонист – максимальный отклик, частичный – вызывают меньшую реакцию даже при оккупации всех рецепторов. Антагонист - лиганды занимающие рецепторы или изменяющие их таким образом, что они утрачивают способность взаимодействовать с другими лигандами, но сами не вызывающие биологической реакции (блокируют действие агонистов). К 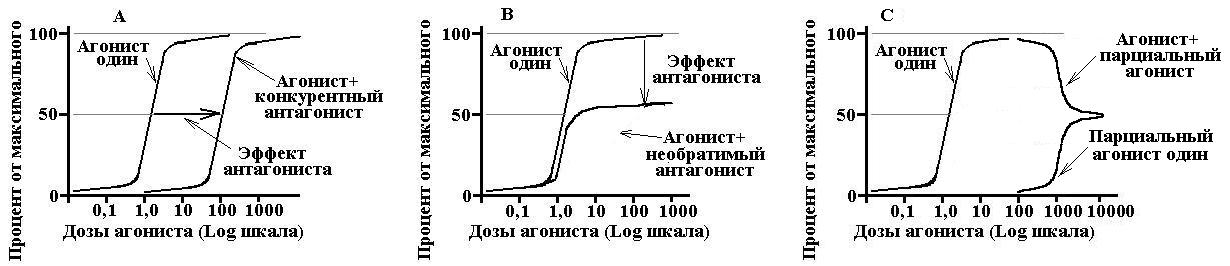 онкурентные антагонисты - взаимодействуют с рецепторами обратимо и тем самым конкурируют с агонистами. Увеличение концентрации агониста может полностью устранить эффект антагониста. Конкурентный антагонист сдвигает кривую «доза-эффект» для агониста, увеличивает EC50, не влияет на Emax. онкурентные антагонисты - взаимодействуют с рецепторами обратимо и тем самым конкурируют с агонистами. Увеличение концентрации агониста может полностью устранить эффект антагониста. Конкурентный антагонист сдвигает кривую «доза-эффект» для агониста, увеличивает EC50, не влияет на Emax.Неконкурентные антагонисты - необратимо изменяют сродство рецепторов к агонисту, связывание часто происходит не с активным участком рецептора, увеличение концентрации агониста не устраняет действие антагониста. Неконкурентный антагонист снижает Emax, не изменяет EC50, кривая «доза-эффект» сжимается относительно вертикальной оси. 36. Количественные закономерности действия лекарств. Закон уменьшения отклика биологических систем. Модель Кларка и ее следствия. Общий вид зависимости концентрация – эффект в нормальных и логнормальных координатах. Модель Кларка-Ариенса: 1. Взаимодействие между лигандом (L) и рецептором (R) обратимы. 2. Все рецепторы для данного лиганда – эквивалентны и независимы (их насыщение не влияет на другие рецепторы). 3. Эффект прямо пропорционален числу занятых рецепторов. 4. Лиганд существует в двух состояниях: свободном и связанном с рецептором. А) Б) Т.к. при возрастании количества лигандов в какой-то момент времени все рецепторы окажутся заняты, то максимально возможное количество образованных комплексов лиганд-рецептор описывается формулой: [RL] = [R] × Эффект определяется вероятностью активации рецептора при связывании с лигандом, т.е. его внутренней активностью (Ке), поэтому E = Ke×[RL]. При этом эффект максимален при Ке=1 и минимален и Ке=0. Естественно, что максимальный эффект описывается соотношением Emax = Ke×[Rобщий], где [Rобщий] – общее число рецепторов для данного лиганда Эффект зависит и от концентрации лиганда на рецепторах [С], поэтому E = Emax Из приведенных соотношений вытекает, что EC50=Kd 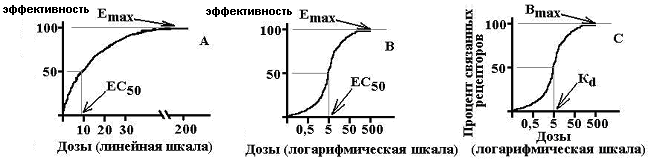 Emax – максимальный эффект, Bmax – максимальное число связанных рецепторов, EC50 – концентрация ЛС, при которой возникает эффект, равный половине от максимального, Kd – константа диссоциации вещества от рецептора, при которой связано 50% рецепторов. Закону убывания отклика соответствует параболическая зависимость «концентрация – эффективность». Ответ на малые дозы ЛС обычно возрастает прямо пропорционально дозе. Однако при увеличении дозы прирост ответной реакции снижается и в конечном счете может быть достигнута доза, при которой не происходит дальнейшего увеличения ответа (за счет оккупации всех рецепторов для данного лиганда). 37. Изменение эффекта лекарств. Градуальная и квантовая оценка эффекта, сущность и клинические приложения. Меры количественной оценки активности и эффективности лекарств в экспериментальной и клинической практике. Все фармакологические эффекты можно условно разделить на две категории: а) градуальные (непрерывные, интегральные) эффекты – такие эффекты ЛС, которые могут быть измерены количественно { действие гипотензивных ЛС – по уровню АД}. Описываются градуальной «кривой доза-эффект» (см. в. 36), на основе которой можно оценить: 1) индивидуальную чувствительность к ЛС 2) активность ЛС 3) максимальную эффективность ЛС б) квантовые эффекты – такие эффекты ЛС, которые являются дискретной величиной, качественным признаком, т.е. описываются всего лишь несколькими вариантами состояний {головная боль после приема анальгетика или есть, или нет}. Описывается квантовой кривой доза-эффект, где отмечают зависимость проявления эффекта в популяции от величины принимаемой дозы ЛС. График зависимости доза-эффект при этом имеет куполообразный вид и идентичен Гауссовой кривой нормального распределения. На основе квантовой кривой можно : 1) оценить популяционную чувствительность ЛС 2) отметить наличие эффекта при данной дозе 3) выбрать среднюю терапевтическую дозу. Различия между градуальной и квантовой характеристикой «доза-эффект»:
Количественная оценка активности и эффективности ЛС проводится на основе построения кривых «доза-эффект» и их последующей оценке (см. в.35) 38. Виды действия лекарственных средств. Изменение действия лекарств при их повторном введении. Виды действия ЛС: 1. Местное действие – действие вещества, возникающее на месте его приложения (анестетик – на слизистую оболочку) 2. Резорбтивное (системное) действие – действие вещества, развивающееся после его всасывания, поступления в общий кровоток, а затем в ткани. Зависит от путей введения ЛС и их способности проникать через биологические барьеры. Как при местном, так и резорбтивном действии лекарственные средства могут оказывать либо прямое, либо рефлекторное влияние: а) прямое влияние - непосредственный контакт с органом-мишенью (адреналин на сердце). б) рефлекторное – изменение функции органов или нервных центров путем влияния на экстеро- и интерорецепторы (горчичники при патологии органов дыхания рефлекторно улучшают их трофику) Изменения действия ЛС при их повторном введении: 1. Кумуляция – увеличение эффекта вследствие накопления в организме ЛС: а) материальная кумуляция - накопление действующего вещества в организме {сердечные гликозиды} б) функциональная кумуляция – нарастающие изменения функции систем организма {изменения функции ЦНС при хроническом алкоголизме}. 2. Толерантность (привыкание) - снижение ответной реакции организма на повторные введения ЛС; для того, чтобы восстановить реакцию на ЛС, его приходится вводить во все бóльших и бóльших дозах {диазепам}: а) истинная толерантность – наблюдается как при энтеральном, так и при парентеральном введении ЛС, не зависит от степени его всасывания в кровоток. В ее основе - фармакодинамические механизмы привыкания: 1) десенситизация – снижение чувствительности рецептора к лекарственному средству {-адреномиметики при длительном применении приводят к фосфорилированию -адренорецепторов, которые не способны ответить на -адреномиметики} 2) Down-регуляция – снижение числа рецепторов к лекарственному средству {при повторных введениях наркотических анальгетиков количество опиоидных рецепторов снижается и требуются все бóльшие и бóльшие дозы лекарства, чтобы вызвать желаемый ответ} . Если ЛС блокирует рецепторы, то механизм толерантности к нему может быть связан с up-регуляцией – увеличением числа рецепторов к лекарственному средству (-адреноблокаторы) 3) включение компенсаторных механизмов регуляции (при повторных введениях гипотензивных препаратов коллапс возникает значительно реже, чем при первом введении за счет адаптации барорецепторов) б) относительная толерантность (псевдотолерантность) - развивается только при введении ЛС внутрь и связан со снижением скорости и полноты всасывания лекарства 3. Тахифилаксия – состояние, при котором частое введение ЛС вызывает развитие толерантности уже через несколько часов, но при достаточно редких введениях ЛС его эффект сохраняется в полной мере. Развитие толерантности связано обычно с истощением эффекторных систем. |
