Сборник всех лекций. Общая характеристика обмена веществ и энергии. Биоэнергетика
 Скачать 3.68 Mb. Скачать 3.68 Mb.
|
ОБМЕН НУКЛЕИНОВЫХ КИСЛОТ. БИОСИНТЕЗ НУКЛЕИНОВЫХ КИСЛОТ И БЕЛКОВ (МАТРИЧНЫЕ БИОСИНТЕЗЫ)ПЛАН: Переваривание нуклеопротеинов пищи в желудочно-кишечном тракте. Катаболизм азотистых оснований. Биосинтез нуклеотидов. Матричная природа синтеза нуклеиновых кислот и белков. Репликация. Транскрипция. Свойства генетического кода. Трансляция. Механизмы генетической изменчивости. Наследственные болезни. Переваривание нуклеопротеинов пищи в желудочно-кишечном тракте. Катаболизм азотистых оснований Пищевые нуклеопротеины в желудке отщепляют белковый компонент и денатурируют под действием НСl желудочного сока. Полинуклеотиды гидролизуются в кишечнике до мононуклеотидов. Под действием ДНК-азы и РНК-азы панкреатического сока сначала образуются олигонуклеотиды, последние под действием фосфодиэстераз панкреатической железы расщепляются до мононуклеотидов. Нуклеотидазы и неспецифические фосфатазы гидролитически отщепляют фосфатный остаток нуклеотидов и превращают их в нуклеозиды, которые либо всасываются клетками тонкого кишечника, либо расщепляются нуклеозидфосфорилазами кишечника с образованием рибозо- или дезоксирибозо-1-фосфата, пуриновых и пиримидиновых оснований. Пищевые пурины и пиримидины не являются незаменимыми пищевыми факторами и очень мало используются для синтеза нуклеиновых кислот тканей. Катаболизм пуриновых оснований У человека основной продукт катаболизма пуриновых нуклеотидов - мочевая кислота. Её образование идёт путём гидролитического отщепления фосфатного остатка от нуклеотидов с помощью нуклеотидаз или фосфатаз, фосфоролиза N-гликозидной связи нуклеозидов пуриннуклеозидфосфорилазой, последующего дезаминирования и окисления азотистых оснований. Промежуточные соединения – продукты дезаминирования – гипоксантин и ксантин. Мочевая кислота удаляется из организма главным образом с мочой в виде конечного продукта обмена. Ежесуточно из организма выводится от 0,4 до 0,6 г мочевой кислоты и уратов. 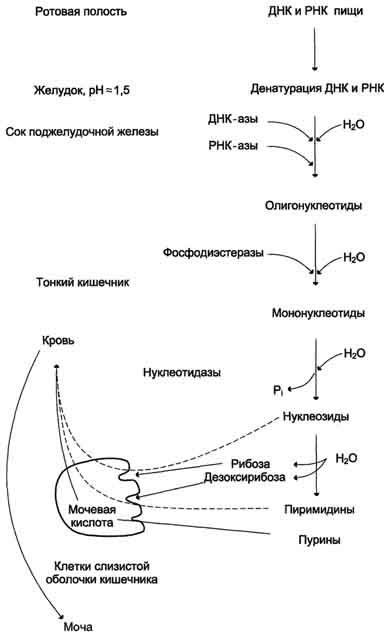 Переваривание нуклеиновых кислот пищи  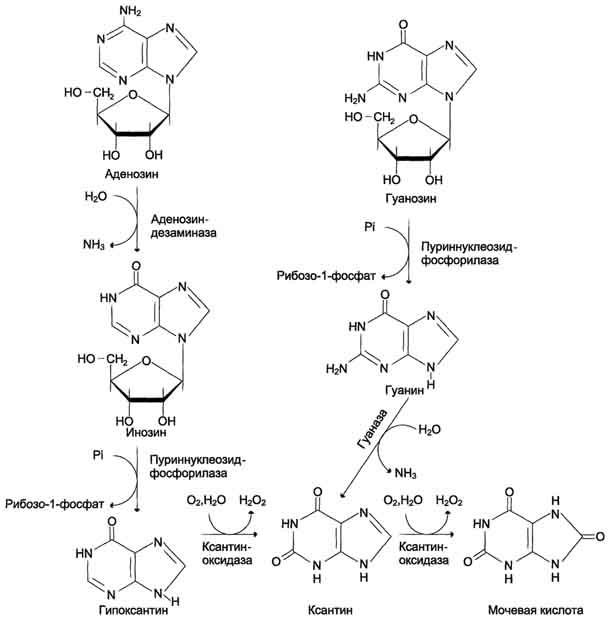  Катаболизм пуриновых оснований Когда в плазме крови концентрация мочевой кислоты превышает норму, то возникает гиперурикемия. Вследствие гиперурикемии может развиться подагра - заболевание, при котором кристаллы мочевой кислоты и уратов откладываются в суставных хрящах, подкожной клетчатке (подагрический артрит). Причиной заболевания может быть наследственная недостаточность какого-либо фермента. При подагре из пищи надо исключить богатые азотистыми основаниями продукты - печень, чай, кофе. Катаболизм пиримидиновых оснований Пиримидиновые основания под действием микрофлоры кишечника расщепляются до NH3, CO2, β-аланина и β-аминоизобутирата. Биосинтез нуклеозидфосфатов Из трёх основных составных частей нуклеотида – азотистого основания, пентозы и фосфорной кислоты – только азотистые основания создаются специфическим путём (фосфорная кислота всегда присутствует в клетках; пентозы образуются при распаде углеводов). Пути возникновения пуриновых и пиримидиновых оснований различны, но есть черты сходства в механизмах их синтеза: - широкое использование глицина, аспарагина и глутамина в качестве источников азота в гетероциклах; Включение в состав азотистых оснований атомов углерода из углекислого газа и формиата; Построение пуринового основания и завершение синтезапиримидинового основания на основе рибозо-5-фосфата; Ферментативный характер всех реакций; -возникновение на определённом этапе предшественников, из которых формируются индивидуальныенуклеозид-5-фосфаты. Биосинтез пуриновых нуклеотидов В различных клетках организма синтезируется до 90% пуриновых и пиримидиновых нуклеотидов из простых предшественников de novo; за счёт повторного использования азотистых оснований или нуклеозидов образуется небольшая часть нуклеотидов. Печень - основное место образования пуриновых нуклеотидов, откуда они могут поступать в ткани. В 40-50-х годах XX столетия опытами с мечеными изотопами удалось выяснить происхождение атомов пуринового ядра при синтезе пуринов de novo. Было установлено, что в формировании цикла принимают участие аминокислоты Асп, Гли, Глн, СО2 и два одноуглеродных производных тетрагидрофолата. Формирование гетероциклического основания осуществляется на остатке рибозо-5-фосфата. Биосинтез пиримидиновых нуклеотидов Пиримидиновое кольцо синтезируется из простых предшественников: глутамина, СО2 и аспарагиновой кислоты и затем связывается с рибозо-5-фосфатом. Биосинтез дезоксирибонуклеотидов Синтез дезоксирибонуклеотидов идёт с заметной скоростью только в тех клетках, которые готовятся к синтезу ДНК и делению. В покоящихся клетках дезоксинуклеотиды практически отсутствуют. Все дезоксинуклеотиды, кроме тимидиловых, образуются из рибонуклеотидов путём прямого восстановления ОН-группы у второго углеродного атома рибозы в составе рибонуклеозиддифосфатов до дезоксирибозы. Матричная природа синтеза нуклеиновых кислот и белков Нуклеиновые кислоты - высокомолекулярные соединения со строго определённой линейной последовательностью мономеров. Структура ДНК и РНК - способ записи информации, обеспечивающий формирование в организме двух информационных потоков. Один из потоков осуществляет воспроизведение информации, заключённой в молекулах ДНК. Информация, содержащаяся в клеточном ядре в ДНК представляет собой генотип. ДНК, содержащаяся в одном наборе хромосом называется геномом. Функциональные отрезки ДНК называют генами. В ДНК различают участки с различными функциями: 1. Структурные гены, в которых закодирована информация о синтезе ферментов и структурных белков. 2. Гены с информацией для синтеза т-РНК. 3. Гены с информацией для синтеза р-РНК. 4. Специфические регуляторные участки - промоторы и операторы. 5. Разделяющие участки между генами - спейсеры. 6. Участки с неизвестной функцией. Предпосылкой для сохранения имеющейся наследственной информации в ряду последовательных поколений клеток и организмов является идентичное удвоение молекул ДНК или репликация генетического материала. В результате репликации и последующего деления дочерние клетки наследуют геном родительской клетки, в котором содержится полный набор генов, отражающих строение РНК и всех белков организма. Второй поток информации реализуется в процессе жизнедеятельности клетки. В этом случае происходит "считывание", или транскрипция, генов в форме полинуклеотидных последовательностей м-РНК и использование их в качестве матриц для синтеза соответствующих белков. В последнем случае осуществляется "перевод" (трансляция) информации, заключённой в м-РНК, на "язык" аминокислот. Он характерен для всех живых организмов, за исключением некоторых РНК-содержащих вирусов. Матричная природа синтеза нуклеиновых кислот и белков обеспечивает высокую точность воспроизведения информации. Так, в ходе репликации дочерние молекулы ДНК синтезируются на нитях материнской ДНК. При образовании всех видов РНК, необходимых для синтеза белков, информация об их структуре "считывается" с определённых генов в молекулах ДНК. В синтезе новых молекул белков матрицей, содержащей информацию об их строении, являются м-РНК. Исправление ошибок, возникающих в структуре ДНК под воздействием факторов внешней и внутренней среды, осуществляет ещё один матричный синтез - репарация. Он является вариантом ограниченной репликации и восстанавливает первоначальную структуру ДНК, используя в качестве матрицы участок неповреждённой нити ДНК. Реализацию потока информации в клетке можно представить схемой ДНК-"РНК-"белок. ДНК-"РНК обозначает биосинтез молекул РНК (транскрипцию); РНК-"белок означает биосинтез полипептидных цепей (трансляцию). 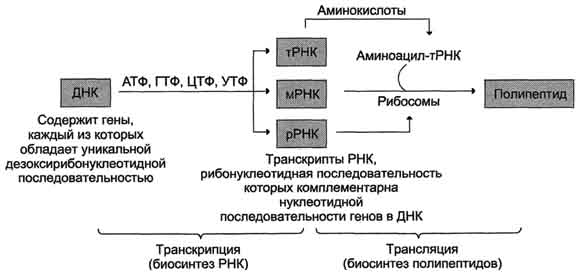 Схема реализации генетической информации Репликация Живые организмы в течение фазы клеточного цикла, предшествующей делению клетки, удваивают содержание ДНК таким образом, что каждая дочерняя клетка после деления получает набор хромосом, идентичный родительской клетке. Процесс удвоения хромосом называют репликацией (редупликацией). Хромосома содержит одну непрерывную двухцепочечную молекулу ДНК. При репликации каждая цепь родительской двухцепочечной ДНК служит матрицей для синтеза новой комплементарной цепи. Вновь образованная двойная спираль имеет одну исходную (родительскую) и одну вновь синтезированную (дочернюю) цепь. Такой механизм удвоения ДНК получил название "полуконсервативная репликация". Первичная структура дочерней цепи определяется первичной структурой родительской цепи, потому что в основе её образования лежит принцип комплементарности оснований (G ≡ С и А = Т). 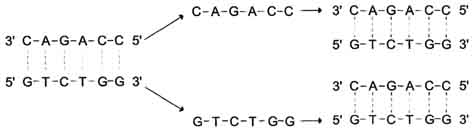 Полуконсервативная репликация Ферменты и белки, участвующие в репликации, должны работать быстро и точно. Эти условия выполняются с помощью особого мультиферментного комплекса. Репликацию можно разделить на 4 этапа: образование репликативной вилки (инициация), синтез новых цепей (элонгация), исключение праймеров, завершение синтеза двух дочерних цепей ДНК (терминация). Инициация репликации Инициацию репликации регулируют специфические сигнальные белковые молекулы - факторы роста. Факторы роста связываются рецепторами мембран клеток, которые передают сигнал, побуждающий клетку к началу репликации. Синтез новых одноцепочечных молекул ДНК может произойти только при расхождении родительских цепей. В определённом сайте (точка начала репликации) происходит локальная денатурация ДНК, цепи расходятся и образуются две репликативные вилки, движущиеся в противоположных направлениях. В образовании репликативной вилки принимает участие ряд белков и ферментов: - ДНК-топоизомеразы (разрывают фосфоэфирную связь в одной из цепей двойной спирали ) - ДНК-хеликазы (разрывают водородные связи в двухцепочечной молекуле ДНК). В результате происходит раскручивание участка суперспирализованной молекулы ДНК. Элонгация Репликация ДНК осуществляется ДНК-зависимыми ДНК-полимеразами. Субстратами и источниками энергии для синтеза продукта служат 4 макроэргических соединения - дезоксирибонуклеозидтрифосфаты дАТФ, дГТФ, дЦТФ и дТТФ, для активации которых необходимы ионы магния. Ферменты проявляют каталитическую активность только в присутствии предварительно раскрученной матричной двухцепочечной ДНК. Синтез цепей ДНК происходит в направлении 5'→3' растущей цепи, т.е. очередной нуклеотид присоединяется к свободному 3'-ОН-концу предшествующего нуклеотидного остатка. Синтезируемая цепь всегда антипараллельна матричной цепи. В ходе репликации образуются 2 дочерние цепи, представляющие собой копии матричных цепей. В синтезе эукариотических ДНК принимают участие ДНК-полимеразы. ДНК-полимераза последовательно наращивает цепь, шаг за шагом присоединяя к ней соответствующие дезоксинуклеотиды. Выбор ДНК-полимеразой очередного нуклеотида определяется матрицей. Включение дезоксирибонуклеозидмонофосфатов в растущую цепь ДНК сопровождается гидролизом макроэргических связей соответствующих нуклеозидтрифосфатов и отщеплением пирофосфата (Н4Р2О7). Энергия макроэргических связей расходуется на образование 3',5'-фосфодиэфирной связи между последним нуклеотидом растущей цепи ДНК и присоединяемым нуклеотидом. В каждой репликативной вилке идёт одновременно синтез двух новых (дочерних) цепей. 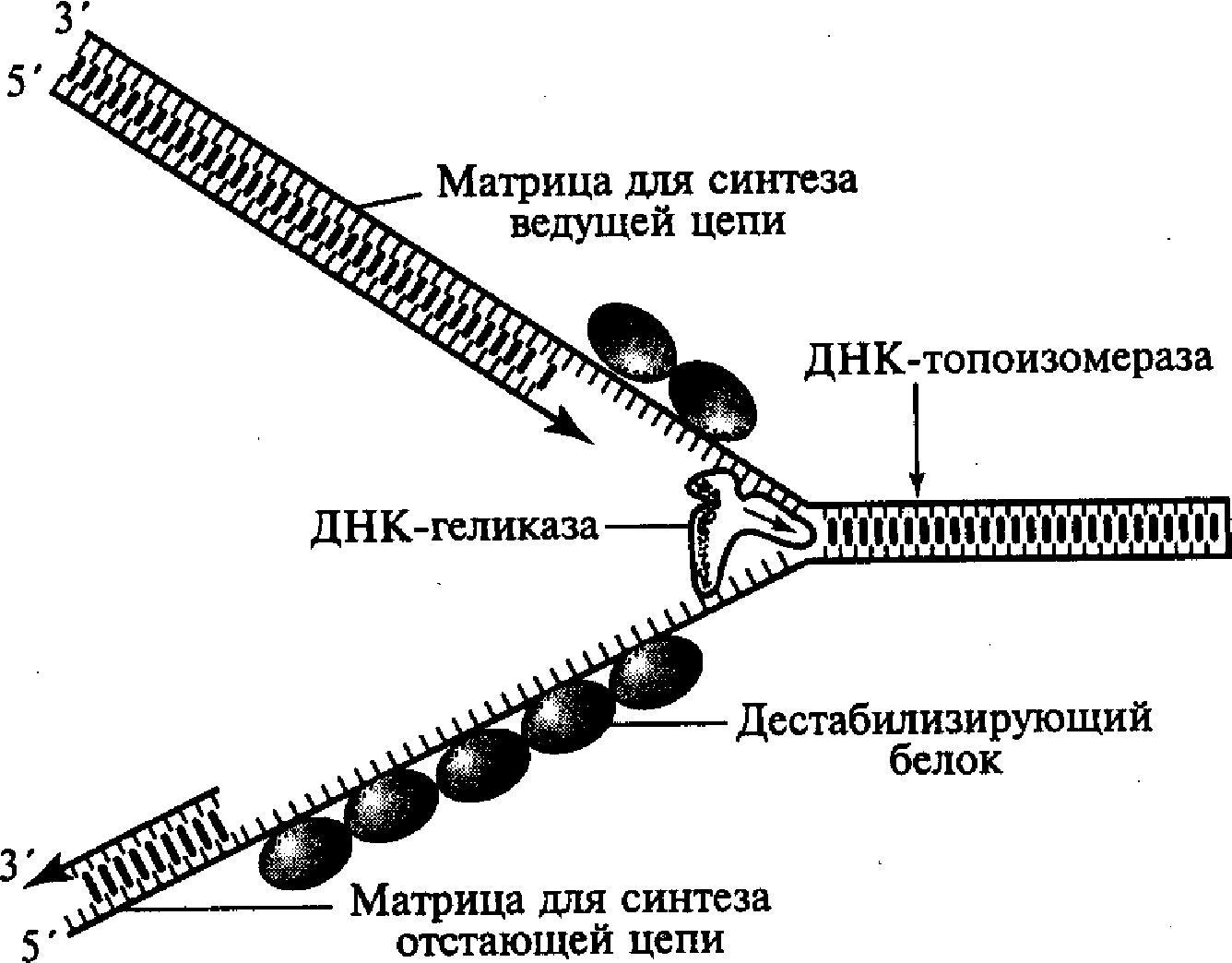 Направление синтеза цепи ДНК совпадает с направлением движения репликативной вилки лишь для одной из вновь синтезируемых цепей (лидирующая цепь). На второй матричной цепи синтез дочерней ДНК осуществляется против движения репликативной вилки. Поэтому вторая цепь синтезируется прерывисто, короткими фрагментами, которые называют "фрагменты Оказаки" (по имени открывшего их исследователя). Дочерняя цепь ДНК, синтез которой происходит фрагментами, называют отстающей цепью. Впоследствии из множества фрагментов Оказаки образуется непрерывная цепь ДНК. Метилирование ДНК После завершения репликации происходит метилирование нуклеотидных остатков вновь образованных цепей ДНК. Наличие метальных групп в цепях ДНК необходимо для формирования структуры хромосом, а также для регуляции транскрипции генов. Репарация Процесс, позволяющий живым организмам восстанавливать повреждения, возникающие в ДНК, называют репарацией. Все репарационные механизмы основаны на том, что ДНК - двухцепочечная молекула, т.е. в клетке есть 2 копии генетической информации. Если нуклеотидная последовательность одной из двух цепей оказывается повреждённой (изменённой), информацию можно восстановить, так как вторая (комплементарная) цепь сохранена. Процесс репарации происходит в несколько этапов. На первом этапе выявляется нарушение комплементарности цепей ДНК. В ходе второго этапа некомплементарный нуклеотид или только основание устраняется, на третьем и четвёртом этапах идёт восстановление целостности цепи по принципу комплементарности. Однако в зависимости от типа повреждения количество этапов и ферментов, участвующих в его устранении, может быть разным. Очень редко происходят повреждения, затрагивающие обе цепи ДНК, т.е. нарушения структуры нуклеотидов комплементарной пары. Такие повреждения в половых клетках не репарируются. Спонтанные повреждения Нарушения комплементарности цепей ДНК могут происходить спонтанно, т.е. без участия каких-либо повреждающих факторов, например в результате ошибок репликации, дезаминирования нуклеотидов, депуринизации. - Ошибки репликации Точность репликации ДНК очень велика, но примерно один раз на 105-106 нуклеотидных остатков происходят ошибки спаривания, и тогда вместо пары нуклеотидов А-Т, G-С в дочернюю цепь ДНК оказываются включёнными нуклеотиды, некомплементарные нуклеотидам матричной цепи. Однако ДНК-полимеразы способны после присоединения очередного нуклеотида в растущую цепь ДНК делать шаг назад (в направлении от 3'- к 5'- концу) и вырезать последний нуклеотид, если он некомплементарен нуклеотиду в матричной цепи ДНК. Этот процесс исправления ошибок спаривания (или коррекция) иногда не срабатывает, и тогда в ДНК по окончании репликации остаются некомплементарные пары. При неправильном спаривании в первичной структуре дочерней цепи ДНК необычные основания не появляются, нарушена только комплементарность. Система репарации некомплементарных пар должна происходить только на дочерней цепи и производить замену некомплементарных оснований только в ней. - Депуринизация (апуринизация) ДНК каждой клетки человека теряет за сутки около 5000 пуриновых остатков вследствие разрыва N-гликозидной связи между пурином и дезоксирибозой. Тогда в молекуле ДНК на месте этих оснований образуется участок, лишённый азотистых оснований, названный АП-сайтом (AP-site, или апуриновый сайт). Термин "АП-сайт" используют также в тех случаях, когда из ДНК выпадают пиримидиновые основания и образуются апиримидиновые сайты. Этот тип повреждений устраняет фермент ДНК-инсертаза (от англ, insert - вставлять), который может присоединять к дезоксирибозе основание в соответствии с правилом комплементарности. В этом случае нет необходимости разрезать цепь ДНК, вырезать неправильный нуклеотид и репарировать разрыв. - Дезаминирование Реакции дезаминирования цитозина и превращение его в урацил, аденина в гипоксантин, гуанина в ксантин происходят значительно реже, чем депуринизация, и составляют 10 реакций на один геном в сутки. Индуцируемые повреждения Индуцируемые повреждения возникают в ДНК в результате воздействия разнообразных мутагенных факторов как радиационной, так и химической природы. Например, образование димеров пиримидиновых оснований (под действием УФО). Удаление пиримидиновых димеров происходит под действием фотолиазы. Фермент расщепляет вновь образовавшиеся связи между соседними пиримидиновыми основаниями и восстанавливает нативную структуру. Повреждения оснований ДНК химическими мутагенами Азотистые основания в ДНК могут подвергаться разнообразным повреждениям: алкилированию, окислению, восстановлению или связыванию основания с формамидными группировками. Репарация АП-сайта может при участии ДНК-инсертазы, которая присоединяет к дезоксирибозе основание в соответствии с правилом комплементарности, или при участии всего комплекса ферментов, участвующих в репарации: АП-эндонуклеазы, АП-экзонуклеазы, ДНК-полимеразы β и ДНК-лигазы. Дефекты репарационных систем и наследственные болезни Репарация необходима для сохранения нативной структуры генетического материала на протяжении всей жизни организма. Снижение активности ферментов репарационных систем приводит к накоплению повреждений (мутаций) в ДНК. Причиной многих наследственных болезней человека выступает нарушение отдельных этапов процесса репарации. Пигментная ксеродерма: у больных в системе репарации снижена активность ферментов, ответственных за удаление неправильных оснований, "застройку" бреши и другие функции. Дефект репарационной системы проявляется в сверхчувствительности к УФ-свету, что приводит к появлению красных пятен на коже, переходящих в незаживающие коросты и нередко в рак кожи. |
