Сборник всех лекций. Общая характеристика обмена веществ и энергии. Биоэнергетика
 Скачать 3.68 Mb. Скачать 3.68 Mb.
|
ОБЩАЯ ХАРАКТЕРИСТИКА ОБМЕНА ВЕЩЕСТВ И ЭНЕРГИИ. БИОЭНЕРГЕТИКАПлан: Основные понятия метаболической биохимии: обмен веществ и энергии, метаболизм, метаболические пути, катаболизм и анаболизм. Взаимосвязь обмена веществ и энергии. Экзергонические, эндергонические реакции и их сопряжение. Макроэргические соединения. Способы образования АТФ. Механизм переноса электронов в биологическом окислении. Хемиоосмотическая теория сопряжения окисления и фосфорилирования. Живые организмы находятся в постоянной связи с окружающей средой. Эта связь осуществляется в процессе обмена веществ и энергии. Обмен веществ и энергии − основа процессов жизнедеятельности ор-ганизма, важнейший специфический признак живой материи. Обмен веществ − это совокупность изменений, которые претерпевают вещества от момента их поступления в пищеварительный тракт до образования конечных продуктов распада. В динамической биохимии наряду с понятием «обмен веществ» используют понятие метаболизм. В общеупотребительном значении (в широком смысле) метаболизм рассматривают как синоним понятия «обмен веществ», включающего процессы различной природы: физиологические (поступление веществ в организм и их выведение); физические (перемещение веществ, сорбцию); химические (химические реакции). Более точно (в узком смысле) под метаболизмом понимать именно химические превращения веществ. Превращения веществ в желудочно-кишечном тракте получили название внешнего обмена. Внутриклеточные химические превращения веществ называют внутренним или промежуточным обменом. Выделяют три этапа обмена веществ: 1) поступление веществ в организм (поступление кислорода в результате дыхания, питание); 2) совокупность биохимических превращений веществ в организме в организме или собственно метаболизм (metabole – превращение, изменение); 3) выделение конечных продуктов из организма. Метаболизм выполняет следующие функции: извлечение энергии из окружающей среды и снабжение ею организма; превращение экзогенных веществ в пластический материал для построения эндогенных веществ; синтез из соответствующих предшественников веществ − компонентов клеток; разрушение биомолекул, выполнивших свои функции. Таким образом, основные функции метаболизма: пластическая и энергетическая. Все живые организмы можно разделить по способности усваивать поступающий из внешней среды углерод на автотрофы и гетеротрофы. Автотрофные организмы могут создавать органические соединения из неорганических веществ, используя дополнительный источник энергии. Для зеленых растений им является солнечный свет, для некоторых бесцветных бактерий − окисление неорганических веществ. Это процессы фотосинтеза и хемосинтеза. К автотрофным организмам относятся растения, бактерии, сине-зеленые водоросли. Гетеротрофные организмы(все животные, в том числе человек, грибы и многие бактерии) должны использовать в качестве источника энергии органические вещества, создаваемые автотрофами. Нам предстоит изучать метаболизм человеческого организма. Обмен веществ неразрывно связан с обменом энергии. Энергия необходима организмам для следующих процессов: преобразования механической работы в мышечное сокращение и другие формы клеточных движений, которые требуют притока энергии; активного транспорта молекул и ионов, поддержания трансмембранных градиентов (Na/K-насоса др.), проведения нервного импульса; синтеза биомолекул из более простых веществ. Одновременно в одной клетке организма человека и животных может протекать около 2000 химических реакций. Особенности метаболических превращений: это ферментативные процессы (ферменты характеризуются высокой эффективностью и специфичностью, что важно для регулирования протекания реакций); протекают, как правило, в несколько стадий. Что произошло бы в организме человека, если, например, окисление глюкозы в нем происходило бы в одну стадию? Если окисление глюкозы в организме происходило бы в одну стадию, это привело бы к гибели организма от избытка выделившейся энергии (при окислении 1 моль глюкозы в одну стадию выделяется огромное количество энергии - 2888 кДж). Окисление углеводов, как и других веществ в организме происходит через ряд промежуточных стадий. На каждой из них выделяется незначительное количество энергии, большая часть которой превращается в работу, и лишь малая часть расходуется на поддержание постоянной температуры тела. Взаимосвязанные, последовательные химические превращения в организме называют метаболическими путями. Различают следующие разновидности метаболических путей: линейные (гликолиз, глюконеогенез или распад и синтез глюкозы); разветвлённые (синтез и распад жиров, фосфолипидов, холестерола); циклические (цитратный, орнитиновый цикл). Метаболические превращения разделяют на анаболические и катаболические. Анаболические процессы (ассимиляция) - биосинтез макромолекул из более простых предшественников, сопровождающийся затратами энергии. Синтез часто включает восстановительные этапы. Катаболические процессы (диссимиляция) - распад биомолекул, обычно связанный с окислением и сопровождающийся высвобождением энергии. В организме взрослого здорового человека реакции анаболизма и катаболизма находятся в состоянии динамического равновесия. Рост, развитие организма, состояние беременности, переедание обычно характеризуются относительным преобладанием анаболических реакций. Физические нагрузки, психоэмоциональные стрессорные реакции, а также старческий возраст, определенные заболевания приводят к преобладанию катаболических реакций. В целом на интенсивность метаболизма влияют различные факторы: совершение мышечной работы, употребление пищи, рост, масса, пол, эмоциональное состояние, возраст, секреция гормонов. При обмене различных групп соединений протекают сходные типы реакций, их назвали центральными путями обмена, они связывают между собой катаболические и анаболические пути. Образующиеся метаболиты называют ключевыми, так через них осуществляются взаимосвязь метаболических превращений веществ. Выделяют три основных этапа катаболизма, когда из белков, углеводов, липидов образуются структурные блоки для реакций биосинтеза и происходит генерация АТФ (или других макроэргических соединений). На 1-ом этапе питательные вещества под действием ферментов пищеварительного тракта расщепляются (гидролизуются) до более простых: белки – до аминокислот, жиры – до глицерола и жирных кислот, сложные углеводы – до моносахаридов, затем они всасываются в кровь и лимфу и переносятся в клетки. Высвобождающаяся энергия невелика, она трансформируется преимущественно в тепловую, образования АТФ не происходит. На 2-ом этапе происходят превращения вышеуказанных веществ с образованием ключевых метаболитов – пировиноградной кислоты (пирувата), ацетил-коэнзима А (активированной формы уксусной кислоты); при этом образуется небольшое количество АТФ. На 3-ем этапе ацетил-КоА подвергается окислению в аэробных условиях в цикле лимонной кислоты (цикле ди- и трикарбоновых кислот) с образованием углекислого газа и воды (называют ещё тканевым дыханием). Цикл трикарбоновых кислот играет центральную роль в генерации АТФ. Это основной амфиболический путь (двойственный: как катаболический, так и анаболический), обеспечивающий, с одной стороны, распад органических веществ, с другой стороны, метаболиты этого цикла используются для биосинтеза. Таким образом, пластические и энергетические процессы в организме тесно взаимосвязаны. Изучением превращений энергии, сопровождающих химические реакции, занимается биоэнергетика или биохимическая термодинамика. В классической термодинамике основополагающими являются представления об изолированной системе и устанавливающемся в ней равновесном состоянии. Биоэнергетика имеет дело с живыми организмами, являющимися примером открытых систем, и здесь вводят представление о стационарном состоянии открытой системы. Для него характерно постоянство параметров системы, неизменность во времени скоростей притока и удаления веществ и энергии. Открытая система в стационарном состоянии во многом сходна с системой, находящейся в термодинамическом равновесии. Для них наблюдается неизменность свойств системы во времени. Это сходство подчеркивается еще и тем, что к стационарным открытым системам, так же как и к равновесным, приложим принцип Ле Шателье. Если в стационарной системе изменить какой-либо из параметров, определяющих ее постоянство (температуру, давление, энтропию, энергию Гиббса и т. д.), то в системе возникают процессы, способствующие уменьшению произведенного воздействия точно так же, как это наблюдается в случае равновесной термодинамической системы. Но между этими типами систем имеются и существенные различия (табл.):
Стационарное состояние живого организма характеризуется тем, что производство энтропии, связанное с процессами усвоения пищи, компенсируется отдачей ее в окружающую среду, а убыль свободной энергии (в связи с протеканием необратимых процессов) восполняется за счет поступления энергии из окружающей среды (главным образом с пищевыми продуктами): S = const, G = const. В процессе усвоения пищи происходит деструкция высокомолекулярных соединений и превращение их в низкомолекулярные, что связано с возрастанием энтропии. Этому процессу противопоставлен синтез в организме высокоэргических (макроэргических) веществ типа АТФ, фосфокреатина, фосфоенолпировиноградной кислоты и др. Эти вещества отличаются сложной структурой многоатомных молекул, низкими значениями энтропии и значительными запасами свободной энергии в весьма подвижной форме. Синтез в живом организме макроэргических веществ с непрочными связями и с большим запасом химической энергии в легко мобилизуемом виде является универсальной формой аккумулирования свободной энергии во всем живом мире. Доля энергии, аккумулирующаяся организмом в виде АТФ и других макроэргических веществ, достигает 60% от калорийности потребляемой пищи. Итак, с точки зрения термодинамики, наиболее существенным свойством живых организмов является устойчивая термодинамическая неравновесность и способность поддерживать ее на определенном уровне. В биологических системах термодинамически невыгодные (ΔG>0) (эндергонические) реакции могут протекать лишь за счёт энергии экзергонических реакций (ΔG<0). Такие реакции называют энергетически сопряжёнными. Многие из этих реакций происходят при участии аденозинтрифосфата (АТФ), играющего роль сопрягающего фактора и основного носителя свободной энергии в организме. В качестве примера сопряжения биохимических реакций рассмотрим фосфорилирование глюкозы; именно в виде фосфорного эфира глюкоза вступает в различные реакции, при фосфорилировании происходит её активация. Реакция фосфорилирования глюкозы свободным фосфатом с образованием глюкозо-6-фосфата является эндергонической: Глюкоза + Н3РО4 → Глюкозо-6-фосфат + Н2О (1) (ΔG = +13,8 кДж/моль) Для протекания такой реакции необходимо её сопряжение с экзергонической реакцией: АТФ → АДФ + Н3РО4 (2) (ΔG = -30,5 кДж/моль) При сопряжении процессов (1) и (2) фосфорилирование глюкозы протекает в физиологических условиях; равновесие реакции сдвинуто вправо, и она практически необратима: Глюкоза + АТФ → Глюкозо-6-фосфат + АДФ (3) (ΔG = -16,7 кДж/моль) В биоэнергетике выделяют 2 основных процесса: химическая энергия запасается посредством образования АТФ, сопряжённого с экзергоническими катаболическими реакциями окисления органических субстратов; химическая энергия утилизируется путём расщепления (гидролиза) АТФ, сопряжённого с эндергоническими анаболическими реакциями и другими процессами, требующими затраты энергии. Т 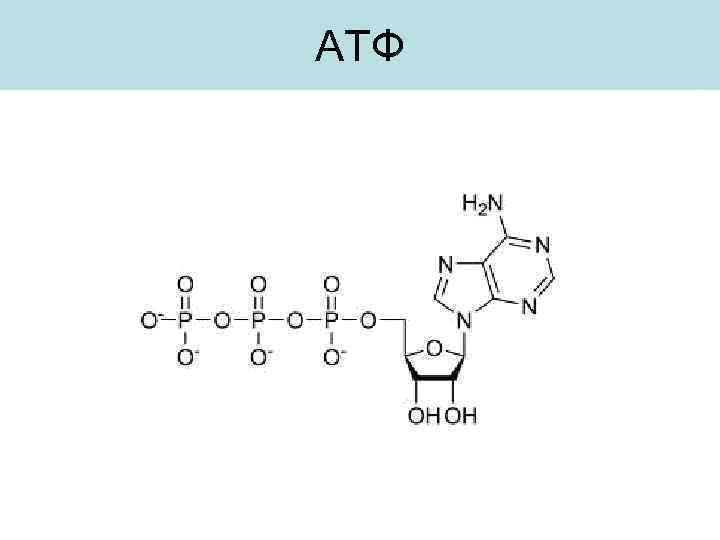 аким, образом, главная роль в биоэнергетике принадлежит АТФ. Как объяснить с позиций строения АТФ: почему именно это соединение выполняет такие важные энергетические функции? аким, образом, главная роль в биоэнергетике принадлежит АТФ. Как объяснить с позиций строения АТФ: почему именно это соединение выполняет такие важные энергетические функции?Структура АТФ АТФ представляет собой термодинамически нестойкое соединение. Причины нестабильности АТФ: – отталкивание одноимённых отрицательных зарядов, возникающих при диссоциации (в физиологических условиях, при рН=7, АТФ представляет собой тетразарядный ион), – конкурентный резонанс – конкуренция атомов фосфора за неподелённые электроны атомов кислорода. Физико-химические напряжения компенсируются наличием достаточно большого количества энергии, заключённой в фосфоангидридных связях, это определяет возможность существования АТФ. Связи, по которым при гидролизе изменение свободной энергии системы составляет 30кДж/моль, называют макроэргическими. К группе высокоэнергетических (макроэргических) веществ, помимо АТФ, относят другие нуклеотиды, аналоги АТФ: гуанозинтрифосфат (ГТФ), уридинтрифосфат (УТФ) и цитидинтрифосфат (ЦТФ), а также фосфоенолпируват, 1,3-дифосфоглицерат, некоторые тиоэфиры, например ацил-КоА. Они, как и АТФ, выступают в роли доноров энергии в эндергонических реакциях анаболических процессов, но для их образования необходима энергия фосфорноэфирной связи АТФ, поэтому именно АТФ является универсальной «энергетической валютой». Синтез АТФ Интенсивность использования АТФ в организме очень велика. В клетке молекула АТФ расходуется в течение одной минуты после её образования. У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 ч. Человек за 24 часа образуется и расходует 40-60 кг АТФ, то есть массу АТФ, примерно равную массе тела. Использование АТФ как источника энергии возможно только при условии непрерывного синтеза АТФ из АДФ: при окислении органических веществ у хемотрофов или при утилизации света у фототрофов. Цикл АТФ - АДФ представляет основной механизм обмена энергии в биологических системах. Синтез АТФ осуществляется двумя основными способами: - субстратное фосфорилирование происходит в цитоплазме, в результате ОВР образуются богатые энергией нестабильные молекулы, фосфатная группа которых переносится на АДФ. Так, АТФ может образоваться за счёт переноса фосфатного остатка от таких высокоэнергетических фосфатов, как, например, фосфоенолпируват или 1,3-дифосфоглицерат. Посредством реакций субстратного фосфорилирования образуется сравнительно небольшое количество АТФ. Главная масса АТФ у аэробных организмов синтезируется путем окислительного фосфорилирования. - окислительное фосфорилирование происходит на мембране митохондрий, где локализована цепь молекул-переносчиков водорода и электронов, участвует дыхательная цепь ферментов или электронотранспортная цепь. Наряду с процессами окисления, сопряженными с образованием АТФ, в организме протекают процессы свободного окисления, при котором высвобождающаяся энергия переходит в тепловую и рассеивается. По типу свободного окисления идут оксигеназные реакции, окислительные реакции, ускоряемые пероксидазами или сопровождающиеся образованием Н2О2, многие реакции, катализируемые оксидазами. Свободное окисление обеспечивает поддержание температуры тела на более высоком энергетическом уровне, чем температура окружающей среды, используется для обезвреживания ксенобиотиков. Протекающие в организме процессы окисления получили название биологического окисления, а их главная функция − обеспечение энергетических потребностей. В развитие концепций биологического окисления важнейший вклад внесли А.Н. Бах, Г. Кребс, О. Варбург, В.А. Энгельгардт, В.И. Палладин, С.Е. Северин, В.П. Скулачев. Окисление субстратов в биологических системах характеризуется отщеплением электронов от субстратов (доноров электронов), которые при участии промежуточных переносчиков передаются на кислород – конечный акцептор электронов у аэробных организмов. Энергия освобождается в процессе ферментативного окисления метаболитов специфическими дегидрогеназами. В реакциях дегидрирования электроны и протоны переходят от органических субстратов на коферменты никотинамид- и флавинзависимых дегидрогеназ. Электроны, обладающие высоким энергетическим потенциалом, передаются от восстановленных коферментов к кислороду через цепь переносчиков, локализованных во внутренней мембране митохондрий. Восстановление молекулы О2 происходит в результате переноса 4 электронов. При каждом присоединении к атому кислорода 2-ух электронов, поступающих к нему по цепи переносчиков, из матрикса поглощаются 2 протона, в результате чего образуется молекула Н2О. Окисление органических веществ в клетках, сопровождающееся потреблением кислорода и синтезом воды, называют тканевым дыханием, а цепь переноса электронов (ЦПЭ) - дыхательной или электронотранспортной цепью. Электронотранспортная цепь – это система окислительно-восстановительных ферментов, встроенных во внутреннюю мембрану митохондрий. Ферменты и коферменты, участвующие в окислительно-восстановительных реакциях Первичные акцепторы водорода окислительно-восстановительных реакций относят к 2 типам дегидрогеназ: никотинамидзависимым, содержащим в качестве коферментов производные никотиновой кислоты, и флавинзависимым, содержащим производные рибофлавина. Никотинамидзависимые дегидрогеназы содержат в качестве коферментов NAD+ (НАД+) или NADP+ (НАДФ+) − производные витамина PP: 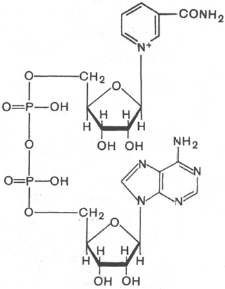 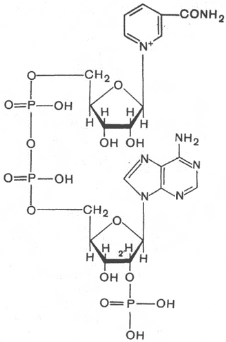 Никотинамидадениндинуклеотид Никотинамидадениндинуклеотидфосфат (НАД+) (НАДФ+) Эти коферменты входят в состав активных центров дегидрогеназ, но могут обратимо диссоциировать из комплекса с апоферментами и включаются в состав фермента в ходе реакции. Субстраты НАД - и НАДФ-зависимых дегидрогеназ находятся в матриксе митохондрий и в цитозоле. Рабочей частью никотинамидных коферментов служит никотинамид: 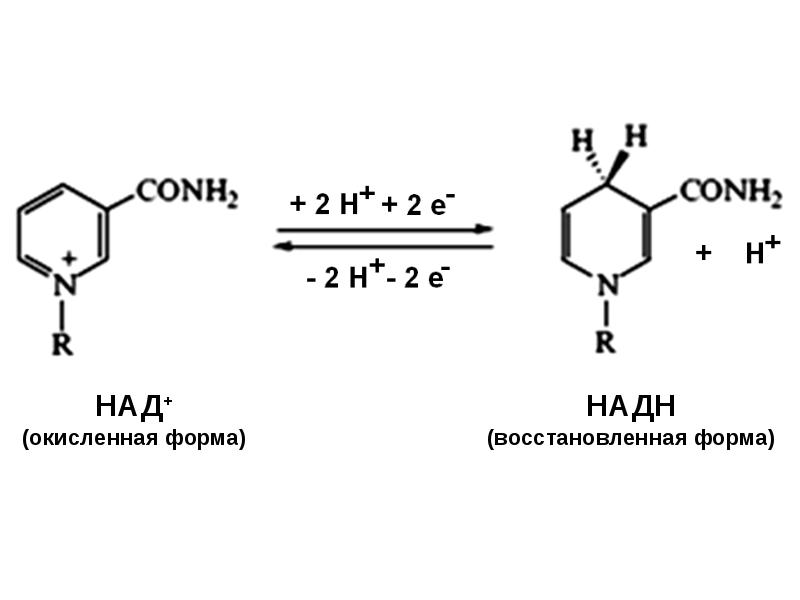 Окисленная форма Восстановленная форма Большинство дегидрогеназ, поставляющих электроны в ЦПЭ, содержат НАД+. НАД+, присоединяя протоны и электроны от различных субстратов, служит главным акцептором энергии окисляемых веществ и главным источником электронов с высоким энергетическим потенциалом для ЦПЭ. НАДФH не является непосредственным донором электронов в ЦПЭ, а используется почти исключительно в восстановительных биосинтезах. Однако возможно включение электронов с НАДФH в ЦПЭ. Большинство ФАД-зависимых дегидрогеназ - растворимые белки, локализованные в матриксе митохондрий. Флавиновые коферменты прочно связаны с апоферментами. Флавиновые дегидрогеназы содержат в качестве коферментов FAD (ФАД) или FMN(ФМН). Эти коферменты образуются в организме человека из витамина В2. Рабочей частью FAD и FMN служит изоаллоксазиновая сопряжённая циклическая система: 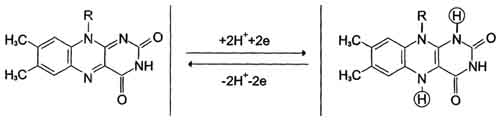 Окисленная форма Восстановленная форма ФАД служит акцептором электронов от многих субстратов в реакциях типа: R-CH2-CH2-R1 + ФАД ↔ R-CH=CH-R1 + ФАДH2, Цепь переноса электронов (ЦПЭ) от НAДH и ФАДH2 на кислород включает большое число переносчиков, которые локализованы во внутренней мембране митохондрий. Убихинон (коэнзим Q или KoQ, Q10) получил такое название из-за повсеместной (ubiquitous) распространённости в природеи принадлежностик хинонам − является производным бензохинона с длинной боковой цепью из 10 изопреноидных единиц: 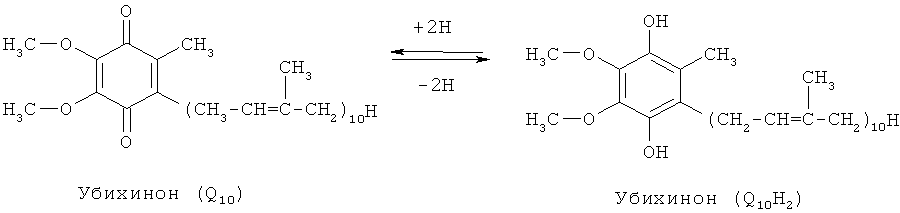 Окисленная форма KoQ Восстановленная форма KoQ∙Н2 Убихинон является промежуточным переносчиком водородных атомов (электронов и протонов) в митохондриальной мембране, он окисляет восстановленную форму флавиновых ферментов. Белки ЦПЭ За исключением убихинона, все компоненты ЦПЭ - белки. В составе этих белков содержатся различные небелковые компоненты: FMN, железо в составе железо-серных белков и в составе порфириновых колец, ионы меди. Цитохромы представляют собой гемопротеины. Различают до 30 цитохромов (группы a, b, cи т.д.). Их функция заключается в переносе электронов за счёт обратимой окислительно-восстановительной реакции с участием железа гема: 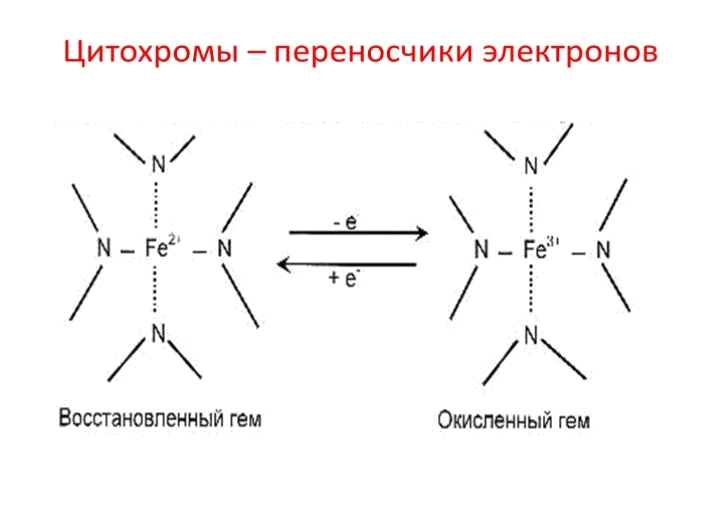 Восстановленная форма Окисленная форма гема гема Цитохромы переносят электроны от убихинона к кислороду, причём комплекс цитохромов, образующий цитохромоксидазу, является терминальным дыхательным ферментом, непосредственно взаимодействующим с кислородом. Железосерные белки содержат железо, связанное с сульфид-ионами или с серой цистеиновых остатков. Они выполняют роль простетической группы в переносе электронов. Большинство компонентов ЦПЭ занимают фиксированное положение в мембране митохондрий; только убихинон и цитохром с являются мобильными компонентами, осуществляя связь с другими компонентами. Компоненты дыхательной цепи встроены в митохондриальную мембрану в виде 4 белково-липидных комплексов:
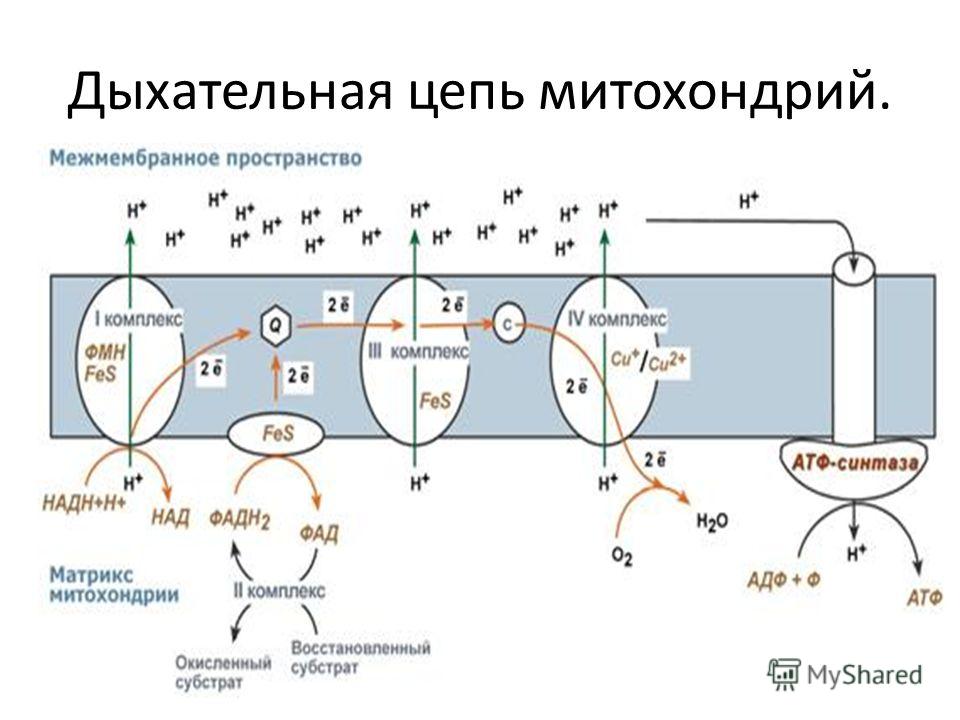 Электроны входят в электронотранспортную цепь при окислении НАДН (через комплекс I) или при окислении сукцината (через комплекс II). Убихинон переносит электроны от комплексов I и II к комплексу III. Цитохром с переносит электроны от комплекса III к комплексу IY. От цитохромоксидазы электроны поступают на кислород, который связывает протоны и восстанавливается с образованием воды. Направление потока электронов при сопряжении одной редокс-системы с другой определяется их стандартными окислительно-восстановительными потенциалами.  Расчёт изменения энергии Гиббса в реакциях переноса электронов: ∆G° = - nF∆E° При переносе пары электронов от NADH∙H+ к кислороду: ∆G° = -2 ∙ 96,556 ∙ (0,82 – (– 0,32)) = 220,2 кДж Механизм сопряжения окисления и фосфорилирования Так как электроны всегда стремятся переходить от электроотрицательных систем к электроположительным, их транспорт по ЦПЭ к кислороду сопровождается снижением свободной энергии. Это позволяет обеспечить энергией синтез АТФ, так как количество выделяющейся свободной энергии приблизительно равно энергии, необходимой для синтеза АТФ из АДФ и фосфата. Экспериментально было подтверждено, что процесс переноса электронов по ЦПЭ и синтез АТФ энергетически сопряжены ( В.А. Энгельгардт, А. Ленинджер, П. Митчелл, С.Е. Северин). Первый процесс − перенос электронов от восстановленных коферментов NADH и FADH2 через ЦПЭ на кислород – экзергонический: NADH + Н+ +1/2 O2 → NAD+ + H2O + 52 ккал/моль(≈220 кДж/моль). Второй процесс − фосфорилирование АДФ, или синтез АТФ, - эндергонический: АДФ + Н3РО4+7,3 ккал/моль (30,5 кДж/моль) = АТФ + Н2О Синтез АТФ из АДФ и Н3РО4 за счёт энергии переноса электронов по ЦПЭ называют окислительным фосфорилированием. Каким же образом осуществляется сопряжение этих двух процессов? Наиболее обоснованный ответ на этот вопрос даёт хемиосмотическая теория Митчелла, предложенная им в 1961 г. Основные положения были подтверждены и разработаны детально совместными усилиями многих исследователей в последующие годы. Протонный градиент и электрохимический потенциал Перенос электронов по дыхательной цепи от NADH к кислороду сопровождается выкачиванием протонов из матрикса митохондрий через внутреннюю мембрану в межмембранное пространство. На эту работу затрачивается часть энергии электронов, переносимых по ЦПЭ. Протоны, перенесённые из матрикса в межмембранное пространство, не могут вернуться обратно в матрикс, так как внутренняя мембрана непроницаема для протонов. Таким образом, создаётся протонный градиент, при котором концентрация протонов в межмембранном пространстве больше, а рН меньше, чем в матриксе. Кроме того, каждый протон несёт положительный заряд, и вследствие этого появляется разность потенциалов по обе стороны мембраны: отрицательный заряд на внутренней стороне и положительный - на внешней. В совокупности электрический и концентрационный градиенты составляют электрохимический потенциал - источник энергии для синтеза АТФ. Окисление молекулы NADH в ЦПЭ сопровождается образованием 3 молекул АТФ; электронам от FAD-зависимых дегидрогеназ соответствует 2 молекулы АТФ. Дыхательный контроль Механизм регуляции образования и потребления АТФ, основанный на сопряжении окисления и фосфорилирования АДФ, называется дыхательным контролем. Скорость использования АТФ регулирует скорость потока электронов в ЦПЭ. Если АТФ не используется и его концентрация в клетках возрастает, то прекращается и поток электронов к кислороду. С другой стороны, расход АТФ и превращение его в АДФ увеличивает окисление субстратов и поглощение кислорода. Если клетка не расходует АТФ и тормозится электронный перенос в дыхательной цепи, то НАДН не может быть вновь окислен в НАД+. Возникающее в результате высокое соотношение НАДН/НАД+ тормозит цитратный цикл и замедляет тем самым окисление субстратов. |
