ыва. Практикум по ОХТ[155]. Основы химической технологии
 Скачать 5.15 Mb. Скачать 5.15 Mb.
|
280 кДж/моль). Процесс окисления с заметной скоростью для различных катализаторов начинается при определенной температуре - температуре зажигания. Реакция ускоряется в присутствии платины (Еа=70 кДж/моль) при температуре не ниже 25О°С, оксида железа (III) (Еа=150 кДж/моль) при температуре не ниже 55О°С, оксида ванадия (V) при температуре не ниже 400°С (Еа=90 кДж/моль). | ||||||||||||||||||||||||||||||||||||||||||||||
| t, o C | 400 | 440 | 480 | 520 | 560 | 590 | 650 |
| Х*, % | 99.2 | 98.0 | 95.4 | 90.7 | 82.5 | 75.0 | 58.5 |
Платиновый катализатор обладает наибольшей активностью, однако дорог и быстро отравляется ядами (мышьяком, селеном, хлором и др.). Оксид железа (III) - малоактивный катализатор. В настоящее время в производстве серной кислоты применяется только ванадиевый катализатор.
Активными компонентами ванадиевых катализаторов являются сульфо- и пиросульфованадаты калия, которые в условиях проведения реакции находятся в расплавленном состоянии на поверхности кремнеземистого носителя. Формы контактной массы - гранулы, кольца. Рабочий интервал температур 400-600°С. При температурах выше 600°С активность катализатора уменьшается из-за разрушения активного комплекса V2О5∙K2S2O7 и взаимодействия компонентов контактной массы с носителем. При температурах ниже 400°С возможно образование каталитически неактивного соединения - сульфата ванадила VOSO4.
Процесс гетерогенного катализа на пористом катализаторе многостадиен. В общем виде различаются следующие стадии:
1). Перенос газообразных веществ из объема к поверхности катализатора (внешняя диффузия);
2). Диффузия реагирующих веществ внутри пор катализатора (внутренняя диффузия);
3). Адсорбция O2 и SO2 на катализаторе;
4). Химическое взаимодействие исходных веществ с участием катализатора;
. Десорбция SO3 ;
. Диффузия SO3 внутри зерна катализатора к его поверхности (внутренняя диффузия);
7). Отвод продукта реакции в газовую фазу (внешняя диффузия).
Скорость всего процесса определяется скоростью наиболее медленной стадии. В зависимости от выбранных условий скорость образования SO3 определяется скоростью внешней или внутренней диффузии или же скоростью химического взаимодействия.
При промышленных скоростях газового потока и при использовании катализатора с диаметром гранул не более 0.5 см и с размером пор 5*10-5 см процесс окисления оксида серы (IV) протекает в кинетической области.
Г.К. Боресков установил, что скорость окисления SO2 на ванадиевом катализаторе приближенно описывается уравнением
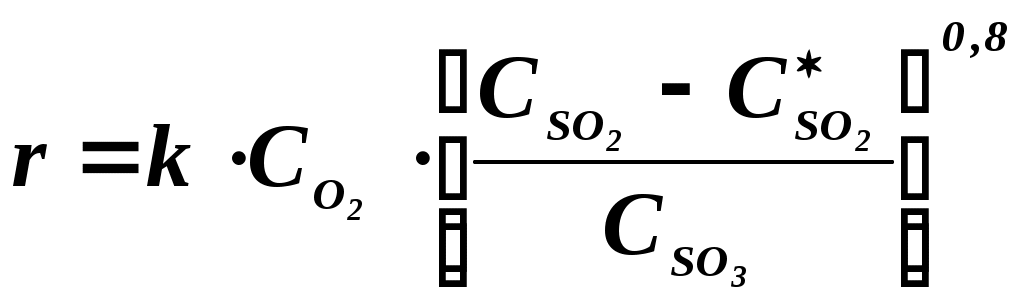 (2.3.1)
(2.3.1)где С - текущие концентрации веществ;
k - константа скорости.
Из уравнения 2.3.1 следует, что скорость реакции зависит от степени приближения к равновесию.
Константа скорости возрастает в пределах температур работы катализатора 400-600°С согласно закону Аррениуса. При изменении температуры с 400 до 500°С она увеличивается в 30 раз, однако при этом наблюдается падение значения движущей силы процесса (
2.3.4. Выбор технологического режима.
Температура.Для получения высокого выхода оксида серы (VI) необходима температура 400-425°С. Однако скорость процесса при этой температуре мала даже при наличии катализатора. Выбор температурного режима, обеспечивающего высокую скорость экзотермической обратимой реакции, довольно сложен, так как изменение температуры противоположным образом влияет на величину равновесного выхода продукта и скорость процесса (рис.2.3.2).
Если вести процесс при постоянной температуре 600°С, то реакция идет быстрее, но, в соответствии с состоянием равновесия, заканчивается при достижении значительно меньшей степени превращения, чем при 400°С. Для обеспечения и высокой интенсивности процесса и высокого выхода, необходимо проводить окисление оксида серы (IV) при меняющемся температурном режиме.
На рис.2.3.3 приведен график зависимости равновесного и практического выхода от температуры при различных временах контактирования. С увеличением времени контактирования максимум на кривых смещается в сторону более низких температур. Кривую, соединяющую максимумы на различных кривых, называют линией оптимальных температур (ЛОТ). При проведении процесса по линии оптимальных температур окисление оксида серы (IV) протекает с максимально возможными скоростями в каждый момент. Понижение температуры к концу процесса с 600 до 400°С позволяет получить высокий выход продукта при достаточной производительности процесса. Схема организации этого процесса приведена на рис.2.3. 4.
Соотношение исходных компонентов. Состав исходной газовой смеси также влияет на величину равновесного выхода и скорость окисления (табл. 2.3.2). Процесс ведут с избытком кислорода относительно стехиометрического. При этом возрастает скорость процесса и увеличивается равновесный выход продукта.
Таблица 2.3.2.
Зависимость равновесного выхода η*
от состава исходной газовой смеси
| Состав газа, % объемн. | Объемное отношение O 2 : SO2 | Равновесный выход η* (при475°С и 0,1 МП а) | |
| О2 | SO2 | ||
| 16,7 13,9 11,0 8,15 5,5 | 3,0 5,0 7,0 9,0 11,0 | 5,57 2,78 1,57 0,9 0,5 | 97,16 96,75 96,07 94,61 92,20 |
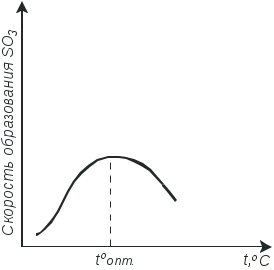
Рис. 2.3.1. Влияние температуры на скорость реакции окисления оксида серы (IV) при постоянном времени контактирования
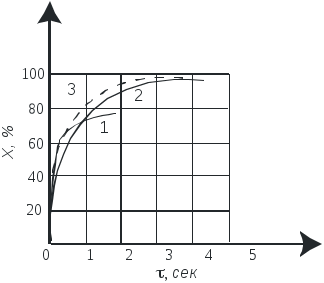
Рис.2.3.2. Изменение степени превращения оксида серы (IV) при различных температурных режимах: 1- 600°С, 2 – 450°С, 3 – 600-400°С
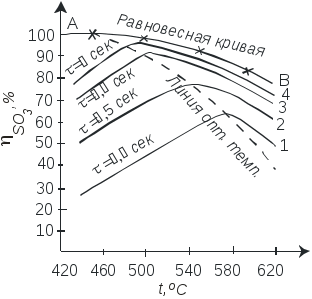
Рис.2.3.3. Зависимость выхода продукта η от температуры при различном времени контактирования.
Обычно газ, поступающий в реакционный аппарат с фильтрующими слоями катализатора, после обжига колчедана содержит 7% SO2, 11% О2 и 82% N2. При таком соотношении О2 и SO2 окисление оксида серы (IV) протекает достаточно полно и автотермично за счет тепла, выделяющегося в ходе окисления, что облегчает создание оптимального температурного режима в первом слое катализатора; при более высокой концентрации SO2 (8-8.5%) перегрев катализатора может вывести его из строя. Дальнейшее увеличение отношения О2 к SO2 путем разбавления газа воздухом при незначительном увеличении выхода приводит к снижению концентрации SO2 в газе и к увеличению объема поступающего на контактирование газа.
Объемное отношение О2 к SO2 может быть увеличено путем разбавления поступающего из обжиговых печей газа воздухом, обогащенным кислородом. Это значительно интенсифицирует процесс, но удорожает и усложняет его.
Давление. В зависимости от выбранной температуры эффективность воздействия давления различна. При низких температурах, когда равновесные степени превращения оксида серы (IV) высокие, давление незначительно сказывается на смещении равновесия, (табл.2.3.3). При высоких температурах, когда окисление происходит далеко не полностью, давление может стать одним из решающих факторов, обеспечивающих высокую степень превращения.
При применении повышенного давления уменьшаются объемы перерабатываемых газов и, следовательно, размеры аппаратов; увеличивается степень превращения и улучшается кинетика процесса; снижается металлоемкость и сокращаются производственные площади; появляется возможность концентрирования энергии и ее утилизации. Все это имеет большое значение для агрегатов большой единичной мощности.
Но применение повышенного давления ведет к усложнению аппаратуры, более высоким энергетическим затратам. Поэтому выбор давления определяется оптимизацией на основе экономических критериев эффективности процесса.
Организация проведения процесса по ЛОТ. Конструкция контактного аппарата должна обеспечивать возможность проведения каталитического окисления оксида серы (IV) в условиях оптимального технологического режима. В данном случае особенно важно обеспечить снижение температуры по высоте слоя в соответствии с линией оптимальных температур (рис.2.3.4).
Таблица 2.3.3.
Зависимость равновесного выхода
| t,°C | Равновесный выход SO3 % при давлении (МПа) | |||||
| 0.1 | 0.5 | 1 | 2.5 | 5,0 | 10,0 | |
| 400 500 600 | 99,2 93,8 73,4 | 99.6 96,9 85,8 | 99,7 97.9 89.5 | 99,9 98,6 93.3 | 99.9 99,0 95,0 | 99.9 99.3 96.4 |
Исходный газ, поступающий в контактный аппарат, нагревают до температуры, несколько превышающей температуру зажигания ванадиевого катализатора (400-440°С) и направляют в первый катализаторный слой. Процесс окисления проводится как в первом слое, так и в последующих, в адиабатическом режиме (без отвода тепла) - прямые 1, 3, 5, 7. При окислении SO2 выделяется тепло, за счет которого повышается температура газовой смеси по линейной зависимости. Угол наклона прямой при этом зависит от концентрации SO2, поскольку с увеличением концентрации SO2 выделяется больше тепла и, следовательно, в большей степени повышается температура. В первом слое (прямая 1) процесс окисления ведут таким образом, чтобы температура газовой смеси на выходе не превышала предельную температуру активности катализатора. Затем, перед поступлением на второй и последующие слои катализатора, газовая смесь охлаждается в промежуточных теплообменниках - кривые 2, 4, 6. 8. Выход при этом остается постоянным. На рис. 2.3.4 видно, что при проведении процесса в неподвижном слое катализатора наблюдается значительное отклонение состояния системы от линии оптимальных температур, которое допускается в промышленности не более чем на 20%.
При проведении процесса в псевдоожиженном слое катализатора скорость теплоотдачи возрастает. Движение в кипящем слое не только потока газов, но и твердых частиц дополнительно способствует выравниванию температуры по всему слою. Это позволяет проводить реакцию в каждом слое при практически постоянной температуре, т.е. при более «правильном» температурном режиме, чем в случае неподвижного слоя. Соответственно и отклонения от линии оптимальных температур меньше.
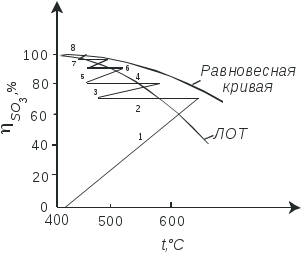
Рис.2.3.4. Диаграмма t-η четырехступенчатого процесса контактирования с промежуточным теплообменом.
Газ, поступая из одного слоя в другой, быстро принимает температуру данного слоя. Избыточное тепло - тепло реакции и физическое тепло поступающего газа - отводится помещенными в слои катализатора теплообменниками. Однако, эти аппараты не нашли широкого применения из-за большого уноса катализатора и запыления газа.
2.3.5.Схема лабораторной установки
Контактное окисление оксида серы (IV) проводят на одноступенчатой установке (рис.2.3.5). Воздух, нагнетаемый воздуходувкой, и оксид серы (IV), подаваемый из газометра, освобождают от водяных паров в промывных склянках 1, заполненных концентрированной серной кислотой. Брызги серной кислоты улавливают стеклянной ватой в склянках 2. Расход оксида серы (IV) и воздуха измеряют реометрами 3 и 4. Газовая смесь заданного состава после смесителя 5 поступает в контактный аппарат 6. Выходящая из контактного аппарата газовая смесь поступает в сосуд 7, в котором улавливается серная кислота, далее в сосуд 8, где оксид серы (VI) абсорбируется серной кислотой, а затем направляется в вытяжной шкаф. Блок анализа состоит из поглотительной склянки Дрекселя 9, которую заполняют титрованным раствором йода, и аспиратора 10.
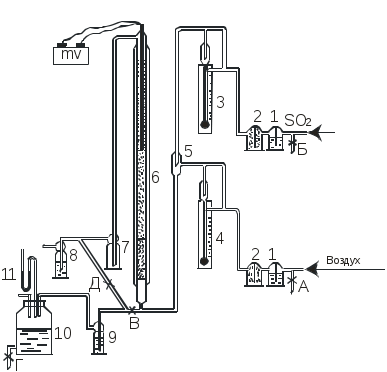
Рис.2.3.5. Схема установки контактного окисления оксида серы (IV) с одноступенчатым контактным аппаратом.
Одноступенчатый контактный аппарат представляет собой кварцевую трубку длиной 800 мм и диаметром 30 мм. Снаружи трубка по всей длине имеет электрообмотку, покрытую теплоизоляцией. Скорость нагревания регулируется ЛАТРом. Внутри контактного аппарата имеется решетка, которая снизу поддерживается кварцевой или фарфоровой трубкой диаметром 22-25 мм. Для лучшего распределения газового потока и его нагревания на сетке помещен слой битого кварца высотой 10 мм. На кварц положен тонкий слой асбестовых волокон, а затем насыпан катализатор. Температура в контактном аппарате определяется по милливольтметру. Датчиком служит термопара, помещенная в кварцевый чехол, впаянный сверху в контактную трубку и доходящий до середины слоя катализатора.

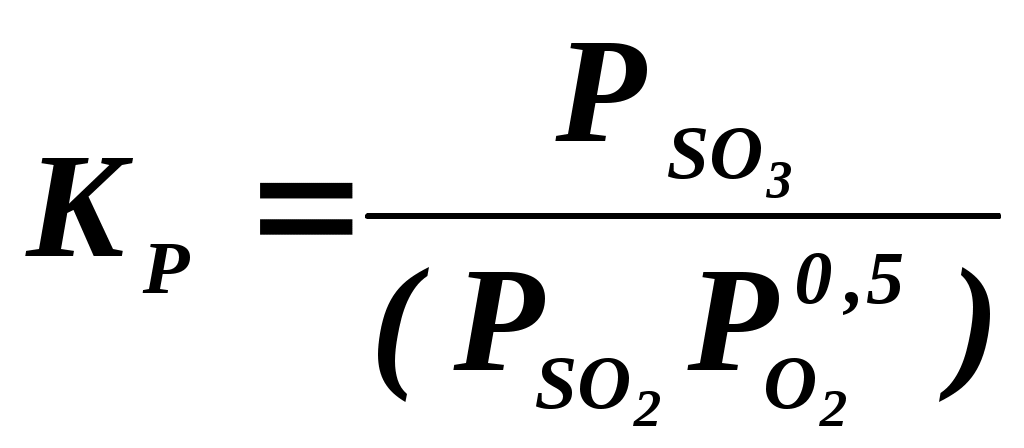 ,
,