Почечные синдромы. Основные клинические синдромы
 Скачать 224 Kb. Скачать 224 Kb.
|
|
НЕФРИТИЧЕСКИЙ СИНДРОМ Острый нефритический синдром Острый нефритический синдром – это совокупность симптомов, напоминающих острый гломерулонефрит. Он характеризуется внезапным возникновением гематурии и протеинурии, признаков азотемии (снижением скорости клубочковой фильтрации, повышением содержания в крови азотистых веществ − мочевины, креатинина и др.), задержкой в организме солей и воды, артериальной гипертензией. Острый нефритический синдром развивается после перенесенных инфекций, таких как стрептококковая инфекция, сепсис, пневмококковая пневмония, брюшной тиф, менингококковая инфекция. Кроме того, острый нефритический синдром может развиться на фоне тяжелых вирусных заболеваний: вирусного гепатита В, инфекционного мононуклеоза, эпидемического паротита, ветряной оспы, инфекций, вызванных вирусами Коксаки и др. После перенесенной инфекции с первичным очагом в верхних дыхательных путях, на коже или в среднем ухе, вызванной β-гемолитическим стрептококком группы А, против антигенов стрептококка вырабатываются антитела. При их взаимодействии образуются патологические иммунные комплексы «антиген – антитело», которые откладываются в стенках капилляров почечных клубочков, активируя систему комплемента, приводя к иммунному воспалению и последующему повреждению ткани почки. При этом происходит инфильтрация клубочков нейтрофилами и моноцитами. Стенки капилляров клубочков становятся истонченными и хрупкими, проницаемыми для белков плазмы крови и эритроцитов. Развитие острого нефритического синдрома наиболее характерно для острого гломерулонефрита. Острый нефритический синдром может развиться и в начале хронического гломерулонефрита, а также впервые возникнуть на фоне давно существующего заболевания почек, иногда приобретая непрерывно рецидивирующий характер. Классическими симптомами острого нефритического синдрома являются гематурия, отеки, артериальная гипертензия и уменьшение выделения мочи (олигурия). Характерно бурное появление или нарастание отеков с типичной бледной одутловатостью лица, сопровождающихся олигурией; протеинурией; гематурией; артериальной гипертензией, особенно диастолической. У трети больных появляется макрогематурия (моча цвета «мясных помоев»). Артериальная гипертензия сопровождается развитием гипертрофии левого желудочка с последующим формированием признаков сердечной недостаточности. Артериальная гипертензия вместе со значительным повышением объема циркулирующей крови является причиной острой левожелудочковой недостаточности (отека легких). Олигоурия и анурия при остром нефритическом синдроме возникают вследствие значительного снижения клубочковой фильтрации. Часто уменьшение объема выделяемой мочи сопровождается жаждой. Непостоянными симптомами острого нефритического синдрома являются повышение температуры тела, анорексия, тошнота, рвота, головная боль, слабость. Возможно появление боли в пояснице и в животе, прибавка массы тела вследствие задержки жидкости в организме. При исследовании общего анализа мочи мочевой осадок содержит большое количество эритроцитов, лейкоцитов, клеток почечных канальцев и цилиндры. Протеинурия достигает 0,5 – 2 г за сутки. В крови обнаруживается увеличение титра антител (антистрептолизина − О, антистрептокиназы, антигиалуронидазы). При проведении ультразвукового исследования размеры почек могут быть не изменены или увеличены. Скорость клубочковой фильтрации снижается. Иммунокомплексный острый нефритический синдром, например при постстрептококковом гломерулонефрите, имеет обычно хороший прогноз при незначительных повреждениях почек и устранении источника антигенной стимуляции. У 1% детей и 10 % взрослых острый нефритический синдром переходит в быстропрогрессирующий гломерулонефрит. Отклонения в анализах мочи (протеинурия и гематурия) обычно выявляют в течение нескольких лет после перенесенного заболевания, а иногда заболевание медленно прогрессирует до ХПН. Лечение. В большинстве случаев специфического лечения нет. Диета № 7а предусматривает ограничение белков, соли (при отеках и артериальной гипертензии). При бактериальной инфекции проводится комплексная антибактериальная терапия. Для снижения объема циркулирующей крови назначаются диуретические средства. Для лечения артериальной гипертензии чаще всего используются ингибиторы АПФ, блокаторы кальциевых каналов и диуретики. При развитии почечной недостаточности рекомендуется проведение гемодиализа и трансплантации почек. Хронический нефритический синдром Хронический нефритический синдром сопровождает заболевания разной этиологии, характеризующиеся диффузным склерозом клубочков почек и приводящие к ХПН. Клинически хронический нефритический синдром проявляется протеинурией, цилиндрурией, гематурией и артериальной гипертензией. Хронический нефритический синдром обычно развивается на фоне очагового или сегментарного склероза почки, мембранозного или мембранозно – пролиферативного гломерулонефрита. При этом синдроме происходит увеличение внеклеточного материала (мезангиального матрикса, базальной мембраны клубочков, спавшихся капиллярных петель), а также отложение иммуноглобулинов в почечных клубочках. Поражение интерстиция почек характеризуется атрофией канальцев и выраженными склеротическими изменениями. Хронический нефритический синдром развивается постепенно и может быть выявлен случайно при медицинском осмотре. Часто у больных субъективные жалобы в начале развития синдрома отсутствуют. При обследовании выявляют рецидивирующие эпизоды протеинурии и гематурии. В более тяжелых случаях могут быть выявлены признаки уремии – тошнота, рвота, одышка, кожный зуд, повышенная утомляемость. В более позднем периоде присоединяются отеки, артериальная гипертензия и азотемия. В общем анализе мочи у больных выявляются протеинурия, гематурия, эритроцитарные и гиалиновые цилиндры. В крови отмечается повышение уровня азота, мочевины и креатинина, анемия, признаки метаболического ацидоза, гиперфосфатемия и другие признаки ХПН. Диагноз подтверждают биопсией почки. Лечение в основномсимптоматическое. Используются диета с ограничением натрия, антигипертензивные препараты. Проводится профилактика и лечение ХПН. ОТЕЧНЫЙ СИНДРОМ Патогенез почечных отеков сложен и складывается из ряда патофизиологических механизмов. Ведущая роль в их образовании принадлежит гипопротеинемии, гипоальбуминемии и диспротеинемии. Однако одними этими факторами патогенез почечных отеков не ограничивается. Вслед за снижением количества белка в крови последовательно включаются и другие механизмы: снижение онкотического давления сыворотки крови, уменьшение объема циркулирующей крови, нарушение сосудистой проницаемости в сторону ее повышения для воды и белков (за счет активации фермента гиалуронидазы, гипокальцемии, гистаминемии, деполимеризации мукополисахаридов межклеточного вещества тканей). Большое значение имеет уменьшение объема циркулирующей крови. Это приводит к возбуждению рецепторов сосудистой стенки и включению компенсаторных механизмов поддержания внутрисосудистого объема с их сложной гормональной регуляцией, в частности, усиленной выработкой в коре надпочечников альдостерона. Развивающийся вторичный альдостеронизм приводит к задержке в организме больных натрия, хлоридов и воды. Это ведет к увеличению секреции антидиуретического гормона, который усугубляет задержку воды за счет усиления ее канальцевой реабсорбции (схема 2). Множественность патогенетических механизмов делает почечные отеки стойкими и распространенными. Они могут развиваться постепенно или же бурно, за одну ночь, достигать степени анасарки. Заметные вначале в области век, лица, поясничной области и половых органов, отеки при прогрессировании почечной патологии распространяются на всю подкожно-жировую клетчатку, растягивая кожу до образования дистензионных стрий. На этой стадии у большинства больных образуются транссудаты в серозных полостях: одно- и Схема 2 ПАТОГЕНЕЗ ПОЧЕЧНЫХ ОТЕКОВ П 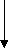 ротеинурия Повышение сосудистой ротеинурия Повышение сосудистойпроницаемости  Г 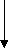  ипоальбуминемия ипоальбуминемияУменьшение коллоидно- о 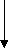 смотического давления смотического давленияТ   ранссудация ранссудация  Уменьшение объема Увеличение секреции Уменьшение объема Увеличение секреции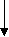  ОЦК АДГ ОЦК АДГУвеличение секреции Задержка воды  альдостерона альдостеронаУменьшение клубочковой  фильтрации Увеличение реабсорбции фильтрации Увеличение реабсорбции натрия натрияОТЕКИ двусторонний гидроторакс, асцит, реже − гидроперикард. Почечные отеки рыхлые и легко перемещаются. При больших отеках бывают видны признаки дистрофии кожи и ее придатков: сухость, шелушение эпидермиса, ломкость и потускнение ногтей, выпадение волос. В период развития асцита состояние больных резко ухудшается: появляются вздутие живота, беспричинные поносы, тошнота и рвота. При нарастании гидроторакса и гидроперикарда появляется одышка при незначительной физической нагрузке и даже в покое. ПОЧЕЧНЫЙ ГИПЕРТОНИЧЕСКИЙ СИНДРОМ Под почечным гипертоническим синдромом понимают артериальную гипертензию, патогенетически связанную с заболеванием почечной паренхимы (гломерулонефрит, пиелонефрит, кистозная почка и др.), почечных артерий (атеросклероз, врожденный стеноз почечной артерии), внутрипочечных сосудов (васкулиты, нефроангиосклероз), гибелью почечной ткани (ХПН), отсутствием почки (ренопривная гипертония) или аномалиями развития почек. Почки играют многообразную роль в регуляции артериального давления, выделяя и сохраняя в организме натрий и воду, являясь местом образования ряда прессорных и депрессорных веществ. Любое заболевание почек может сопровождаться артериальной гипертензией – от легкой, лабильной, до злокачественной. Поэтому почечный гипертонический синдром является одним из ведущих признаков заболевания почек. В начале своего развития почечный гипертонический синдром заметно связан с почечной патологией и может быть частично или полностью обратимым в случае успешного лечения заболевания почек. Если стабильный почечный гипертонический синдром существует более 2 лет, то в дальнейшем его выраженность менее отчетливо связана с течением и лечением почечного заболевания. Повышение артериального давления при болезнях почек обусловлено тремя основными механизмами: задержкой натрия и воды, активацией прессорной системы и снижением функций депрессорной системы (схема 3). Нарушение функции почек чаще всего проявляется снижением клубочковой фильтрации и расстройством канальцевой реабсорбции с уменьшением выделения натрия и воды. Уровень в крови натрия влияет на содержание других ионов – калия, хлоридов, кальция, магния, а также на секрецию ренина, альдостерона и антидиуретического гормона. Задержка натрия и воды приводит к гиперволемии – увеличению объема циркулирующей крови, а также к повышению содержание натрия в сосудистой стенке. Последнее способствует набуханию сосудистой стенки и увеличению ее чувствительности к прессорным влияниям ангиотензина и катехоламинов. Вслед за задержкой натрия происходит накопление кальция в сосудистой стенке с повышением контрактильности сосудистого тонуса, что приводит к повышению общего периферического сопротивления. Этот механизм, наряду с развитием гипергидратации, гиперволемии и повышением сердечного выброса имеет основное значение в развитии артериальной гипертензии при остром гломерулонефрите, ОПН и ХПН. Вторым механизмом, обусловливающим развитие артериальной гипертензии при болезнях почек, является повышение активности ренин − ангиотензин − альдестероновой и симпатико − адреналовой систем. Одной из эндокринных функций почек является выработка ренина юкстагломерулярными клетками, которые представляют собой своеобразный волюморецепторный аппарат, очень тонко реагирующий на изменения гемодинамики почки посредством выделения в кровь ренина. Секреция ренина стимулируется ишемией почки, падением концентрации ионов натрия в крови, β-адреностимуляторами. Повышенная активность ренина играет роль в развитии гипертензии при тех заболеваниях почек, при которых функция их сохранена, но имеется ишемия в области юкстагломерулярного аппарата: при стенозе почечной артерии, ХПН, хроническом гломерулонефрите. В плазме крови ренин реагирует с продуцируемым в печени ангиотензиногеном (α2 – глобулином), образуя малоактивный ангиотензин-1, который под влиянием ангиотензинпревращающего фермента переходит в ангиотензин − 2, являющийся самым сильным вазоконстриктором. Ангиотензин − 2 вызывает системный спазм артериол с повышением общего периферического сопротивления, стимулирует секрецию альдостерона корой надпочечников, увеличивает реабсорбцию натрия в канальцах почек. Посредством связи с симпатическим отделом нервной системы он активизирует выделение катехоламинов надпочечниками. Схема 3 ПАТОГЕНЕЗ ПОЧЕЧНОЙ ГИПЕРТЕНЗИИ Ангиотензиноген Р  енин енин Ангиотензин-1  Ангиотензин-превращающий фермент  А   нгиотензин-2 нгиотензин-2С  пазм артериол пазм артериол Повышение р 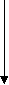 еабсорбции натрия еабсорбции натрияСтимуляция секреции альдостерона Роль активизации симпатико-адреналовой системы в развитии почечной гипертензии связана с повышением образования катехоламинов при феохромоцитоме или их задержкой при нарушении экскреторной функции почек (при ХПН). Участие катехоламинов в происхождении почечной гипертензии при заболеваниях почек опосредовано также вазоконстрикцией, повышением общего периферического сопротивления, а также увеличением сердечного выброса. Альдостерон задерживает в организме натрий, увеличивая его реабсорбцию в собирательных трубочках, и повышает выведение калия. Прессорное действие альдостерона связано с его влиянием на клеточную мембрану с повышением ее проницаемости для натрия. Кроме того, вслед за усилением реабсорбции натрия увеличивается реабсорбция воды. Накопление натрия в стенках сосудов также способствует вазоконстрикции. Повышение концентрации ионов натрия в крови вызывает раздражение осморецепторов и повышенное выделение гипофизом антидиуретического гормона, что еще больше увеличивает реабсорбцию воды в дистальных отделах канальцев. Задержка натрия приводит к повышению чувствительности рецепторов сосудистой стенки к прессорным влияниям. Депрессорная система, противостоящая действию прессорных факторов, включает в себя простагландины и каллекреин − кининовую систему. Простагландины снижают тонус артерий, уменьшают их реакцию на вазопрессорные вещества, являются мощными натрийуретиками и гидроуретиками. Выраженными сосудорасширяющими свойствами обладают и конечные продукты каллекреин − кининовой системы – брадикинин и каллиидин. Поражение почечной паренхимы приводит к снижению активности депрессорных почечных механизмов. Лишь при немногих патологических состояниях можно говорить об одном ведущем механизме развития гипертонического синдрома. У большинства больных с хроническими заболеваниями почек артериальная гипертензия имеет смешанное происхождение. В свою очередь, длительная и стойкая почечная гипертензия, независимо от вызвавших ее причин, способствует развитию склеротических изменений сосудов (артериол) почки с повторным запуском многочисленных патогенетических механизмов почечной гипертензии. Таким образом, формируется своеобразный «порочный круг» с постоянной сменой причинно − следственных отношений. Клиническая характеристика почечного гипертонического синдрома широко варьирует – от лабильной, бессимптомной или малосимптомной гипертензии, до злокачественного гипертонического синдрома. Между характером поражения почек (включая морфологические особенности) и выраженностью почечного гипертонического синдрома нет строгой зависимости. Симптоматика почечного гипертонического синдрома в принципе не отличается от симптоматики любого другого симптоматического гипертонического синдрома и гипертонической болезни. Клиника почечного гипертонического синдрома определяется степенью повышения артериального давления, выраженностью вторичного поражения сердца и сосудов. Больные жалуются на головную боль, ухудшение зрения, боли в области сердца, одышку. При лабильной гипертензии больные предъявляют жалобы на быструю утомляемость, возбудимость, сердцебиение, реже на головную боль. Величина артериального давления не является достаточным критерием оценки тяжести почечного гипертонического синдрома. Правильнее ориентироваться на уровень диастолического, а не систолического артериального давления. Злокачественная почечная гипертензия характеризуется особенно высоким и стойким систолическим и особенно диастолическим давлением, которое приводит к значительному увеличению сердца, изменениям ЭКГ, выраженной ретинопатии (с очагами кровоизлияний, отеком диска зрительного нерва, снижением зрения вплоть до слепоты), гипертонической энцефалопатии, сердечной недостаточности. Гипертрофия левого желудочка, являющаяся признаком длительно существующей почечной артериальной гипертензии, определяется по усиленному, разлитому, резистентному верхушечному толчку, смещению границ относительной сердечной тупости влево и вниз, акценту второго тона на аорте, а также по характерным изменениям на рентгенограмме (увеличение тени левого желудочка, аортальная конфигурация сердца) и на ЭКГ. ЭКГ-признаками гипертрофии левого желудочка являются увеличение амплитуды зубца R, косонисходящая депрессия сегмента ST, низкие или отрицательные зубцы Т в отведениях Ι, V4 – V6. Осложнения почечного гипертонического синдрома такие же, как при гипертонической болезни − сердечная недостаточность, гипертонический криз, острое нарушение мозгового кровообращения, инфаркт миокарда, почечная недостаточность, тяжелая ретинопатия, энцефалопатия. Выраженность симптомов сердечной недостаточности соответствует стойкости и продолжительности почечной артериальной гипертензии. Первоначально у больных развивается левожелудочковая недостаточность – с одышкой, цианозом, приступами сердечной астмы, отеком легких, рентгенологическими и физикальными признаками застоя венозной крови в легких. В дальнейшем развивается застой и по большому кругу кровообращения. Возможно появление пресистолического или протодиастолического ритма галопа, свидетельствующего о нарушении сократительной функции миокарда. Обязательным симптомом является гипертрофия левого желудочка. При остро возникшем почечном гипертоническом синдроме, например, при остром нефрите, ОПН, гипергидратация может вызвать дилатацию сердца и острую сердечную недостаточность, которая является второй по частоте причиной смерти подобных больных после почечной недостаточности при злокачественной почечной гипертензии. Гипертонический криз проявляется острым и значительным подъемом артериального давления. Он может быть спровоцирован обострением заболевания почек, а также, как и при гипертонической болезни, эмоциональной или физической нагрузкой. Клинически гипертонический криз проявляется ухудшением мозговой, сердечной или глазной симптоматики, вплоть до потери зрения, развития острой левожелудочковой недостаточности или острого нарушения мозгового кровообращения. Гипертоническая энцефалопатия, как следствие ишемии и отека мозга, проявляется слабостью, сонливостью, головными болями, ухудшением памяти, снижением интеллекта, депрессией. Частым следствием высокой артериальной гипертензии может быть нарушение мозгового кровообращения с параличами, расстройством чувствительности, нарушением функции тазовых органов, а также инфаркт миокарда. Тяжелый почечный гипертонический синдром ускоряет развитие ХПН у лиц, страдающих заболеванием почек. |
