|
|
Методичка ОХТ. Практикум для студентов специальностей 148 01 01 Химическая технология производства и переработки неорганических материалов
Порядок выполнения работы
Исходя из заданного соотношения реагентов и общего объема реагентов произвести расчет необходимого количества вводимого эфира и щелочи.
Включить кондуктометр и подготовить его к проведению замеров.
Залить в реактор через воронку необходимое количество 0,1 М раствора эфира и включить перемешивание.
Быстро ввести в реактор рассчитанное количество 0,1 раствора NaOH. Начало введения второго реагента считать началом опыта (продолжительность реакции контролируется по секундомеру).
Периодически замерять сопротивление реакционной массы. Четыре-пять первых измерений провести через каждые 30 с, следующие – через 1 мин, затем несколько измерений – через 3 мин. И, наконец, делать измерения через 5 мин, пока изменение значений сопротивления станет незначительным.
После завершения измерений выключить мешалку и кондуктометр, слить из реактора полученную смесь и промыть реактор водой.
6.2.2. Расчет показателей процесса омыления эфира в периодическом реакторе
Начальные концентрации щелочи и эфира в смеси непосредственно в момент их смещения рассчитывают исходя из значений концентраций исходных растворов и соотношения их объемов. Текущая концентрация эфира рассчитывается с учетом его начальной концентрации и количества эфира вступившего в реакцию. Последнее эквивалентно количеству прореагировавшего NaOH, и его можно определить, зная начальную и текущую концентрацию NaOH. Для определения текущей концентрации NaOH в реакционной смеси используются таблицы или калибровочные графики изменения удельного сопротивления раствора в зависимости от концентрации щелочи.
Степень превращения реагентов ХА определяется по формуле
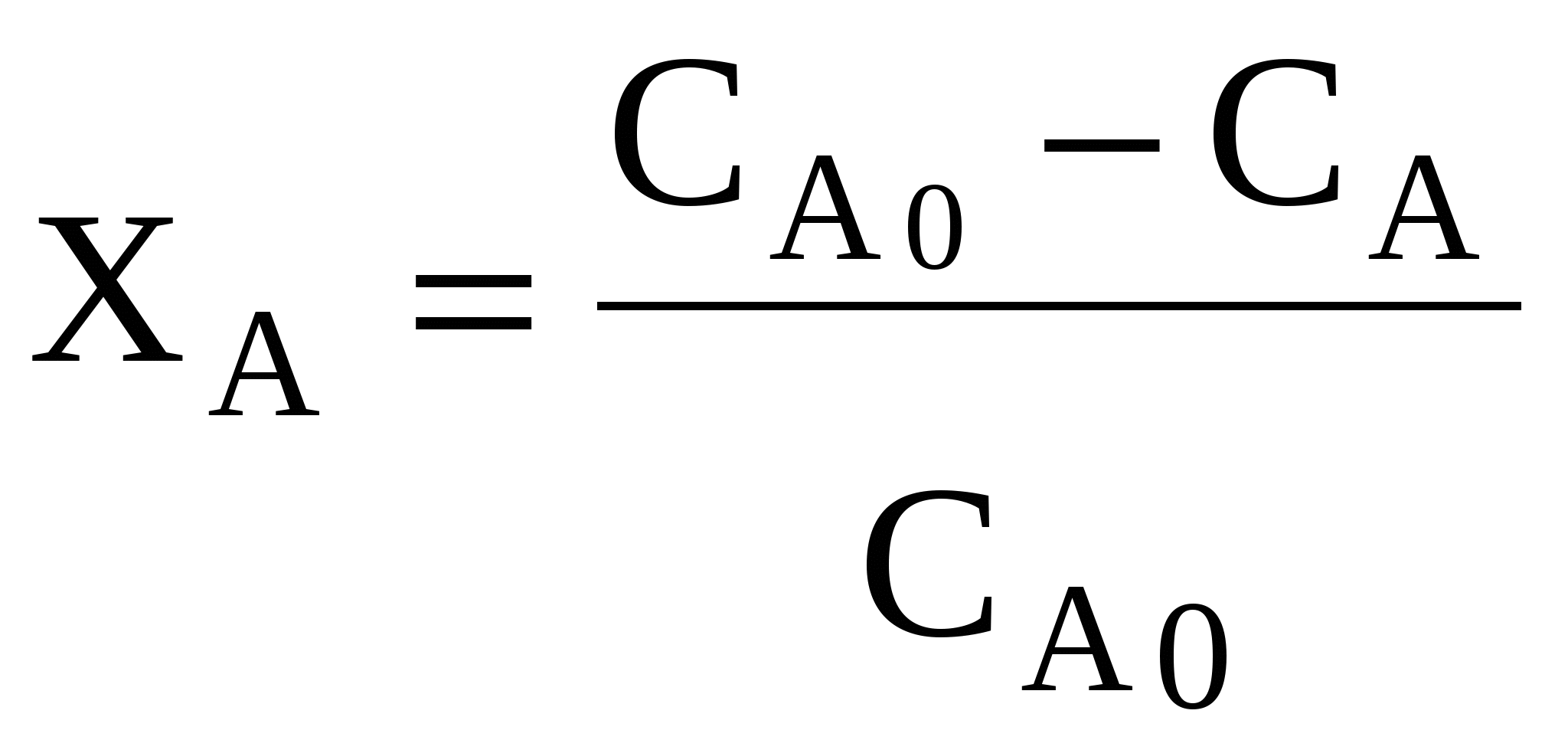 , (83) , (83)
где 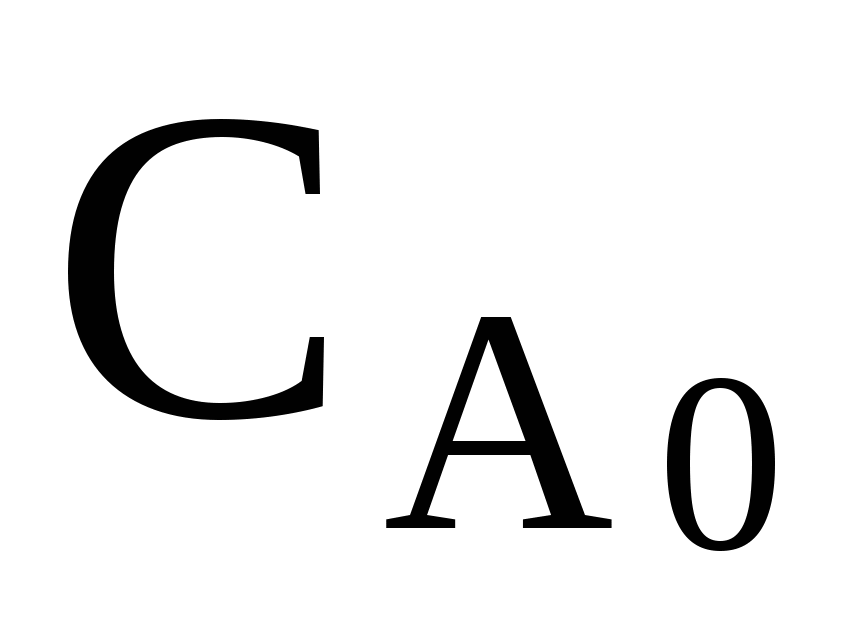 – начальная молярная концентрация реагента в растворе, моль/л; СА – текущая молярная концентрация реагента в растворе, моль/л. – начальная молярная концентрация реагента в растворе, моль/л; СА – текущая молярная концентрация реагента в растворе, моль/л.
Условия опыта, экспериментальные и расчетные данные представьте в табл. 12.
Табл. 12. Экспериментальные и расчетные данные
№
опы-
та
|
Время
от
начала
опыта,
мин
|
Сопро-
тивле-
ние
раст-
вора,
Ом
|
Текущая
концент-
рация
NaOH
в растворе,
СNaOH, моль/л
|
Текущая
концент-
рация
эфира
в растворе,
Сэфира,
моль/л
|
Степень
превращения
NaOH,
X NaOH
|
Степень
превращения эфира, Xэфира
|
Интенсивность работы реактора
|
6.2.3. Задание к лабораторной работе
Рассчитать изменения концентрации и степени превращения NaOH и эфира во времени при заданной температуре. Построить кинетические кривые и проанализировать ход изменения кривых.
Исследовать влияние вида эфира (вид эфира – СН3СООСН3, СН3СОО(СН2)2СН3, СН3СООС2Н5, НСООСН3, НСОО(СН2)2СН3 или НСООС2Н5 задает преподаватель) на степень и скорость его омыления при протекании реакции в реакторе периодического действия.
С использованием характеристического уравнения для реактора идеального смешения рассчитать время, необходимое для достижения заданной степени превращения и сравнить с экспериментальным значением. Проанализировать полученный результат и сделать вывод об интенсивности работы реактора.
СОДЕРЖАНИЕ
Введение………………………………………………………….….
Порядок выполнения и оформления лабораторных работ……
Водоподготовка………………………………………………….
Общие положения………………………………………..
Качество воды и требования к ней……………………….
Промышленная водоподготовка…………………………
Методика выполнения работы……………………………
Задание к лабораторной работе…………………………..
Гетерогенные процессы в системах газ – твердое, твердое – твердое…………………………………………………………….
Восстановление диоксида углерода……………………..
Разложение карбонатов и синтез силикатов…………….
Обжиг сульфидных руд…………………………………..
Система твердое – твердое………………………………..
Гетерогенные процессы в системе газ – жидкость……………..
Общие положения…………………………………………
Абсорбция диоксида серы………………………………..
Гетерогенно-каталитические процессы………………………..
Общие положения…………………………………………
Каталитическое окисление диоксида серы………………
Химические реакторы……………………………………………
Общие положения…………………………………………
Периодический реактор идеального смешения………….
Приложения…………………………………………………………
|
|
Учебное издание
Ещенко Людмила Семеновна
Соколов Михаил Тимофеевич
Дормешкин Олег Борисович
Кордиков Василий Дмитриевич
ОБЩАЯ ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ
Лабораторный практикум
Редактор Р.М. Рябая
Подписано в печать 03. 2004 Формат 60х84 1/16.
Бумага офсетная. Гарнитура Таймс. Печать офсетная.
Усл. печ. л. ___. Уч.-изд. л. ____.
Тираж 350 экз. Заказ___________
Учреждение образования
«Белорусский государственный технологический университет».
220050. Минск, Свердлова, 13а. Лицензия ЛВ № 276 от 15.04.03.
Отпечатано в лаборатории полиграфии учреждения образования
«Белорусский государственный технологический университет».
220050. Минск, Свердлова, 13.
|
|
|
 Скачать 0.72 Mb.
Скачать 0.72 Mb.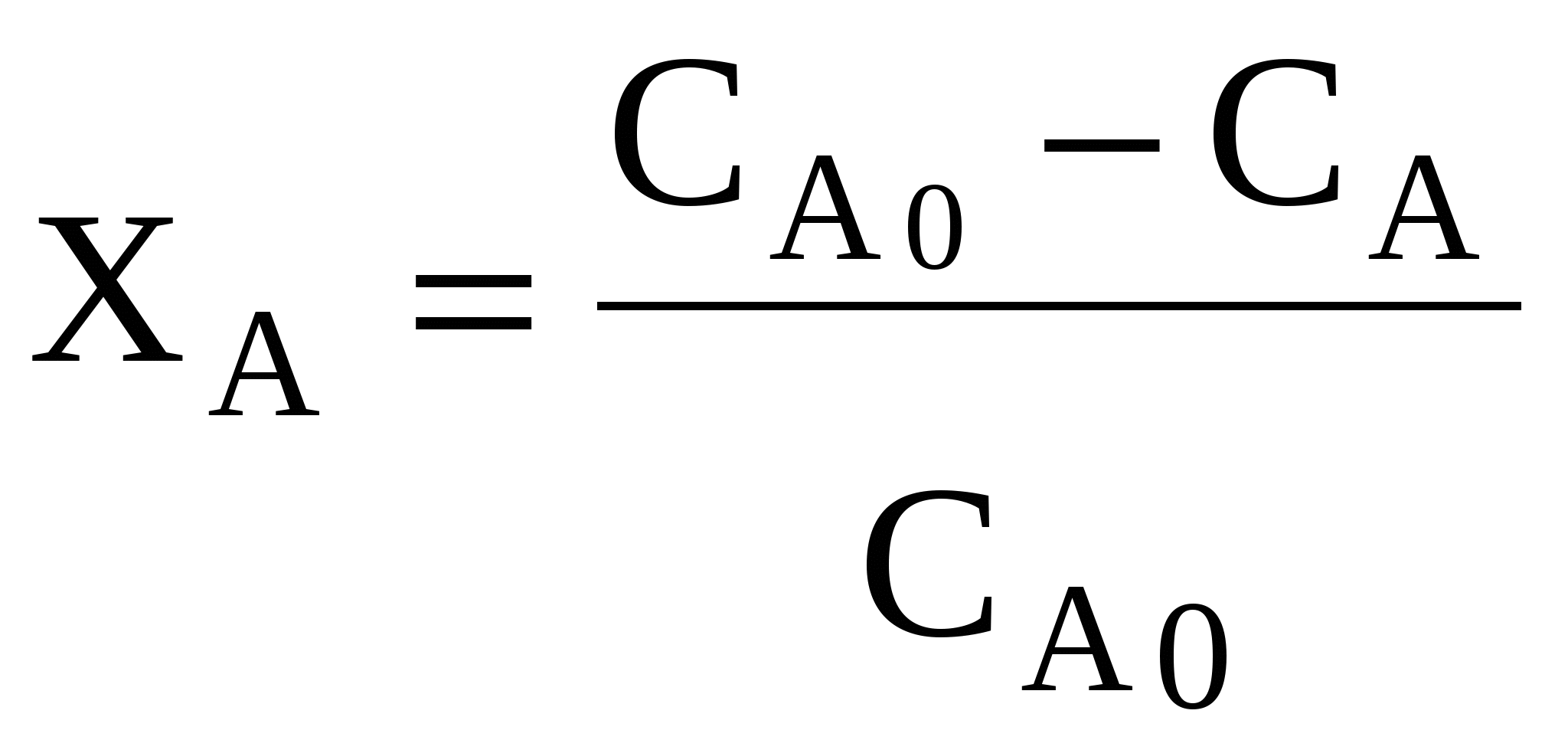 , (83)
, (83)