Практикум по бх. Практикум по биологической химии Для студентов лечебного и педиатрического
 Скачать 5.3 Mb. Скачать 5.3 Mb.
|
Тема 9.2. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| | Опыт 1, мл | Опыт 2, мл |
| Свежее растительное масло Старое растительное масло Бутанол 1,0% раствор фенолфталеина | 0,5 –– 0,5 1-2 капли | –– 0,5 0,5 1-2 капли |
| 0,1 М раствор КОН | Титруют до светло-розового окрашивания, не исчезающего в течение минуты | |
Расчет
Кислотное число =
а – количество раствора щелочи (мл), израсходованное на титрование; 0,00561 – титр 0,1 М раствора КОН; б – объем жира (мл);
0,9 – плотность жира (г/мл); 1000 – коэффициент перевода мг в г.
Нормальные величины
Свежее растительное масло 1-3 ед
Практическое значение
Кислотное число жира отражает количество жирных кислот в пищевом продукте и используется для определения качества пищевого жира.
Изменение количества и состава пищевого жира при хранении носит название прогоркания жиров. Прогоркание жира обусловлено появлением в его составе летучих альдегидов, кетонов, жирных кислот невысокой молекулярной массы и нелетучих веществ перекисного характера.
Причиной прогоркания служат два вида факторов: биологические и химические. К группе биологических факторов относят микроорганизмы, осуществляющие превращение и гидролиз жирных кислот. Химическое прогорание (перекисное окисление липидов) связано с ультрафиолетовым облучением, тепловыми процессами, с окислением кислородом воздуха двойных связей жирных кислот, находящихся в составе триацилглицеролов и фосфолипидов.
Оформление работы
Записывают принцип метода, ход работы. Отмечают результаты для свежего и прогорклого растительного масла. Делают вывод об особенностях состава жирных кислот.
Лабораторная работа 2
Определение концентрации триацилглицеролов
в сыворотке крови
Принцип
Метод основан на использовании сопряженных ферментативных реакций, осуществляемых: 1) липазой, катализирующей гидролиз триацилглицеролов до спирта глицерола и жирных кислот; 2) глицеролкиназой, катализирующей фосфорилирование глицерола; 3) глицеролфосфатоксидазой, окисляющей глицерол-3-фосфат в присутствии О2 до диоксиацетонфосфата с образованием Н2О2; 4) пероксидазой, катализирующей в присутствии хлорфенола окисление перекисью водорода 4-аминоантипирина с образованием хинонимина, окрашенного продукта розового-малинового цвета.
Материал исследования
Сыворотка крови.
Реактивы
Рабочий реактив: раствор липазы, глицеролкиназы, глицеролфосфатоксидазы, пероксидазы, хлорфенола, 4 аминоантипирина в буферном растворе.
Стандартный раствор триацилглицерола (триолеат), 2,29 ммоль/л.
Проведение анализа
| | Опыт, мл | Стандарт, мл |
| Сыворотка крови | 0,03 | –– |
| Стандартный р-р триацилглицерола | –– | 0,03 |
| Рабочий реактив | 3,0 | 3,0 |
| | Инкубируют 20 минут при 20-25°С, измеряют оптическую плотность опытной и стандартной проб против воды при 540 нм (зеленый светофильтр) | |
Расчет
Концентрация триацилглицеролов, ммоль/л =
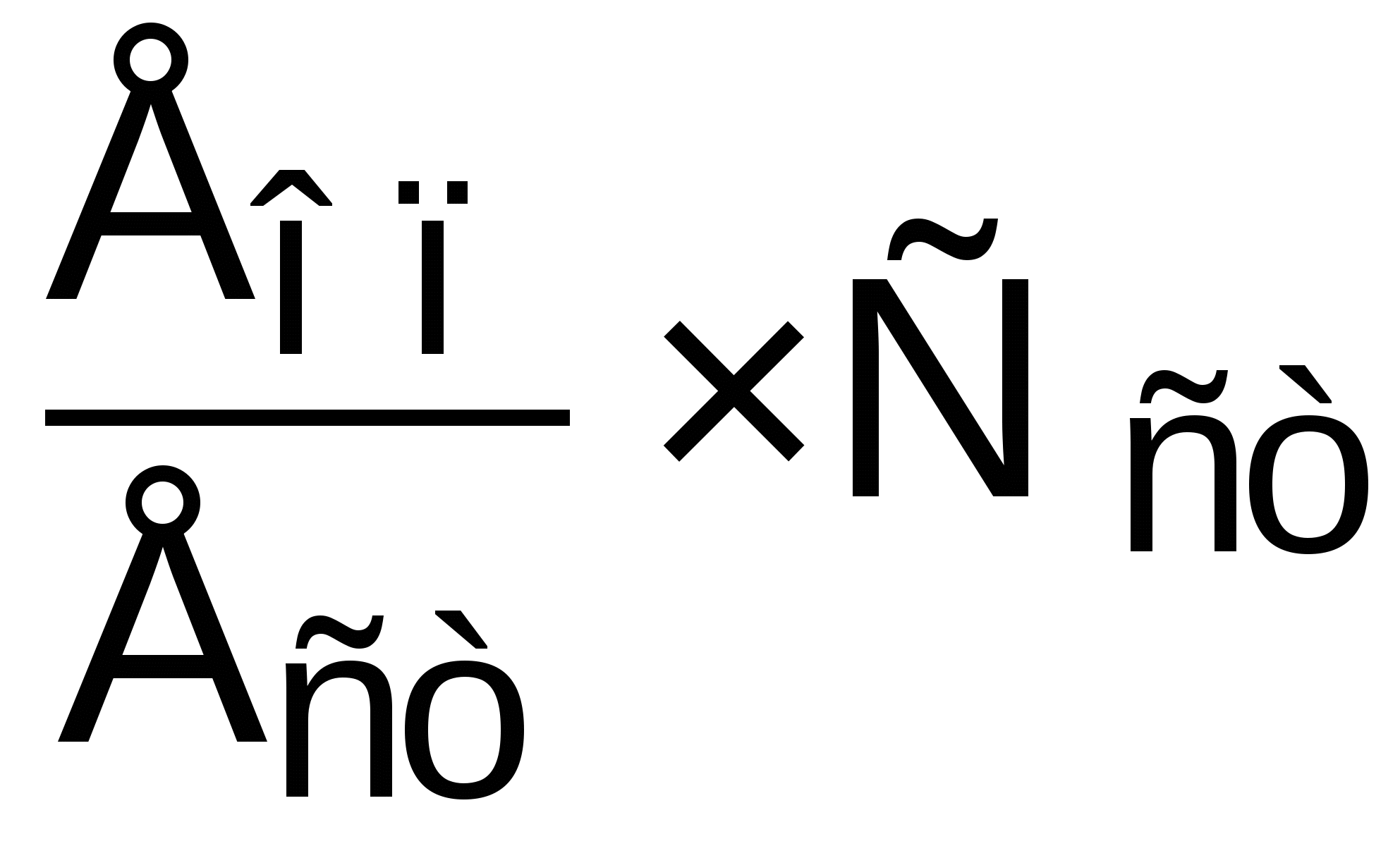 , где
, гдеЕоп и Ест – оптическая плотность опытной и стандартной проб,
Сст – концентрация стандартного раствора
Нормальные показатели
| Сыворотка крови | дети | 0,15-1,56 ммоль/л |
| | взрослые | 0,45-1,71 ммоль/л |
Клинико-диагностическое значение
Определение концентрации триацилглицеролов наиболее информативно для типирования первичного нарушения их обмена – гиперлипопротеинемий.
Повышение уровня триацилглицеролов наблюдается при ожирении, сахарном диабете, гипертонической болезни, ишемической болезни сердца, панкреатитах, хронической почечной недостаточности и нефротическом синдроме, гипотиреозе, атеросклерозе, алкоголизме.
Снижение концентрации триацилглицеролов отмечается при гипертиреозе, хронических обструктивных заболеваниях легких, терминальных стадиях поражения печени, синдроме мальабсорбции.
Оформление работы
Указывают принцип метода, ход работы, нормальные величины и результаты исследования, отмечают клинико-диагностическое значение показателя и делают выводы о возможной патологии.
Лабораторная работа 3
Обнаружение кетоновых тел в моче
Материал исследования
Нормальная моча и моча с ацетоном.
Реактивы
1) 10% р-р нитропруссида натрия, 2) 10% р-р NaOH, 3) р-р Люголя, 4) 5% р-р FeCl3, 5) конц. CH3COOH.
Качественная проба Легаля на ацетон и ацетоуксусную кислоту
Принцип
Метод основан на способности ацетона и ацетоуксусной кислоты в щелочной среде образовывать с нитропруссидом натрия комплексы оранжево-красного цвета, переходящие при подкислении раствора в соединения вишнево-красного цвета.
Проба более чувствительна к ацетоуксусной кислоте, чем к ацетону, с гидроксимасляной кислотой реакция не идет.
Проведение анализа
| | Опыт 1, капли | Опыт 2, капли |
| Нормальная моча Моча с ацетоном 10% р-р нитропруссида Na 10% раствор NaOH | 10 –– 2 4 | –– 10 2 4 |
| | Появляется оранжево-красное окрашивание | |
| Конц. CH3COOH | 10 | 10 |
| | При наличии кетоновых тел появляется вишнево-красное окрашивание. Если кетоны отсутствуют, то при подкислении цвет раствора переходит в желтый (происходит реакция на креатинин в моче) | |
Нормальные величины
| Моча | отсутствие |
Качественная проба Либена на ацетон
Принцип
Ацетон в щелочной среде в присутствии раствора Люголя (раствор йода в KJ) образует желтый осадок йодоформа, обладающего специфическим запахом.
Проведение анализа
| | Опыт 1, капли | Опыт 2, капли |
| Нормальная моча Моча с ацетоном 10% р-р NaOH | 20 –– 2 | –– 20 2 |
| Р-р Люголя | Добавляют до слабо-желтой окраски раствора. | |
| | При наличии ацетона жидкость мутнеет вследствие выделения бледно-желтого осадка йодоформа, обладающего характерным запахом | |
Нормальные величины
| Моча | отсутствие |
Клинико-диагностическое значение
Кетоновые тела в моче (кетонурия) появляются при кетонемии, которая возникает при голодании, сахарном диабете, при повышении концентрации жиромобилизующих гормонов в крови.
Оформление работы
Записывают принцип методов, отображают получаемую окраску, присутствие (+) или отсутствие (–) кетоновых тел. В выводах указывают состояния, при которых в моче обнаруживаются кетоновые тела.
| Название метода | Материал исследования | Результаты реакции | Наличие кетоновых тел | |
| Проба Легаля | Моча | нормальная | | |
| с ацетоном | | | ||
| Проба Либена | Моча | нормальная | | |
| с ацетоном | | | ||
