практикум по биохимии. Практикум по биологической химии, изданный в 1986 году, подвергся существенной переработке, а также дополнен новыми лабораторными работами в разделах белки, липиды,
 Скачать 1.79 Mb. Скачать 1.79 Mb.
|
Фотометрические приборыФотометрия (абсорбциометрия) – метод качественного и количественного анализа, основанный на измерении интенсивности поглощения или рассеяния веществом светового потока. Светопоглощение или экстинкция, согласно закону фотометрии Ламберта-Бугера-Бера прямо пропорционально концентрации поглощающего вещества, толщине слоя раствора и молярному коэффициенту экстинкции (Е). Последний представляет собой поглощение раствора вещества концентрацией 1моль/л, помещенного в кювету с толщиной слоя 1см, и измеряется в л·моль-1·см-1. 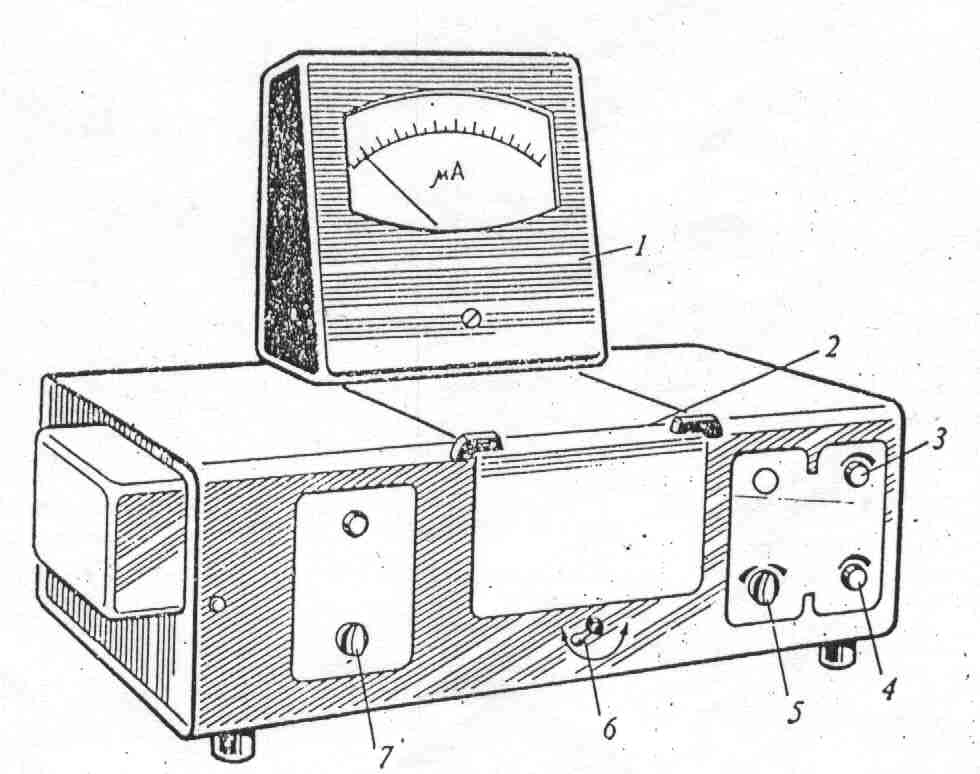 Рис. 1. Общий вид колориметра фотоэлектрического концентрационного1 – гальваномер; 2 – крышка кюветного отделения; 3 – ручка установки «грубо»; 4 – ручка установки «точно»; 5 – ручка чувствительности; 6 – ручка кюветодержателя; 7 – переключатель светофильров. Часто используют и другой показатель – удельный коэффициент экстинкции Е1см1%, т.е. поглощение света 1%-ным раствором вещества в кювете с толщиной слоя 1см. Для определения содержания какого-либо компонента биологического материала строят калибровочный график, отражающий зависимость между экстинкцией (Е) и концентрацией (С) этого вещества в растворе и представляющий собой прямую линию в прямоугольной системе координат. Для фотометрического анализа используют фотоэлектроколориметры, фотоэлектроколориметры-нефелометры и спектрофотометры. Фотоэлектроколориметры (ФЭК) различных моделей применяют для анализа светопоглощения окрашенных растворов веществ в видимой области спектра (рис.1). Фотоэлектроколориметры-нефелометры применяют для измерения интенсивности светорассеивания или ослабления светового потока изучаемых веществ в мутных средах. Колориметр фотоэлектрический концентрационный позволяет благодаря большому набору узкополосных светофильтров проводить измерения в определенной области спектра в диапазоне длин волн 315-980 нм. Этот прибор используют для определения светопоглощения веществ, а также коэффициент пропускания рассеивающих взвесей, эмульсий и коллоидных растворов в проходящем свете. Порядок работы изложен в инструкции. 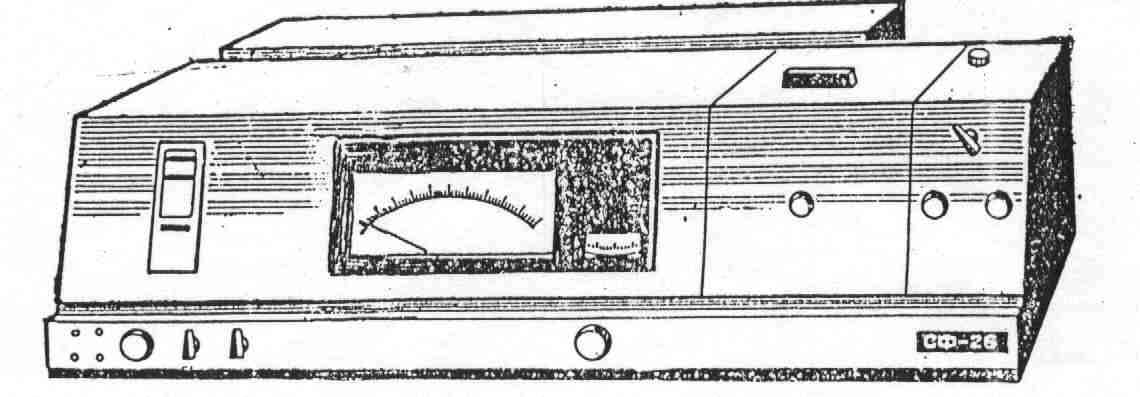 Рис. 2. Общий вид спектрофотометра. Спектрофотометры (рис.2) используют для изучения строения, качественного и количественного анализа вещества по интенсивности поглощения его в монохроматическом свете. В клинико-биохимических и научных исследованиях широко применяются спектрофотометры СФ-16, СФ-26, СФ-46 и их современные модификации, работающие в области спектра от 186 до 1100 нм. Правила работы на спектрофотометре изложены в инструкциях к прибору. Флуориметрические приборыДля качественного и количественного анализа веществ, которые, поглощая энергию, способны к люминисценции (флуоресценции) применяются флуороскопы и флуориметры. Флуороскоп позволяет проводить полуколичественный анализ путем визуального сравнения интенсивности флуоресценции опытного раствора со стандартным, где концентрация вещества известна. Флуориметры позволяют проводить количественный анализ. В этих приборах выделение области спектра, необходимого для возбуждения данного вещества, осуществляется первичными светофильтрами, а пропускание характерного для него участка излучения (свечения) – с помощью вторичных светофильтров. ЦентрифугиЦентрифугирование – метод разделения смеси компонентов жидких сред под действием центробежной силы. Его используют для отделения форменных элементов крови от плазмы, для осаждения и выделения клеток из мочи, спинно-мозговой жидкости и других сред организма, а также для отделения осадков от жидкой фазы (надосадочная жидкость, или супернатант). В клинико-биохимических лабораториях для этой цели используют малогабаритные центрифуги общего назначения. Они дают максимальную скорость около 6000 об·мин-1. Для специальных биохимических исследований применяют ультрацентрифуги с охлаждением (рефрижераторные), например ЦР-2-25, УЦП-1-75 и др. Они позволяют проводить дифференциальное центрифугирование, т.е. разделение частиц, отличающихся друг от друга размерами и плотностью. Скорость осаждения частиц определяется центробежным ускорением, которое обычно выражают в единицах g (гравитационная постоянная, равная 980 см·с-2). Величину g обозначают как относительное центробежное ускорение. Она зависит от скорости вращения ротора (п, об·мин-1) и расстояния (r, см) от оси вращения ротора до середины столбика жидкости в пробирке и определяется по формуле g = 1,11∙10-5n2r На практике g устанавливают по номограмме, прилагаемой к инструкции для каждой ультрацентрифуги. С помощью дифференциального центрифугирования выделяют субклеточные частицы – ядра, митохондрии, лизосомы, микросомы и др. |
