ЛАБОРАТОРНЫЙ ПРАКТИКУМ ПО ХИМ ТЕРМОДИНамиКЕ. Практикум по химической термодинамике учебное пособие для студентов всех специальностей
 Скачать 2.28 Mb. Скачать 2.28 Mb.
|
ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
а) с простой эвтектикой; б) с образованием устойчивого химического соединения; в) с образованием неустойчивого химического соединения; г) с неограниченной взаимной растворимостью компонентов в твердом состоянии; д) с ограниченной растворимостью компонентов в твердом состоянии; е) с ограниченной взаимной растворимостью компонентов в жидком состоянии На каждой диаграмме покажите значение отдельных полей, линий, точек, число компонентов, степеней свободы, фаз. ПРИМЕР РЕШЕНИЯ ЗАДАЧНа диаграмме состояния системы Pt – Sb:
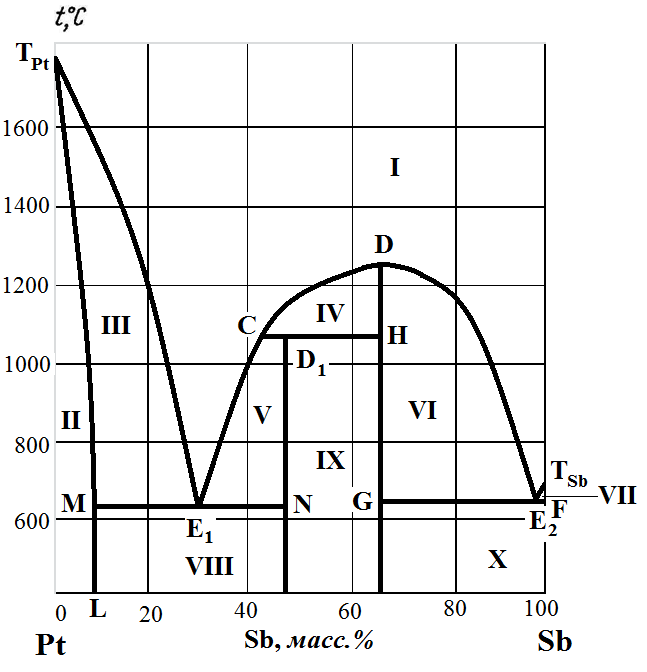 Рис. 3.16. Диаграмма состояния системы Pt – Sb. Решение:
М(Pt) = 195 г/моль; М(Sb) = 121 г/моль. 1) Неустойчивое химическое соединение D1. По диаграмме определяем соотношение масс компонентов: Рассчитываем формулу химического соединения: Следовательно, формула неустойчивого химического соединения Pt2Sb3. 2)Устойчивое химическое соединение D. По диаграмме определяем соотношение масс компонентов: Рассчитываем формулу химического соединения: Следовательно, формула неустойчивого химического соединения PtSb3.
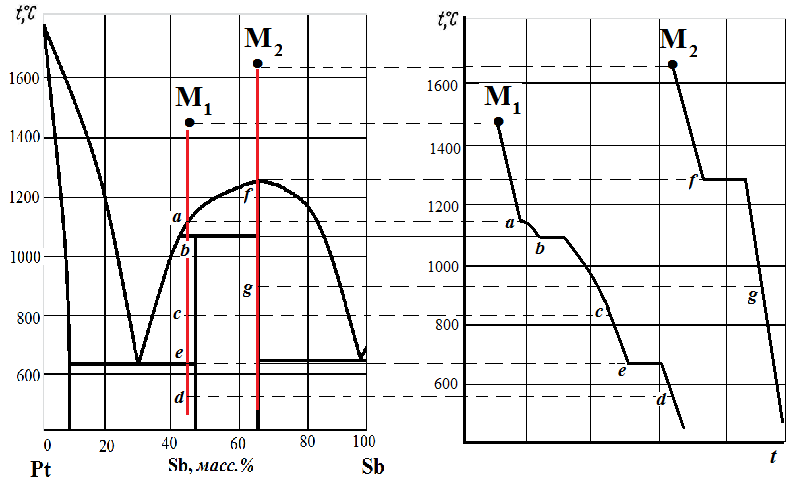 а б Рис. 3.17. Процесс охлаждения расплава заданного состава (а) и кривые охлаждения (б) Результат рассмотрения процесса охлаждения расплава из точки М1.
Точка M2 отвечает составу устойчивого (конгруэнтно плавящегося) химического соединения D. Результат рассмотрения процесса охлаждения расплава из точки M2.
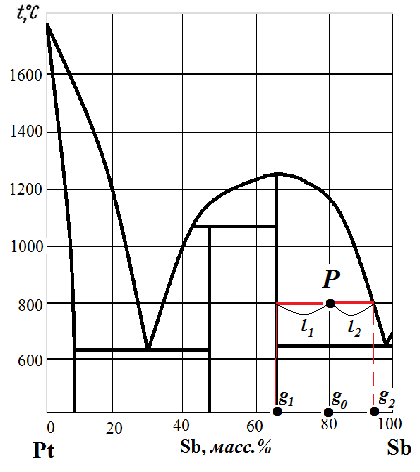 Рис. 3.18. Определение соотношения масс твердой и жидкой фаз по правилу рычага На диаграмме состояния поставим точку P, соответствующую температуре 800ºС и 80 масс.% Sb. В точке P в равновесии находятся кристаллы устойчивого химического соединения Dи расплав. Определим соотношение между фазами по правилу рычага: Из условия задачи следует, что Решаем совместно систему двух уравнений: 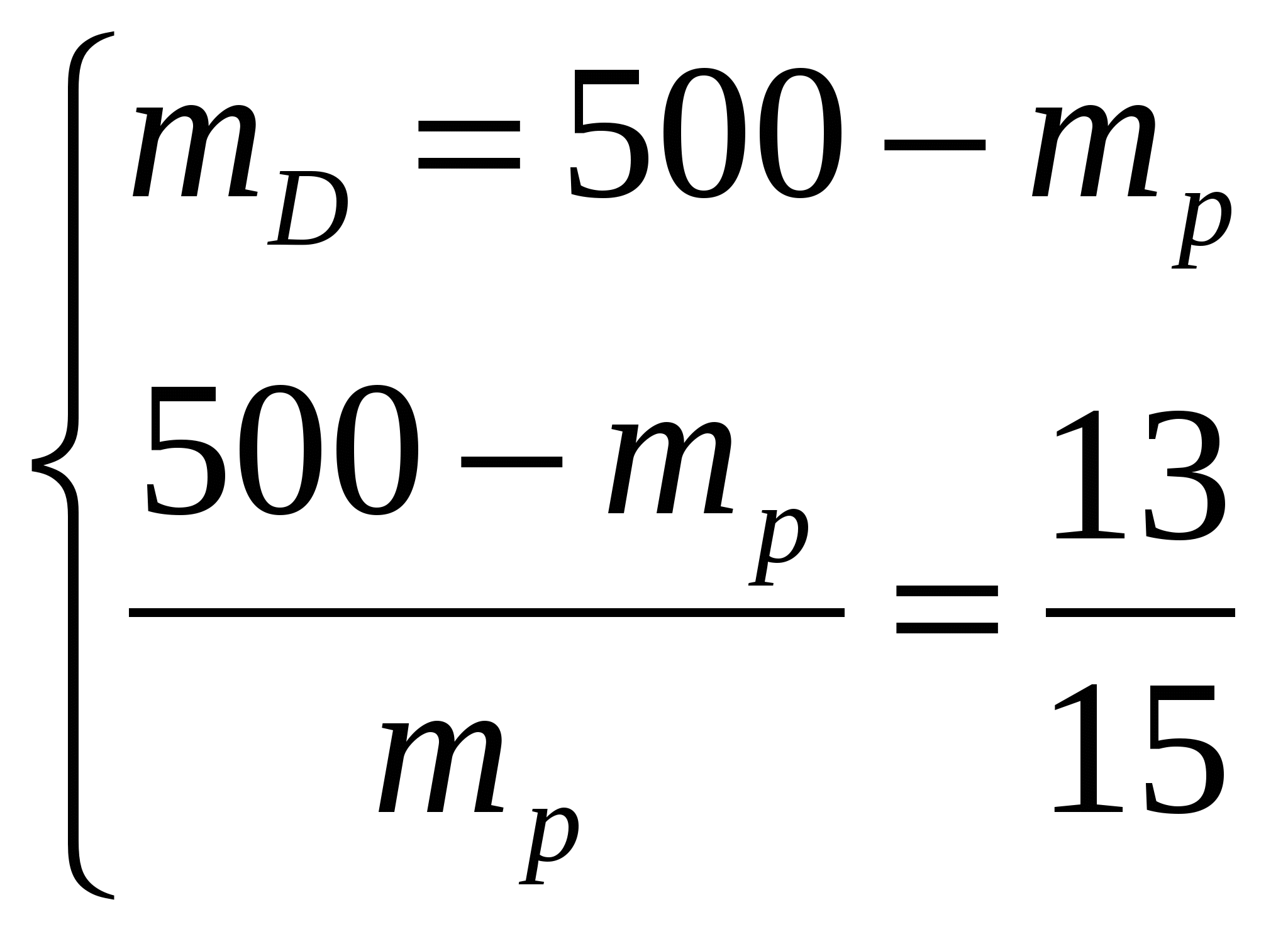 15 (500 mр) 13 mp 6500 15 mр 13 mp 6500 28 mp mpасплава 232 г mD 500 232 267 г Таким образом, из 500 г первоначального состава масса расплава составит 232 г, а масса кристаллов химического соединения D 267 г. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
